燃煤烟气脱除SO2催化反应动力学研究
2015-06-12尹云萍吴宇鸣王承学
尹云萍, 吴宇鸣, 王承学*
(1.长春工业大学 化学工程学院,吉林 长春 130012;2.吉林大学 化学学院,吉林 长春 130012)
0 引 言
我国煤炭产量居世界第一位,且多为高硫煤,煤燃烧所排放的SO2占全国SO2总排放量的87%,我国煤产量的20%用于直接燃烧,燃烧发电的产电量占总电力的71%~74.5%[1]。煤燃烧所产生的污染物有:SO2、CO、烃类、醛类、氮氧化物以及固体颗粒物烟尘等,其中SO2是燃煤烟气的主要成分之一[2-3]。空气中的SO2浓度高于20×10-6~100×10-6时,人受到刺激而引起咳嗽、泪流等症状;100×10-6~400×10-6时,人可产生咽喉异常感,疼痛、胸痛并且呼吸困难;400×10-6~500×10-6时,人立刻引起严重中毒,呼吸道闭塞导致窒息死亡[4]。长期吸入低浓度的SO2将引起或加重人的呼吸道疾病[5]。值得注意的是SO2与水汽、烟尘等结合形成硫酸烟雾及硫酸盐等气溶胶微粒PM2.5和PM10后,能够侵入肺的深部组织,造成的危害远比气态的SO2大得多。SO2形成的酸雨对水资源生态系统、农业生态系统、森林生态系统、建筑物、各种材料以及人体健康都会造成危害[6]。随着经济的不断发展,煤耗量的增加,我国大气环境和生态环境严重恶化。严格治理和控制SO2污染已经迫在眉睫。现将燃煤烟气中的SO2直接催化氧化生成对应的盐类,是脱除SO2污染的一个新的有效途径[7]。
关于燃煤烟气脱硫反应动力学研究文献报道很少[8-12],由于燃煤烟气中SO2浓度很低。在催化剂和氨气存在下利用连续流动固定床条件下进行改变条件实验,对测得的数据经过整理,再利用积分法和线性作图法来寻找宏观上反应条件范围内的动力学方程。
1 反应原理与动力学方程基本形式
由于燃煤烟气中的硫氧化物98%以上都是SO2,在大于210℃以上的主要脱除原理为:
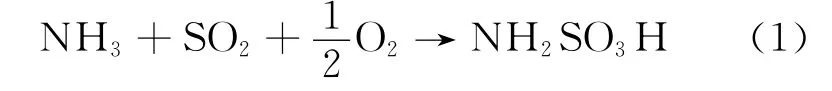
实验用钢瓶配制模拟烟气,气体组成为[13]NH38.5%,SO21.613%,O22.5%,其余为N2。
在常压下、反应温度450~460℃、空时1.54s时,在催化剂直径为2~4mm的固定床反应器中连续流动条件下测得实验数据[14]。
根据化学反应方程式(1),假设反应动力学方程为:
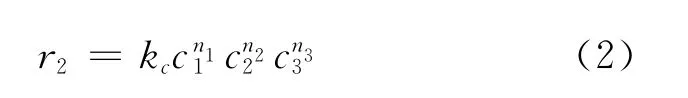
式中:n1,n2,n3——分别代表O2,SO2,NH3的反应级数;
c1,c2,c3——分 别 代 表O2,SO2,NH3的 反应浓度。
根据进料组成与化学反应方程式,SO2含量最少为体系的限定组分A,r2为限定组分定义的反应速率。
在常压和一定的反应温度下,虽然体系在反应前后分子数有所改变,由于SO2含量很低可以
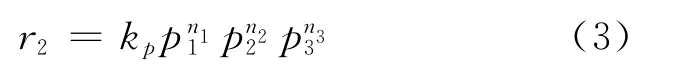
式中:kp——以分压表示的反应速率常数,kp=
kc——以浓度表达的反应速率常数;
R,T——分别代表气体常数和反应温度;
n1+n2+n3——反应的总级数n。
由反应计量关系,式(2)可以转化成用限定组分表达的动力学方程:

2 V2O5/HZSM-5催化剂上的反应总级数确定
通过已知的实验数据[11]:在催化剂V2O5/HZSM-5上,实验得出的空速和SO2脱除率的关系见表1。
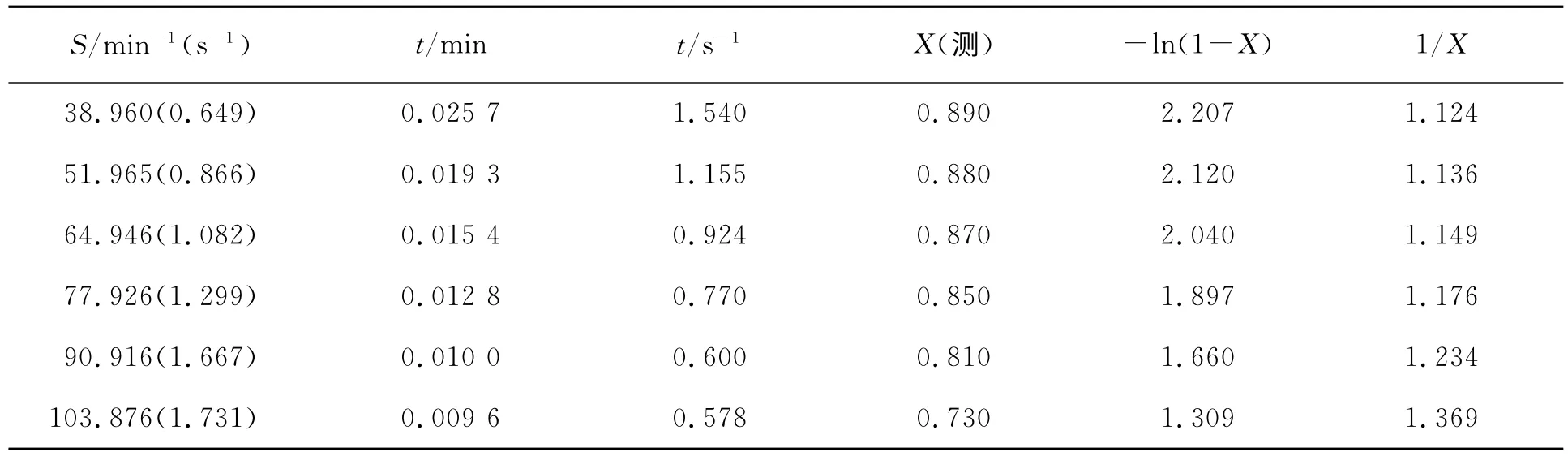
表1 空速S、空时t和SO2脱除率X之间的关系
这里空时(t)代表了反应时间,通过反应时间与SO2去除率的关系就可以确定反应条件下的宏观速率方程。
当总反应级数n=0时,式(2)化为:
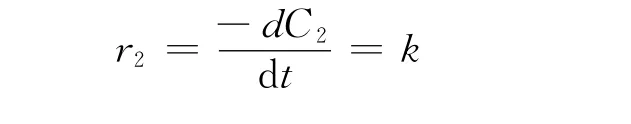
对此式积分,当SO2初始浓度为C20,反应时间为0,反应到浓度为C2时,所用时间为t,作定积分,可得出:
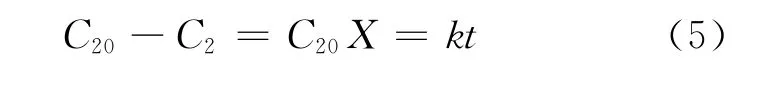
式中:X——SO2去除率。
从式(5)可以看出,SO2去除率和反应时间符合0级反应时,X与t应为直线关系,用表1实验数据对X-t绘图,如图1所示。
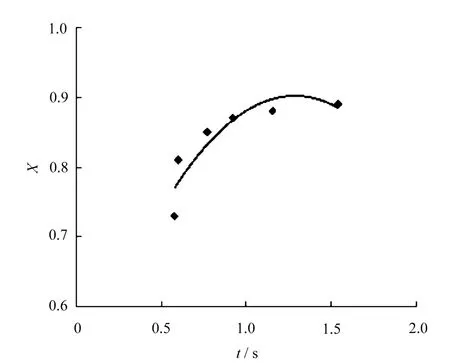
图1 零级反应SO2脱除率与反应时间关系
由图1的直线性可以看出,实验数据不符合零级反应规律。
同理,当反应为一级和二级时,用同零级反应同样的边界条件,从式(4)积分可分别得:
一级:
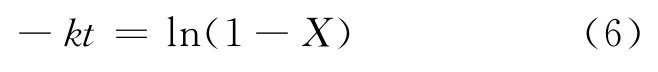
二级:
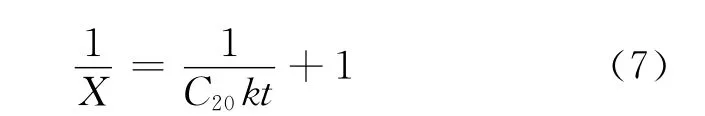
利用表1数据作图,如图2和图3所示。
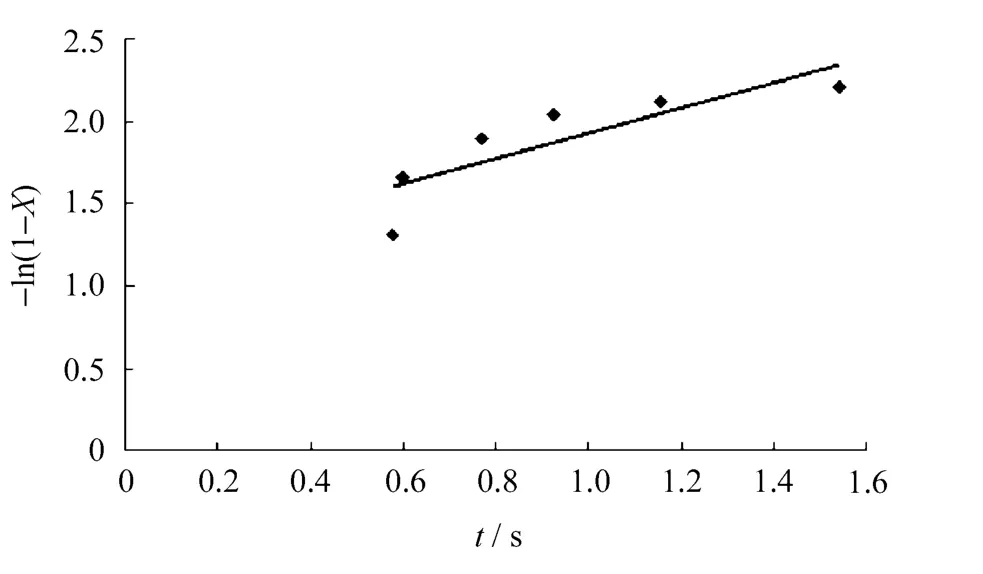
图2 一级反应假设的数据处理结果
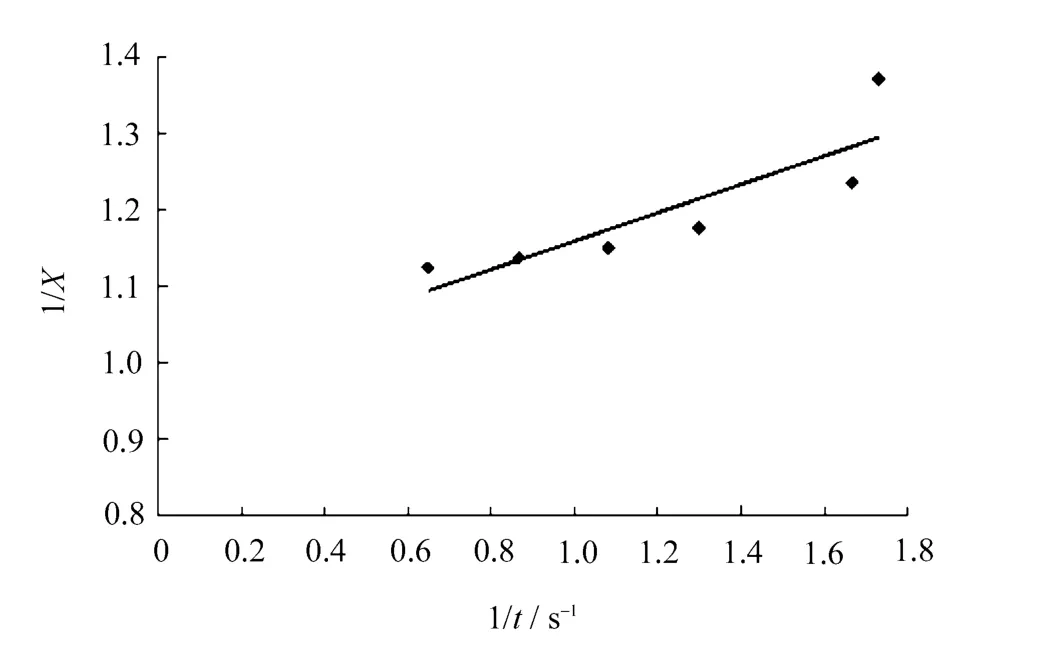
图3 二级反应假设的数据处理结果
由图2和图3可以看出,两条曲线都近似符合一级直线关系。
3 CuO/γ-Al2O3催化剂上的反应级数确定
在CuO/γ-Al2O3催化剂测定的实验数据和同样处理数据结果见表2。
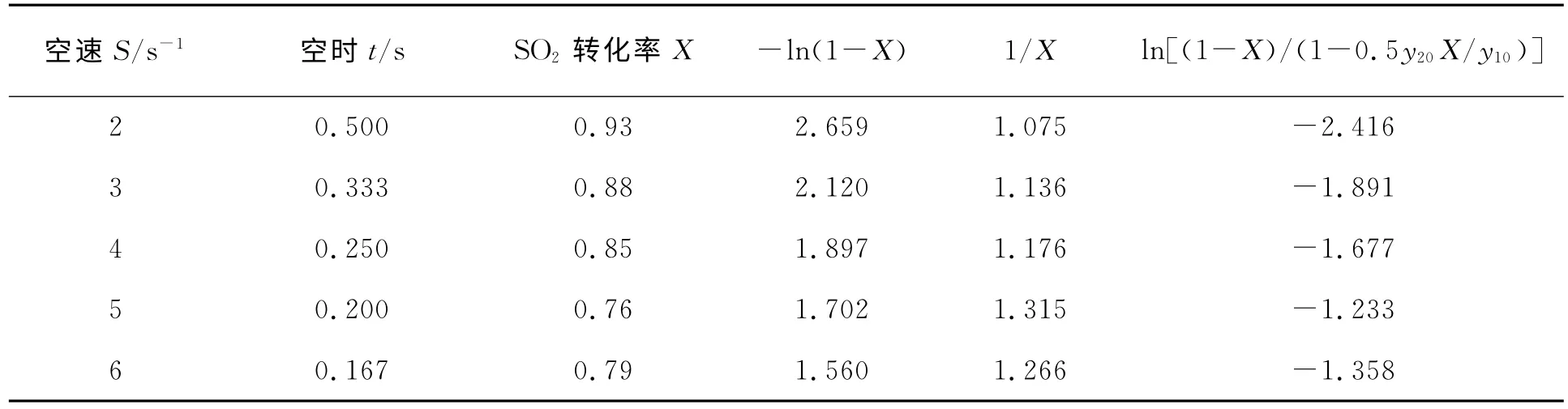
表2 CuO/γ-Al2O3催化剂上的实验数据
根据零级、一级和二级反应假设式(5)、式(6)和式(7),分别以表2中的数据t-x,t-1/ln(1-x)和1/t-1/x作图,如图4~图6所示。
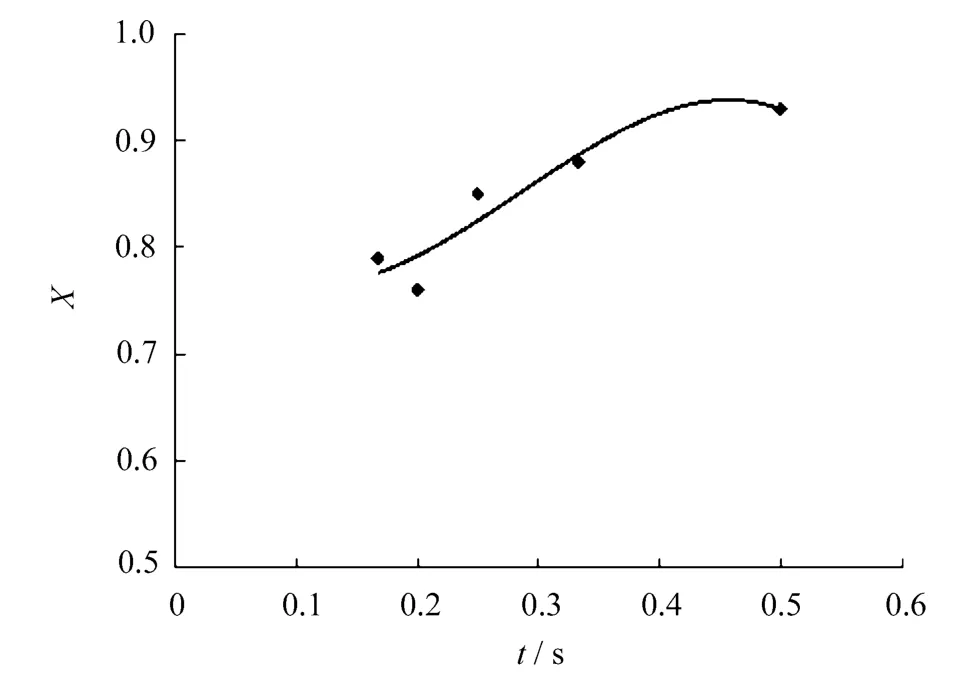
图4 零级反应假设曲线关系
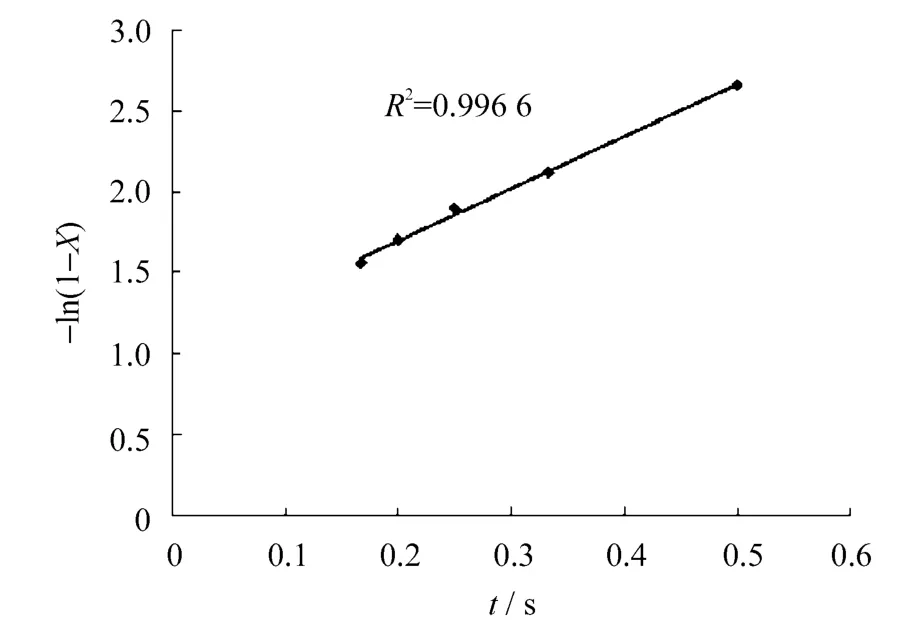
图5 一级反应假设曲线关系
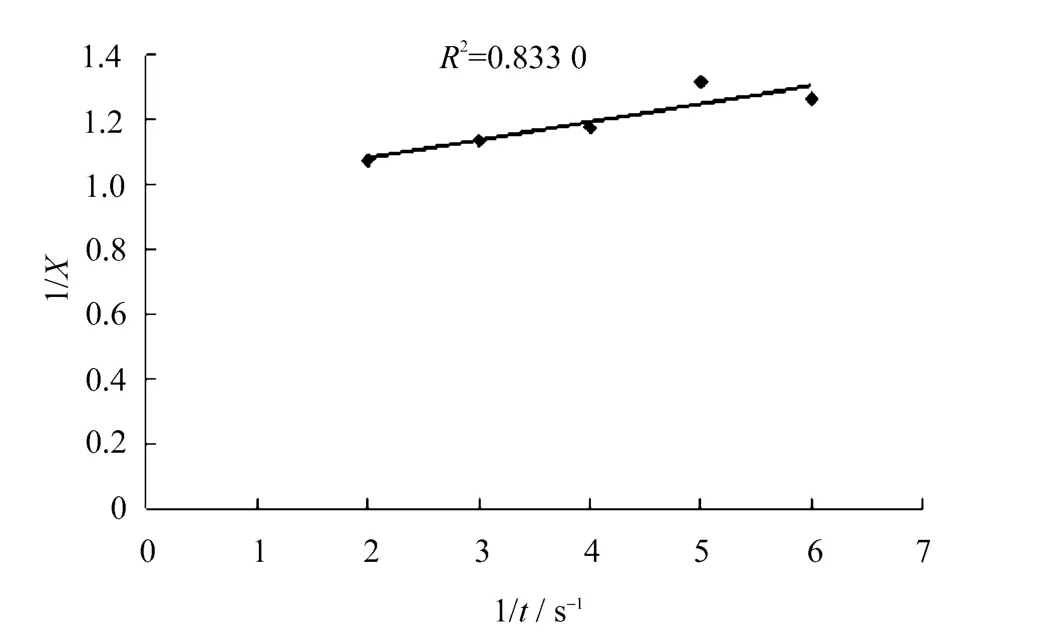
图6 二级反应假设曲线关系
从图4、图5和图6中看出,零级假设反应动力学不符合直线关系,而一级假设虽然符合直线,但仍偏离原点,只有二级反应动力学比较符合直线关系,相关系数为0.833。
结合两种催化剂上的反应级数,认为该反应宏观动力学总级数为二级。
4 O2分级数的确定
在V2O5/HZSM-5催化剂、最佳反应温度460℃和反应空时1.54s条件下,通过改变O2初始测得的O2浓度变化与SO2转化率的关系数据见表3。
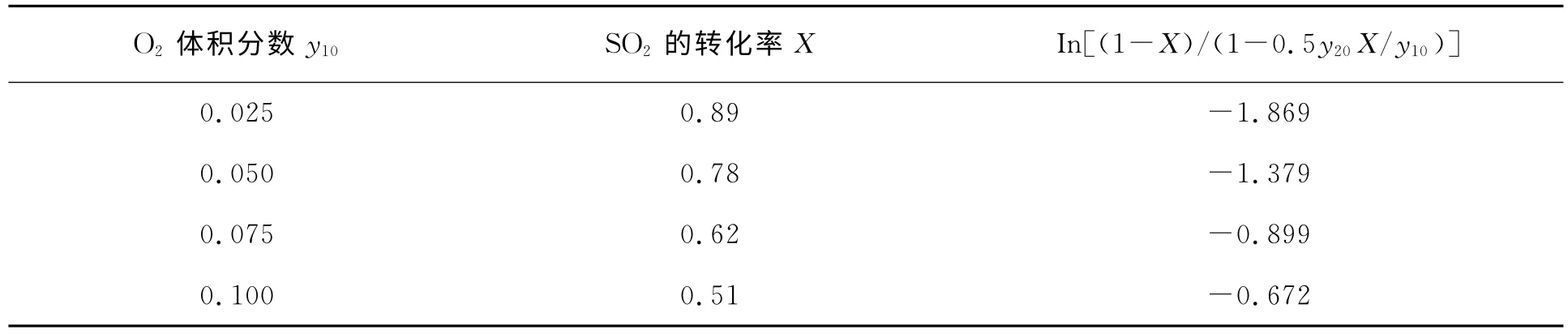
表3 实验测得的O2浓度变化与SO2转化率的关系
在恒温恒压恒容条件下,O2的体积分数就代表了它的分压。在体系中改变氧气的分压时,氨气和SO2初始含量不变。可将式(3)表示为:
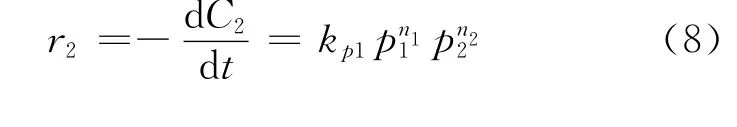
任意时刻转化掉的SO2为n20X,各物质反应到任意时刻时的mol分数为:
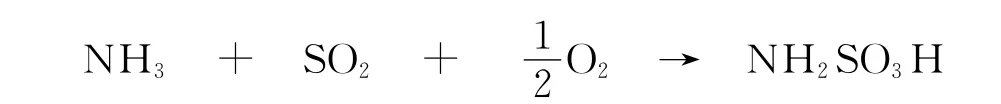
初始加入: n30n20n100
任意时刻剩余: n30-n20X n20-n20X n10-0.5n20X n20X
初始加入的总量为:
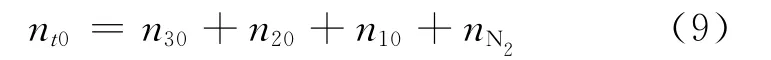
因此,可得任意时刻各物质的摩尔分数为:
SO2摩尔分数:
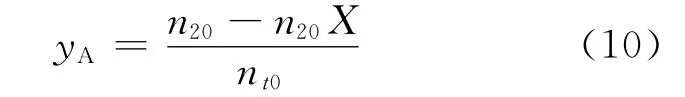
氧气摩尔分数:
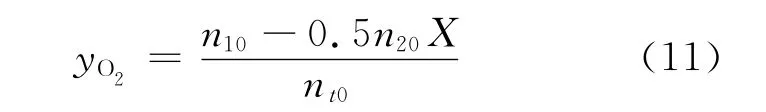
氨气的摩尔分数:
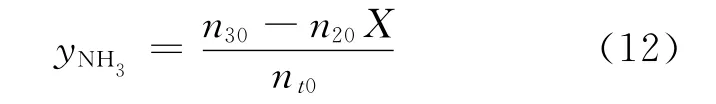
氨基磺酸摩尔分数:

假设SO2和氧气级数都为1时,即n1=n2=1,将式(10)~式(13)代入式(8)得:
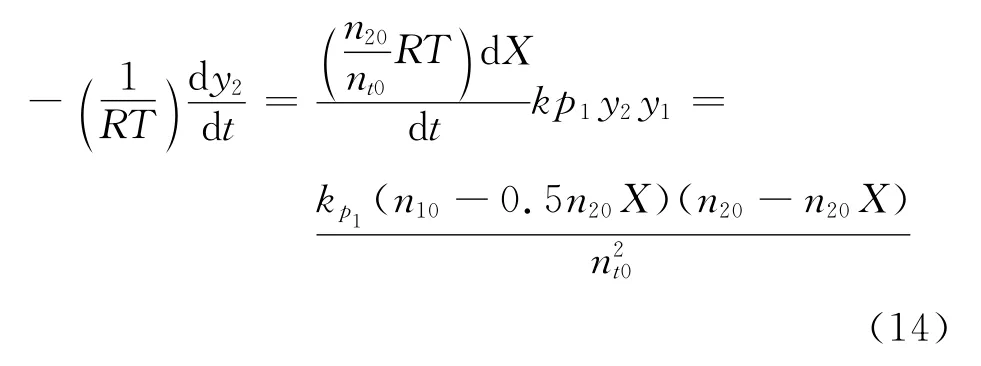
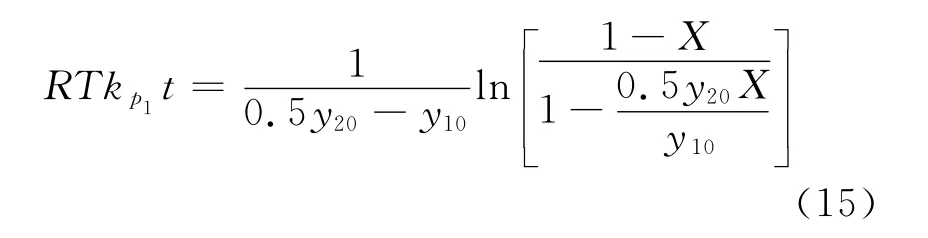
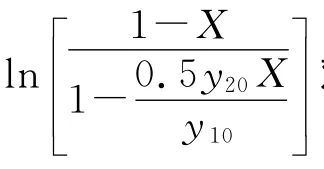
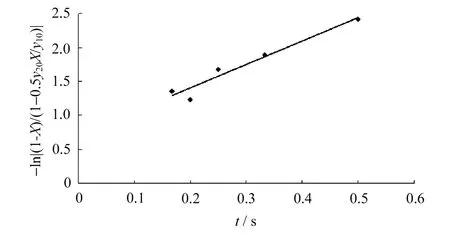
图7 O2和SO2都为一级假设时积分式的线性关系
从图7中可以看出,基本符合直线关系。
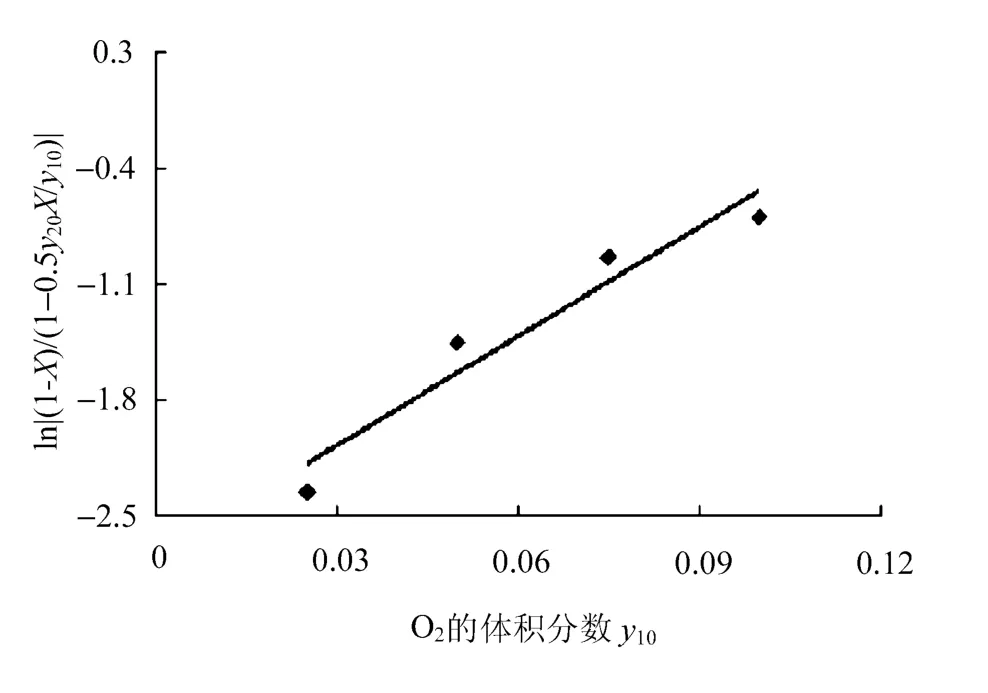
图8 O2加入体积分数化对于SO2的转化率影响
当SO2浓度固定(y20=1.163%)时,只改变O2加入浓度y10,这时式(15)变为:
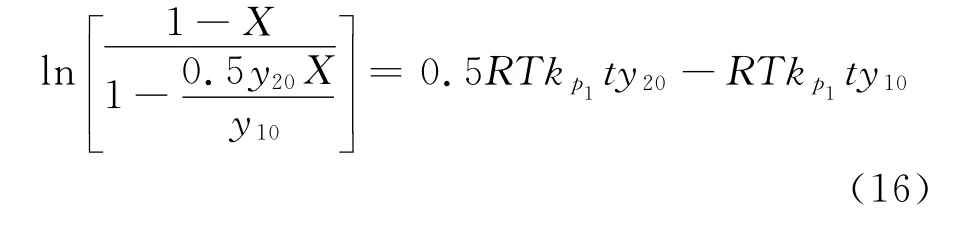
5 反应速率常数和速率方程的确定
由于氨气过量,反应速率与氨气浓度无关。因此,可给出催化反应宏观速率方程为:
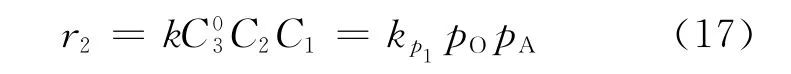
在V2O5/HZSM-5催化剂上,可利用图3的斜率和截距求取速率常数。当速率单位为mol·s-1·L-1,浓度单位为mol·L-1,当用分压表示速率方程时,kp1的单位是(mol·s-1·L-1)/(MPa)2。
通过式(15)斜率RTkp1值读取图8斜率值为1.807。
此时

因此,脱硫反应宏观动力学方程为:
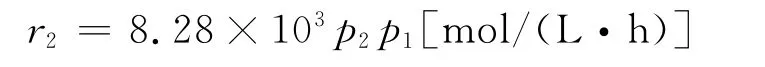
[1] 郝吉明,马广大.大气污染控制工程[M].北京:高等教育出版社,2002.
[2] 杨飏.二氧化硫减排技术与烟气脱硫工程[M].北京:冶金工业出版社,2004.
[3] 郝吉明,王书肖,陆永琪.燃煤二氧化硫污染控制技术手册[M].北京:化学工业出版社,2001.
[4] 童志权.工业废气净化与利用[M].北京:化学工业出版社,2001:198-208.
[5] 胡和兵.王牧野.吴勇民,等.二氧化硫化的污染与治理方法[J].环境保护科学,2006,32(4):5-9.
[6] 童志权.工业废气净化与利用[M].北京:化学工业出版社,2001:198-208.
[7] 许涛,张岗,刘波,等.烟气脱硫技术及评价方法[J].广东电力,2002,15(4):13-25.
[8] Ma Zh W,Zheng X R,Chang L P.Desulfurization kinetics of ZnO sorbent loaded on semi-coke support for hot coal gas[J].天然气化学,2012,21(5):556-562.
[9] Zhao Y,Xu P Y,Sun X J.Experimental and mechanism studies on simultaneous desulfurization and denitrification from flue gas using a flue gas circulating fluidized bed[J].中国科学B辑:英文版,2007,50(1):135-144.
[10] Li F,Yan B,Zhang J.Study on desulfurization efficiency and Products of Ce-doped nanosized ZnO desulfurizer at ambient temperature[J].稀土学报:英文版,2007,25(3):306-310.
[11] Zhao D S,Zhou E P,Liu H R.Oxidation desulfurization activity of phosphotungstic acid supported on yttrium-modified USY[J].稀土学报:英文版,2007,25(z1):104-108.
[12] Zheng X R,Bao W R,Jin Q M.Impact of impregnation pressure on desulfurization performance of Zn-based sorbents supported on semi-coke[J].天然气化学:英文版,2012,21(1):56-60.
[13] 付挽得.脱硫脱硝用铜基催化剂的制备与评价[D]:[硕士学位论文].长春:长春工业大学化学工程学院,2009.
[14] 刁振恒.HZSM-5分子筛催化剂脱硫脱硝研究[D]:[硕士学位论文].长春:长春工业大学化学工程学院,2011.
