帕立骨化醇治疗血液透析患者伴继发性甲状旁腺功能亢进
2015-06-09王泰娜贾凤玉章海涛龚德华刘志红
王泰娜 徐 斌 贾凤玉 章海涛 龚德华 刘志红
·论著·
帕立骨化醇治疗血液透析患者伴继发性甲状旁腺功能亢进
王泰娜 徐 斌 贾凤玉 章海涛 龚德华 刘志红
目的:观察起始剂量0.06~0.08μg/kg的帕立骨化醇治疗血液透析伴继发性甲状旁腺功能亢进患者12周的有效性和安全性。方法:入选南京军区南京总医院肾脏科血液净化中心维持性血液透析>3个月的患者11例(男性8例,女性3例),全部全段甲状旁腺激素(iPTH)>600 pg/m l,血钙≤2.60 mmol/l,钙磷乘积≤65 mg2/dl2,帕立骨化醇起始剂量0.06~0.08μg/kg,每4周复查iPTH,每2周复查钙、磷,治疗12周。根据iPTH下降幅度调整药物剂量,主要疗效指标为治疗12周iPTH较基线水平下降>30%;次要疗效指标包括:治疗12周iPTH下降率,iPTH降至正常范围(150~300 pg/ml)的患者例数,药物剂量变化,血钙、血磷、钙磷乘积变化及不良事件发生。结果:基线iPTH 1 087.0 pg/ml(802.9~1 413.0 pg/ml),血钙2.30±0.19mmol/L,血磷1.60±0.24mmol/L。帕立骨化醇起始剂量6例为0.06μg/kg,5例为0.08μg/kg,第12周时帕立骨化醇平均用量为0.11μg/kg,有6例患者在第8周即调整达到治疗剂量。11例患者有8例iPTH下降>30%,其中4例降至150~300 pg/ml,血钙平均升高8.6%,血磷平均升高21.2%,无明显不良反应发生。结论:中等起始剂量的帕立骨化醇能有效降低iPTH水平,同时血钙、磷变化相对稳定。
帕立骨化醇起始剂量继发性甲状旁腺功能亢进血液透析
继发性甲状旁腺功能亢进(SHPT)是终末期肾病和透析患者的常见并发症,与骨病、软组织和血管钙化及心血管疾病的高发生率、高死亡率密切相关[1]。目前,活性维生素D类药物是治疗SHPT的主要药物,但临床使用发现此类药物会增加胃肠道对钙磷的吸收而导致高钙、高磷血症,进而增加血管钙化的风险[2]。选择性维生素D受体激动剂——帕立骨化醇问世以来,已被证明在抑制甲状旁腺激素(PTH)分泌的同时可以较少激活肠道维生素D受体[3],从而一定程度避免肠道钙磷吸收及骨钙动员增加的问题[4],目前在临床使用越来越广泛。
文献报道帕立骨化醇起始剂量有两种方案,即欧洲方案,[根据iPTH(pg/ml)水平决定,iPTH/80]和美国方案(根据体重决定,0.04μg/kg)[5]。临床应用发现,欧洲方案虽然iPTH下降快,很显然起始剂量偏大,特别是iPTH相对较高患者,如患者iPTH>1 500 pg/ml时,可能所需起始剂量达0.31μg/kg(假设体重60 kg,远超最大推荐剂量0.24μg/kg),因此使用过程中患者可能出现较大幅度的血磷及血钙升高,甚至部分患者因此而需终止治疗,同时考虑到药物价格,此方案成本较大。而美国方案以0.04μg/kg为起始剂量,在临床应用中发现,多数患者需经过较长时间的不断增加剂量的过程[6],才可能达到有效控制iPTH,因此起效慢、剂量调整周期长是此方案的主要缺陷。而药物说明书推荐起始剂量则为一个较宽的范围值0.04~0.1μg/kg。因此选择何种起始剂量还需更多临床研究验证。本研究拟用小样本前瞻性观察研究,探讨以中等起始剂量(0.06~0.08μg/kg)帕立骨化醇治疗血液透析(HD)伴SHPT患者的有效性和安全性。
对象和方法
研究对象本研究为单中心、前瞻性、小样本研究,在南京军区南京总医院肾脏科血液净化中心入组11例患者,均签署知情同意书,研究方案得到南京军区南京总医院伦理委员会批准。
入选标准行HD>3个月,年龄为18~65周岁,iPTH>600 pg/ml者,服骨化三醇或含钙磷结合剂的患者经历2周的洗脱期。
排除标准既往接受过西那卡塞或帕立骨化醇治疗;对活性维生素D或相关药物过敏者;高钙血症(>2.6 mmol/L)或钙磷乘积>65 mg2/dl2;患者预期寿命<6个月;重度肝损伤、活动性炎症性疾病、确诊的恶性肿瘤;孕期、哺乳期女性或进入研究后6个月内计划怀孕的女性。当患者在以下情况时退出: (1)进行肾移植;(2)甲状旁腺切除术;(3)药物调整后仍出现明显的高钙血症(2.85 mmol/L)、钙磷乘积>75 mg2/dl2;(4)治疗过程中出现严重的或不能忍受的不良反应;(5)患者自愿退出。
观察指标主要疗效指标为治疗12周iPTH较基线水平下降>30%的患者例数;次要疗效指标包括:治疗12周iPTH下降率,iPTH降至正常范围(150~300 pg/ml)的患者例数,药物剂量变化,血钙、血磷、钙磷乘积变化及不良事件发生。
帕立骨化醇剂量调整研究药物的起始剂量为0.06~0.08μg/kg,最大剂量不超过0.24μg/kg,在血液透析结束前0.5h内给药,3次/周,每4周调整药物剂量,剂量调整见表1。
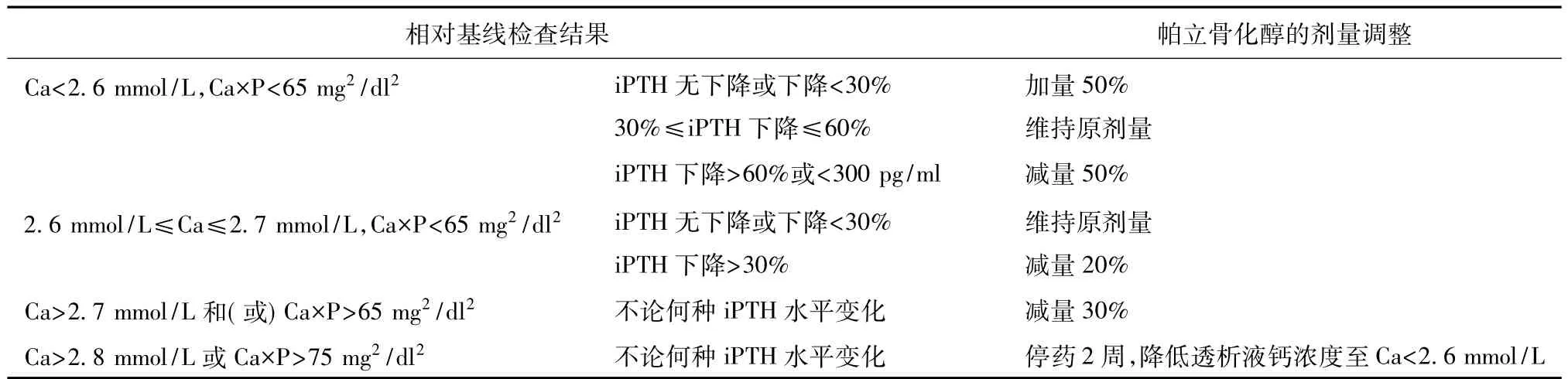
表1 帕立骨化醇用药调整方案
实验室检查指标血钙、血磷在随访期间每2周复查一次,iPTH、肝酶每4周复查1次,血常规,透析前血生化(胆红素、白蛋白、球蛋白、碱性磷酸酶、血糖、尿素氮、肌酐、尿酸、钾、钠、氯)在基线及治疗结束时复查。
统计方法应用SPSS19.0统计软件进行数据分析。正态分布计数资料以均数±标准差表示,偏态分布资料以中位数(四分位间距)表示,计数资料采用百分比描述,基线及随访结束时数据比较采用独立样本t检验,P<0.05为差异有统计学意义。
结果
患者基线特征本项研究共观察11例患者,其中男性8例,女性3例,平均年龄49.1±11.9岁,平均透析龄6.25±2.30年。有10例患者完成了研究,1例患者因行甲状旁腺切除术退出(表2)。
所有患者均采用高通量透析,3次/周,透析液钙浓度1.5 mmol/L,基线iPTH中位水平1 087.0 pg/ml(802.9~1 413.0 pg/ml),入组前分别有6例患者接受骨化三醇及碳酸钙治疗,最低值为626.9 pg/m l,最高值为3 341.0 pg/m l。除例4、例6及例10患者外,余患者均存在甲状旁腺增生。

表2 患者入组时基本信息
帕立骨化醇用药剂量iPTH<1 000 pg/m l的患者,帕立骨化醇起始剂量为0.06μg/kg有6例,0.08μg/kg有1例,4例iPTH>1 000 pg/m l的患者起始剂量为0.08μg/kg,3次/周,具体剂量调整参见表1。8例患者在随访中有不同程度的剂量增加,第12周时帕立骨化醇平均用量为0.11 μg/kg,其中1例患者(例3)药物剂量不断调整,iPTH无下降趋势,在第10周药物达到最大剂量;有6例患者在第8周时即达到治疗剂量而保持不变(图1A)。
慢性肾脏病矿物质与骨异常(CKD-MBD)相关指标变化
血清钙、磷的变化基线时血钙、磷平均水平分别为2.30±0.19 mmol/L、1.60±0.24 mmol/L。随访结束时,血钙升高幅度平均为8.6%,1例患者发生高钙血症(血钙=2.64mmol/L);血磷上升幅度平均为21.2%,血磷变化幅度较大的4例患者有2例用药初停磷结合剂,1例患者在第11周时帕立骨化醇加量。帕立骨化醇开始应用后,血钙、磷会有一个升高的趋势,但用药1个月后即使后续逐渐加大剂量,钙、磷变化趋于稳定(图1B~D)。
iPTH变化有8例(80%)患者在治疗12周后iPTH较基线下降>30%,iPTH在第4周、第8周较基线下降>30%的患者分别有3例、6例,有4例患者iPTH降至正常范围,11例患者平均iPTH下降率为48.6%±26.8%(16.8%~76.9%),首次iPTH下降>30%的平均时间为7周(图2)。
碱性磷酸酶变化患者治疗结束时碱性磷酸酶水平较基线明显下降[(186.7±284.7)U/L vs (330.1±403.2)U/L,P=0.017]。

图1 应用帕立骨化醇患者帕立骨化醇剂量(A)、血钙(B)、血磷(C)及钙磷乘积(D)随时间的变化
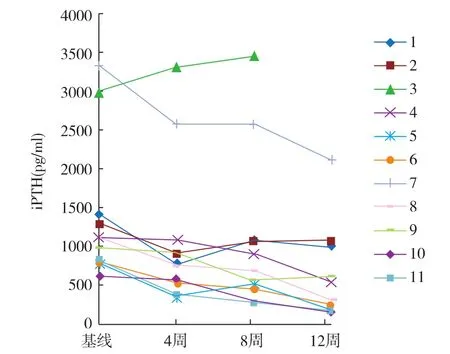
图2 应用帕立骨化醇患者iPTH随时间的变化
不良反应随访中所有患者血白细胞、血红蛋白、肝酶较治疗前无明显变化,有1例患者自用药开始出现双上肢轻度皮疹并伴瘙痒,持续至用药结束; 1例患者用药1月后左侧面部鼻翼侧出现约2 cm×2 cm硬结,无疼痛等不适,后硬结不断增大,且iPTH无下降趋势,患者退出行甲状旁腺切除手术。
讨论
帕立骨化醇治疗透析患者的SHPT的有效性已在很多临床试验中得到验证[7,8]。Ketteler等[9]研究发现,基线iPTH为540~630 pg/ml一组患者在应用帕立骨化醇第21~28周时,iPTH降至150~300 pg/ml的患者占57.7%;在唯一关于中国人群使用帕立骨化醇的报道中[6],根据欧洲方案药物剂量,最终iPTH下降>30%、达到KDIGO及K/DOQI标准的患者分别为88.6%、59.3%和17.6%,使用美国方案的患者达到以上标准的分别为59.0%、54.6%、19.4%。本研究11例患者的基线iPTH中位水平是1 087.0 pg/ml(802.9~1 413.0 pg/ml),iPTH下降>30%、且分别达到KDIGO及K/DOQI标准的患者有8例、6例、4例患者,效果与文献报道相当。有文献报道,达到主要观察目标后的维持治疗中,iPTH仍会有不同程度的下降[11,12],但本研究未再进一步观察长期维持剂量对iPTH的效果。
现有三种方案确定帕立骨化醇治疗起始剂量,除前文所述欧洲及美国方案外,药物说明书推荐方案为0.04~0.1μg/kg,因此临床面临如何选择起始剂量的问题。Martin等[5]的研究显示起始剂量为iPTH/80的一组患者达到主要观察终点的时间明显短于起始剂量为0.04μg/kg的患者,但前者的血钙、磷变化波动较大。对于iPTH水平轻~中度升高的患者而言,采用何种起始剂量差别可能并不大,但对于iPTH较高的患者,欧洲方案起始剂量过大,虽然起效快,但成本高,且治疗过程中相应高钙、高磷发生率高;而美国方案起始剂量过小,起效慢,药物剂量调整周期长,需监测相关指标的频次高,最终可能导致患者依从性差而难以坚持使用。通过本文小样本的观察性研究显示,采用中等起始剂量帕立骨化醇一定程度上可减少上述两种方案存在的问题。起始剂量为0.06~0.08μg/kg时,一般到第8周即可达稳定治疗剂量(平均治疗剂量0.11μg/kg),相对而言调整幅度并不大、调整周期并不长,即使对于4例iPTH>1 000 pg/m l的重度SHPT患者亦较快达到治疗效果。
此外,本研究发现,帕立骨化醇治疗对钙磷的影响在最初4周较明显,而后即使继续增加剂量,钙磷变化亦不明显。这一点提示,较大起始剂量易造成明显高钙及高磷,而以中等起始剂量治疗,则可能避免开始1个月内的这种明显高钙高磷作用,有助于减少不良反应。基于此,我们建议使用帕立骨化醇时如出现血钙、磷的升高可暂不予下调剂量,以待药物适应期后减弱对血钙及磷影响。
本文中在帕立骨化醇治疗前后患者碱性磷酸酶有不同程度的下降,这与既往的一些研究结果相似[15,16],帕立骨化醇可改变甚至纠正SHPT引起的骨组织形态学变化[17],可能是其在骨代谢方面的独特作用。碱性磷酸酶升高,是高iPTH引起破骨细胞和骨重吸收活性增加的体现,有研究认为高碱性磷酸酶与CKD患者的高心血管疾病发病率及死亡率有关[18],还与HD患者的全因死亡率升高有关[19]。本研究中有7例患者用药后骨痛或关节活动障碍症状明显好转,是否也与此有关有待进一步研究。
帕立骨化醇治疗HD伴SHPT患者的有效性已在很多临床试验中得到验证,在中国透析人群使用帕立骨化醇的较大样本的研究也已发表。该研究在药品用量的推荐范围内选择了一个中等剂量开始治疗,但是因观察病例仅11例,观察时间较短,所得研究结果需要扩大样本量和增加对照组以验证其可靠性。
1 Imanishi Y,Tahara H,Palanisamy N,et al.Clonal chromosomal defects in themolecular pathogenesis of refractory hyperparathyroidism of uremia.JAm Soc Nephrol,2002,13(6):1490-1498.
2 Brancaccio D,Bommer J,Coyne D.Vitamin D receptor activator selectivity in the treatment of secondary hyperparathyroidism: understanding the differences among therapies.Drugs,2007,67(14): 1981-1998.
3 Stein MS,Wark JD.An update on the therapeutic potential of vitamin D analogues.Expert Opin Investig Drugs,2003,12(5):825-840.
4 Brown AJ,Coyne DW.Vitamin D analogs:new therapeutic agents for secondary hyperparathyroidism.Treat Endocrinol,2002,1(5):313-327.
5 Martin KJ,González E,Lindberg JS,et al.Paricalcitol dosing according to body weightor severity of hyperparathyroidism:a doubleblind,multicenter,randomized study.AAm JKidney Dis,2001,38(5 Suppl 5):S57-63.
6 Yan Y,Qian J,Chen N,etal.Efficacy and initial dose determination of paricalcitol for treatment of secondary hyperparathyroidism in Chinese subjects.Clin Nephrol,2014,81(1):20-29.
7 Coyne DW,Andress DL,Amdahl MJ,et al.Effects of paricalcitol on calcium and phosphate metabolism and markers of bone health in patients with diabetic nephropathy:results of the VITAL study.Nephrol Dial Transplant,2013,28(9):2260-2268.
8 Martin KJ,González EA,Gellens M,et al.19-Nor-1-alpha-25-dihydroxyvitamin D2(Paricalcitol)safely and effectively reduces the levels of intact parathyroid hormone in patients on hemodialysis.JAm Soc Nephrol,1998,9(8):1427-1432.
9 Ketteler M,Martin KJ,Wolf M,et al.Paricalcitol versus cinacalcet plus low-dose vitamin D therapy for the treatment of secondary hyperparathyroidism in patients receiving haemodialysis:results of the IMPACT SHPT study.Nephrol Dial Transplant,2012,27(8): 3270-3278.
10 Sprague SM,Llach F,Amdahl M,et al.Paricalcitol versus calcitriol in the treatment of secondary hyperparathyroidism.Kidney Int,2003,63 (4):1483-1490.
11 Llach F,Yudd M.Paricalcitol in dialysis patients with calcitriolresistant secondary hyperparathyroidism.Am JKidney Dis,2001,38(5 Suppl 5):S45-50.
12 Lund RJ1,Andress DL,Amdahl M,et al.Differential effects of paricalcitol and calcitriol on intestinal calcium absorption in hemodialysis patients.Am JNephrol,2010,31(2):165-170.
13 Teng M,Wolf M,Lowrie E,et al.Survival of patients undergoing hemodialysis with paricalcitol or calcitriol therapy.N Engl J Med,2003,349(5):446-456.
14 Dobrez DG,Mathes A,Amdahl M,et al.Paricalcitol-treated patients experience improved hospitalization outcomes compared with calcitrioltreated patients in real-world clinical settings.Nephrol Dial Transplant,2004,19(5):1174-1181.
15 Jacome-Galarza CE,Lee SK,Lorenzo JA,et al.Parathyroid hormone regulates the distribution and osteoclastogenic potential of hematopoietic progenitors in the bone marrow.J Bone Miner Res,2011,26(6):1207-1216.
16 Kalantar-Zadeh K,Shah A,Duong U,et al.Kidney bone disease and mortality in CKD:revisiting the role of vitamin D,calcimimetics,alkaline phosphatase,and minerals.Kidney Int Suppl,2010,(117): S10-21.
17 Yamamoto N.Morphological analysis of bone dynamics and metabolic bone disease.Bone Histomorphometry in CKD-MBD(chronic kidney diseasemineral bone disorder).Clin Calcium,2011,21(4):589-592.
18 Fahrleitner-Pammer A,Herberth J,Browning SR,et al.Bone markers predict cardiovascular events in chronic kidney disease.JBone Miner Res,2008,23(11):1850-1858.
19 Kovesdy CP,Ureche V,Lu JL,et al.Outcome predictability of serum alkaline phosphatase in men with pre-dialysis CKD.Nephrol Dial Transplant,2010,25(9):3003-3011.
Treatment of secondary hyperparathyroidism in hemodilysis patients by paricalcitol
WANG Taina,XU Bin,JIA Fengyu,ZHANG Haitao,GONG Dehua,LIU Zhihong
National Clinical Research Center of Kidney Diseases,Jinling Hospital,Nanjing University School of Medicine,Nanjing 210016,China
LIU Zhihong(E-mail:zhihong--liu@hotmail.com);GONG Dehua(E-mail:gong_doctor@126.com)
Objective:To observe the efficacy and safety of paricalcitol in treatment of secondary hyperparathyroidism(SHPT)inmaintenance hemodialysis(MHD)patients atamedium initial dose of0.06~0.08μg/kg.
M ethodology:Eleven MHD patients(8 males and 3 females)were enrolled to receive intravenous injection of paricalcitol thrice weekly for treatment of SHPT,with inclusion criteria as follows:maintenance on HD>3 months,serum intact parathyroid hormone(iPTH)≥600 pg/ml,serum Ca(calcium)≤2.6mmol/L,and Ca×phosphorus(P)≤65mg2/dl2.During 12-weeks-follow-up,serum Ca and P were measured per 2 weeks and iPTH was measured per 4 weeks.Dose of paricalcitolwas adjusted according to themeasurements results.Results:The baseline levels of iPTH,Ca,and Pwere 1 087 (627~3 341)pg/ml,2.30±0.19 mmol/L,and 1.60±0.24 mmol/L,respectively.The initial dose was 0.06μg/kg in 6 patients and 0.08μg/kg in other 5 patients.The final average dosewas 0.11μg/kg at the end of follow-up,with 6 patients achieving dose adjustment reaching desired levelwithin 8 weeks.One patient dropped out due to skin lesion.The proportion of patientswith iPTH reduction by>30%and with iPTH reducing to 150~300 pg/mlwas 73%and 36.4%,respectively,with one patient experiencing hypercalciumemia.No other adverse events were observed.Conclusion:It seemed feasible to initiate paricalcitol treatment at amedium dose in SHPT hemodilysis patients,with few effect on serum Ca and P levels.
paricalcitol initial dose secondary hyperparathyroidism hemodialysis
2014-12-12
(本文编辑 莫非)
国家科技支撑课题(2013BAI09B04)
南京大学医学院附属金陵医院(南京军区南京总医院)肾脏科硕士研究生(王泰娜),国家肾脏疾病临床医学研究中心全军肾脏病研究所(南京,210016)
刘志红(E-mail:liuzhihong@nju.edu.cn);龚德华(E-mail:gong_doctor@126.com)
2015年版权归《肾脏病与透析肾移植杂志》编辑部所有
