环氧化季戊四醇油酸酯的合成
2015-06-09杨延雷司动磊刘福胜
杨延雷,司动磊,刘福胜
(青岛科技大学 化工学院,山东 青岛 266042)
环氧类增塑剂作为一种无毒、可生物降解的环保型增塑剂已成为国内外应用研究的热点[1]。目前环氧增塑剂的主要合成方法分为溶剂法和无溶剂法,其中无溶剂法由于其操作简单、工艺流程短、对环境污染小的特性已逐步取代了溶剂法作为企业生产的首选方法。无溶剂法按所用催化剂种类,可分为强酸催化和非强酸催化。强酸催化一般选择硫酸、磷酸、硝酸等为催化剂。其中以硫酸的催化效果较好、操作相对简单,是生产当中比较常用的方法。但是以硫酸作催化会造成设备腐蚀、三废排放量大、产品色泽较深等问题[2-3]。因此非强酸类的催化体系逐渐成为研究的热点。
非强酸催化剂方法主要包括甲酸自催化体系[4-5]、离子交换树脂催化、硫酸盐类催化等。甲酸自身可以解离出活泼H+,所以不加入其它催化剂甲酸体系就可以完成环氧化反应,但是毕竟甲酸酸性不高,其自催化反应时间较长且产品环氧值较低。于兵川等[6]利用阳离子交换树脂作为催化剂合成环氧大豆油,克服了硫酸催化的设备腐蚀和环境污染等问题,催化剂在活性降低后通过活化可重新使用,有效降低了成本。曹卫东[7]以硫酸铝作催化剂,合成了环氧大豆油。不过催化剂要严格控制Fe2+含量,Fe2+含量过高会催化双氧水分解,使反应温度难控制造成双氧水利用率较低。近几年也出现了一些不使用有机羧酸的催化体系。邓芳[8]等研究了在无羧酸条件下,以乙酸乙酯为溶剂,甲基三辛基硫酸氢铵为相转移催化剂,用过氧化氢作氧化剂直接将大豆油进行环氧化反应合成环氧大豆油环氧值可达6.4%。李坤兰、高爽[9]等使用一种磷钨杂多酸类反应控制相转移催化剂,以1,2-二氯乙烷作溶剂合成了环氧化大豆油,催化剂可重复使用,但催化剂的回收率约75%。相对于传统催化剂相转移催化剂的成本较高,所以此种方法离工业化生产还有一定的距离。
可以看出,离子交换树脂作为催化剂具有对设备腐蚀小、反应结束后易与产物分离、后处理简单、三废排放量少的特点[10-11]。采用离子交换树脂作催化剂对一种新型增塑剂环氧化季戊四醇油酸酯的合成工艺进行了研究,并取得了预期效果。
1 实验部分
1.1 试剂与仪器
季戊四醇油酸酯:工业品,聊城瑞捷化学有限公司;732#阳离子交换树脂:AR,国药集团化学试剂有限公司;甲酸:AR,天津市富宇精细化工有限公司;过氧化氢:CP,莱阳经济技术开发区精细化工厂;氢氧化钠:AR,天津博迪化工股份有限公司。
DW-3H数显电动搅拌器:郑州英峪予华仪器有限公司;DF-101s集热式恒温加热磁力搅拌器:郑州长城科工贸易有限公司;101-1A型电热鼓风干燥箱:天津市泰斯特仪器有限公司;SHB-Ⅲ循环水式多用真空泵:郑州长城科工贸有限公司。
1.2 实验方法
1.2.1 阳离子交换树脂的预处理
将一定量的树脂置于0.5 mol/L的盐酸溶液中浸泡12 h,其中盐酸溶液的体积约等于被处理树脂体积的2倍,然后放净盐酸溶液,用清水漂洗至中性;然后再用2倍于树脂体积的质量分数为4%~5%氢氧化钠溶液浸泡12 h,放净碱液后,用清水漂洗3~4次至排出水呈中性;最后再用2倍于树脂体积的0.5 mol/L的盐酸溶液浸泡12 h,然后以清水洗涤至排出的水呈中性,滤出树脂干燥后备用[6]。
1.2.2 环氧季戊四醇油酸酯的合成
向装备好搅拌器、温度计、滴液漏斗的烧瓶中按照预定的比例加入原料季戊四醇油酸酯、甲酸、催化剂在搅拌下逐渐升温至反应温度,随后将预定比例的过氧化氢滴加到反应烧瓶中,因为本反应为放热反应所以要严格控制滴加速度,防止滴加速度过快而引起温度骤升。过氧化氢滴加结束后保温反应一定的时间。
反应结束后将反应物过滤回收树脂,粗产品静置于分液漏斗中分离出下层水相,然后用温水洗涤油层,洗去残存的酸及双氧水,然后减压蒸馏除去低沸点杂质即得淡黄色透明的油状产品,随后测定产品的各项指标。
1.3 分析方法
(1) 环氧值:按GB 1677—81方法测定,即盐酸-丙酮法。
(2) 酸值:按按GB 11406—1989 方法测定。
(3) 碘值:按碘酊法测定。
2 结果与讨论
2.1 甲酸用量的影响
控制m(过氧化氢)∶m(季戊四醇油酸酯)=60%,m(催化剂)∶m(季戊四醇油酸酯)=3%,反应温度60 ℃,反应时间6 h,考察不同甲酸添加量对反应的影响,结果见图1。

m(甲酸)∶m(季戊四醇油酸酯)/%图1 甲酸添加量对产品环氧值和碘值的影响
从图1可以看出在m(甲酸)∶m(季戊四醇油酸酯)=10%~20%时产品的环氧值随着甲酸的添加量的增加而增长,碘值逐渐降低。环氧值在m(甲酸)∶m(季戊四醇油酸酯)=20%时取得最大值。随后,在m(甲酸)∶m(季戊四醇油酸酯)>20%后,虽然产品碘值仍在小幅下降,但是产品的环氧值则随着甲酸添加量的增加而减小。这是因为甲酸用量较少时,随着量的增加,生成过氧酸的速度加快,使环氧化反应速率加快,碘值下降,环氧值有所提高;而当甲酸用量过大时,由于反应中酸浓度过大,导致环氧基的开环副反应加剧,即便碘值降低产物的环氧值也不会升高。所以,最佳添加量m(甲酸)∶m(季戊四醇油酸酯)≈20%。
2.2 反应温度的影响
控制m(过氧化氢)∶m(季戊四醇油酸酯)=60%,m(甲酸)∶m(季戊四醇油酸酯)=20%,m(催化剂):m(季戊四醇油酸酯)=3%,反应时间6 h,考察了不同反应温度对反应的影响,其结果见图2。

t/℃图2 反应温度对产品环氧值和碘值的影响
从图2可以看出反应温度在50~60 ℃时,随着温度的升高产品的环氧值逐渐增高碘值逐渐下降,说明随着温度的升高,双键在不断转化为环氧基,在约60 ℃时环氧值达到最大值。而当温度高于60 ℃之后,随着温度的进一步增高,碘值基本不变,产品的环氧值反而会下降。这是因为环氧基开环温度为65 ℃。开始的时候温度的升高加快了反应速率,提高了环氧化的选择性,使环氧值提高;当温度过高超过65 ℃后,反应速率加快的同时,副反应增多,也使产物发生水解开环[12]。
2.3 催化剂用量的影响
控制反应温度为60 ℃,m(过氧化氢)∶m(季戊四醇油酸酯)=70%,m(甲酸)∶m(季戊四醇油酸酯)=20%,反应时间5 h,考察了不同催化剂添加量对反应的影响,结果见图3。

m(催化剂)∶m(季戊四醇油酸酯)/%图3 催化剂添加量对产品环氧值和碘值的影响
从图3可以看到m(催化剂)∶m(季戊四醇油酸酯)=3%~5%时,随着催化剂的增加产品的碘值快速下降,环氧值也会相应地提高,而当m(催化剂)∶m(季戊四醇油酸酯)>5%后,继续增加催化剂的添加量碘值虽然有所下降但是产品的环氧值不再升高反而会下降。这是因为当催化剂用量较少时,随着催化剂用量的增大,催化剂的活性点位增加,催化效果明显;不过当催化剂用量达到一定程度后,催化剂活性点位就会达到饱和,继续增大催化剂用量,反而使反应体系的酸介质增加,加快环氧大豆油的开环副反应速率,从而使环氧值降低。因此,从资金投入及催化效果两方面考虑,选择m(催化剂)∶m(季戊四醇油酸酯)=5%为宜。
2.4 过氧化氢添加量的影响
控制m(催化剂)∶m(季戊四醇油酸酯)=5%、m(甲酸)∶m(季戊四醇油酸酯)=20%、反应时间6 h考察了不同过氧化氢添加量对反应的影响,其结果见图4。
从图4可以看出:在m(过氧化氢)∶m(季戊四醇油酸酯)<70%时,随着过氧化氢量的增加,产品碘值急速下降,环氧值逐渐增大。不过当m(过氧化氢)∶m(季戊四醇油酸酯)>70%时,虽然碘值仍在下降但环氧值不再增加反而下降。这是因为过氧化氢用量较少时,随着过氧化氢用量的增加,使原料环氧化反应越来越充分,碘值不断降低使得环氧值提高;而当过氧化氢用量过大时,反应体系的水含量过大,过氧甲酸不稳定易分解,而且过多的水分也会使产物水解开环而生成了双羟基化合物等其他的副产物,环氧值降低[13]。因此,选择m(过氧化氢)∶m(季戊四醇油酸酯)=70%为宜。

m(过氧化氢)∶m(季戊四醇油酸酯)/%图4 过氧化氢添加量对产品环氧值和碘值的影响
2.5 反应时间的影响
控制m(过氧化氢)∶m(季戊四醇油酸酯)=70%、m(催化剂)∶m(季戊四醇油酸酯)=5%、m(甲酸)∶m(季戊四醇油酸酯)=20%、反应温度60 ℃考察了不同反应时间对反应的影响,其结果见图5。
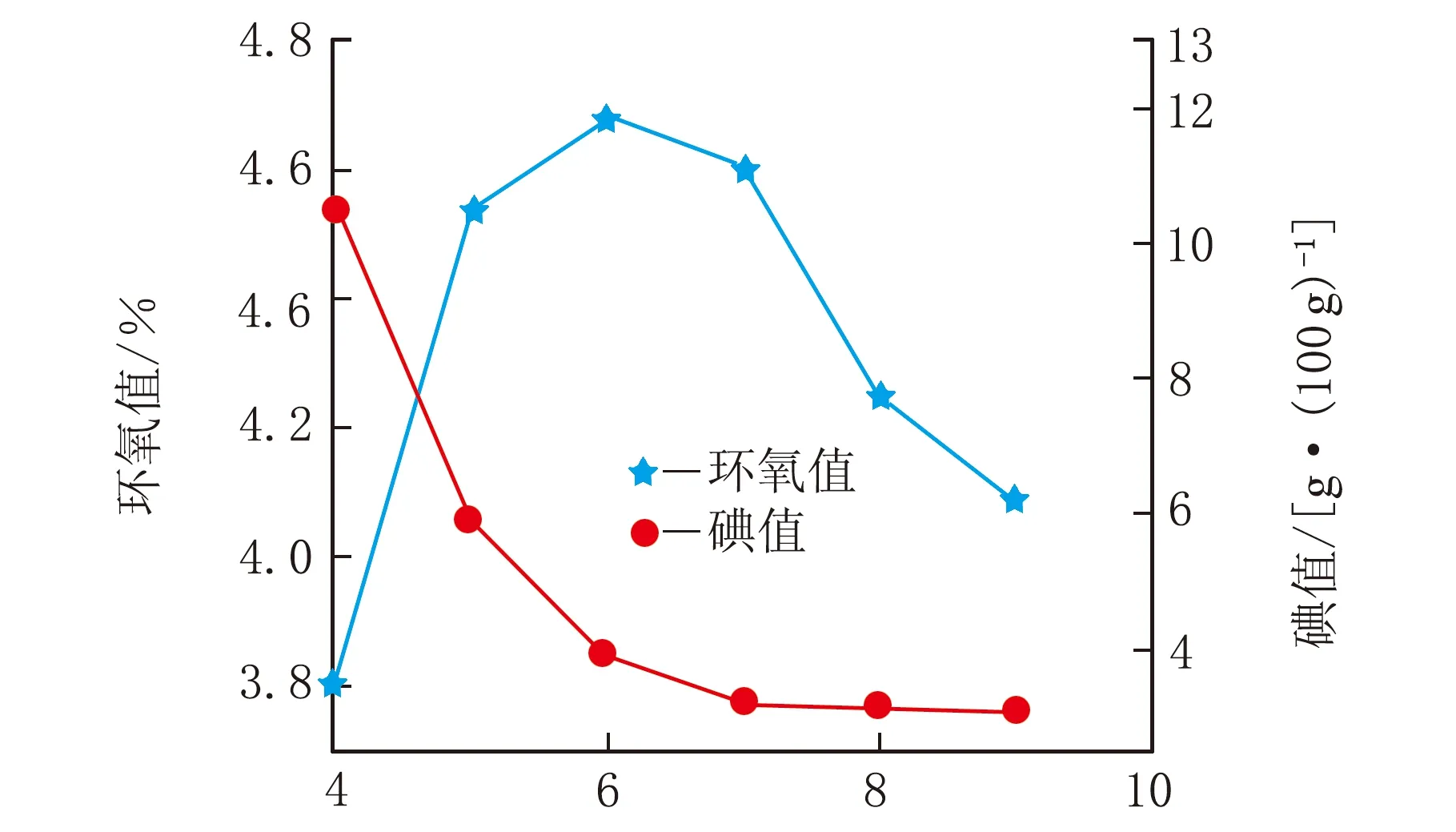
t/h图5 反应时间对产品环氧值和碘值的影响
从图5可以看出:在反应时间为4~6 h时随着反应时间的延长,碘值不断下降,环氧值不断升高,当反应时间超过6 h后,继续延长反应时间,产品的碘值会继续下降但环氧值不会继续增加而是开始下降。这是因为反应初期,原料反应不完全,随着反应时间的延长,越来越多的双键转化为环氧基环氧值增加;当反应时间超过6 h后,大豆油中的双键几乎完全环氧化,继续增加反应时间,只会使已经生成的环氧基再次开环造成环氧值的减少。因此,最佳的反应时间为6 h。
2.6 较佳条件下的重复实验
在上述实验过程得到的较佳条件下即m(季戊四醇油酸酯)∶m(甲酸)∶m(过氧化氢)∶m(离子交换树脂)=1∶20%∶70%∶5%时,60 ℃下反应6 h。进行重复实验检验实验的重现性,得到结果见表1。

表1 较佳工艺条件的重复试验
由表1可以看出本反应的较佳条件具有较好的重现性。
3 结 论
以阳离子交换树脂为催化剂,过氧化氢为氧化剂,制得了一种新型环氧类增塑剂环氧季戊四醇油酸酯。考察了催化剂用量、反应温度、过氧化氢用量、甲酸用量、反应时间等因素对季戊四醇油酸酯环氧化反应的影响,得到了较佳合成条件,当m(季戊四醇油酸酯)∶m(甲酸)∶m(过氧化氢)∶m(离子交换树脂)=1∶20%∶70%∶5%时,60 ℃下反应6 h制得环氧化季戊四醇油酸酯。其环氧值可达4.6%,碘值低于3 g/100 g。实验结果重复性较好。
[ 参 考 文 献 ]
[1] 邓斌,尚刚,纪振杰.环氧大豆油制备工艺研究[J].食品与机械,2011,27(2):98-100.
[2] 曹玮,马新启,曲波,等.环氧大豆油新工艺的研究[J].化工时刊,2002,16(2):49-51.
[3] 高广颖,张玉军,李靖靖,等.无溶剂法快速制备环氧大豆油的研究[J].化学工程师,2001,2(2):12-14.
[4] 施赛泉,蒋平平,史润萍.无硫酸环境环氧化大豆油合成条件优化[J].化工进展,2008,27(5):753-756.
[5] CAMPANELLA A,FONTANINI C,BALTANAS M A.High yield epoxidation of fatty acid methyl esters with performic acid generated in situ [J].Chemical Engineering Journal,2008,144(3):466-475.
[6] 于兵川,吴洪特,向罗京.改进型无溶剂法工艺合成环氧大豆油的研究[J].中国油脂,2005,30(4):42-44.
[7] 曹卫东.由硫酸铝催化合成环氧大豆油[J].辽宁化工,1994(5):36-37.
[8] 邓芳,魏俊发,石先莹.无羧酸条件下清洁合成环氧大豆油[J].石油化工,2006,35(3):281-283
[9] 李坤兰,高爽,奚祖威.反应控制相转移催化合成环氧大豆油[J].应用化学,2007,24(10):1177-1181
[10] GUENTERS,IETH R,OWBOTTOM K T.Ullmann,s encyclopedia of industrial chemistry [M].Berlin:John Wiley and Sons,2003:269-284.
[11] 吴广铎,宋向前,王萍.环氧大豆油合成工艺的研究[J].塑料助剂,2008(5):35-37.
[12] 彭元怀,韦禄菁,凌泳.阳离子树脂催化合成环氧化大豆油的研究[J].中国油脂,2012,37(3):63-65.
[13] 陈利峰,林铃,刘振华,等.对甲苯磺酸催化大豆油环氧化反应[J].石油化工,2011,40(9):978-981.
