全国首台投入临床使用的西门子顶级Prism a3.0T MRI落户深圳市龙岗中心医院
2015-06-01
全国首台投入临床使用的西门子顶级
Prism a3.0T MRI落户深圳市龙岗中心医院
深圳这座风景如画的滨海城市,改革开放的春风劲吹,胜利的喜讯连连。2015年10月西门子顶级科研型的Prisma3.0T MRI在深圳市龙岗中心医院投入临床使用。深圳市龙岗中心医院是深圳市东部地区最大的一所综合性三级甲等医院,该院在医疗改革过程中不断提高医疗质量和服务质量,以患者满意为办院宗旨。在提高医疗质量的过程中高度重视人才培养和学科建设,以国家博士后科研工作站为抓手推动医院医疗、教学、科研全面发展。该院是多家院校的硕士研究生培养基地、广州中医药大学博士研究生培养基地、深圳市博士后创新实践基地、国家博士后科研工作站。该院医学影像科已培养了38名研究生,现有在站博士后3名、在读博士研究生1名、硕士研究生5名,《视觉刺激脑温度改变与药物依赖者心理渴求程度的相关性研究》是深圳市唯一获得国家自然基金项目的放射影像学科。为满足临床和博士后科研工作站及学科发展的需要配置了这款西门子顶级科研型Prisma3.0T MRI。

Prisma3.0T MR I
具备FDA的“7T”磁共振
为了弥补以往3T与7T科研平台的巨大差距,西门子推出业界顶级科研型3T磁共振Prisma,具备与7T相同的射频发射TrueShape雕刻平台,可以提供未来无限的开发潜能;具备超越7T的人类连接组学(Human Connectome Project,HCP)梯度;具备超越7T的射频接收平台DirectRF+Tim4G;具备与7T相当的极致均匀磁体和与7T相同的完善的科研合作网络。自2013年获得FDA配准以来,迅速被全球近百家顶尖科研院所预定,国内的北京大学、北京师范大学、神经外科研究所和中科院生物物理研究所是它在中国的首批装机用户,它在科研方面的潜力毫不逊色于7T,临床应用前景和研发领域甚至超过7T,因此我们称Prisma为具备FDA的“7T”磁共振。
唯一可用于HCP研究的产品化磁共振
以往3T磁共振的梯度场强和梯度切换率都保持在50 mT/m和200 T/m/s以下,而HCP则要求梯度场强达到100 mT/m、200 mT/m甚至300 mT/m同时梯度切换率保持在200 T/m/s,因为更高的梯度场强和更高的B值可以显示更多的交叉纤维束。针对HCP的要求,西门子是唯一一家NIH认可的供货商,所有用于HCP研究的数据只有在Prisma和两台经过梯度升级的Skyra上完成才有效。Prisma通过以下途径同时实现最大梯度场强80和最大梯度切换率200:
(1)采用专利放大器技术,保证快速的梯度切换和高幅度脉冲。
(2)采用特殊传导材料结合三轴并行水冷,保证长时间扫描最高的梯度稳定性。
(3)利用超强梯度控制实时调整梯度的施加和切换,保证梯度更加精确有效。正是因为这些先进技术,Prisma成为唯一可用于HCP研究的产品化磁共振,也是唯一一款可以实现最大梯度场强80和最大梯度切换率200同时达到的产品化磁共振。
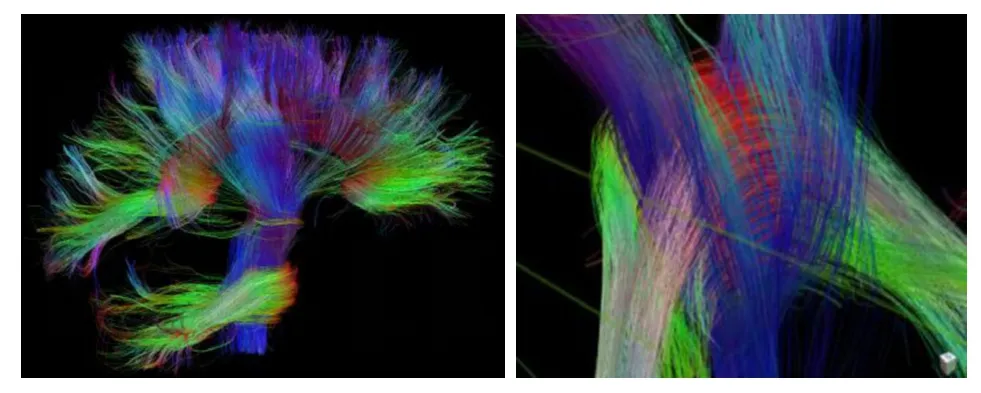
HCP梯度与常规梯度相比,TE时间缩短,SNR更高,图像变形和模糊效应减少,可实现512个方向的弥散谱成像DSI
7T TrueShape“雕刻”射频科研平台
相对于多通道射频接收技术的发展,TrueShape射频并行发射技术是对射频发射平台的一大革命。射频发射体线圈和两个独立射频源整合于Tim4G DirectRF架构,直接内置于磁体旁。两个独立的并行发射源射频脉冲独立调节,与x/y/z三组梯度线圈任意梯度波形同步,相互配合,可以实现任意形状的激发,犹如立体雕刻技术,打破以往传统非并行发射磁共振只能激发一层或一厚块的射频激发模式,从而带来磁共振应用的革命,为我们带来无限拓展的科研平台,如选择性动脉自旋标记、曲面饱和带、任意形状激励雕刻成像等。
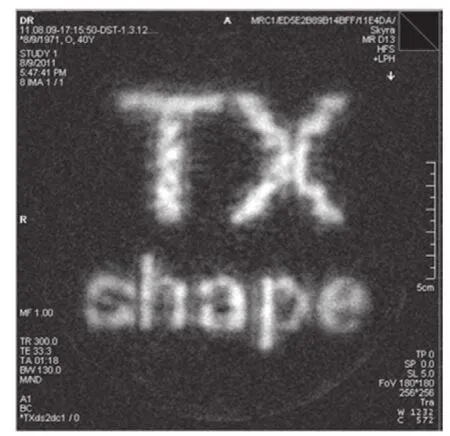
传统非并行发射射频系统

并行发射射频系统(ZOOMit)
TrueShape雕刻技术使得2DRF序列的成像质量得到大幅提升,速度加快,序列实现也更加轻松(ZOOM it)。与传统的射频系统相比,ZOOM it的临床优势在于:
(1)更高的图像质量:对于放大的视野,可以采用更少的回波链达到相同的空间分辨率,减少变形和模糊效应,尤其适用于DWI EPI、fMRI EPI或者HASTE序列。视野外的区域如运动器官或搏动血管不被激发,可以减少对信号的影响,减少伪影的发生。在感兴趣区,只有部分视野需要进行相位编码,在相同时间内可以获得更高的空间分辨率。
(2)更快的速度:对于被放大的视野,虽然相位编码线减少但可以获得相同的空间分辨率,与传统SPACE序列图像相比,可缩短大约三分之一的时间。
超越7T业界最高64接收平台+D irectRF+Tim 4G神经功能学专用线圈
Prisma采用第三代射频技术全内置射频,实现了全数字化成像链,射频发射组件和射频接收组件均内置于磁体。射频发射和射频接收路径均实现数字化,抗干扰能力更强,且邻近射频发射体线圈,大大减少了射频能量在传输过程中的损失和信号的衰减。动态调整射频场的稳定性和精确触发,射频的时间稳定性显著提升,对脑功能成像、精准的灌注采集和分析等高端应用提供了最先进的科研平台。
Prisma具备业内最高的64个独立的射频接收通道,是目前其他公司3T磁共振的两倍,甚至超越7T,极大地加快了成像速度。Prisma还配备了与之相匹配的64通道Tim4G神经功能学专用线圈,真正实现更高的系统接收通道所带来的应用优势,以满足认知和脑功能等高端科研和临床研究的需要。与20通道线圈相比,64通道神经功能学专用线圈总体信噪比提高52%,外周信噪比提升92%,对于BOLD脑功能成像、神经系统波谱成像、弥散张量成像等的功能性研究具有重要的意义。

Dot智多星平台是西门子在磁共振扫描和检查效率方面的里程碑,其在简化磁共振成像的同时为科研提供一致性和可重复性的结果。通过Tim 4G+Dot能够根据病人状态或临床情况实现一致性、可重复性、高质量检查结果,从而减少20%的检查时间和重复扫描的次数,日检查量提高50%,带来磁共振检查全方位的真正的灵活性、一致性和高效性。
与7T相当的极致均匀磁体
西门子创新的靶向匀场技术致力于改善动态主磁场的均匀性,从而进一步实现了3T应用的里程碑。靶向匀场技术是基于集成在梯度线圈中的额外5个匀场通道和32组匀场线圈,通过全新的匀场序列极大地提高了静态和患者进入磁体腔后的动态磁场均匀度。
Prisma作为顶级科研型3T磁共振,不仅采用最先进的磁体技术以及零液氮消耗技术,同时具有业内最佳的静态磁场均匀度和动态磁场均匀度,甚至优于目前7T磁场均匀度。与当前主流厂商全线3T相比,Prisma静态磁场均匀度领先其他主流厂商全线3T产品2~40倍,动态磁场均匀度领先其他主流厂商全线3T产品3~20倍。经过检测,Prisma磁场均匀性为40 cm DSV~0.2 ppm,其成像视野为50 cm×50 cm×50 cm。

传统匀场系统TrueFisp序列伪影严重,无法用于诊断

智多星靶向匀场TrueFisp序列成为常规,没有伪影
与7T相同的完善的全球科研网络
目前Prisma的全球订单已超过60台,且第一批装机用户全部为顶尖科研院所。西门子是全球医疗领域最大的设备供应商之一,平均每个工作日产生三项专利,目前,有超过70%的3T科研论文均来自西门子磁共振。同时,西门子拥有大量高级用户及研发合作伙伴,美国50%以上的大学医院使用西门子的磁共振,而欧洲的比例更高。在亚太地区,西门子医疗系统集团投资3000万元进一步扩大在华投资,建立西门子(亚洲)磁共振研发生产基地。国内一流的科研用户中西门子占有绝对的市场占有率(达到66.6%),并且还在不断地扩大。
西门子顶级科研型Prisma3.0T MRI在深圳市龙岗中心医院投入使用,这是深圳市龙岗区广大患者的福音,使该院医学影像科的医疗、教学、科研增添新的动力,让深圳市龙岗中心医院博士后科研工作站增光添彩,为推动深圳市龙岗中心医院的医疗、教学、科研快速健康发展做出新贡献。
政策法规
食品药品监管总局发布医疗器械使用质量监督管理办法
2015年10月21日,国家食品药品监督管理总局发布《医疗器械使用质量监督管理办法》(以下简称《办法》)。《办法》共六章35条,将于2016年2月1日起施行。
使用环节的医疗器械质量对确保用械安全有效至关重要。《办法》针对当前医疗器械使用单位采购渠道不规范、进货查验不落实、维护保养不严格、质量管理不完善等问题,对《医疗器械监督管理条例》规定的进货查验、信息记录、贮存运输、质量检查、维护保养等使用环节质量管理义务作了细化和补充完善。
《办法》明确了医疗器械采购、验收、贮存、使用、维护、转让等与使用质量密切相关的各个环节的管理规定,要求医疗器械使用单位建立覆盖质量管理全过程的医疗器械使用管理制度,并每年对质量管理工作进行全面自查。一是严格质量查验管理要求。规定使用单位要对医疗器械采购实行统一管理,严格查验供货商资质和产品证明文件,妥善保存相关记录和资料,并建立医疗器械使用前质量检查制度。二是加强维护维修管理。针对实践中存在的突出问题,详细规定了使用单位自行维护维修、委托维修服务机构维护维修、约定生产经营企业维护维修等不同情形的管理要求,明确规定在使用单位自行维护维修或者委托维修服务机构维护维修时,生产经营企业应当严格按照合同约定,提供维护手册、故障代码表、维修密码等维护维修必需的材料和信息。三是完善在用医疗器械转让和捐赠管理。规定使用单位转让医疗器械应当确保所转让的医疗器械安全、有效,及时移交说明书、维修记录等资料,受让方应当参照相关要求进行进货查验。针对越来越多的医疗器械捐赠行为,《办法》对捐赠方和受赠方均提出了要求,并规定使用单位之间的捐赠参照转让管理。四是强化分类监管和信用监管。强调依风险实施监管的原则,对较高风险或者有特殊储运要求的医疗器械,以及有不良信用记录的医疗器械使用单位等实施重点监管。
《办法》的出台进一步丰富了《医疗器械监督管理条例》配套规章体系,对加强医疗器械监督管理,保障用械安全具有重要意义。
食品药品监管总局发布关于规范含银盐医疗器械注册管理有关事宜的公告
为解决含银盐(如硝酸银、磺胺嘧啶银等)医疗器械注册管理的有关问题,进一步规范申报和审批程序,食品药品监管总局11月9日发布了《关于规范含银 盐医疗器械注册管理有关事宜的公告》(2015年第225号),对于含有硝酸银、磺胺嘧啶银等银盐的产品,明确了相关管理属性、注册申请受理、审批和过渡期要求。
一是若产品主要通过银盐的抗菌作用实现其预期用途,如含有银盐的溶液、凝胶等,不作为医疗器械管理;若产品所含的银盐仅为复合在医疗器械上增加抗菌功能,抗菌为辅助作用,如含银盐涂层的导尿管、含银盐敷料等,按照第三类医疗器械管理。
二是自公告发布之日起,按照上述管理属性和类别受理含银盐产品的医疗器械注册申请。
三是已经按照医疗器械受理的注册申请,继续按照医疗器械进行审评审批,准予注册的,发给医疗器械注册证。其中,所含的银盐以游离或释放的方式发挥作用的溶液、凝胶等产品,限定其注册证书的有效截止日期为2018年12月31日。
四是已获得医疗器械注册证的产品,其中属于所含的银盐以游离或释放的方式发挥作用的溶液、凝胶等产品的,原医疗器械注册证在证书有效期内继续有效;所涉及企业应按照相应管理属性和类别的有关要求积极开展转换工作,在2018年12月31日之前完成转换。开展转换工作期间注册证书到期的,如产品上市后未发生严重不良事件和质量事故的,企业可按照原管理属性和类别向原审批部门提出延期申请,予以延期的,原医疗器械注册证书有效期不得超过2018年12月31 日。
来源:CFDA网站
CFDA医疗器械召回公告
Medtronic Navigation Inc.对脊柱和创伤手术导航系统(商品名:Stealthstation)进行召回
美敦力(上海)管理有限公司报告,该公司代理的脊柱和创伤手术导航系统(商品名:Stealthstation)[注册证号:国食药监械(进)字2013第3543992号],由于以上产品的Solera改锥存在头端断裂、弯曲或损伤的投诉,其生产商Medtronic Navigation Inc.对该产品进行主动召回。该公司称本次召回产品未在中国销售。请各省、自治区、直辖市食品药品监督管理局加强对此类产品的监督管理。
来源:CFDA网站
