黄蜀葵花总黄酮定量研究
2015-05-30钱芳张芹
钱芳 张芹
【摘要】目的:用高效液相色谱法测定黄蜀葵花总黄酮中金丝桃苷的含量。方法:色谱柱:依利特-C-18-柱(250×4.6 mm,5μm),以乙腈-0.1%磷酸溶液为流动相进行梯度洗脱,流速:1.0ml/min,检测波长:360nm,柱温:30℃。结果:金丝桃苷在11.4059~364.99μg/ml范围内与峰面积的积分值呈现良好的线性关系(r=1.0000),平均加样回收率97.14%,RSD1.86%(n=6)。结论:HPLC法简便易行、结果准确、重复性好,可用于测定黄蜀葵花总黄酮中金丝桃苷含量。
【关键词】黄蜀葵花总黄酮;HPLC法;金丝桃苷
【中图分类号】R284.1 【文献标志码】A 【文章编号】1007-8517(2015)23-0014-02
黄蜀葵花为锦葵科秋葵属黄蜀葵(Abelmoschus manihot L·Medic)的干燥花。黄蜀葵花含丰富的黄酮类化合物,可用于治疗缺血性心脏病和缺血性脑血管病。黄蜀葵花总黄酮对缺氧损伤、急性心肌缺血具保护作用,并对不完全缺血性脑损伤有一定的保护作用[1-4]。有研究表明,主要由金丝桃苷为主的黄酮醇苷及其苷元组成黄酮类成分[5]。文献[6-8]报道的金丝桃苷的含量测定方法多为等度HPLC法,对于黄蜀葵花中金丝桃苷的有效分离检测不易实现。本试验将梯度HPLC法用于测定黄蜀葵花总黄酮中金丝桃苷的含量。
1 仪器与试药
1.1 仪器 高效液相色谱仪:Agilent1100,G1322A脱气机,G1311A四元泵,G1316A柱温箱,G1314A VWD检测器,Agilent ChemStation,美国安捷伦公司;1/10万电子分析天平:BP-211D型,德国Sartorius;超声波清洗器:KQ-1000E,江苏昆山超声仪器公司;电热鼓风干燥箱:101-1A型,江苏南通市沪通制药机械设备公司;数显型恒温水浴锅:HH-4,江苏金坛荣华仪器公司。
1.2 试药 金丝桃苷对照品(批号111521-201205),中国药品生物制品检定所购买,含量测定用; 黄蜀葵花总黄酮(批号141009、141010、141011),本实验室制备;液相色谱所用试剂:色谱纯;水:超纯水;其它试剂:分析纯。
2 方法与结果
2.1 色谱条件 色谱柱:依利特C-18-柱(250×4.6mm,5μm);流动相:乙腈-0.1%磷酸溶液,进行梯度洗脱:0~35min(16∶84),35~37min(30∶70), 37~53min(30∶70),53~55min(16∶84),55~60min(16∶84);检测波长:360nm;柱温:30℃;流速:1.0 ml/min;进样量10μl。
2.2 溶液制备
2.2.1 对照品溶液的制备 取金丝桃苷对照品,精密称定,甲醇溶解制成1ml含729.98μg的溶液。
2.2.2 供试品溶液的制备 精密称取黄蜀葵花总黄酮100mg,置于25ml量瓶中,加入甲醇,超声30min,放冷,再加甲醇至刻度,摇匀,滤过,取续滤液,即得。
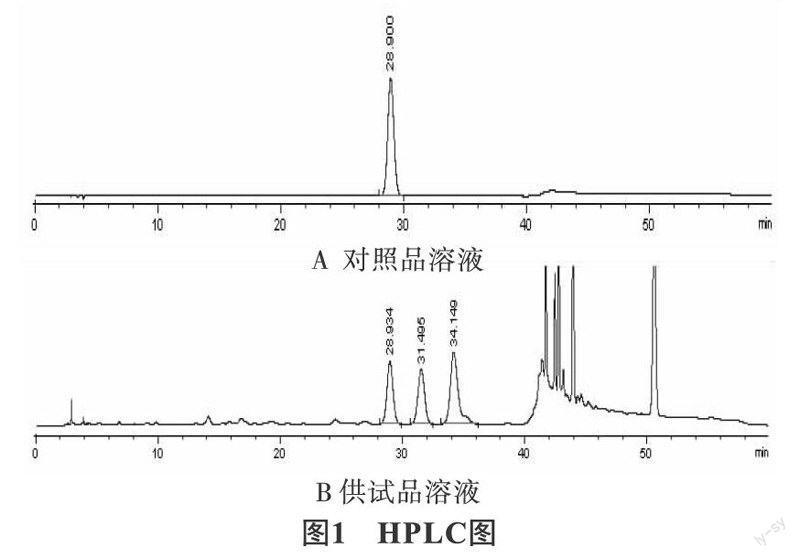
2.3 系统适应性试验 取供试品溶液、对照品溶液,进样10 μl,在上述液相色谱梯度洗脱条件下,液相色谱图中,金丝桃苷达基线分离,理论板数按金丝桃苷计在10000以上,分离度大于2.0。(见图1)
2.4 线性关系考察 取上述对照品溶液,用甲醇分别稀释至364.99、182.495、91.2475、45.6238、22.8119、11.4059μg/ml,在高效液相色谱仪中,注入不同浓度的对照品溶液10μl,测定。经线性回归,得金丝桃苷回归方程y=21.93x+27.36,r=1.0000,金丝桃苷在11.4059~364.99μg/ml范围内,同峰面积的积分值呈良好线性关系。
2.5 精密度试验 同一对照品溶液,精密吸取10μl后,注入液相色谱仪,重复测定6次,以峰面积计算,RSD为0.58%(n=6)。
2.6 稳定性试验 同一供试品溶液,于0、2、4、6、8、12h进样,测定峰面积,RSD为0.84%(n=6),结果表明:供试品溶液12h内稳定。
2.7 重复性试验 取同一批号(141009)的黄蜀葵花总黄酮,约100mg,共6份,精密称定,依法制备供试品溶液,测定,以金丝桃苷含量计算,RSD为1.21%(n=6)。结果表明,重复性较好。
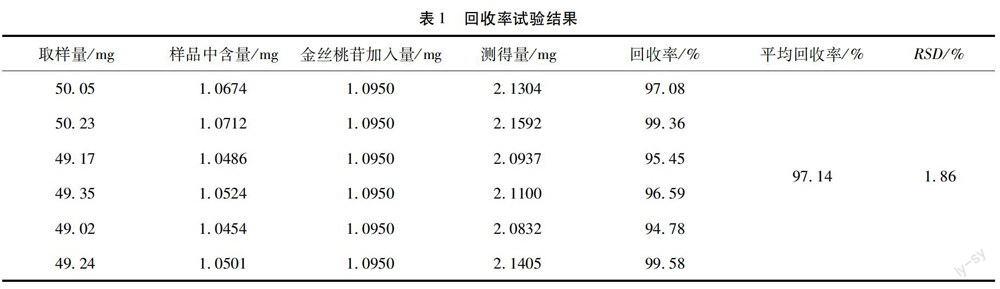
2.8 加样回收率试验 根据加样回收率试验的要求,取已知含量的黄蜀葵花总黄酮(141009)约50mg,共6份,精密称定后,加入金丝桃苷对照品,依法制备供试品溶液,液相色谱仪中注入精密吸取的10μl,测定,计算,平均回收率为97.14%,RSD为1.86%。
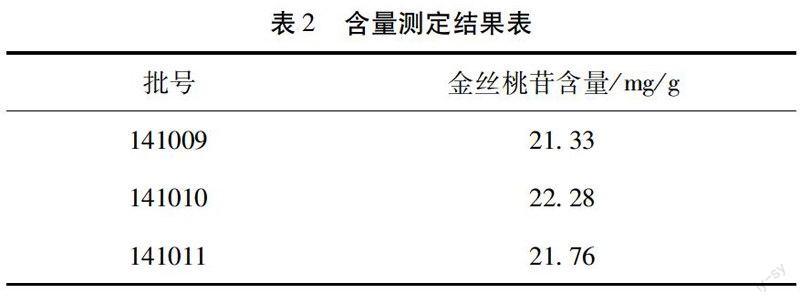
2.9 样品含量测定 取3批黄蜀葵花总黄酮,每批2份,根据上述方法,制备供试品溶液,进样,测定,计算结果如下。见表2。
3 讨论
试验中曾参考药典[9] :以乙腈-0.1%磷酸溶液(15∶85)为流动相,结果分离效果不好,又尝试乙腈-0.1%磷酸溶液,不同比例等度洗脱系统,金丝桃苷未能有效分离,且分析时间过长。通过反复试验,最后以乙腈-0.1%磷酸溶液,梯度洗脱:0~35min(16∶84),35~37min(30∶70), 37~53min-(30∶70)-,53~55min(16∶84),55~60min(16∶84),实现了较好的分离效果。
HPLC法测定黄蜀葵花总黄酮中金丝桃苷含量简便易行、结果准确、重现性好,可用于其质量控制。
参考文献
[1]李春梅,安雅婷,王涛,等.中药黄蜀葵花化学成分的分离与鉴定(Ⅲ)[J].沈阳药科大学学报,2011,28(7):520-525.
[2]范丽,郭岩,陈志武,等.黄蜀葵花总黄酮预处理对家兔心肌缺血再灌注损伤的影响[J].中国药理学通报,2006,22(1):106-109.
[3]李庆林,王成永,彭代银,等.黄蜀葵花总黄酮对心肌缺血再灌注损伤的保护作用研究[J].中国实验方剂学杂志,2006,12(2):39-42.
[4]刘爽,江蔚新,吴斌.黄蜀葵化学成分及药理活性研究进展[J].中国现代中药,2010,12(8):5-9.
[5]赖先银,赵玉英,梁鸿.黄蜀葵花化学成分的研究[J]. 中国中药杂志,2006,31(19):1597-1600.
[6] 田元春,刘倩,韦水林,等. HPLC测定参杞强精胶囊中金丝桃苷含量[J]. 中国实验方剂学杂志,2013,19(14): 149-151.
[7] 韩霖,刘妍如,杨建云,等. 贯叶连翘提取物中金丝桃苷含量的RP-HPLC法测定[J]. 时珍国医国药,2012,23(10):2432-2434.
[8] 杨海丽.HPLC法测定加味水陆丸中金丝桃苷的含量[J].中医药导报, 2014,20(3):72-73.
[9] 国家药典委员会.中华人民共和国药典一部[M].北京:中国医药科技出版社,2010:287.
(收稿日期:2015.09.08)
