式构型铂配合物抗癌药物的探讨
2015-05-30关蒙恩
摘 要:人们一直认为反式构型铂配合物无抗癌活性.但是,近来研究发现,一些反式构型的铂配合物显示了良好的抗癌活性.本文综述了这些配合物的结构、活性以及抗癌机理.
关键词:铂配合物;胞毒性;平面配位体;抗癌活性
一、反式构型铂配合物的抗癌活性
1.平面配位体反式构型Pt(Ⅱ)配合物
此类配合物的通式为trans-〔PtCl2(L)(L′)〕,其中离去基团L和L′至少有一个是平面配位体,它有三种基本类型:1)L=L′=吡啶、N-甲基咪唑(N-MeIm)或噻唑(Tz);2)L=喹啉(quin)、L′=R′R″SO(R′=Me,R″=Me,CH2Ph或Ph);3)L=喹啉(quin),L′=NH3.
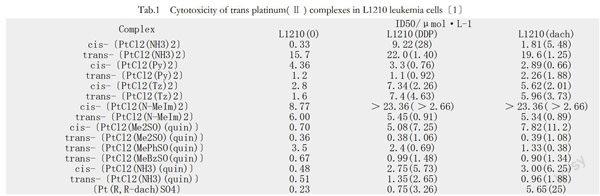
从表1可见,大多数具有平面配位体的反式铂配合物都有抗癌活性,而且,细胞毒性比相应的顺式配合物要高。某些含喹啉配位体的反式铂配合物其ID50值已经大体与顺铂相当。可见,用喹啉取代trans-〔PtCl2(NH3)2〕中的一个NH3分子使化合物的性质发生了极为重要的变化。
在〔PtCl2(R′R″SO)(quin)〕系列配合物中抗癌活性的大小依R′R″SO的性质而定,含有较惰性的亚砜配位体的配合物是胞毒性最大的化合物,如trans-〔PtCl2(Me2SO)(quin)〕和trans-〔PtCl2(MeBzSO)(quin)〕的胞毒性与顺铂相当。这可能与亚砜作为一种惰性配位体存在有利于键的稳定有关。有趣的是,在trans-〔PtCl(R′R″SO)(diamine)〕+系列中,含较不稳定的亚砜配位体的配合物具有最高的抗肿瘤活性。可见,即使是同类配位体,在不同类型的配合物中所起的作用也是截然不同的。
从表1中的L1210/DDP的数值可以看出,所有的配合物都具有明显较低的抗药因子。有一些配合物的ID50值与相应的细胞敏感性数值相当。因此,体积较大的平面配位体的反式配合物的一般特征是此类配合物与顺铂无交叉抗药性,即反式配合物对抗顺铂细胞有活性。类似地,反式配合物与〔Pt(R,R-dach)SO4〕也是非交叉抗药性的。这提示反式铂配合物可以與顺铂或〔Pt(R,R-dach)SO4〕联合用药。反式喹啉配位体Pt(Ⅱ)配合物氧化为相应的Pt(Ⅳ)配合物时,也显示了比较好的体内抗癌活性。
2.亚胺基醚为配位体的反式铂(Ⅱ)配合物
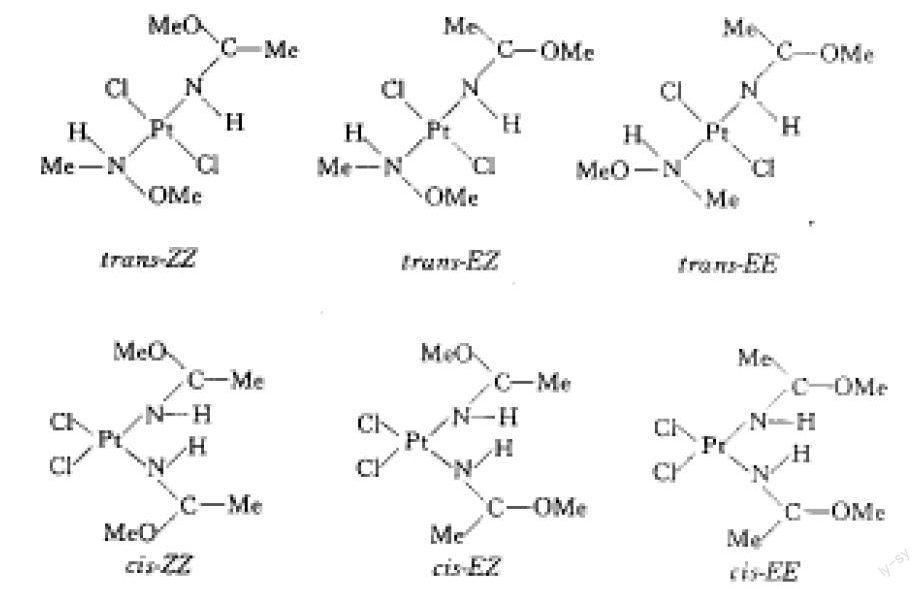
此类配合物的通式为式中R=烷基或苯基,R′=烷基.此类配合物实际上是〔PtCl2(NH3)2〕中的NH3被亚胺基醚取代的产物.从几何异构来看,除了有顺反式外,由于CN键的存在,还可形成E和Z构型,并且可以产生顺式和反式三种不同的几何异构即trans-ZZ,trans-EE,trans-EZ和cis-ZZ,cis-EE,cis-EZ.化合物结构见图1。
Resistance factor,defined as ID50(resistance)/ID50(senitive),is given in parentheses.
3.混胺配位体反式铂配合物
此类配合物一般有两类:trans-〔PtCl2(NH3)(RNH2)〕和trans-〔PtCl2(OH)2(NH3)(RNH2)〕.Loyd R.Kelland等〔3〕合成了41种反式配合物,发现,反式Pt(Ⅳ)的二羟基配合物即trans-〔PtCl2(OH)2(NH3)(RNH2)〕的抗癌活性一般而言要比其相应的Pt(Ⅱ)配合物高。但是,并不是所有的反式Pt(Ⅳ)配合物都有活性,当其中R为脂肪烃、脂环烃、芳环或杂环化合物时,配合物显示较好的抗癌活性。而当R为短脂肪链、吗啉、吡啶、喹啉等环时,配合物没有活性。此外,这些反式配合物对三种抗顺铂的细胞系显示了相似的反应模式:对41McisR与顺铂无交叉抗药性,对CH1cisR与顺铂有部分交叉抗药性,对A2780cisR与顺铂有部分或较高的交叉抗药性。
二、反式铂配合物的抗癌机理研究
M.V.Beusiche等〔1〕认为反式铂配合物的抗癌机理与顺铂是不同的,对抗顺铂细胞胞毒性的持久度及用NCI比较程序独立分析支持这种观点。影响胞毒性和细胞内抗顺铂的原因包括摄取变化、内源硫醇如谷胱苷肽和金属硫酮的活性和DNA修复率变化。这些因素都受结构变化的影响,反式铂配合物中,这种结构变化是以trans-〔PtCl2(NH3)2〕为基本结构进行的。A.Eastman等〔4〕通过测定含有标记胸苷的trans-〔PtCl2(Py)2〕发现,这种化合物抑制了分子内DNA的合成。因此,反式铂配合物的抗癌机理也呈现在DNA的键合上。值得注意的是,有一些反式铂配合物不能提供氢键的配位体,而迄今为止分子中存在能提供氢键的配位体被认为是化合物与DNA键合以及具有抗癌活性的必要特征。trans-〔PtCl2(NH3)2〕的键区专一性在—GC—位置增加键合与顺铂有点不同〔5,6〕。平面配位体的存在可能强调了这种差异对随后生成的加合物的结构和构型变化的影响.M.Kharatishvili等〔8〕证实了喹啉作为平面配位体对trans-〔PtCl2(NH3)(quin)〕与DNA的键合是有影响的。
三、结论
trans-EE有抗癌活性的原因也是它抑制了DNA的合成.此外,亚胺基醚铂配合物的抗癌机理也涉及到增加的摄取或与细胞内硫醇不同的反应性。
反式混胺铂配合物是一类值得注意的化合物,尤其是其Pt(Ⅳ)配合物,它可能是一类极有发展前途的新型抗癌药物。目前,对反式异构铂配合物的抗肿瘤机理的研究十分有限,对反式铂配合物的构效关系也不完全清楚。研究并揭示铂配合物的抗癌机理对寻找新的更为有效、毒副作用更小的抗癌药物具有重要意义。
参考文献:
[1]Beusichem MV,Farrell N.Activation of the trans geometry in platinum antitumor complexes.Synthesis,characterization,and biological activity of complexes with the planar ligands pyridine,N-methylimidazole,thiazole,and quinoline,crystal and molecular structure of trans-dichlorobis(thiazole)platinum(Ⅱ).Inorg Chem,1992,31:634~639.
[2]Coluccia M,Nassi A,Loseto F,et al.A trans-platinum complex showing higher antitumor activity than the cis congeners.J Med Chem,1993,36:510~512.
[3]Kelland LR,Bamard CFJ,Evans IG,et al.Synthesis and in vitro and in vivo antitumor activity of a series of trans platinum antitumor complexes.J Med Chem,1995,38:3016~3024.
作者简介:
关蒙恩((1962.2— ),女,满族,北京市人,东北师范大学本科毕业,副教授,研究方向:高等有机化学、煤化工技术。
(作者单位:辽源职业技术学院)
