RDX直接硝解法的真空氧化结晶工艺
2015-05-10叶志文吕春绪
徐 乾, 叶志文, 吕春绪
(南京理工大学化工学院, 江苏 南京 210094)
1 引 言
目前,我国仅有的几条RDX生产线都采用直接硝解法[1-2]。直接硝解法制备RDX具有原料来源广泛、廉价,工艺过程和设备装置简单,生产过程容易控制,安全度高等优点[3]。但是这种方法生产RDX的过程中必须使用大量高浓度的硝酸,且产生大量的废酸,对环境造成严重污染。每生产1 t RDX就要处理约9.21t废酸,按照我国每年RDX的使用量计算,每年将产生十几万吨的废酸,对企业是一沉重的负担[4]。
叶志文等[5]在专利CN 103242253中介绍了利用真空氧化结晶法进行硝解液后处理的新方法。该法通过减少稀释水的用量,将硝化母液中硝酸浓度稀释至60%~80%,然后利用减压浓缩使RDX全部析出。该法减少了稀释水的用量,从而降低了废酸量,可有效地降低生产成本和大量废酸对环境的污染,所得产率较传统生产工艺略有提高。但该法中硝化母液中硝酸浓度稀释至60%~80%,该浓度仍较高,硝化母液中副产物浓度也较高,氧化激发过程较剧烈,危险性较高。
本研究组在传统生产工艺的基础上,将硝化母液中硝酸浓度稀释至51.8%~62.3%,并研究了其真空氧化结晶过程的最佳工艺条件,此工艺能够使氧化激发过程更平稳、有效、安全地进行,为真空氧化结晶法应用于RDX工业生产提供理论参考。
2 实验部分
2.1 试剂与仪器
乌洛托品(HA),分析纯,国药集团化学试剂有限公司; 发烟硝酸(浓度95%),分析纯,国药集团化学试剂有限公司。
低温恒温反应浴,DFY-5型,河南省予华仪器有限责任公司; 集热式恒温加热磁力搅拌器,DF-101SA型,南京科尔仪器设备有限公司; 循环水式多用真空泵,SHZ-D(Ⅲ)型,河南省予华仪器有限责任公司; 显微熔点仪,X-4型,上海精密科学仪器有限公司; 精密电子天平,J-300型,美国杰克兄弟集团有限公司; 真空干燥箱,DZF-6020型,上海新苗医疗器械制造有限公司。
2.2 实验
向250 mL的三口烧瓶中,加入11.44 g发烟硝酸,置于低温反应浴中搅拌,分批加入1 g HA,控制投料温度为10~15 ℃,投料时间为20 min,在15 ℃反应30 min。反应结束将烧瓶移至一定温度的水浴中,以一定速率向硝解母液中加入3.51 g稀释水,搅拌,使母液激发氧化,氧化结束后,升至85.0 ℃,以650 r·min-1的速率搅拌,开始减压蒸发,直至蒸干。产品经水洗、过滤、真空干燥后得成品。测得熔点为201.9~203.6 ℃,与文献[6]相近。
3 结果与讨论
硝化母液的氧化结晶过程是先氧化后结晶过程。氧化过程主要是通过加入稀释水使副产物氧化分解,以利于母液的后续处理。结晶过程是通过抽滤或真空结晶等方法使RDX析出。氧化过程和真空结晶过程的目的和影响因素各不相同,为此,本研究对氧化过程和真空结晶过程分别讨论。
3.1 氧化过程
3.1.1 稀释水加入量
直接硝解法的传统生产工艺中,每投入1 g HA可得到1.28 g RDX,硝解工序结束后硝酸的浓度约为92.1%,后处理时加入4.68 g稀释水,产生11.52 g浓度为50%的废酸[7]。为了确定不同稀释水量时硝化母液中硝酸的浓度和产生的废酸量,本研究以文献[7]的传统氧化结晶工艺为基础,通过测定真空结晶后回收液的质量和硝酸的浓度[8],确定了废酸量和硝酸浓度,研究了不同稀释水量与稀释水减少量、废酸量、废酸减少量、废酸中硝酸浓度的关系,结果见表1。
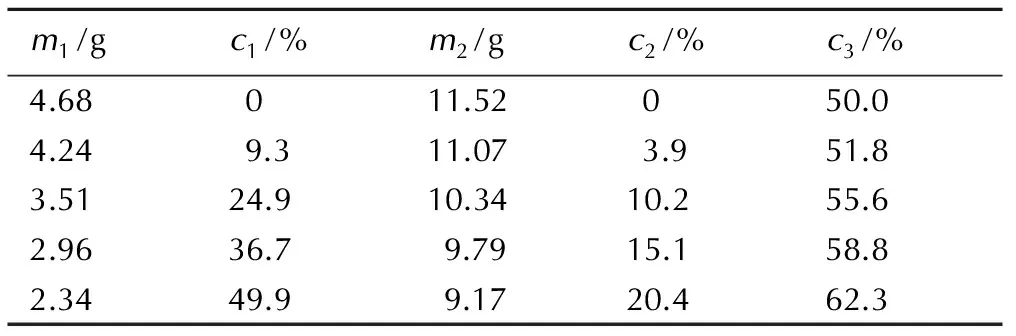
表1稀释水量与稀释水减少量、废酸量、废酸减少量、废酸中硝酸浓度的关系
Table1Relationship of the amount of dilution water with the dilution water reduction quantity, the amount of waste acid, the waste acid reduction quantity and the concentration of nitric acid in waste acid
m1/gc1/%m2/gc2/%c3/%4.68011.52050.04.249.311.073.951.83.5124.910.3410.255.62.9636.79.7915.158.82.3449.99.1720.462.3
Note:m1is the amount of dilution water.c1is dilution water reduction quantity.m2is the amount of waste acid.c2is the waste acid reduction quantity.c3is the concentration of nitric acid in waste acid.
由表1可知,与文献[7]相比,稀释水量由4.68 g降至2.34 g时,稀释水减少量由0增至49.9%,废酸量由11.52 g降至9.17 g,废酸减少量由0增至20.4%,废酸中硝酸的浓度由50%提高至62.3%。影响废酸量的因素有: 硝化结束时硝化母液中的含水量、硝酸量、加入稀释水量,当硝化工艺确定后,相同的投料量硝化结束时,硝化母液中含水量和硝酸量相同,废酸量取决于稀释水加入量。因此,研究通过减少稀释水用量,提高了硝酸的浓度,减少了废酸量。
3.1.2 稀释水量与最低激发温度的关系
氧化过程中先发生甲二醇二硝酸酯的水解,水解中生成的N2O3将甲醛和硝酸铵等氧化[9-11],同时放出红棕色气体。从反应热力学角度,任何反应的发生都需克服一定能垒,即最低活化能,当反应体系确定时,最低活化能随之确定,而最低活化能仅与温度有关。因此,不同稀释水量时水解反应的最低活化能不同,对应的最低激发温度也不同。确定不同稀释水量所对应的最低激发温度,有利于氧化过程的顺利进行。加入稀释水的过程中,释放出大量热量,母液温度不稳定,不利于最低激发温度的研究,因此,为了研究不同稀释水量与最低激发温度的关系,通过控制低温反应釜加入稀释水过程中母液的温度低于20 ℃,后通过加热使母液缓慢升温,当升至最低激发温度时,开始发生水解和氧化反应,母液中逸出红棕色气体,此时母液温度即为该稀释水用量所对应的最低激发温度。图1为不同稀释水量与最低激发温度的关系。

图1稀释水量与最低激发温度的关系
Fig.1Relationship of the amount of dilution water with the lowest excited temperature
由图1可知,最低激发温度随稀释水量的减少而升高,当稀释水量由4.68 g降至2.34 g时,最低激发温度由27.9℃升至 57.8 ℃ 。实验表明,当稀释水加入量小于3.51 g时,氧化结束后在后续的升温蒸发过程中仍会有少量红棕色气体产生,可能的原因是: 氧化过程中产生大量气体,气体逸出体系时带走大量热量,使氧化后期母液温度降低,与此同时,随着氧化过程的进行,硝化副产物浓度不断下降,当母液中副产物的浓度和温度降至不足以使硝化副产物继续水解时,激发进程中断,出现激发不完全的现象。在后续升温蒸发过程中,当体系温度升至能使硝化副产物继续水解时,体系被再次激发,进而产生红棕色气体。因此,最佳稀释水量为3.51 g,最低激发温度为49.4 ℃。
3.1.3 稀释水加入速率对激发过程的影响
在3.1.2的研究中,仅通过加热的方式使母液激发,稀释过程释放的热量未被利用。而在确定了稀释水量与最低激发温度的关系后,通过控制稀释水加入速率控制母液的升温,以利用稀释释放的热量使母液升温,降低能耗。稀释水量为3.51 g时,最低激发温度为49.4 ℃,为避免母液激发不完全,加热温度需比最低激发温度高。若加热温度过高,氧化过程过激烈; 若加热温度过少,仍会出现激发不完全,因此,设定加热温度为60 ℃。考察了加热温度为60 ℃时,稀释水加入速率对激发过程的影响,结果见表2。
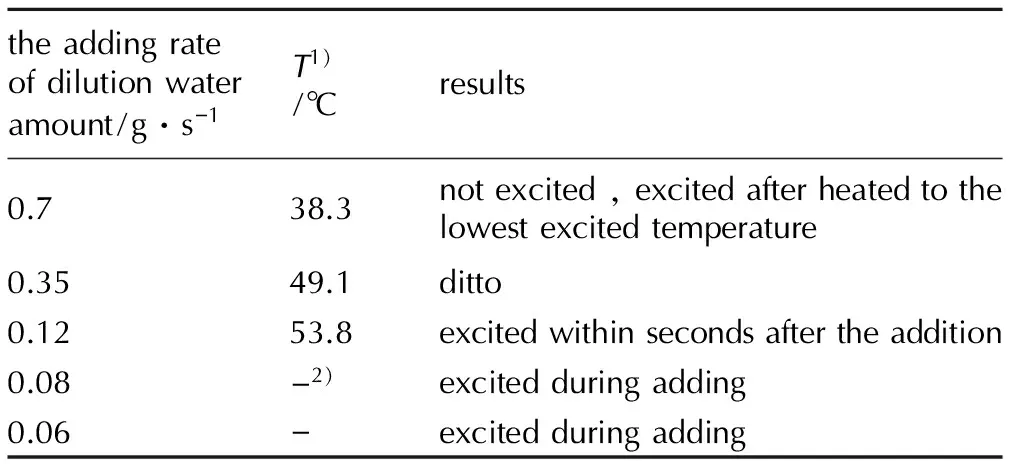
表2稀释水量加入速率对激发过程的影响
Table2Effect of the adding rate of dilution water amount on the excitation process
theaddingrateofdilutionwateramount/g·s-1T1)/℃results0.738.3notexcited,excitedafterheatedtothelowestexcitedtemperature0.3549.1ditto0.1253.8excitedwithinsecondsaftertheaddition0.08-2)excitedduringadding0.06-excitedduringadding
Note: 1)the temperature of exactly finishing adding; 2)“-” indicates that the data can’t be accurately measured.
由表2可知,当稀释水加入速率为0.7 g·s-1时,稀释结束时母液温度仅38.3 ℃,未激发。随着稀释水加入速率的降低,稀释结束时母液温度升高。可能是由于稀释用时变长,加热介质传递的热量增多,能达到更高的温度。当稀释水加入速率为0.12 g·s-1时,稀释结束时母液温度为53.8 ℃,稀释结束母液迅速被激发,不仅实现了母液被激发,而且充分利用了稀释过程释放的热量。当稀释水加入速率继续降低时,母液提前被激发,稀释热利用率低,且继续加水过程中体系的情况变的更为复杂,难以控制。因此,最佳稀释水加入速率为0.12 g·s-1。
3.1.4 加热温度对激发过程的影响
实验表明,当加热温度低于最低激发温度时,氧化过程后期母液温度会低于最低激发温度,使激发时间长且激发不完全,可能是由于激发过程中产生的大量气体在逸出体系时带走了大量热量,使母液温度降低; 而过高的加热温度会使母液温度迅速升高,氧化过程过于剧烈,不易控制。考察了稀释水加入速率为0.12 g·s-1时,不同加热温度对激发过程的影响,结果见表3。
由表3可知,加热温度低于60 ℃时,激发不完全; 加热温度高于65 ℃时,激发完全,但激发过程过于剧烈。加热温度为60 ℃和65 ℃时,激发过程均可进行完全,且过程平稳。综合考虑,最佳加热温度选择为60 ℃。
表3加热温度对激发过程的影响
Table3Effect of heating temperature on the excitation process

heatingtemperature/℃results45incompleteexcitation50incompleteexcitation55incompleteexcitation60completeexcitation,stationary65completeexcitation,stationary70completeexcitation,severe
3.2 真空结晶过程
3.2.1 真空度与共沸点的关系
常压下,硝酸-水共沸体系硝酸浓度为68.4%,共沸点为121.9 ℃[12],可通过减压的方式降低共沸点。将激发结束后的母液升温至100 ℃,随即保持一定真空度,随着温度的不断变化,最终在某一温度保持不变,该温度即为对应真空度下硝酸-水体系的共沸点。考察了不同真空度与共沸点的关系,如图2所示。
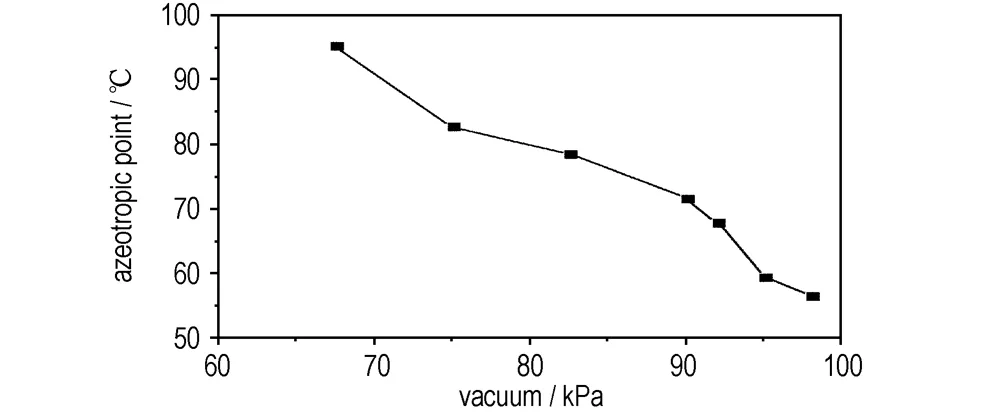
图2真空度与共沸点的关系
Fig.2Relationship of vacuum tightness with the azeotropic point
由图2可知,真空度由67 kPa增加至98 kPa时,共沸点由95.3 ℃降至56.4 ℃。真空度为92 kPa时,共沸点为67.8 ℃; 真空度为82 kPa时,共沸点为78.4 ℃; 真空度为75 kPa时,共沸点为82.7 ℃。不同真空度时,共沸点不同。由此可见,研究真空度与共沸点的关系,有助于确定适宜的真空度和初始的蒸发温度。
3.2.2 真空度对蒸发时间的影响
真空度的升高,使共沸点降低,蒸发时间缩短。在真空度考察范围内,共沸点为56.4~95.3 ℃。在3.2.1的研究时发现,减压蒸发初期,温度迅速下降至共沸点以下,温度不断波动后稳定在共沸点,尤其真空度较低时,波动过程用时较长,适当提高初始蒸发温度,可缩短波动过程用时,进而缩短实验进程,因此,选择80.1 ℃作为初始蒸发温度。而搅拌速率过小时,蒸发用时过长,搅拌速率过大,液体易飞溅,因此,搅拌速率应适中,选择为433 r·min-1。考察了初始蒸发温度为80.1 ℃,搅拌速率为433 r·min-1时,真空度与蒸发时间的关系,结果如图3所示。
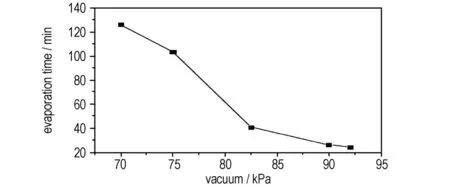
图3真空度对蒸发时间的影响
Fig.3Effect of vacuum tightness on the evaporation time
由图3可知,真空度为82 kPa时,蒸发时间为40.9 min。继续降低真空度,蒸发时间变长。高真空度下蒸发时间虽短,但考虑到工业生产中较难达到过高的真空度,因此,选择真空度为82 kPa是最适宜的。
3.2.3 初始蒸发温度对蒸发时间的影响
由3.2.1和3.2.2可知,真空度一定时,共沸体系中硝酸浓度和共沸点随之确定,且初始蒸发温度的选择直接影响到蒸发过程用时的长短。当硝酸的浓度低于共沸体系中硝酸的浓度时,蒸馏时,气相中所含的水分较液相中的多; 反之,当硝酸的浓度高于共沸体系中硝酸的浓度时,气相中所含硝酸较液相的多[13]。随着稀释水量减少,硝酸的浓度上升,但仍小于共沸物中硝酸的浓度(68.4%)。因此,蒸发过程分为两个阶段: 硝酸浓度小于68.4%时,以蒸发水分为主,硝酸浓度为68.4%时,以共沸物形式被蒸出。实验表明,若初始蒸发温度较低,体系温度将长期保持波动,之后升至共沸点保持不变。温度波动过程可能是以蒸发水分为主,由于硝酸浓度不断变化,因此温度也不断波动; 当硝酸浓度达到68.4%时,硝酸浓度不再变化,故温度保持不变。由于始蒸发温度较低时,波动过程用时较长,因此,分别考察了两个过程,温度波动过程称为蒸发前期,温度保持不变过程称为蒸发后期。考察了真空度为82 kPa,搅拌速度为433 r·min-1时,初始蒸发温度对蒸发过程的影响,结果见表4。
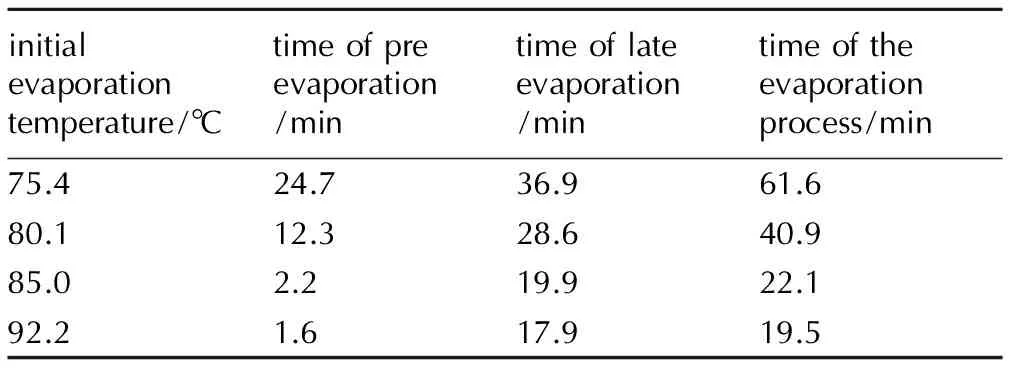
由表4可知,当初始蒸发温度低于共沸点78.4 ℃时,蒸发前期用时较长,初始蒸发温度对蒸发前期的影响较明显; 且初始蒸发温度较低时,对蒸发后期用时也有影响,可能是初始蒸发温度对蒸发前期的传质、传热过程的影响延续到了蒸发后期,从而对蒸发后期产生间接影响。随着初始蒸发温度的提高,蒸发前期用时明显缩短,当初始蒸发温度升至85.0 ℃时,蒸发前期用时缩短至2.2 min,继续升温蒸发前期、蒸发后期和蒸发过程用时均未明显缩短。考虑到工业生产过程中更高的温度需要更多的加热介质,因此,选择初始蒸发温度为85.0 ℃比较适宜。
表4初始蒸发温度对蒸发过程的影响
Table4Effect of initial evaporation temperature on the evaporation process
initialevaporationtemperature/℃timeofpreevaporation/mintimeoflateevaporation/mintimeoftheevaporationprocess/min75.424.736.961.680.112.328.640.985.02.219.922.192.21.617.919.5
3.2.4 搅拌速率对蒸发时间的影响
真空结晶过程中,搅拌速率影响蒸发过程的传质、传热,进而影响整个真空结晶过程。考察了真空度为82 kPa,初始蒸发温度为85.0 ℃时,搅拌速率对蒸发时间的影响,结果如图4所示。
由图4 可知,随着搅拌速率的提高蒸发时间随之缩短。当搅拌速率增至650 r·min-1时,蒸发时间为16.9 min。继续提高搅拌速率,蒸发时间未明显缩短。因此,选择最佳的搅拌速率为650 r·min-1。
3.3 真空氧化结晶工艺与传统氧化结晶工艺的对比
真空氧化结晶工艺在最佳工艺条件下,每投入1 g HA,加入稀释水3.51 g,产生废酸10.34 g。该工艺与传统氧化结晶工艺相比,稀释水用量和产生废酸量分别减少24.9%和10.2%,结果如图5所示。
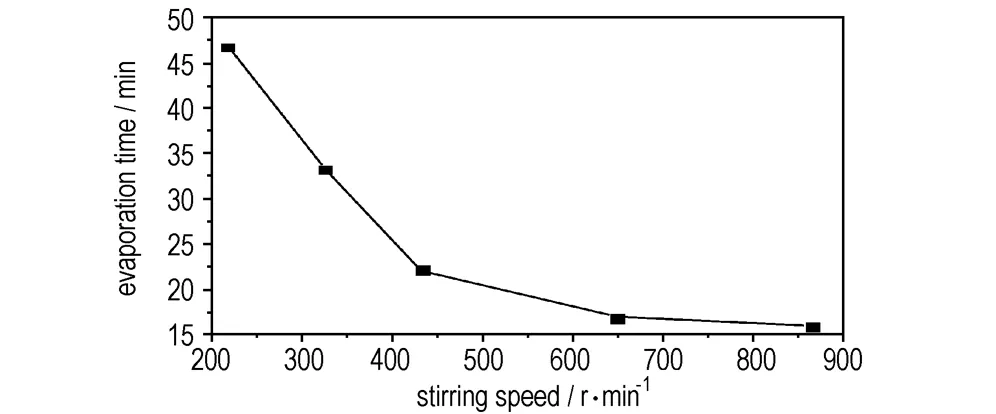
图4搅拌速率对蒸发时间的影响
Fig.4Effect of stirring speed on the evaporation time
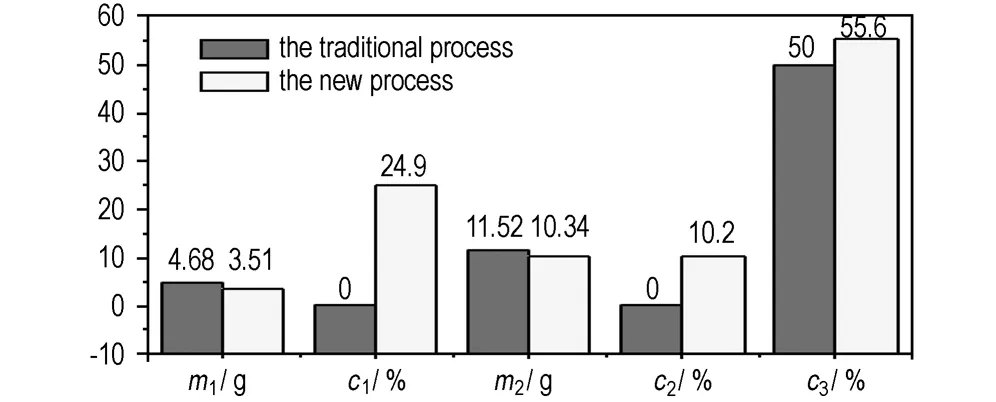
图5新工艺与传统氧化结晶工艺的对比
Fig.5Comparison of the new process with the traditional oxidation crystallization process
4 结 论
研究了真空氧化结晶法在直接硝解法制备RDX中的应用,确定最佳工艺条件为: 以投入1 g HA计,氧化过程: 加入稀释水量为3.51 g,稀释水加入速率0.12 g·s-1,最低激发温度49.4 ℃,加热温度60 ℃; 真空结晶过程: 真空度82 kPa,初始蒸发温度85.0 ℃,搅拌速率650 r·min-1,产生废酸10.34 g。该工艺与传统氧化结晶工艺相比,稀释水量和废酸量分别减少24.9%和10.2%。
参考文献:
[1] 于天梅. 黑索金绿色合成工艺的研究[D].南京: 南京理工大学,2009.
YU Tian-mei. Progress on Green Synthesis Technology of RDX[D]. Nanjing: Nanjing University of Science and Technology, 2009.
[2] 齐秀芳,王明,魏丽程, 等.硝酸镁辅助直接硝解法合成黑索金[J].精细化工,2013,30(11): 1201-1202.
QI Xiu-fang,WANG Ming,WEI Li-cheng.Synthesis of RDX by Direct Nitrolysis with the Acid of Mg(NO3)2[J].FineChemicals,2013,30(11): 1201-1202.
[3] 陈文靖,叶志文. RDX的合成工艺研究进展[J]. 爆破器材,2012,41(2).
CHEN Wen-jing, YE Zhi-wen.Progress on Synthesis Technology of RDX[J].DemolitionEquipmentsandMaterials, 2012,41(2).
[4] 刘耀鹏.火炸药生产技术[M].北京: 北京理工大学出版社,2009.
LIU Yao-peng.Technology of Producing Explosives and Propellants [M].Beijing:Beijing Institute of Technology Press,2009.
[5] 叶志文,程刘锁,颜小东.一种黑索金的制备方法: CN 103242253[P],2013.
YE Zhi-wen, CHENG Liu-suo, YAN Xiao-dong. A Method of Producing RDX: CN103242253[P], 2013.
[6] 米向超,胡立双,陈毅峰, 等. 黑索今工业生产技术进展[J].化工中间体,2013 (8): 26-27.
MI Xiang-chao, HU Li-shuang, LI Yi-feng, et al. Progress of producing RDX in industry[J].ChemicalIntermediates, 2013 (8): 26-27.
[7] 刘耀鹏.火炸药生产技术[M]. 北京: 北京理工大学出版社,2009.
LIU Yao-peng.Technology of Producing Explosives and Propellants [M].Beijing:Beijing Institute of Technology Press,2009.
[8] 张云.分析化学[M].上海: 同济大学出版社,2003.
ZHANG Yun. Analytical Chemistry[M].Shanghai:Tong Ji University Press, 2003.
[9] 石煜.黑索今的合成工艺研究[D].南京: 南京理工大学,2010.
SHI Yu. Study on Synthetic Process of RDX[D]. Nanjing: Nanjing university of science and technology, 2010.
[10] Gilpin V,Winkler C A. Studies of RDX and relate compounds Ⅷ. Thermochemisty of RDX reactrons[J].CanJChem,1952,30(10): 743-748.
[11] Bell J A,Dunstan I. Chemistry of nitramines. Part Ⅵ. Reaction of hexamethylene-tetramine with nitric acid[J].JChemSocC,1969,11(5): 1559-1562.
[12] 唐文骞,段煜洲.超共沸酸精馏制取浓缩酸与联产多种浓度稀硝酸新工艺[J].化肥工业,2014,41(1):30-31.
TANG Wen-qian,DUAN Yu-zhou.New Process of making concentrated nitric acid by super azeotropic acid rectification and co-producing dilute nitric acids with several concentrations[J].JournaloftheChemicalFertilizerIndustry, 2014,41(1):30-31.
[13] 孙荣康,任特生,高怀琳. 猛炸药的化学与工艺学[M]. 北京:国防工业出版社,1981.
SUN Rong-kang, REN Te-sheng, GAO Huai-lin. Chemistry and Technology of High Explosive[M]. Beijing: National Defense Industry Press,1981.
