氮肥对地下水中氮迁转机理研究
2015-05-09陈建平丁际豫吴子杰
陈建平,丁际豫,吴子杰
(1.辽宁工程技术大学 环境科学与工程学院,辽宁 阜新 123000;2.中国科学院大学 水系统安全研究中心,北京 100049;3.丹东港集团有限公司,辽宁 丹东 118000; 4.辽宁省地质勘查院,辽宁 大连 116100)
氮肥对地下水中氮迁转机理研究
陈建平1,2,丁际豫3,吴子杰4
(1.辽宁工程技术大学 环境科学与工程学院,辽宁 阜新 123000;2.中国科学院大学 水系统安全研究中心,北京 100049;3.丹东港集团有限公司,辽宁 丹东 118000; 4.辽宁省地质勘查院,辽宁 大连 116100)
为研究地下水中“三氮”迁移转化的主要影响因子,以江西省泰和县境内的千烟洲试验站为研究对象,根据研究需要进行了实验区域的划定,对研究区域的地下水位、“三氮”、铁、锰和pH值进行了长期的监测,通过数据整理、作图分析后,利用SPSS软件对“三氮”、总铁、可滤态锰和pH值的相关性进行分析。结果表明:研究区地下水已经受到了农业氮面源污染的影响;地下水中铁、锰具有显著的伴生性;铵态氮和亚硝酸盐态氮与铁、锰存在显著的正相关。总铁、可滤态锰、pH值、温度和降雨是地下水中“三氮”迁移转化的主要影响因子。通过“三氮”迁移转化影响因子的分析,可为农业氮面源污染的防治提供一定的理论基础。
地下水;污染;“三氮”迁移;影响因子;监测
当前,世界范围内严重的农业氮污染对区域生态环境和人类健康形成严重的威胁。在欧洲和美国等发达国家,由于农业造成的地下水面源污染也是普遍存在的[1]。从全球范围来看,30%~50%的地球表面已受到污染,农业污染引起14 400亿m2耕地不同程度退化[2]。据调查,我国532条河流中,82%不同程度地受到氮污染[3],这些氮主要来自于农业污染,受污染的地表水进入到浅层地下水中,进而影响这个地下水系统。因此,研究氮肥在浅层地下水中迁移转化机理具有重要的现实意义。
1 研究区概况
1.1 自然地理条件
千烟洲试验站位于江西省吉安市泰和县境内,北纬26°44′48″,东经115°04′13″,面积204.17 hm2。该试验区由3个封闭良好的小流域和81个红壤小山丘组成,海拔60~115 m左右,相对高差20~50 m,属吉泰盆地典型红壤丘陵区。研究区地形起伏,下垫面的坡度为2.8°~13.5°,由白垩系红色-紫红色砾岩、砂岩和泥岩组成,该区风化层一般厚度为30~50 cm,主要土壤类型为红壤土、水稻土、潮土、草甸土等[4-5]。吉泰盆地由7种沉积体类型组成,包括:冲击扇沉积体、辫状河沉积体、滨湖沉积体、浅湖沉积体、深湖沉积体、湖三角洲沉积体和残湖-沼泽沉积体,7种沉积体类型分布在整个吉泰盆地,厚度分布也不均匀[6]。对研究区域的地质条件进行钻井勘察,22 m钻井深度下显示研究区域内的地质结构主要可以划分为4层。第1层为表土层,厚约2.3~2.5 m,以亚黏土和亚砂土为主,主要是红色和棕黄色的水稻土;第2层为砂层,厚约0.5 m,以粗砂土和砂砾为主,渗透系数较大;第3层为砾石层,厚约3.5 m,以鹅卵石为主,局部混有红泥;第4层为基岩,厚约17 m,以白垩纪红色砂岩为主[7]。
研究区属于长江鄱阳湖水系流域二级支流架竹河的流域范围,架竹河流域面积77 km2,多年平均流量1.78 m3/s,年径流量为5.609×107m3,干流长18 km,落差95 m,千烟洲位于架竹河流域的中下游,占架竹河流域面积的3.26%[8]。监测区面积26余公顷(400多亩),地势较为平坦,相对高差1~6 m,属山体与河流间的冲积平原地貌。区内的土地有不同的利用类型(见图1)。研究区地势西南高,东北低,架竹河自东南向西北流。南侧和西侧均为山体,地下水从山前向河流补给。
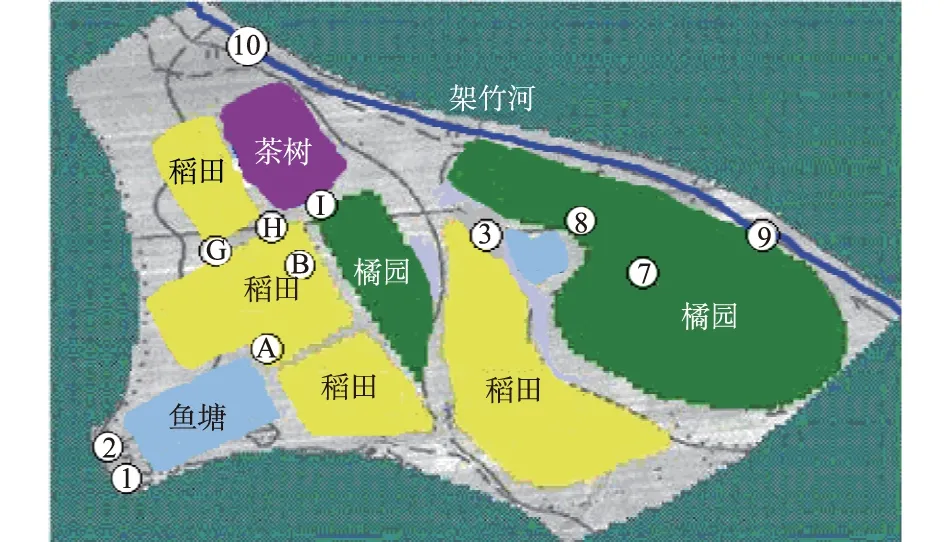
图1 研究区监测点分布情况Fig.1 Distribution of monitoring points in the study area
1.2 氮肥施加量
研究区内的水稻种植区一年两季水稻,共施肥2次,橘园种植区和油茶树种植区1年施肥1次,施肥时间和施肥量如表1所示。
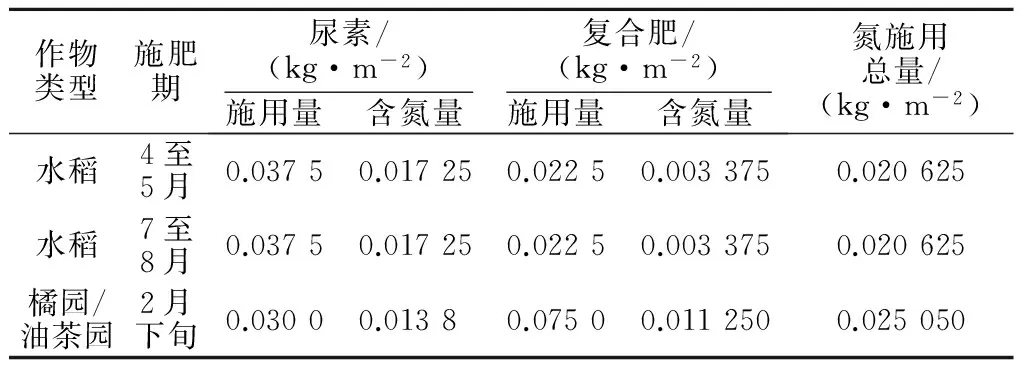
表1 农业施肥情况统计Table 1 Statistics of agricultural fertilizers
1.3 监测方案
研究区监测点的布置在覆盖全部区域的同时,还要考虑不同土地的利用类型。监测点的位置如图1所示。2号点位于鱼塘附近,用于监测研究区的地下水初始浓度,同时可以观察鱼塘补给对2号点地下水体的影响;3点、G点、I点、7点、8点分别位于未开垦的湿地附近、水稻种植区域、橘园旁边、橘园内、居民区,用于监测地下水体中“三氮”的浓度变化情况。1点、3点、G点、H点、I点为研究区内水位变化监测点。9号和10号监测点为架竹河水质监测点,用于研究地下水中“三氮”向地表水体中的迁移。A,B 2个区域为“三氮”垂向运移的监测区,根据土层分布特点布设采样深度分别为:耕作层0.2 m;犁底层0.4 m;淀积层0.8,1.2 m;渗育层1.6,2.0,2.4 m。 研究区地下水水位整体较浅,土壤中的氮素会随着降雨垂向进入到浅层地下水中,研究氮在土壤中运移机理进而预测降雨能否对地下水中氮素分布产生影响。
1.4 采样时间及方法
实验数据时间跨度达到2年半,包含2010,2011年的全部种植期及2010—2012年之间的2个农闲期。
地下水采样时间为上午6:00~8:00,时间间隔1~2 d,2012年开始,周期加长为3~4 d。采样选用真空泵抽吸法。7号点和8号点为饮用压水井,在采样前需要将管内水压出去,待新鲜水出来再采样。
采样容器选择具塞聚乙烯塑料瓶,使用前用10%稀盐酸浸泡,再用蒸馏水反复冲洗,风干后盖好待用。为防止采样瓶对水中铁离子的吸附作用,水样需经盐酸酸化到pH=1,测定总铁的水样单独选用聚乙烯瓶,瓶中事先加入适量盐酸。样品需及时送到实验室进行化学分析。为防止监测组分发生变质,所有样品要求在24 h之内完成采样及全部化学分析工作,分析结果如果有误差较大的数据,第2天重新进行相应点采样的数据分析。
1.5 实验方法
地下水水质检测指标包括:pH值、总铁(TFe)、可滤态锰、亚硝酸盐态氮(NO2-—N)、铵态氮(NH4+—N)和硝酸盐态氮(NO3-—N)。在化学分析的间隔期间,水样贮存于5℃左右的冰箱中,测定时,恢复到常温,防止热胀冷缩造成的体积误差。监测顺序为:亚硝酸盐态氮、铵态氮、硝酸盐态氮、pH、总铁、可滤态锰。为了避免人为误差和水样不均匀造成的影响,每个监测指标都有一个平行样进行实验结果准确性的确定,如果遇到误差较大的情况需要进行该组分的重新测定。
亚硝酸盐态氮选用N—(1—萘基)—乙二胺光度法进行测定;铵态氮选用纳氏试剂分光光度法测定;硝酸盐态氮选用酚二磺酸分光光度法进行测定;pH值采用玻璃电极法(Glass Electrode Method)进行测定;总铁选择邻菲罗啉(又称邻二氮杂菲)分光光度计法测定;可滤态锰选用高碘酸钾分光光度法测定。
2 研究区“三氮”迁移转化机理研究
研究区具备典型的红壤丘陵农业种植区特点,土壤中总铁、可滤态锰的含量较高,因此根据实验条件和研究区特点,对研究区“三氮”迁移转化的影响因子选取了总铁、可滤态锰、pH值、温度和降雨等5个影响因子。总铁、可滤态锰、pH值由现场取样测试和实验室监测得到,降雨量和土壤温度信息由监测站自动监测设备完成。
通过数据整理、作图分析后,利用SPSS软件对不同采样点的“三氮”、总铁、可滤态锰和pH值的相关性进行分析,根据分析结果找出农业面源污染对地下水中“三氮”的响应及变化规律。
2.1 总铁和可滤态锰对“三氮”转化的影响
表2为Ⅰ,2,3,G号点地下水中总铁和可滤态锰与“三氮”的相关性分析结果。
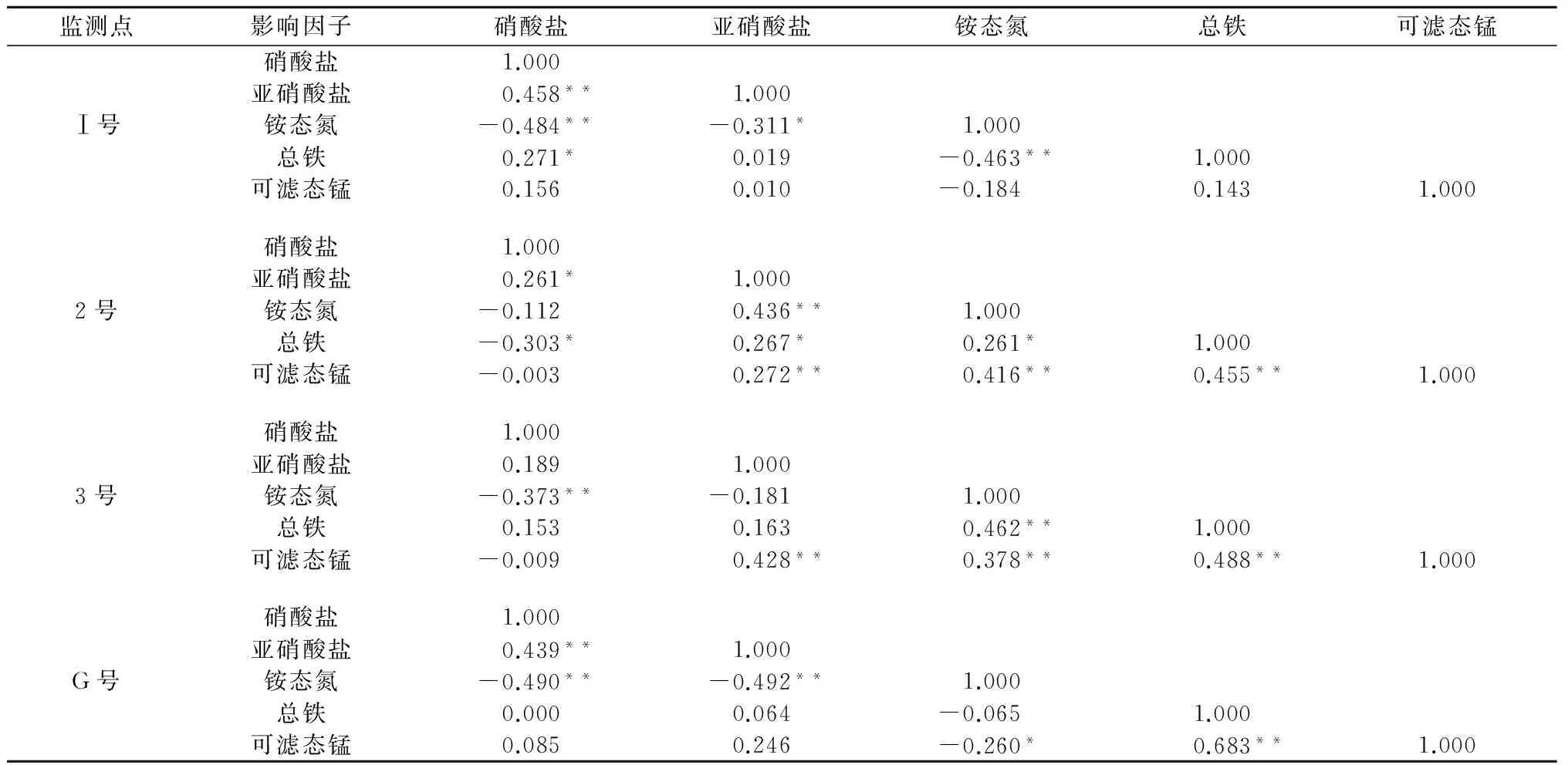
表2 地下水中总铁和可滤态锰与三氮的相关性Table 2 Correlation of total Fe and manganese in filtering state with ammonia-nitrite-nitrates in groundwater
注:样本重度45;**表示相关性极显著:*表示相关性显著,-表示负相关。
表2呈现出“三氮”之间的关系为:铵态氮与硝酸盐态氮呈显著的负相关,硝酸盐态氮与亚硝酸盐态氮呈显著的正相关。“三氮”的这种分布状态说明硝化反应处于主导地位。2号和3号点长期处于饱水状态,环境中缺氧,反硝化占主导地位,使得这2点“三氮”的相关性表现的不明显。
2,3,G号点的铁锰均呈极显著性正相关,表明在红壤地区地下水中的铁锰具有明显的伴生性,铁锰以某种复杂分子结构共生存在,或以某种液溶胶的形式存在。水稻种植、鱼塘养殖对于地下水中的铁锰伴生性影响不大;而橘园种植区(I点)总铁含量明显偏低,且铁锰不具备显著相关性,反映出橘树对铁元素有吸收和固定作用。
在2号和3号点处,总铁和可滤态锰与铵态氮和亚硝酸盐态氮都存在一定的正相关性,而在G号点处的锰与铵态氮呈现出一定的负相关性(橘树对铁离子的特殊作用I点不予考虑)。由于2号、3号点长期处于高水位、缺氧地带,导致地下水中原生铁锰产生微耗氧铁锰细菌,铁锰细菌利用地下水中的溶解氧对低价态铁猛的氧化(地下水中Mn2+性质比较稳定,故忽略其还原性),使包气带中的溶解氧维持在一个较低的水平,见式(1)。当溶解氧不足时,就会发生式(2)反应[9],此时铁锰与硝酸盐态氮相关性不是很显著;铁锰对于氧的竞争力强于铵态氮,因此铁锰与铵态氮和亚硝酸盐态氮呈显著的正相关性。
4Fe(OH)2+O2+2H2O铁细菌→ 4Fe(OH)3;
(1)
(2)
水稻的生长需要大量的氮肥和及少量的铁锰,而铵态氮又是氮肥的主要来源,这就使得G点处铁锰与铵态氮呈负相关性表现。
2.2 pH值对“三氮”迁移转化的影响
分析实验数据表明pH值与“三氮”之间符合线性相关关系,线性相关性分析结果如表3所示。
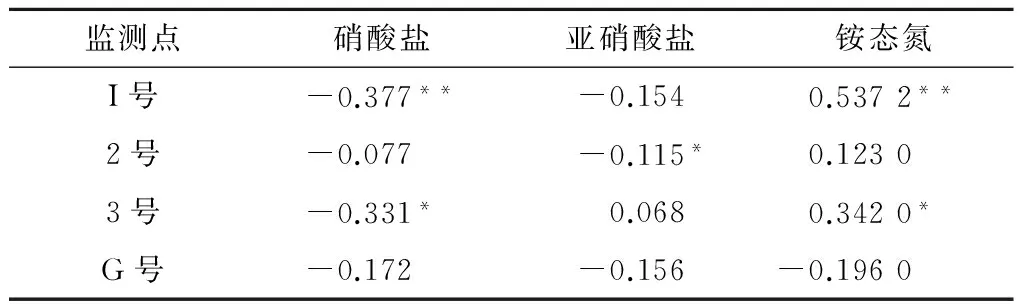
表3 pH值与“三氮”的相关性Table 3 Correlation of pH value with ammonia-nitrite-nitrates in groundwater
由表3所示的相关性是因为“三氮”的相互转化过程中细菌起到重要作用,而pH值的范围影响了土壤中各细菌的活性,因此pH值与“三氮”具有一定的相关性[10]。2,3,G,I号采样点的pH值跨度区间分别为:6.41~7.2,6.52~7.37,6.8~7.71,6.1~6.93,可见pH值对“三氮”浓度分布的影响具有一定的区间性,其中I号点pH值与“三氮”呈极显著性相关,从而可以认为在橘园中pH值在6.1~6.9之间的时候,酸性越强硝化细菌活性越强,酸性越弱反硝化细菌活性越强。由G点pH值与铵态氮和硝酸盐态氮都表现出负相关性且相关性不是很显著,说明当硝化细菌和反硝化细菌都处在适宜生长的pH范围内(反硝化细菌的适宜生长pH为7.0~8.5,硝化细菌的适宜生长pH为6.0~7.5[11]),pH对硝化和反硝化反应的影响效果不是十分明显。
2.3 温度对“三氮”转化的影响
温度对于土壤中的微生物具有最直接的影响,不管是硝化作用还是反硝化作用都需要微生物来完成。图2至图4为2点、3点氮素的温度分布图,如图所示,由于硝化反应和反硝化反应不断的交替起到主导作用,这2个过程都能产生亚硝酸盐,因此在5~35℃的亚硝酸盐态氮浓度变化没有太明显的规律性。
如图2和图3,温度在5~13℃时,铵态氮浓度逐渐降低,温度在13~20℃时,铵态氮浓度有一个明显的上升趋势。这是由于温度<5℃时,不论是硝化细菌还是反硝化细菌的活性都比较低,当温度从5℃上升的过程中硝化细菌首先表现出活性,而反硝化细菌不明显;温度高于 13℃,反硝化细菌活性增强,铵态氮浓度有一个回升的趋势;当温度在19℃时,反硝化细菌表现出最强的活性;温度在19~25℃时,铵态氮浓度逐渐降低;温度在25~30℃时,铵态氮浓度又有一个明显的上升趋势。分析得出,当温度在20~30℃之间时,硝化细菌活性较高,在25℃时硝化细菌活性达到最大,之后随着温度升高活性减弱,图4验证了部分的结论。这与徐斌等人[12]研究结果基本一致,不同点在于研究区内硝化作用和反硝化作用同时进行。反硝化作用在19℃时达到一个峰值,然后有不变或者有变小的趋势,这就是图2(b)在19℃时铵态氮浓度出现峰值的原因。3号点硝酸盐态氮的温度分布图可以看出反硝化反应的强弱表现的不是很明显,这与3号点的包气带常年处于一种饱水状态、反硝化强度一直维持在一个较高的水平有关。
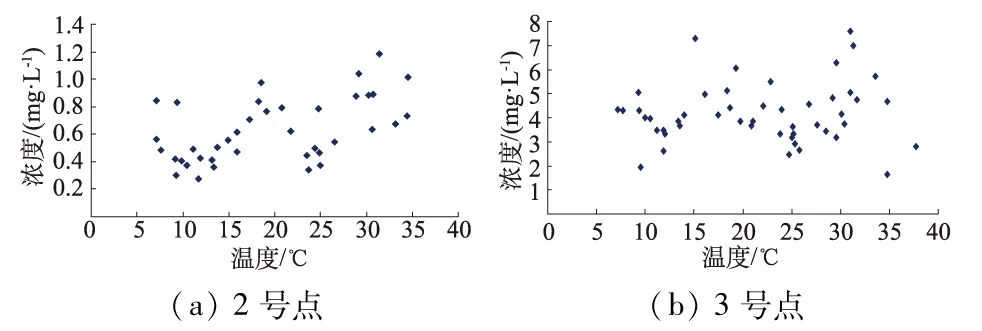
图2 铵态氮浓度分布
Fig.2 Distribution of ammonia nitrogen concentration
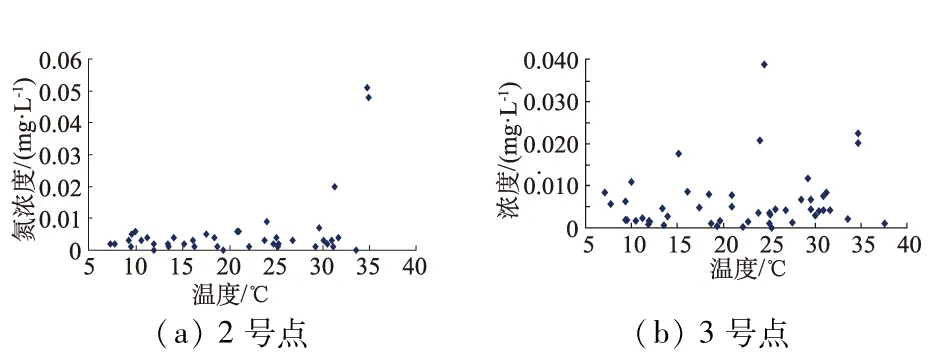
图3 亚硝酸盐态氮浓度分布
Fig.3 Distribution of nitrite nitrogen concentration
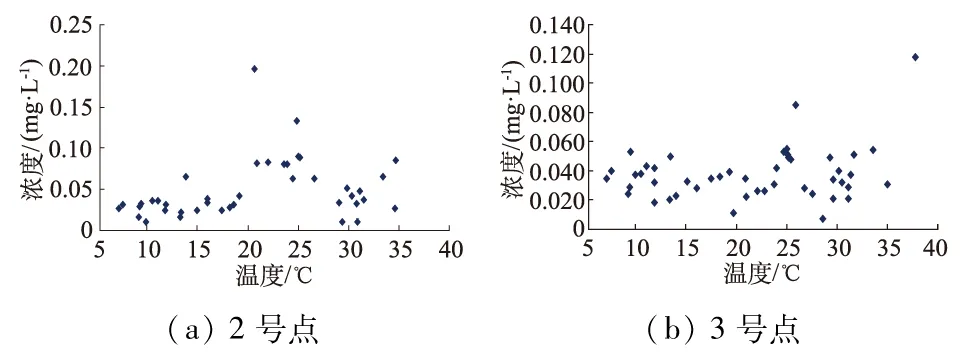
图4 硝酸盐态氮浓度分布
Fig.4 Distribution of nitrate nitrogen concentration
2.4 降雨对“三氮”迁移的影响
降雨是影响氮素垂向迁移的主要因素。降雨强度的变化会导致氮素的垂向迁移呈现出不同的分布状态。从弱降雨(0~0.4 mm)和强降雨(>5 mm)2个方面分析降雨对氮素垂向迁移的机理。研究表明[13]:地下水环境中氮的主要存在形式是硝酸盐态氮,而铵态氮是化肥的主要成分,所以研究降雨对氮素迁移的影响时主要考虑硝酸盐态氮和铵态氮两种元素。

图5 弱降雨强度下地下水中铵态氮和硝酸盐态氮浓度的纵向分布情况Fig.5 Longitudinal distribution of ammonia nitrogen and nitrate nitrogen concentration in groundwater in the presence of weak rainfall intensity
2.4.1 弱降雨对“三氮”迁移的影响
图5为2010,2011年弱降雨强度下农田纵向不同深度氮素的浓度变化曲线。由于犁底层具有很强的托水保肥能力,撒施的氮肥不能轻易的进入到地下水体之中,因此在0.2 m监测点处(耕作层)的氮素浓度最高。在淀积层中,由于铁锰氧化物在该层运移明显,且该层长期处于包气带和饱水带之间,导致淀积层中铵态氮发生硝化反应生成硝酸盐态氮,在弱降雨条件下硝酸盐态氮不易迁移,使得铵态氮浓度下降,硝酸盐态氮浓度上升。潜育层常年受地下水浸渍,铵态氮处于缺氧环境中,硝化反应受到很大的抑制,而部分硝酸盐发生反硝化反应生成铵态氮或氮气等,同时硝酸盐特别容易随地下水流动而发生横向及垂向迁移,所以潜育层硝酸盐态氮浓度变化不大,1.6 m和2.0 m两点的铵态氮浓度升高;较深的2.4 m处铵态氮已经被各土层不断吸附拦截,因此浓度有所下降。监测结果认为:表层土和深层土对NH4+的吸附和解吸能力是不同的,表层土的吸附能力比深层土的吸附能力强,而解吸能力比深层土弱,这也是造成潜育层铵态氮浓度高于淀积层的原因之一[14]。
2.4.2 强降雨对“三氮”迁移的影响
图6为2010,2011年强降雨强度下农田垂向不同深度氮素的浓度变化曲线(2 a中强降雨总量与弱降雨总量基本一致),图6中可以看出氮素在耕作层中浓度仍然处在最高水平,不过强降雨的影响导致犁底层托水能力饱和,一部分降雨发生地表径流,一部分降雨发生垂向渗透,因此耕作层中的氮素随着降雨的下渗进入到了淀积层中;这使得与弱降雨强度下硝酸盐态氮浓度在0.4 m和0.8 m处的值比较,硝酸盐态氮浓度有明显增加,有些时间点的浓度甚至超过了0.2 m处的浓度,随着垂向深度的变化硝酸盐态氮浓度呈现出平稳并略有下降的趋势;由于土壤的吸附作用使得铵态氮下渗速率得到缓解,在0.8 m和1.2 m处的铵态氮含量较弱,降雨强度时有明显变化。强降雨的垂向渗透对铵态氮在潜育层的分布有较明显的影响,2.4 m处的铵态氮浓度随着强降雨的发生,平均浓度由0.4 mg/L左右增大到0.5 mg/L左右,与1.6 m和2.0 m两点处的铵态氮浓度达到同一水平。可以看出,强降雨程度下,降雨入渗比较明显,同时也会带着较浅层的氮素向深层地下水中迁移,这会导致农业面源氮污染迁移进入到深层地下水体中,造成地下水的污染。
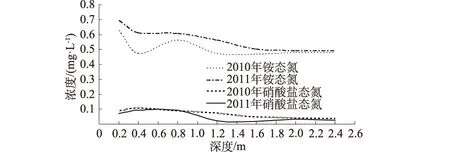
图6 强降雨强度下地下水中铵态氮和硝酸盐态氮浓度的纵向分布情况Fig.6 Longitudinal distribution of ammonia nitrogen and nitrate nitrogen concentration in groundwater in the presence of heavy rainfall intensity
3 结 论
(1) 红壤丘陵水稻种植区,地下水中铁锰具有显著的伴生性,橘园种植区对于地下水中的铁离子有明显的吸收和固定作用,从而改变地下水氧化还原环境,间接影响“三氮”的迁移转化。在缺氧、无氧环境中,铵态氮和亚硝酸盐态氮与铁锰存在显著的正相关性。
(2) 在氧化环境较强,硝化反应占主导地位的地下水中,pH值在6.1~6.9之间变化时,酸性越大硝化细菌活性越强,酸性越小硝化细菌活性越弱,说明pH值是决定地下水中“三氮”浓度分布的重要影响因子,同时具有一定的区间性。
(3) 温度过低时硝化细菌和反硝化细菌活性都受到抑制,当温度在19℃左右时,反硝化细菌表现出最强的活性,当温度达到25℃左右时硝化细菌表现出最强的活性。
(4) 不降雨或者弱降雨强度下,地表的硝酸盐态氮以及铵态氮不易发生垂向迁移,铵态氮在微生物的作用下缓慢地向硝酸盐态氮转化。当降雨强度较大时,加快了稻田水向地下水的入渗速度,稻田水携带铵态氮以及硝酸盐态氮渗入地下,对浅层地下水造成污染。由图5和6可以看出:短时强降雨发生后,0.2 m和0.4 m处仍然有明显的峰值出现,而历时长的相同降雨量已经导致硝酸盐达到最小值并稳定,因此得出短时强降雨没有长时分散降雨导致硝酸盐损失严重。
[1] ROBERTSON W D, PTACEK C J, BROWN S J. Geochemical and Hydrogeological Impacts of a Wood Particle Barrier Treating Nitrate and Perchlorate in Groundwater[J]. Groundwater Monitoring & Remediation, 2007, 27(2):85-95.
[2] 赵永宏, 邓祥征. 我国农业面源污染的现状与控制技术研究[J]. 安徽农业科学, 2010, 38(5):2548-2551.(ZHAO Yong-hong, DENG Xiang-zheng. Study on Current Situation and Controlling Technologies of Agricultural Non-point Source Pollution in China[J]. Journal of Anhui Agricultural Sciences, 2010, 38(5):2548-2551. (in Chinese))
[3] 张青松, 刘 飞, 辉建春,等. 农业化肥面源污染现状及对策[J]. 亚热带水土保持, 2010, 22(2):44-52.(ZHANG Qing-song, LIU Fei, HUI Jian-chun,etal. Non-point Pollution Status & Solution Measures of Agricultural Fertilizers[J]. Subtropical Soil and Water Conservation, 2010, 22(2):44-52.(in Chinese))
[4] 陈春阳,杨凤亭,王绍强.CDM造林再造林项目方法学的实证研究—以千烟洲生态试验站为例[J]. 林业科技, 2011, 36(5): 1-5.(CHEN Chun-yang, YANG Feng-ting, WANG Shao-qiang. An Empirical Study on Afforestation and Reforestation CDM Project: Taking the Qianyanzhou Ecological Experimental Station as an Example[J]. Forestry Science & Technology, 2011, 36(5): 1-5.(in Chinese))
[5] 贺有为, 王秋兵, 温学发,等.季节性干旱对中亚热带人工林显热和潜热通量日变化的影响[J]. 生态学报, 2011, 31(11): 3069-3081.(HE You-wei, WANG QIU-bing, WEN Xue-fa,etal. The Diurnal Trends of Sensible and Latent Heat Fluxes of a Subtropical Evergreen Coniferous Plantation Subjected to Seasonal Drought[J]. Acta Ecologica Sinica, 2011, 31(11): 3069-3081. (in Chinese))
[6] 廖瑞君.江西吉安—泰和陆相红色盆地沉积体研究[J].中国区域地质,2000,19(2): 181-186.(LIAO Rui-jun. Study on Sedimentary Deposits in the Red Continental Basin of Ji’an-Taihe, Jiangxi[J]. Regional Geology of China, 2000,19(2): 181-186. (in Chinese))
[7] 虞子静.农业生态系统地下水氮面源污染数值模拟研究 [D].北京:中国科学院研究生院, 2008.(YU Zi-jing. Numerical Modeling of Groundwater Contamination from Non-point Sources of Nitrogen in Agricultural Ecosystems[D]. Beijing: Graduate University of the Chinese Academy of Sciences,2008. (in Chinese))
[8] 李杰新.千烟洲红壤丘陵水资源合理开发利用途径[J].资源科学,1993,(3):48-54.(LI Jie-xin. Approach on Rational Development and Utilization of Water Resources in the Red Earth Hilly Area of Qianyanzhou[J]. Resources Science, 1993, (3): 48-54. (in Chinese))
[9] 梁秀娟,肖长来,盛洪勋,等.吉林市地下水中“三氮”迁移转化规律[J].吉林大学学报(地球科学版),2007,37(2):335-340.(LIANG Xiu-juan, XIAO Chang-lai, SHENG Hong-xun,etal. Migration and Transformation of Ammonia-nitrite-nitrates in Groundwater in the City of Jilin[J]. Journal of Jilin University(Earth Science Edition), 2007,37(2):335-340. (in Chinese))
[10]李 晶.氮污染在地下水中迁移转化规律的研究[J]. 环境保护科学, 2010, 36(1): 21-23.(LI Jing. Study on Transfer of Nitrogen Pollution in Groundwater[J]. Environmental Protection Science, 2010, 36(1): 21-23. (in Chinese))
[11]陈旭良,郑 平,金仁村,等. pH和碱度对生物硝化影响的探讨[J]. 浙江大学学报(农业与生命科学版),2005,31(6): 755-759.(CHEN Xu-liang, ZHENG Ping, JIN Ren-cun,etal. Effect of pH on Nitrification[J]. Journal of Zhejiang University (Agriculture&Life Sciences), 2005,31(6): 755-759. (in Chinese))
[12]徐 斌,夏四清,高廷耀,等.悬浮生物填料床处理微污染原水硝化试验研究[J].环境科学学报,2003,23(6):742-747.(XU Bin, XIA Si-qing, GAO Ting-yao,etal. Study on Nitrification of the Micro-polluted Raw Water in a Suspended Packing Bioreactor[J]. Acta Scientiae Circumstantiae, 2003,23(6):742-747. (in Chinese))
[13]MACILWAIN C. US Report Raises Fears over Nitrate Levels in Water[J]. Nature, 1995, 5(4): 377-381.
[14]WANG F L, ALVA A K. Ammonium Adsorption and Desorption in Sandy Soils[J]. Science Society of America Journal, 2000, 64(5): 1669-1674.
(编辑:赵卫兵)
Mechanism of Migration and Conversion ofNitrogen Fertilization in Groundwater
CHEN Jian-ping1,2,DING Ji-yu1,3,WU Zi-jie4
(1.College of Environmental Sciences and Engineering, Liaoning Technical University, Fuxin 123000,China;2.Center for Water System Security, University of Chinese Academy of Sciences, Beijing 100049, China;3.Dandong Port Group Co., Ltd., Dandong 118000,China;4.Liaoning Provincial Institute of Geological Exploration, Dalian 116100,China)
By analysing main factors affecting the migration and conversion of ammonia-nitrite-nitrates in groundwater, we aim to provide theoretical basis for the prevention and control of agricultural non-point source nitrogenous pollution. Qianyanzhou test station in Jiangxi Province was selected as research object and experiment plots were divided. The groundwater table, ammonia-nitrite-nitrates, ferrum-manganese and pH value of groundwater in the research area were monitored in long term. Through data sorting, diagram analysis and SPSS software, we analysed the correlation among ammonia-nitrite-nitrates, total iron, manganese in filtering state and pH value. Results suggest that the groundwater in the study area has been affected by agricultural non-point nitrogenous pollution. Ferro-manganese in groundwater are apparently associated. Ammonium nitrogen and nitrite nitrogen are positively related with ferro-manganese. Total iron, manganese in filtering state, pH value, temperature and rainfall are the main impact factors of the transport and transformation of ammonia-nitrite-nitrates in the groundwater.
groundwater; pollution; conversion and transport of ammonia-nitrite-nitrates; impact factor; monitoring
2013-10-05;
2013-11-05
国家重点基础研究发展计划“973”项目(2010CB428801)
陈建平(1972-),男,山西保德人,副教授,博士,主要从事地质工程、环境工程等方面的教学与科研工作,(电话)13804181164(电子信箱)chenjianp123000@163.com。
丁际豫(1988-),女,河南巩义人,助理工程师,硕士,主要从事环境工程、地下水环境等方面的研究工作,(电话)15841830520(电子信箱)dingjiyu@126.com。
10.3969/j.issn.1001-5485.2015.02.006
X523
A
1001-5485(2015)02-0024-06
2015,32(02):24-29
