动脉留置针在大鼠体脑组织灌注中的应用*
2015-05-05韦晓勇陆波闵红星王毅李军
韦晓勇 陆波 闵红星 王毅 李军
免疫组化等病理学实验研究中,为避免脑组织细胞的变形及自溶现象,动物处死前需行灌注固定处理[1-2],故动物在体脑组织的灌注固定效果对试验结果尤为重要。就脑组织灌注固定方面,报道的文献不少,有经心脏灌注、颈总动脉灌注、经股动脉灌注等方法;灌注过程中有夹闭腹主动脉、胸主动脉等;灌注针有用静脉输液器针、自制灌流针(去掉输液器针头的针尖或12-16号针头上套一长约1.5 cm的塑料管并将塑料管前端剪成针尖状)和普通针头等。对此,为寻求一种操作简单易行且灌注固定效果好的方法,笔者在大鼠体脑组织的灌注固定实验过程中,采用动脉留置针夹闭胸主动脉经心脏灌注的方法,现将实验操作过程的体会介绍如下。
1 材料与方法
1.1 试剂和器械 BD动脉留置针(货号:REF682245,规格型号:20 G、1.10 mm× 45 mm、49 mL/min),见图1,4%多聚甲醛新鲜配置(天津市光复精细化工研究所),0.9%复方氯化钠注射液(500 mL/4.5 g、宁夏启元药业),10%水合氯醛(成都金山化学试剂有限公司),三通(舒尔康、批号:120225)、止血钳、组织剪、眼科剪、小动脉夹、皮镊、输液管(2副)等。

图1 BD动脉留置针
1.2 实验动物 选取体重450~500 g,健康雄性18个月龄SD大鼠24只[购于宁夏医科大学动物实验中心,清洁级,合格证号:SCXK(宁)2011-0001],常规条件下饲养,自由饮水,普通饮食。
1.3 实验方法 将灌注所用的0.9%复方氯化钠注射液加热至37 ℃[3]、新鲜配置4%多聚甲醛滤去杂质[3]、输液管(两副输液管用三通连接好)、手术器械等物品准备就绪后,放置盛有上述0.9%复方氯化钠和4%多聚甲醛的输液瓶距离操作台1.5 m高的位置[4]。雄性SD大鼠经10%水合氯醛(0.4 mL/100 mg)麻醉,待大鼠反正反射消失后,将其仰卧位于实验台上,固定头部和四肢,暴露胸部,沿胸骨中线自剑突向上依次剪开皮肤和胸骨,充分暴露胸腔,显露心脏和主动脉弓,迅速用皮镊提起左侧肺,可见其下位于大鼠脊柱左侧的胸主动脉( 胸主动脉右侧为食管)[5],以小动脉夹夹闭胸主动脉。并迅速用眼科剪剪开心包,用动脉留置针在心尖波动最明显处进针,进入约0.5 cm时,右手往外退针芯,同时左手持针翼将套管自左侧心室推送至升主动脉直至套管针尾部,此时,关闭套管针尾端的开关,防止血液外溢,连接输液管,剪破右心耳,打开套管尾端和输液管开关,灌注0.9%复方氯化钠注射液,先快后慢,待自右心耳流出液体颜色清亮,此时旋转三通开关,由快及慢灌注4%多聚甲醛,待大鼠颈部及上肢僵硬,说明灌注固定成功[6]。随后断头取脑,之后将脑组织置于4%多聚甲醛固定4 ℃保存[7]。
1.4 观察指标 (1)观察并记录灌注后大鼠组织的色泽、质感及是否含有血丝。(2)观察并记录实验中所用的0.9%复方氯化钠注射液和4%多聚甲醛的量、灌注插管时间、总灌注时间。灌注插管时间是指从针进入心尖开始至插管成功所用时间,总灌注时间是从针进入心尖开始至灌注固定成功所用时间。(3)观察并记录灌注过程中大鼠颈部、胡须、四肢和尾巴是否抽搐。(4)观察并记录灌注过程中是否发生肺循环灌注。发生肺循环途径灌注的现象时鼻腔中会有灌流液流出[8]。(5)观察并记录在灌注插管过程中损伤血管、穿破心腔和灌注过程中套管脱出等不良事件的发生率。
2 结果
灌注后大鼠脑组织呈乳白色,质地较硬,且未含血丝(图2)。实验中所用的0.9%复方氯化钠注射液和4%多聚甲醛的量分别为(107±9.2)mL、(175±17.3)mL,灌注插管时间和总灌注时间分别为(10±1.8)s、(41±4.1)min。灌注过程中大鼠颈部、胡须、上肢明显抽搐,下肢及尾巴未抽搐。灌注过程中均未发现大鼠鼻腔中有灌流液流出,故未发生肺循环灌注。灌注插管过程中未出现损伤血管、穿破心腔和灌注过程中套管脱出等不良事件。
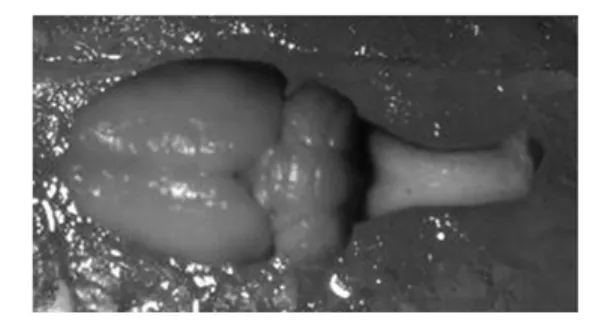
图2 灌注后大鼠脑组织
3 讨论
免疫组化等病理学实验研究中需对组织进行定性、定位或定量研究。因此,在组织切片之前,需对组织进行灌注固定,因为固定好的组织能抑制细胞内溶酶体酶的释放和活性, 防止自溶;抑制组织中细菌的繁殖,防止组织腐败,使细胞的蛋白质、脂肪、糖等各种成分凝固成不溶性物质,以防止物质扩散,维持原有组织的形态结构[9]。大鼠在体脑灌注过程中,通过大鼠天然的循环系统直接进行灌注固定,固定液可快速、均匀地分布到脑组织各个部位,所以脑组织标本制备多采用此法[10-11]。
灌注固定主要坚持两个原则:一要尽量保持活体的状态;二要尽量行动迅速从而避免动物长时间处于痛苦和濒死状态,引起病理假象,从而干扰科研结果[12]。目前,据文献[12]报道,小动物灌注多采用经心脏灌注方法,而经颈总动脉因操作难度大,费时而逐渐被淘汰。脑组织灌注过程中为节省灌注液,依研究报道有夹闭腹主动脉、胸主动脉等[5],但夹闭腹主动脉需进行开腹,增加操作难度,延长灌注总时间,降低实验效率。灌注针是保证整个灌注过程的必要条件,因此,灌注针的选择对整个灌注过程尤为重要。有研究报道灌注针可用静脉输液器针[8]、自制灌流针[5,13-14]和普通针头[14]等,这些灌注针虽可进行灌注,但都有各自弊端。如静脉输液器针和普通针头因针尖锋利,在插管过程中可刺破心脏及心室,且易脱出,使灌注失败或发生肺循环灌注。而自制的灌流针[5,13],一般因针尖钝圆,不易刺入心脏,需借助眼科剪[12],又因心脏跳动,增加眼科剪的操作难度,在心尖处剪的口可能过大或过小,也可能剪破心脏,影响灌注固定效果,而通过剪口,插入灌注针,动作要轻慢[5],从而延长灌注时间甚至导致灌注失败。陈浩宇等[14]自制的灌注针因塑料前端成针尖状,在灌注插管时可损伤血管及心腔,并可能引起肺循环灌注。
因此,笔者采用动脉留置针夹闭胸主动脉经心脏灌注的方法,可避免上述弊端,且依据许晓泉等[15]研究,在灌注开始时加热至37 ℃的0.9%复方氯化钠注射液的速度要快,能更好地排出脑组织内的血流,灌注新鲜配置滤去杂质的4%多聚甲醛时速度需放慢,让多聚甲醛在脑组织内停留更长的时间,以便有效固定。本实验结果表明:灌注过程中大鼠颈部、胡须、上肢明显抽搐,下肢及尾巴未抽搐,说明完全夹闭胸主动脉,可节省灌注液;另外,灌注过程中未发生肺循环灌注,保证了体循环灌注的效果,进而灌注后大鼠脑组织呈乳白色,未见血丝,且质地较硬;灌注插管时间仅用了(10±1.8)s,可见操作简单且节约时间;灌注插管过程中未出现损伤血管、穿破心腔和灌注过程中套管针脱出等不良事件,保证了灌注过程顺利进行,且可节约实验成本。
本研究的创新点:采用动脉留置针为灌注针,在整个灌注过程中,发现采用动脉留置针具有以下优势:(1)进针易:动脉留置针芯针尖锋利,心尖处进针容易,进针约0.5 cm时退出针芯,将套管从左心室顺利推送至升主动脉,可节约灌注插管时间;(2)出血少:动脉留置针套管的外径较针芯大[16],可完全占据心尖穿刺点,减少出血;(3)损伤小:在退出针芯推送套管过程中,由于套管顶端钝圆,可避免损伤心腔及升主动脉;(4)推送顺:动脉留置针套管原料采用聚四氟乙烯,管壁硬度适宜、光滑,可顺利推送至升主动脉;(5)明插管:在动脉套管推送过程中,可看到套管进入升主动脉的全过程,确保插管成功,同时可避免肺循环灌注的发生;(6)易固定:套管尾端两侧有针翼,较其他灌注针容易固定;(7)难脱出:动脉套管长度45 mm,插管成果后,套管很难脱出,有利于灌注的顺利进行;(8)速度可:动脉留置针套管管腔直径1.10 mm,流量49 mL/min,可保证灌注速度,强化灌注效果,节约灌注时间和灌注液。
综上所述,本实验操作简单,灌注插管迅速、损伤小,可避免肺循环灌注,总个灌注过程省时、省液,且灌注固定效果好,值得推广应用。
[1]季正剑,张冬霞,张立波,等.大鼠在体脑组织灌流方法的比较[J].实验动物与比较医学,2009,29(6):390-392.
[2]郭林芝,李灵敏. 大鼠脑组织石蜡切片免疫组化的体会[J].山西医科大学学报,2013,44(4):311-312.
[3]刘乃慧,张莉,邵颖,等. 在体心脏灌流术在大鼠脑组织切片观察中的应用[J].实验动物科学与管理,2005,22(2):52-53.
[4]高永强,杨巧莲,王伟.大鼠局灶性脑缺血模型制备及取脑方法实验研究[J].包头医学院学报,2009,25(4) : 6-9.
[5]卢文朋,栗世方.大鼠脑组织灌注固定方法的改进[J].医学研究生学报,2014,27(6):627-629.
[6]李晶晶,朱鸿,施彩虹.三种方法对大鼠视网膜固定效果的比较研究[J].上海交通大学学报(医学版),2011,31(8):1105-1107.
[7] Stoltenberg M,Danscher G,Pamphlett R,et al.Histochemical tracing of bismuth in testis from rats exposed intraperitoneally to bismuth subnitrate[J].Reproductive Toxicology,2000,14(14):65-71.
[8]王章敬,李煌元.静脉输液器应用在小鼠体脑组织灌注方法[J].微量元素与健康研究,2014,31(1):9.
[9]陈广斌,谢玲,林坚涛.不同固定方法对新生大鼠脑组织切片的影响[J].中国民康医学,2008,20(15):1730-1731.
[10]陈玉玺,王晓莉,牟青杰,等.骨髓间充质干细胞对脑缺血大鼠星形胶质细胞影响的实验研究[J].医学研究生学报,2013,26(6):564-567.
[11]李丹,王志萍,宗剑,等.富氢液联合浅低温对大鼠脑缺血再灌注海马氧化应激水平的影响[J].医学研究生学报,2012,25(1):26-30.
[12]周传龙,方剑乔,邵晓梅.大动物灌注固定方法的探讨[J].实验动物科学,2010,27(1):70-71.
[13]刘海燕.灌注固定大鼠的技术操作及常见问题[J].齐齐哈尔医学院学报,2006,27(11):1341.
[14]陈浩宇,高亚兵,彭瑞云,等.一种改进的大鼠脑组织灌注固定方法[J].军事医学科学院院刊,2002,26(3):208-212.
[15]许晓泉,刘圣,祖庆泉,等. 在体脑灌流技术在犬脑梗死实验研究中的应用[J].江苏医药,2011,37(20):2357-2359.
[16]蔡云亮,潘春杰,王新,等. 动脉留置针颈内静脉直接穿刺置管在休克抢救中的应用[J].广东医学院学报,2014,32(3):386-388.
