血清淀粉酶测定结果的溯源与方法学分组的关系
2015-05-03王卫兵
王卫兵
(首都医科大学 产业经营与管理中心,北京 100069)
在一项血清酶测定结果可溯源性研究中[1],研究者在市三级医院的50家检验科或其他临床实验室统一发放由日本临床化学协会(JSCC)推荐的酶参考物(ERM)1支(日本旭化成株式会社生产),各实验室按现行操作规程要求进行定标(用K值计算时省略此步)和室内质控测定,再测定ERM,重复测定10次,在指定日期内完成检测,取均值上报检验中心统计计算,统计中一次性排除大于均值±2SD的数据。作者对50家ERM的测定结果均值与ERM标示值比较。按研究中采用的实验方法和统计方法,每个实验项目用来与标示值比较的均值乃是10次测定结果的均值/每个实验室×50个实验室共500个数据的均值,并且一次性剔出50个均值中大于均值±2SD数据;在测定ERM的同时做了室内质控,应当是在控状态。有鉴于此,对ERM的测定结果均值与标示值间的相对偏倚属系统误差。相对偏倚大的项目之一是淀粉酶(AMY)为负的16.8%,同时室间变异达29%。作者对此讨论指出“AMY实验室测定结果CV高达29%,提示可能存在方法学上的问题”,而对16.8%的系统误差出现原因未进行讨论。我们查对了50家实验室所用11个不同来源AMY试剂盒主要的测定原理和试剂组成,现就AMY测定结果溯源性[2]如何科学合理进行方法分组进行讨论。
1 AMY常规测定方法和试剂盒应用现状
目前在临床实验室常规化验中使用的AMY试剂盒主要有7个不同来源[3](见表1)。其中有5个是使用相同底物4,6-亚乙基-(G7)-1,4-对-硝基酚-(G1)-α-麦芽七糖苷(EG7P),其结构式见图1。

图1 EG7P结构式
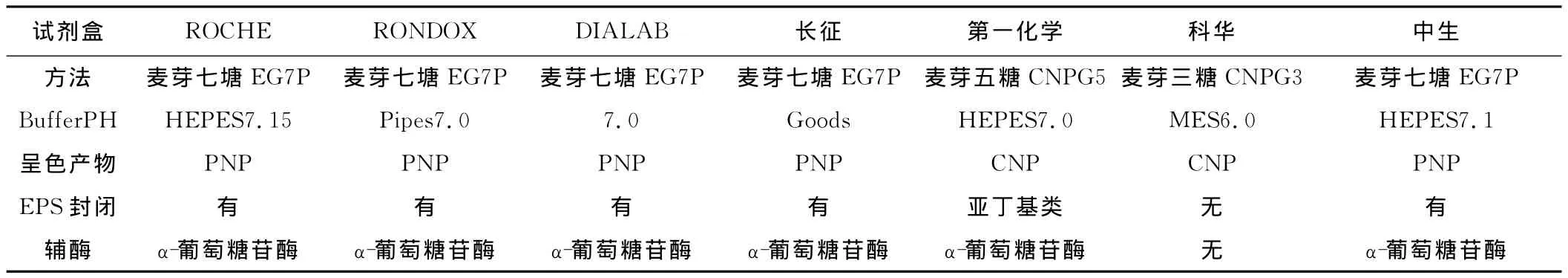
表1 7种常用AMY试剂盒测定原理、成分比较
但这五家之间所用缓冲液种类有差别其中二家与IFCC推荐法[4]所用缓冲系统相同是HEPES,而另二个分别用Pipes和Goods缓冲液。另一来源的AMY试 剂 盒 用 的 底 物 是 2-氯-4-硝 基 酚-α-麦 芽 三 糖 苷CNPG3),只有一家AMY试剂盒使用的底物是苯甲基-对-硝基酚-麦芽五糖苷(BG5P)。AMY测定方法分组主要依据即是AMY作用底物结构,不同方法组间存在有统计学意义的明显系统误差。这正是为什么采用这7种不同来源AMY试剂盒检测ERM的AMY活性会出现如此大的负偏倚的主要原因。
2 BG5P法与EG7P法之间的系统误差
日本旭化成株式会社生产的酶校正血清AMY测定采用的底物是对硝基酚-苯甲基-α-麦芽5糖苷(BG5P),JSCC釆用以BG5P(其结构式见图2)和EG7P为底物的2个方法测定一批血清AMY活性,相关散点图见图3。

图2 BG5P结构式
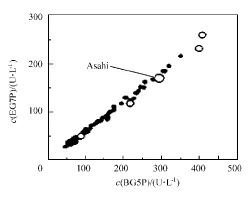
图3 血清AMY活性测定BG5P法与EG7P法相关散点图
从图3可见,用BG5P测出的AMY活性比在EG7P中测出的活性高出约1.67倍。那么,上述研究中50家医院临床实验室测定旭化成ERM中AMY活性均值为274U/L,ERM标示值329U/L,比其高1.20倍,两者相差55U/L,这应是50家参评实验室釆用不同底物试剂盒与ERM的BG5P之间系统误差的均值[5]。这是不同方法间客观存在偏差正常表现,而不能依此作出参评实验室AMY测定不准确的结论。
3 EG7P法与PNPG7法之间的系统误差
麦芽七糖非还原端不封闭底物1,4—对—硝基酚—(G1)—α—麦芽七糖苷(PNPG7)与EG7P比较,就是因为麦芽七糖苷非还原端被亚乙基封闭,改变了底物结构进而导致AMY与底物之间“诱导契合”相互作用的继发改变。二者的酶促反应时间曲线见图4。

图4 AMY.活性测定2种方法酶促反应时间曲线的比较
可见,EG7P法比PNPG7法37℃反应延迟时间缩短约2min,线性反应围扩展,在整个测量范围内维持零级反应动力学;但二者测定结果在3个仪器系统做血清AMY活性平行测定,PNPG7法比EG7P法高[6],部分实验数据见表2。

表2 AMY活性测定EG7P(Y)与PNPG7(X)2种方法比较
实验证明,二者相关及回归与温度无关,EG7P测定结果乘以系数2.5即可转换为心PNPG7结果,截矩a可略而不计。可见,不能笼统地将AMY测定方法分为“麦芽七糖组”。“麦芽七糖组”至少应分开3组,即EG7P、BG7P和PNPG7,AMY校正物的选择应用和结果溯源也应按此原则分组进行。
4 EG7P法与其他几种底物方法的相关与回归分析
回归分析[7]结果见表中。从表3数据可见,因底物结构的差异而导致各方法组间AMY结果分布在-1.11~3.89U/L之间;b值分布在0.444~1.728之间。此结果的偏倚、回归分析表明4种不同底物方法与EG7P方法组比较,a值分组结果同样说明AMY的必须科学严谨进行方法分组,做到“对号入座”、“各就各位”。
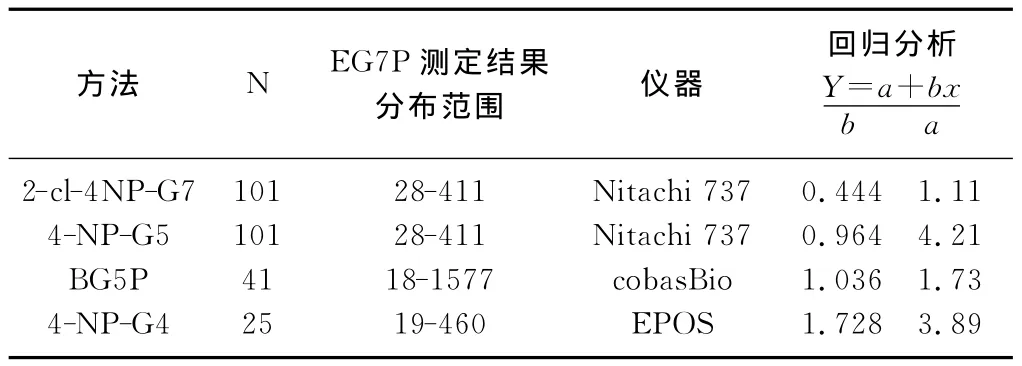
表3 EG7P法与其他几种底物方法的相关与回归分结果
5 讨论
影响AMY测定结果,除底物不同外,还会有其他因素如底物浓度、缓冲液、pH值、离子强度、辅助酶、辅因子的种类和浓度等,试剂盒的性能质量、校正方法、仪器性能、仪器分析中的参数设置、仪器维护保养、操作规程等凡构成“AMY检测系统”的各要素中任一环节出现问题都会影响到最后的结果。我们需从“检测系统”宏观上去看待每个具体的一个个要素;而在分析一个个具体要素对结果的影响时,又要依据“检测系统”的概念综合考虑。在AMY“检测系统”间,影响检测结果的主要因素是底物的种类和试剂的配方。在一系列关于不同检测系统血清酶测定结果的偏倚评估与可比性研究中都发现检测系统间AMY测定值的系统误差不能被接受,其原因也应按上述思路进行分析[8]。
为了做好血清酶测定结果的溯源,应学习IFCC发布的文件〔PⅡS0009—9120(98)00039—3〕[9],该文件以实例证明酶校正物的可交换性,只能在有相同分析特异性的方法组内进行,一再强调的是“同方法组”概念。不问酶校正物定值的检测系统与常规实验室检测系统间是否存在可比性,一律要求在常规实验室中将不属同一检测系统的结果硬拉到校正物定值上,这不仅无助于提高酶测定实验质量,相反会造成测定结果和临床应用的混乱[10]。正如关于“酶校正物在血清酶测定中的应用”[11]一文表明的那样:一个厂家的校正品一般是在自己的测定系统内进行评估的,在同类系统内它能很好地把测定结果的值在参考方法和常规方法间传递,但不一定适合另一个厂家的测定系统,因此不要把一个厂家在特定检测系统生产的校正品用来校正另一个检测系统[12]。徐国宾等在分析研究酶校正物定值流程和定值传递流程后强调:“目前临床化学在进行血清酶活性浓度测量校准时张家校准品张冠李戴的情况应该纠正”[13]。可见,在酶活性测定结果可溯源性研究中,不问AMY常规方法所用底物种类,根据常规实验室用常规方法测出ERM结果偏离ERM标示值即认定常规方法不准确是不符合酶活性测定结果可溯源基础理论和准则的。
(
)
[1]王清涛,童清,郭健.血清酶测定结果可溯源性研究[J].中华检验医学杂志,2003,26(12):761-763.
[2]北京市医疗器械检验所.GB/T 21415—2008体外诊断医疗器械生物样品中量的测量 校准品和控制物质赋值的计量学溯源性[S].北京:中国标准出版社,2008.
[3]韩志军,黄志锋,卢业成,等.临床化学常用项目自动化分析法[M].3版.沈阳:辽宁科学技术出版社,2005:826-835.
[4]Gerhard Schumann,Ryozi Aoki,Carlo A Ferrero.IFCC primary reference procedures for the measurement ofcatalytic activity concentrations of enzymes at 37℃[J].Clin Chem Lab Med ,2006:44(9).
[5]Katsuhiko Kuwa.Scientiifc Division of Japan Society of Clinical Chemistry:Proposed standard for certified enzyme reference materials(ERM)[J].Japan J Chem,2000,29:77-92.
[6]Kruse/Jarres J D.C.Kaiser Evalution of a new a-Amylase Assay Using 4,5-Ethylidene-(GT)-1-4-nitrophenyl-(G1)-a-D-maltoheptaoside[J].Clin.Biochem,1989,27:103-113.
[7]张连祥,刘晨梅,蔡忠,等.七种试剂盒检测a-淀粉酶结果的比较及分析[J].天津医药,2002,30(9):554-555.
[8]张秀明,庄俊华.不同检测系统血清酶测定结果的偏倚评估与可行性研究[J].中华检验医学杂志,2006,29(4):369-349.
[9]Georges F,John E,Takashi K.Validation of an Enzyme Calibrator-An IFCC Guideline〔PⅡS0009-9120(98)00039—3〕[J].Clin Biochem,1998,31(6):495-500.
[10]文庆成.临床酶测定标准化的几个问题[J].中华检验医学杂志,1998,21(1):60-61.
[11]苏增留,张克坚,郭健,等.酶校品在血清酶测定结果标准化中的应用[J].上海医学检验,2001,16(2):79-83.
[12]汤蓓,石凌波,李尔凡.酶校正品在血清酶测定中的应用[J].检验医学,2005(20):143-145.
[13]徐国宾,吴南,王清涛.要重视血清酶学测定的标准化工作[J].临床检验杂志,2007,25(3):161-164.
