增免肽颗粒增强鸡新城疫疫苗免疫效果试验
2015-04-29胡莉萍
胡莉萍
摘 要:首先取11日龄青脚黄羽肉鸡150只分为5组,每组30只,分别为给予1%、0.8%、0.6%、0.4%浓度的增免肽颗粒混饮4个给药组和1个空白对照组,经连续给药7d、观察14d的药物耐受性试验证实,增免肽颗粒以1%浓度下连续对雏鸡无不良反应和毒性作用,且0.4%以下浓度混饮有明显的促进生长作用。再取462只11日龄雏鸡,随机分为7组。空白对照组30只隔离饲养,不做任何处理。其余6组每组72只,设3个重复,每个重复24只;次日3个药物剂量组开始混饮高、中、低剂量的增免肽颗粒,药物对照组混饮盐酸左旋咪唑-黄芪多糖粉,连续5d,疫苗对照组和攻毒对照组不给药;14日龄各组用ND-La Sota苗滴鼻点眼免疫;26日龄重复以上给药,连续5d,28日龄重复免疫;40日龄重复以上给药,连续5d,42日龄除疫苗对照组外各组均用新城疫强毒攻毒。分别于21、28、35、42日龄每组随机抽取12只颈静脉采血,分离血清,用血凝抑制法测定新城疫抗体效价;于21、35、42日龄每组随机抽取6只,采血分离外周血淋巴细胞,用MTT法测定其增殖;于21和42日龄每组随机抽取6只称重、扑杀,测免疫器官指数;攻毒后每天观察14d内各组发病和死亡情况,计算发病率、死亡率和免疫保护率;于21、42、56日龄统计攻毒前后的平均日增重、耗料量和料重比。结果表明,增免肽颗粒显著提高血清抗体效价,促进外周血淋巴细胞增殖,提高免疫器官指数和攻毒保护率,并能提高增重和降低料重比。高、中剂量组效果较好,明显优于盐酸左旋咪唑-黄芪多糖,两组之间多无显著差异,建议中剂量(按0.2%混饮)为临床应用剂量。
关键词:增免肽颗粒;药物耐受;鸡新城疫;免疫效果;免疫保护
中图分类号:S858.312.4 文献标识码:B 文章编号:1673-1085(2015)03-0043-05
增免肽颗粒主要成分为黄芪、白术等纯中药成分,有补气健脾、益卫固表功能,主要用于免疫功能低下、免疫抑制等。依据有关临床试验指导原则,我们对增免肽颗粒进行了耐受性试验和增强免疫效果试验。
1 材料与方法
1.1 药物、试剂和仪器 受试药物增免肽颗粒,每1ml含生药1g,批号:2014020402。由青岛农业大学农用生物制药实验室提供。
对照药物:盐酸左旋咪唑-黄芪多糖可溶性粉,每出口袋100g,含盐酸左旋咪唑5g、黄芪多糖8g,批号:20140114。湖南湘大兽药有限公司出品。
疫苗和病毒:鸡新城疫低毒力活疫苗(La Sota株),批号:20140104。武汉中博生物科技股份有限公司出品。新城疫强毒株(NDV-F48E8)、新城疫抗体效价测定(血凝抑制法)抗原SPF鸡胚NDV-La Sota尿囊液、新城疫抗体阳性血清,均由青岛农业大学预防兽医学实验室提供。其中NDV-F48E8种毒用10日龄SPF鸡胚增殖,经Reed-Muench法测定其EID50为10-7.97,临用前用PBS稀释成104、105、106、107EID50。
主要仪器:CO2培养箱,倒置显微镜,超净工作台,酶标仪,离心机,分析天平等。
1.2 动物 1日龄青脚黄羽肉鸡,购自山东省农业科学院家禽研究所。试验前按常规饲养,喂不含任何药物的全价饲料,自由采食及饮水,饲养至11日龄用于试验。
1.3 方法
1.3.1 药物耐受性试验 选150只11日龄临床健康的雏鸡,公母兼有,称重,按体重(兼顾公母)随机分成5组,参照中华人民共和国兽药典[1]和大鼠急性毒性试验结果[2],其中4个给药组分别按1%、0.8%、0.6%、0.4%的增免肽颗粒混饮连续给药7d,1个空白对照组则不给药。每天观察1次,仔细记录动物的采食、饮水、排便和毒性反应出现的时间、死亡情况,连续观察14d。观察期内动物自由采食和饮水。观察期结束后分别称重,统计各组的日均增重、日均采食量和料重比,最后处死所有存活鸡,进行眼观病理学检查。
1.3.2 增强免疫效果试验 同上选462只11日龄临床健康的雏鸡,随机分为7组。空白对照组30只隔离饲养,不做任何处理。其余6组每组72只,设3个重复,每个重复24只,疫苗对照组和攻毒对照组各加24只用于攻毒剂量测定;次日起3个药物剂量组开始混饮高、中、低剂量的增免肽颗粒,药物对照组混饮盐酸左旋咪唑-黄芪多糖粉,连续5d,疫苗对照组和攻毒对照组不给药;14日龄时(测得母源抗体效价为2.8±0.3log2)各组均用新城疫La Sota苗滴鼻点眼免疫,2羽份/只;26日龄开始重复以上给药,连续5d;28日龄时重复免疫;40日龄开始重复以上给药,连续5d;42日龄时除疫苗对照组和空白对照组外各组用新城疫强毒F48E8攻毒。具体分组与处理(药物浓度参照耐受性试验结果确定)如表1。
1.3.3新城疫抗体效价测定 分别于21、28、35、42日龄时,3个试验药物组、药物对照组和疫苗对照组每组随机抽取12只,颈静脉采血,分离血清,用血凝抑制法[3]测定新城疫抗体效价的动态变化。首先测抗原血凝价(HA),主要步骤为:在96孔“V”形微量反应板上,用生理盐水50μl/孔自左向右将NDV-La Sota尿囊液抗原病毒作2倍比稀释至第11孔(21~211),第12孔为生理盐水对照孔,向各孔加入1%鸡红血球50μl,振荡混匀1min,37℃静置作用20min左右观察结果,以100%凝集(红血球呈颗粒性伞状凝集沉于孔底)的病毒最大稀释孔为该病毒血凝价(即1个凝集单位)。实测的NDV-La Sota尿囊液抗原病毒的凝集价为1:29。其次用4单位(1:27即128倍稀释的尿囊液)病毒测各时间点血清中新城疫抗体的红细胞凝集抑制效价(HI),主要步骤为:在96孔“V”形微量反应板上,用生理盐水50μl/孔自左向右将50μl/孔待检血清作2倍比稀释至第10孔(21~210),第11孔为病毒对照,第12孔阳性血清对照,1~11孔加入4单位病毒50μl/孔,振荡混匀1min,置37℃温箱作用20min,再加入1%鸡红血球50μl/孔,再振荡混匀1min,37℃静置作用20min左右观察结果,以100%抑制凝集的血清最大稀释度为该血清的抗体滴度(即抗体效价),用-log2表示。
1.3.4 外周血淋巴细胞增殖测定 分别于21、35、42日龄时,3个试验药物组、药物对照组和疫苗对照组每组随机抽取6只(设3个重复),每只颈静脉无菌采血(肝素抗凝)1.5ml,用淋巴细胞分离液分离外周血淋巴细胞,采用MTT法[4,5,6]测定外周血淋巴细胞增殖。
1.3.5 免疫保护效果测定
1.3.5.1 攻毒剂量预试 另取分别于14日龄和28日龄经新城疫La Sota苗滴鼻点眼,2羽份/只,2次免疫的32日龄雏鸡96只,随机均分为4组,每组24只,分别用104、105、106、107 EID50的NDV-F48E8 0.2ml经滴鼻点眼攻毒,之后每天观察1次,仔细记录每组的发病及死亡情况,观察10d,统计各组死亡率,作为攻毒剂量依据。
1.3.5.2 攻毒试验 42日龄时,3个试验药物组、药物对照组和攻毒对照组每组取12只(设3个重复),每羽经滴鼻点眼106EID50的NDV-F48E8 0.2ml攻毒(参照上述攻毒剂量测试结果)。每天观察各组鸡的发病和死亡情况,死亡鸡剖检观察病理变化,连续观察14d,计算各组的发病率、死亡率和免疫保护率。免疫保护率=存活健康鸡数/样本数。
1.3.6 免疫器官指数测定 于21和42日龄时,3个试验药物组、药物对照组和疫苗对照组每组随机抽取6只称重,扑杀,分离胸腺、脾脏和法氏囊、称重,计算免疫器官指数。免疫器官指数=免疫器官(g)/体重(g)。
1.3.7 生长性能测定
1.3.7.1 日均增重 分别于14、21、42、56日龄时,各组称重,分别计算14~21、22~42、43~56日龄3个时间段的日均增重。日均增重(g/d/羽)=(平均末重-平均始重)/饲喂天数。
1.3.7.2 日均采食量 分别计算14~21、22~42、43~56日龄3个时间段的耗料量,计算日均采食量。日均采食量(g/d/羽)=耗料量/饲喂天数/羽。
1.3.7.3 料重比 分别计算各组3个时间段的总耗料量和总增重,计算料重比。料重比(g/g)=总耗料/总增重。
1.3.8 数据统计 数据用平均数±标准差表示,用SPSS软件比较各组抗体效价、淋巴细胞增殖和生长性能的差异,用卡方检验[7]比较各组发病率、死亡率、保护率的差异。
2 结果
2.1 药物耐受性 4个给药组分别按1%、0.8%、0.6%、0.4%的增免肽颗粒混饮连续给药7d,观察至14d。观察期内各用药组和空白对照组所有雏鸡采食、饮水、排便等均正常,未出现不良反应及死亡。观察期结束后分别称重,处死存活雏鸡,眼观病理学检查心、肝、肾、肺、腺胃、肌胃及肠道等组织器官,均未发现明显病理变化;各组日均增重、日均采食量和料重比统计结果显示,与空白对照组相比,0.4%和0.6%增免肽颗粒混饮组日均增重略高,0.4%组的料重比略小,但经卡方检验没有显著性差异(P>0.05),详细结果见表2。因日均采食量为组内平均值,故未作显著性统计分析。
2.2 抗体效价变化 21日龄(21d,首免后第7天)时,3个增免肽颗粒组和阳性药物组的抗体效价显著高于疫苗对照组(P<0.05);28d时,3个增免肽颗粒组的抗体效价最高,显著高于药物对照和疫苗对照组(P<0.05),而后两组之间亦有显著差异(P <0.05);35d和42d时,增免肽颗粒高、中剂量组的抗体效价显著高于其余3组(P<0.05),而低剂量组和药物对照组则显著高于疫苗对照组(P<0.05);由于空白对照组没有免疫,其没得的抗体效价是残留的母源抗体,故不与其他各组作统计学差异分析;这阶段攻毒对照组与疫苗对照组处理完全一样,测得结果基本一致,故亦不再列出统计分析。详细结果见表3。
■
2.3 淋巴细胞增殖的变化 21d(首免后第7天)时,增免肽颗粒高、中剂量组和药物对照组的A570值显著高于其余2组(P<0.05),3组间无显著差异(P>0.05),而增免肽颗粒低剂量组又显著高于疫苗对照组(P<0.05);35d和42d时,增免肽颗粒高、中剂量组的A570值显著高于低剂量组和药物对照组(P<0.05),后2组与疫苗组间亦存在显著差异(P<0.05);与空白对照组相比,所有其他试验组各时间的淋巴细胞增殖都显著高于空白对照组(P<0.05),表明新城疫La Sota苗的免疫对鸡外周血淋巴细胞增殖具有显著促进作用。详细结果见表4。
■
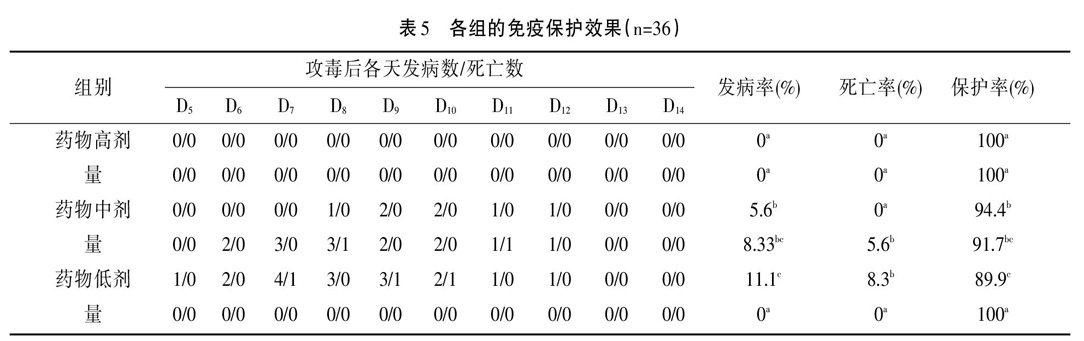
2.4 免疫保护效果 32日龄雏鸡的攻毒后经10d观察发现:107EID50剂量组于攻毒后第4天开始发病,第5天出现死亡,最终死亡率为20.8%;106EID50剂量组于攻毒后第5天发病、出现死亡,最终死亡率为12.5%;105EID50剂量组于攻毒后第7天发病,第8天出现死亡,最终死亡率为4.17%;104EID50剂量组未见发病。因此选择106EID50的NDV-F48E8 0.2ml为攻毒剂量。各计划攻毒组于42日龄经滴鼻点眼攻毒后,除增免肽颗粒高、中剂量组外,其余3组鸡于攻毒后第5天(D5)开始零星出现绿色稀便、精神、饮食下降等发病症状,到第7天时攻毒对照组已死亡1只,各组鸡的具体发病时间、数量和死亡时间、数量详见表5。
死亡鸡剖检,可见新城疫病理变化,如口腔、嗉囊有粘液,鼻孔有干酪样鼻液,气管内有粘性分泌物、黏膜充血出血,腺胃乳头及肠粘膜出血。
至第13天时所有存活鸡全部恢复健康。增免肽颗粒高、中剂量组的免疫保护率达100%,显著高于其余3组(P<0.05),而增免肽颗粒低剂量组的94.4%,略高于药物对照组的91.7%(P>0.05),明显高于攻毒对照组的89.9%(P<0.05),见表5。
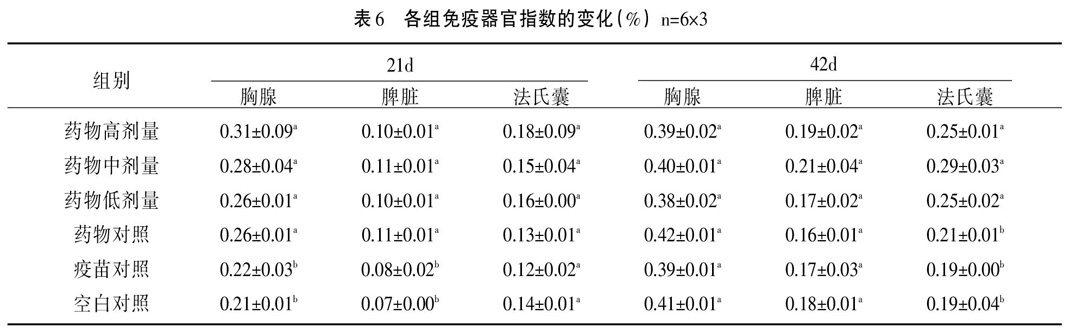
2.5 免疫器官指数 21日龄(21d)时,增免肽颗粒3个剂量组和药物对照组的胸腺指数、脾脏指数显著高于疫苗对照和空白对照组(P<0.05),增免肽颗粒3个剂量组的法氏囊指数均高于其余3组,但无显著性差异;42d时,增免肽颗粒3个剂量组的法氏囊指数均显著高于其余3组(P<0.05),中剂量组的脾脏指数虽明显高于其余各组,但无显著性差异(P>0.05)。因攻毒对照组与疫苗对照组处理完全一样,故没列出统计分析。详细结果见表6。
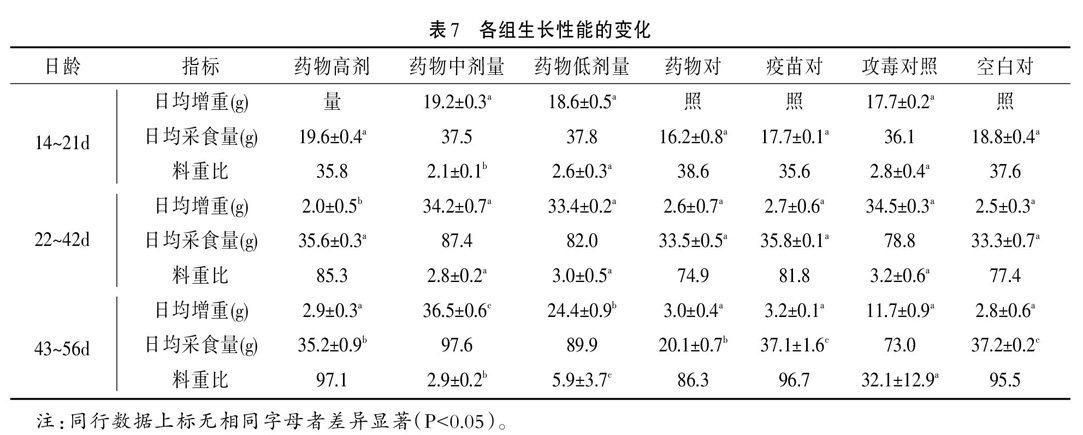
2.6 生长性能的变化 在攻毒前(14~42d),除增免肽颗粒高、中剂量组14~21d时的料重比明显小于各组(P<0.05)外,其余各的日均增重、日均采食量和料重比无显著差异(P>0.05)。但攻毒后(43~56d),增免肽颗粒高、中剂量组的日均增料重比与其余3个攻毒组有差异显著(P<0.05),而与没攻毒的疫苗对照组、空白对照组之间却没有显著差异(P>0.05)。详细结果见表7。
3 讨论
药物耐受性试验结果表明,增免肽颗粒1%以下浓度连续混饮7d,对雏鸡无不良反应和毒性作用,且0.4%以下有明显的促进生长作用。
增强免疫效果试验结果显示,首先增免肽颗粒高、中剂量组的抗体效价和淋巴细胞转化率迅速上升,各观察时间点的抗体效价、淋巴细胞增殖和攻毒保护率最高,明显高于其余各组(P<0.05),增免肽颗粒低剂量组和药物对照组亦显著高于疫苗对照或攻毒对照组;其次增免肽颗粒能显著增加21日龄前胸腺指数、脾脏指数和21~42日龄的法氏囊指数。表明增免肽颗粒可以明显提高新城疫苗的免疫应答。同时也有一定的促进增重和降低料重比作用,以高、中剂量效果最好,与疫苗对照无显著差异;其次是低剂量组和药物对照组则明显优于攻毒对照组。因此,鉴于高、中剂量之间多无显著差异,建议中剂量作为临床应用剂量。
4 结论
增免肽颗粒以1%浓度下连续对雏鸡无不良反应和毒性作用,且0.4%以下浓度混饮有明显的促进生长作用。
增免肽颗粒具有明显的增强免疫作用,推荐中剂量(按0.2%混饮)为临床应用剂量。
(参考文献略)
