大孔树脂回收甘草酸生产废水中有效成分的研究
2015-04-25葛振红田维亮李国柱孟庆艳刘文杰
葛振红 田维亮 李国柱 罗 碧 孟庆艳 刘文杰*
(1 塔里木大学生命科学学院, 新疆 阿拉尔 843300)(2 新疆生产建设兵团塔里木盆地生物资源保护与利用重点实验室, 新疆 阿拉尔 843300)
大孔树脂回收甘草酸生产废水中有效成分的研究
葛振红1,2田维亮1李国柱1,2罗 碧1,2孟庆艳1,2刘文杰1,2*
(1 塔里木大学生命科学学院, 新疆 阿拉尔 843300)(2 新疆生产建设兵团塔里木盆地生物资源保护与利用重点实验室, 新疆 阿拉尔 843300)
研究大孔树脂富集并回收甘草酸生产废水中有效成分的工艺条件。以甘草酸生产废水的OD415及COD值为指标,从7种不同性质的树脂中筛选最佳树脂,对影响其吸附性能的单因素进行考察,并用液相色谱对废水原液和洗脱液回收成分进行定性分析。XDA-8大孔树脂为最佳,在最优工艺条件下,有效成分回收率为76. 07%,COD去除率为76. 49%,色谱分析结果表明洗脱液回收成分与原液的主要成分相同。采用XDA-8大孔树脂回收废水中的有效成分方法简单、高效,具有良好的经济效益和环境效益。
大孔树脂; 回收; 甘草酸; 废水; 有效成分;
甘草是豆科植物,各大药典均有记载。甘草中的化学成分复杂,主要活性成分为甘草酸、甘草次酸等三萜类化合物、黄酮类化合物以及甘草多糖[1-3]。甘草除药用外,还被广泛用于食品、饮料、化工、烟草、印染、酿造、国防等工业中[4]。
甘草酸生产废水是工业提取甘草中甘草酸时酸沉后产生的上清液。废水具有强酸性,化学耗氧量高,色度在1 000倍左右。用生化法不易处理,直接排放污染环境;同时,在废水中含有大量的氨基酸、糖、黄酮等物质,直接排放也造成了资源的严重浪费。甘草酸生产废水的处理及综合利用引起了普遍关注。李祝等[5]用单一絮凝剂,经正交试验确定最佳工艺条件,COD值下降了76. 3%。崔朝亮[6]采用PAC絮凝预处理甘草酸废水,固形物絮凝率为45. 81%,但这些方面仅着眼于废水的处理,对其中有效成分的回收利用没有进行进一步研究。
大孔吸附树脂是一种有机高聚物吸附剂[7-10],具有吸附性能好、效率高、树脂再生容易等优点[11]。树脂吸附法处理有机废水已有大量成功的先例[12-13]。本文采用大孔吸附树脂富集甘草酸生产废水中的成分,考察树脂对有机化合物的吸附能力,确定最佳工艺条件,为后期的研究提供依据。
1 材料与方法
1.1 实验仪器及试剂
仪器:Tu-1810 紫外-可见分光光度计(北京普析通用仪器有限责任公司);BP211D 电子天平(北京赛多利斯有限公司);DK-80 电热恒温水槽、ZDP-250 型振荡培养箱(上海精宏实验设备有限公司);HZ100R 高速冷冻离心机(湖南湘仪实验室仪器开发有限公司);KQ-400KDE 型高功率数控超声波清洗器(昆山市超声仪器有限公司);实验吸附玻璃柱内径1. 5 cm×40 cm(瑞鑫玻璃仪器公司);LC-20AT高效液相色谱仪(日本岛津);GZX-9246 数显鼓风干燥箱(上海博迅实业有限公司医疗设备厂);PHS-3B精密pH计(上海仪电科学仪器有限公司)试剂:XDA-8、D-101大孔吸附树脂(天津海光化工有限公司);AB-8、X-5大孔吸附树脂(西安蓝晓科技有限公司);XAD-7HP、HPD-300、HPD-20大孔吸附树脂(沧州恩宝化工有限公司);硫酸、氢氧化钠、无水乙醇(分析纯,西安化学试剂厂);草酸钠(分析纯,天津致远化学试剂有限公司);高锰酸钾(分析纯,上海市金山县光塔化工厂);甲醇(色谱纯,SIGMA公司)。
1.2 实验材料
实验中所用的甘草酸生产废水直接取自阿拉尔新农甘草公司,运回实验室后冷藏备用。
1.3 检测波长的选择
将甘草酸生产废水原液10 mL 5 000 rpm离心10 min,蒸馏水稀释2倍,用紫外-可见分光光度计在190-800 nm进行光谱扫描,结果如图1所示。
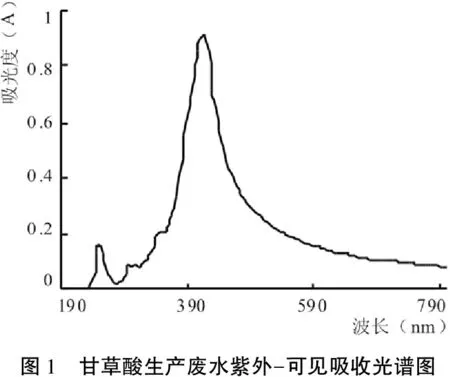
图1 甘草酸生产废水紫外-可见吸收光谱图
从光谱扫描图中可以看出,废水在415 nm处有最大吸收峰。因此,可用415 nm处的吸光度表示废水中成分的含量。分别移取1. 5 mL、2. 0 mL、2. 5 mL、3. 0 mL、3. 5 mL、4. 0 mL、4.5 mL原液定容到10 mL容量瓶中,根据溶液中的可溶性固形物含量可得其浓度分别为0. 225 mg/mL、0. 300 mg/mL、0. 375 mg/mL、0. 450 mg/mL、0. 525 mg/mL、0. 600 mg/mL。以蒸馏水作为参比液,用紫外-可见分光光度计于415 nm处测定系列标准溶液的吸光度。以废水浓度C为横坐标,吸光度A为纵坐标作图得标准曲线,其线性回归方程为:
A = 2. 6103C - 0. 02529 (r2=0. 9992)。
1.4 高效液相色谱(HPLC)分析
色谱柱为waters色谱柱(C18,5 μm,250 mm × 4. 6 mm),柱温为40 ℃,进样量为20 μL。流动相为甲醇-水,梯度洗脱(0 ~10 min,40%~90%甲醇;10 ~12 min,90%~100%甲醇;12 ~15 min,100%甲醇),流速为1 mL / min,检测波长254 nm。
1.5 甘草酸生产废水的pH、色度、COD值及可溶性固形物含量的测定
利用玻璃电极法GB/T6920-1986测定生产废水的pH;“目视稀释倍数法”测定生产废水的色度;GB/T 15456-2008 工业循环冷却水中化学需氧量(COD)高锰酸钾法测定废水的COD值;鼓风干燥箱测定可溶性固形物含量。废水参数见表1。
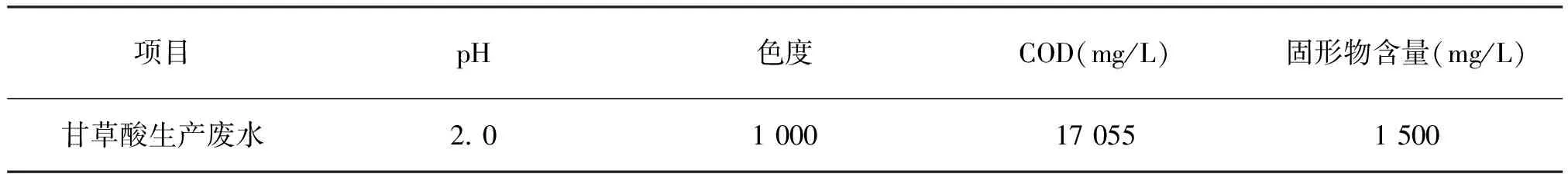
表1 甘草酸生产废水参数
1.6 树脂预处理
将7种树脂分别置于玻璃柱中,用无水乙醇以2~4 BV/h的流速通过树脂层,全部通入后将液面在树脂层上20~30 mm处保留24 h,用蒸馏水冲洗至无醇味。再以同样方法分别用4% HCl和4% NaOH溶液依次冲洗树脂柱,每次操作完冲至中性。
2 结果与讨论
2.1 树脂的筛选实验
称取预处理后的7种湿树脂各2 g分别置于250 mL具塞锥形瓶中,各加入可溶性固形物含量为1. 5 mg/mL的甘草酸生产废水100 mL,置于振荡器上,于25 ℃恒温振荡吸附24 h,每隔1 h取1次样测定有机物的吸光度计算吸附率,并测定COD值,直至测定的数值不再发生变化。吸附平衡后取出树脂,分别加入60 mL 90%乙醇溶液进行解吸。各树脂的吸附率、解吸率、最大吸附量按下式计算:
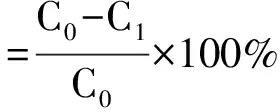
(1)
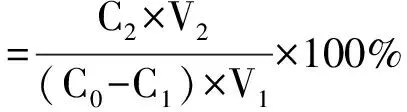
(2)
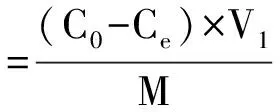
(3)
式中:C0为样液中有机物的初始浓度;C1为吸附后滤液中有机物的浓度;V1为样液体积;C2为解吸液中有机物的浓度;V2为解吸液体积;Ce为吸附平衡后样液中有机物的浓度; M为树脂的质量。
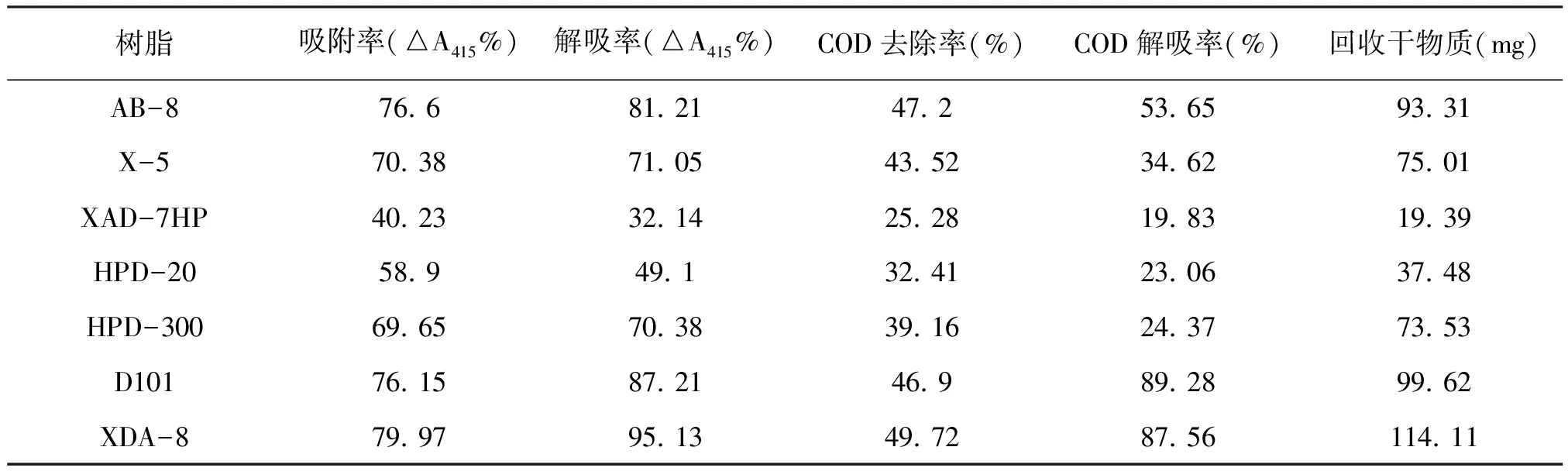
表2 树脂静态吸附-解吸实验结果
由表2可知,XDA-8对废水中有机物的最大吸附率为79. 97%,解吸率为95. 13%;COD去除率为49. 72%,解吸率为87. 56%。干物质回收量为114. 11 mg,优于其它几种树脂。XDA-8 吸附5 h后可达到吸附平衡,1 g湿树脂的最大吸附量为61. 93 mg有机物,处理废水原液量为41. 29 mL。
2.2 pH对树脂静态吸附效果的影响实验
用NaOH将原废水的pH分别调节至2. 0、3. 0、4. 0、5. 0、6. 0、7. 0、8. 0、9. 0,在废水水质、体积(100 mL)相同的条件下,选用确定的树脂2 g,置于振荡器上,以100 r/min的速度恒温振荡至静态吸附平衡,测定吸光度计算吸附率,并测定COD值,计算不同pH下,有机物的吸附率及COD值,确定最佳pH。
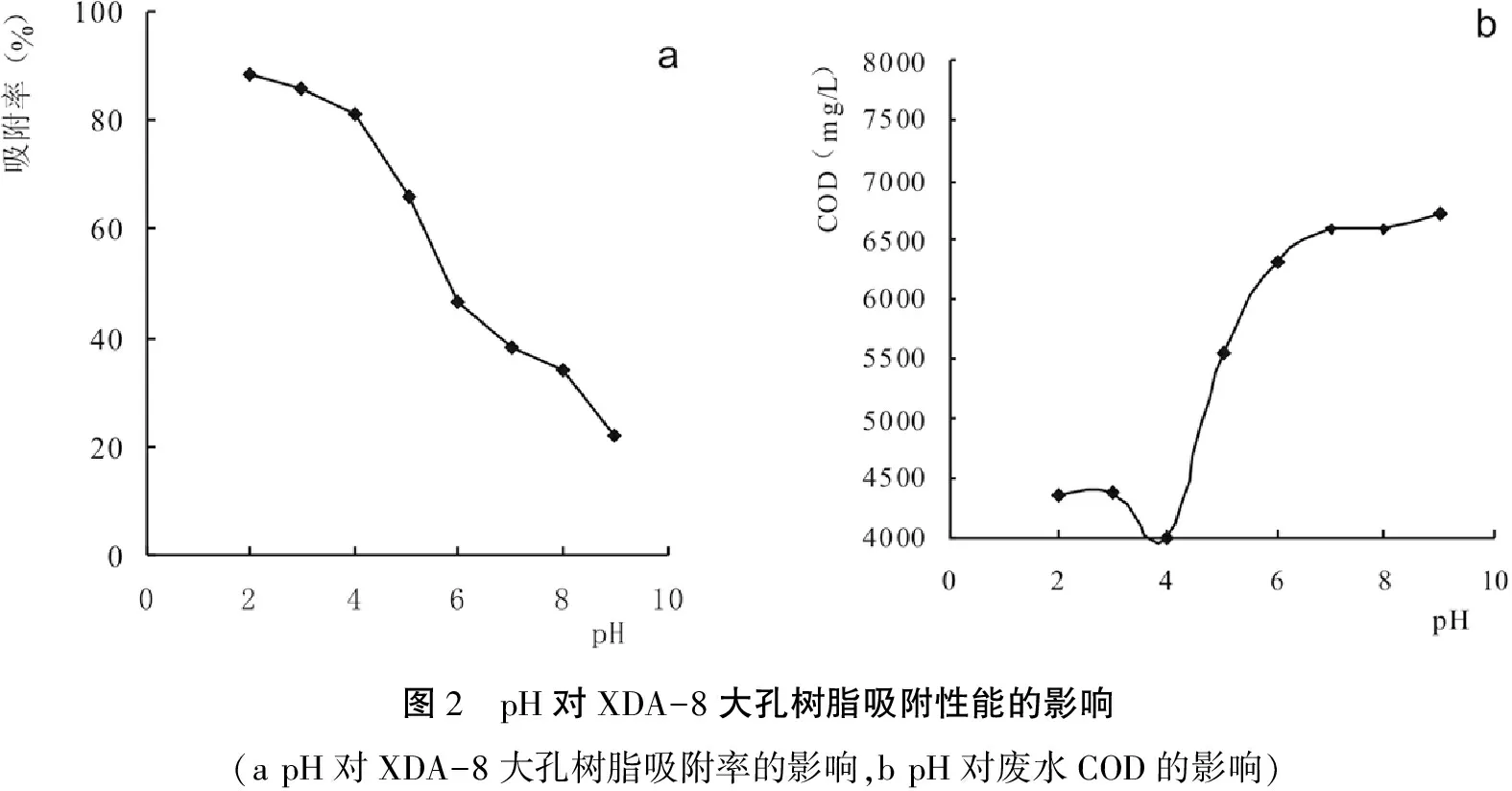
图2 pH对XDA-8大孔树脂吸附性能的影响
溶液的pH会影响大孔树脂的吸附性能,这是因为pH的变化,改变了有机物在溶液中的存在形式;其次,溶液pH变化可以改变有机物在溶液中的溶解度。从图2 a可以看出,pH在2. 0~4. 0范围内时,吸附率缓慢下降;pH在4. 0~9. 0范围内时,吸附率急剧下降。图2 b中在pH为4. 0时,COD值达到最低,为4010. 15 mg/L;但当pH大于4. 0时,COD值急速上升,说明吸附率降低。结果表明,溶液在酸性条件下有利于XDA-8树脂对有机物的吸附和COD的脱除。因此,pH值在2. 0时吸附效果最佳。
2.3 温度对树脂静态吸附效果的影响实验
称取5份预处理好的XDA-8大孔树脂各2. 0 g,均加入pH为2. 0的甘草酸生产废水100 mL,将吸附温度分别调节为25 ℃、30 ℃、35 ℃、40 ℃、45 ℃置于振荡器上,以100 r/min的速度振荡,吸附平衡后测定吸光度和COD值,计算不同温度下样液中有机物的吸附率,确定最佳操作温度。
由图3可以知,在25 ℃~35 ℃之间,随着温度增加,吸附率明显降低,COD值明显增大;35 ℃~45 ℃之间,温度升高,吸附率、COD值的变化趋于平缓。这主要是因为甘草酸生产废水中有机物如黄酮类、皂苷类化合物与树脂是通过分子间作用力吸附的,属物理吸附,温度升高,有机物与树脂间的吸附能力降低;另一方面,温度升高,导致溶液中有机物的溶解度增大,不利于吸附的进行。在实验所选择的温度范围内,最佳吸附温度为25 ℃。
2.4 上样浓度对树脂吸附效果的影响实验
称取6份经过预处理的大孔树脂各20. 0 g装于同规格层析柱中。配制可溶性固形物浓度分别为0. 45 mg/mL、0. 60 mg/mL、0. 75 mg/mL、0. 90 mg/mL、1. 05 mg/mL、1. 20 mg/mL,pH为2. 0的样液上柱,控制流速为2 BV/h,测定流出液的吸光度值计算吸附率,并测定COD值,选择适宜的上样浓度。
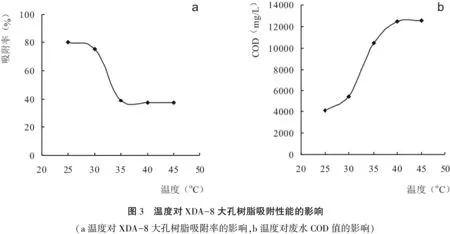
图3 温度对XDA-8大孔树脂吸附性能的影响

图4 上样浓度对XDA-8大孔树脂吸附效果的影响
上样浓度是影响树脂吸附性能的重要因素之一。若上样浓度太低, 在一定流速下, 溶液通过树脂床时流速较快,有机物未被充分吸附就泄漏;若上样浓度过大,则废水粘度较大,不利于有机物的扩散,有些没有吸附就流出来。因此要选择适当的上样浓度。图4表明:上样浓度在0. 45~1. 05 mg/mL范围内,随着上样浓度的增加,吸附率明显增加,废水的COD值下降;上样浓度在1. 05~1. 20 mg/mL范围内时,随着上样浓度的增加吸附率反而下降,COD值明显增高;上样浓度在1. 05 mg/mL时,吸附率达到最大,COD值达到最小值,确定其为最佳上样浓度。
2.5 不同流速下树脂的动态吸附实验
量取3份20 mL湿树脂装于层析柱中,上样流速分别设置为3 BV/h、4. 5 BV/h、6 BV/h ,其它均选取最佳条件,进行甘草酸生产废水的动态吸附实验。测定不同体积流出液的吸光度计算其浓度,测定COD值,绘制泄露曲线。
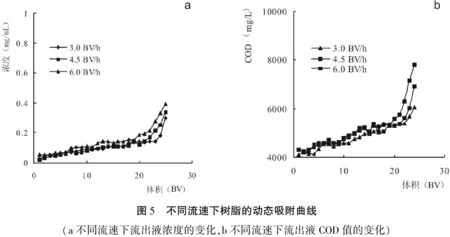
图5 不同流速下树脂的动态吸附曲线
由图5 a可知,树脂的泄漏点所对应的流出液体积分别是23 BV、21 BV、19 BV。流速越快,泄露点越提前。泄漏点的废水处理量随流速的增加而减少,树脂的工作吸附量也相应降低。图5 b可知,在三种流速状态下,流出液COD的初始值较低,随着流出液体积的增加COD值缓慢升高,当达到泄露点时,COD值明显增加。一般来说,在动态吸附实验中,上样流速越低,越有利于吸附质分子进行扩散[14],树脂的吸附效果越好;流速越高,流体停留时间越短,吸附质分子在树脂床中进行扩散越不充分,导致泄漏点提前。从吸附效果考虑,低流速下的操作是有利的,但在实际应用中,综合考虑吸附效果与时间因素,选择操作流速为4. 5 BV/h,最大上样量为21 BV。
2.6 脱附剂浓度的优化
取满负载的树脂2 g置于250 mL具塞锥形瓶中,分别加入20%、30%、40%、50%、60%、70%、80%、90%、100%的乙醇脱附剂,置于振荡器上,以100 r/min的速度振荡,24 h后测定样液的吸光度计算吸附率,并测定COD值,选择最佳脱附剂浓度。(由以上实验结果看出,吸光度与COD值呈相应关系,因此解吸实验只做了吸光度的测定)
由图6可以看出,在浓度20% ~80%范围内,解吸率明显增加,几乎呈线性关系;浓度在80%~90%范围内,解吸率趋于平缓;90%~100%范围内,解吸率不变,在90%时,解吸率达到最大为95. 13%。从解吸效果和经济效益综合考虑,90%为最优的脱附剂浓度。
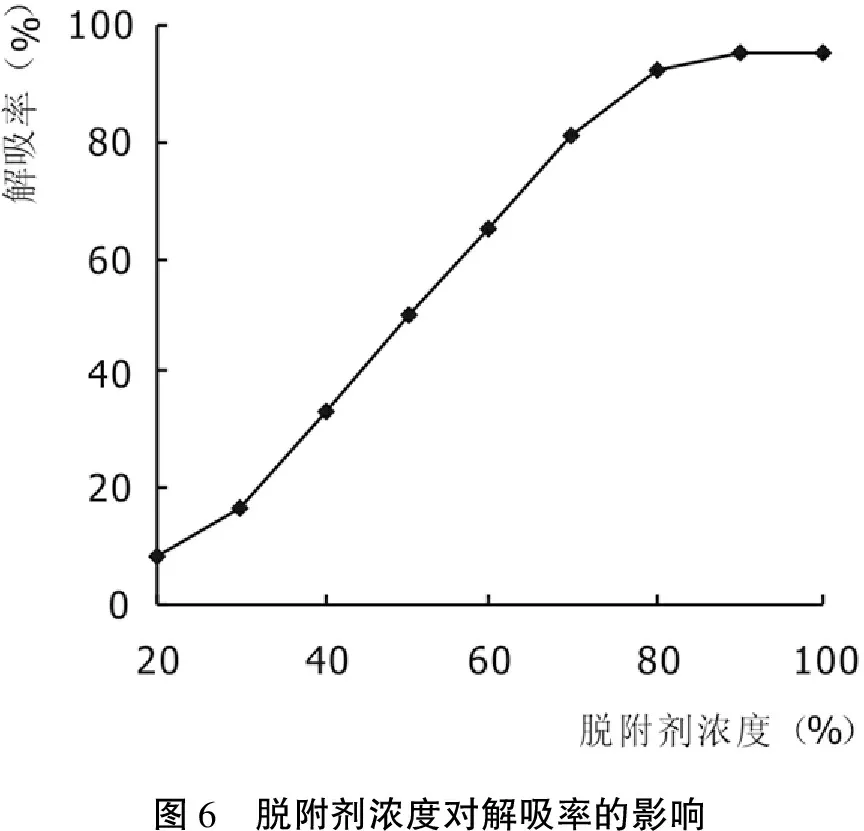
图6 脱附剂浓度对解吸率的影响
2.7 动态解吸实验
动态吸附达到饱和后,加入90%乙醇脱附剂,温度25 ℃,控制流速为3. 0~4. 5 BV/h,分别取1 BV、2 BV、3 BV、4 BV、5 BV、6 BV、7 BV、8 BV、9 BV、10 BV流出液,测定每段流出液的吸光度计算有机物的浓度,绘制解吸曲线,确定脱附剂的最佳用量。
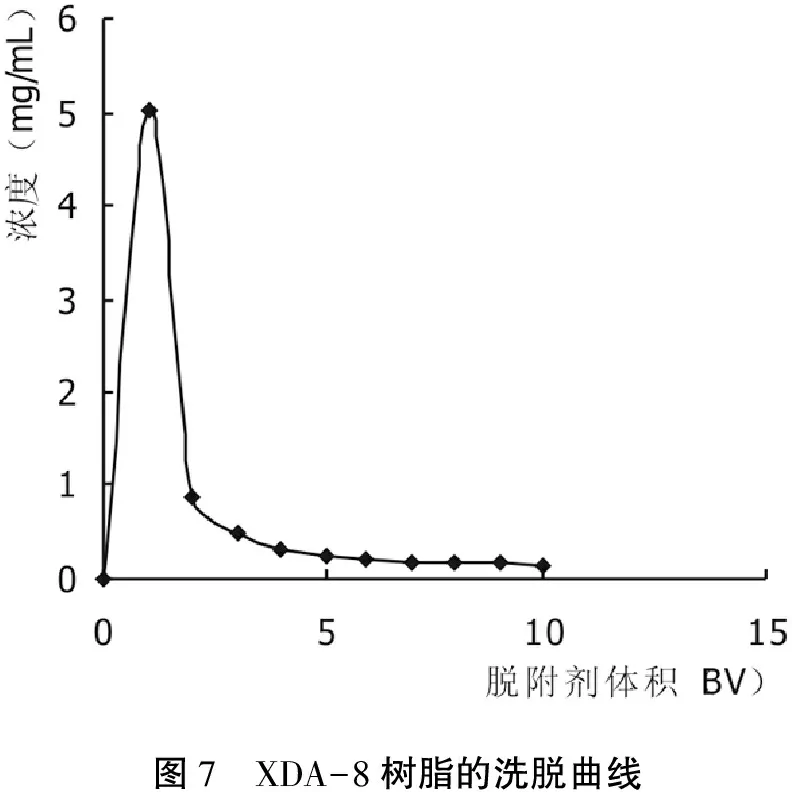
图7 XDA-8树脂的洗脱曲线
由图7可以看出,90%的乙醇作脱附剂,用量1 BV时,有机物的浓度达到5. 05 mg/mL;用量6 BV,几乎可以完全解吸,解吸率可达到95. 1%。,因此,脱附剂的用量在6 BV时为最佳。
2.8 HPLC检测
准确称取废水原液浓缩浸膏、解吸后洗脱液浓缩浸膏各5. 0 mg,用蒸馏水配制成浓度为1. 0 mg/mL的溶液,经0. 45 um的滤膜过滤后,按方法1.4操作条件进样。
如图8所示,用大孔树脂富集甘草酸生产废水中的有效成分,废水原液浓缩浸膏和解吸后洗脱液浓缩浸膏经液相色谱分析主成分相同,表明废水中的有效成分全部回收。说明用XDA-8大孔树脂回收废水中的有效成分是可行的。原液浓缩浸膏中黄酮类化合物的含量为5. 37%,经树脂富集后得到的浸膏中其含量提高了26. 51%。树脂解吸后,用蒸馏水冲至中性,可循环利用,工艺过程简单,成本较低。
3 结论
本论文以甘草酸生产废水为研究对象,通过静态和动态实验,探索了树脂回收有效成分的工艺条件。实验结果表明:XDA-8大孔吸附树脂处理甘草酸废水的效果优于所选的其它树脂;XDA-8树脂处理甘草酸生产废水时,最佳的工艺条件为:pH 2. 0,温度25 ℃,上样浓度为可溶性固形物含量1. 05 mg/mL;在优化的条件下,最大吸附率为79. 97%,有效成分回收率为76. 07% ,COD值从17055 mg/L降至4010. 15 mg/L,去除率为76. 49%;动态吸附的最佳流速为4. 5 BV/h,处理体积为21BV;脱附剂90%的乙醇用量为6BV,脱附率可达到95. 1%。本实验结果表明,用XDA-8大孔树脂回收甘草酸生产废水中的有效成分方法操作简单,树脂再生方便,成本较低,具有良好的经济效益和环境效益。

图8 废水原液中成分与大孔树脂吸附回收成分的比较
[1] Al-Hazimi , HMA, Al-Jaber NA. Phenolic compounds from Glycyrrhiza plants( Leguminosae) review article[J]. Saudi Chem Soc, 2005, 9( 2): 347.
[2] XING Guo-xiu( 邢国秀), LI Nan( 李楠), WANG Tong( 王童), et al. Advances in studies on flavonoids of licorice( 甘草中黄酮类化学成分研究进展)[J]. China Chin Mater Med( 中国中药杂志), 2003, 28 (7): 593.
[3] Zhang Q ,Ye M. Chemical analysis of the Chinese herbal medicine Gan-Cao( licorice)[J]. Chromatogr A, 2009, 1216( 11): 1954.
[4] 张继, 姚健, 丁兰, 等. 甘草的利用研究进展[J]. 草原与草坪. 2000, (2): 12-17.
[5] 李祝, 胡立新, 程亮, 等. 正交试验优选絮凝法处理甘草酸废水的研究[J]. 中草药, 2007, 05: 713-714.
[6] 崔朝亮. 甘草酸的清洁生产工艺研究[D]. 湖北工业大学, 2007.
[7] 聂仁强, 钱孟, 冉启文. 大孔树脂在中药提取工艺中的应用[J]. 基层中药杂志, 2002, 16(6): 59.
[8] 刘国庆, 朱翠, 王占生. 大孔树脂对大豆乳清废水中异黄酮的吸附特性研究[J]. 离子交换与吸附, 2003, 19(3): 229-234.
[9] 潘廖明, 姚开, 贾冬英, 等. 大孔树脂吸附大豆异黄酮特性的研究[J]. 食品与发酵工业, 2003, 29(5): 17-18.
[10] 孙越, 曹喜红, 潘艳丽. 大孔吸附树脂在中草药研究中的应用[J]. 中医药信息,2002,19(2):23-24.
[11] Fu BQ, Liu J, Li H, et al. The application of macroporousresins in the separation of licorice flavonoids and glycyrrhizic acid[J]. Chromatogr A, 2005, 1089(1-2): 18-24.
[12] Sánchez Polo M, Rivera Utrilla J, Prados Joya G, et al. Removal of pharmaceutical compounds, nitroimidazoles, from waters by using the ozone/carbon system[J]. Water Res, 2008, 42(15): 4163-4171 .
[13] Wang Jinnan, Li Aimin, Xu Li, et al. Adsorption studies of tannic acid by commercial ester resin XAD-7[J]. Chinese Journal of Polymer Science, 2010, 28(2): 231-239.
[14] 徐汶, 王为国, 张俊峰, 等. 树脂吸附法豆腐柴叶果胶提取液脱色的研究[J]. 离子交换与吸附, 2005, 21( 4 ):323-328.
Recovery Processing of the Effective Components from Glycyrrhizic Acid Production Wastewater with Macroporous Resin
Ge Zhenhong1,2Tian Weiliang1Li Guozhu1,2Luo Bi1,2Meng Qingyan1,2Liu Wenjie1,2*
(1 College of Life Science, Tarim University, Alar, Xinjiang 843300)
(2 Key Laboratory of Protection & Utilization of Biological Resources in Tarim Basin of Xinjiang Production and Construction Corps, Alar, Xinjiang 843300)
To study the technological parameters of the effective components process from Glycyrrhizic acid production wastewater with macroporous resin. It is showed that the maximum absorption at 415 nm through UV-VIS on Glycyrrhizic acid production wastewater, and then choose the absorbance and COD value as the index. The best resin was selected from 7 different properties macroporous resins, the factors which influence the absorbation performance were investigated, the qualitative of the untreatment wastewater and the recovery components were analyzed by HPLC . XDA-8 resin was screened as the best, the recovery rate of the effective components is 76. 07% and the removal rate of COD is 76. 49% under the optimal condition, result from HPLC showed that the untreatment wastewater and the recovery components have the same main ingredients. Using XDA-8 resin to recovery the effective components from Glycyrrhizic acid production wastewater is feasible. It is showed that the method has good economic benefit and environmental benefit.
macroporous resin; recovery; Glycyrrhizic acid ; wastewater; effective components
201410.28
新疆生产建设兵团科技攻关项目(2011AB030)
葛振红(1978-),女, 汉族,硕士研究生,主要从事天然产物分子结构与功能研究。 E-mail:gzhtlmdx@163.com
*为通讯作者 刘文杰(1973-),男,汉族,硕士,副教授,主要从事天然产物分子结构与功能研究。 E-mail:lury@sina.com
1009-0568(2015)01-0124-08
TQ09
A
10.3969/j.issn.1009-0568.2015.01.022
