新型 4-{4,5-二[(E)-苯乙烯]-1H-咪唑-2-基}苯甲醛共价键连单羟基四苯基卟啉化合物的合成及其分子内能量转移性能*
2015-04-23龙凌亮吴燕俊
龙凌亮,王 林,吴燕俊
(江苏大学科学研究院,江苏 镇江 212013)
具有分子内能量转移性能的有机荧光分子被广泛应用于有机发光材料[1]、太阳能捕获[2]、荧光分子探针[3]以及非线性光学[4]等领域。因此,合成出具备能量转移性质的荧光染料分子引起了科研人员的广泛兴趣,并且已经成为当前的热门研究课题。
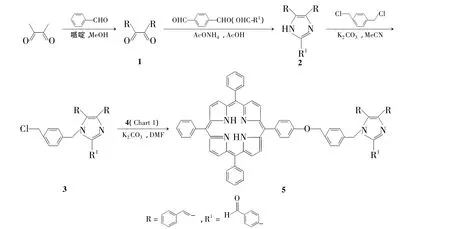
Scheme 1

Chart 1
卟啉及其衍生物是一类特殊的含有四个吡咯结构的大环共轭芳香体系,具有环内电子流动性好,能够提供π-π*电子跃迁等性质[5]。卟啉化合物拥有极好的光学性能,在可见光区域具有很强的光谱吸收能力,能够发出纯的红色荧光,在激光照射下能产生很强的反饱和吸收[6]。在能量转移分子体系中,卟啉基团通常用作能量受体。另一方面,4,5-二[(E)-苯乙烯]-1H-咪唑类化合物是一类具有Y型结构的荧光分子,具有很好的光学性能,常被应用于荧光探针[7]和非线性光学等领域[8]。为研究新型的具备能量转移性质的荧光染料分子,本文以2,3-丁二酮为原料,依次与苯甲醛和对苯二甲醛经缩合反应制得4-{4,5-二[(E)-苯乙烯]-1H-咪唑-2-基)苯甲醛}(2);以对二氯苄作为连接链,2与其经取代反应制得4-{1-[4-(氯甲基)苄基]-4,5-二[(E)-苯乙烯]-1H-咪唑-2-基}苯甲醛(3);3与单羟基四苯基卟啉(4)连接合成了 4-{4,5-二[(E)-苯乙烯]-1H-咪唑-2-基}苯甲醛共价键连单羟基四苯基卟啉化合物(5,Scheme 1),其中2,3和5为新化合物,其结构经1H NMR,MS和元素分析表征。并用荧光光谱研究了5中取代基团3与4之间的能量转移过程。
1 实验部分
1.1 仪器与试剂
XT-4型显微熔点仪(温度未校正);岛津UV 2450型紫外分光光度计;Photon Technology International型高级稳态瞬态荧光测试系统(荧光激发和发射狭缝均为3 nm);Bruker Avance 400型核磁共振仪(CDCl3为溶剂,TMS为内标);Thermo Scientific型质谱仪;Flash EA-1112型元素分析仪。
[[9]方法合成【产率9%,m.p.>300 ℃;1H NMR δ:9.0 ~8.7(m,8H),8.25 ~8.20(m,6H),8.13(d,J=8.8 Hz,2H),7.76(m,9H),7.28(d,J=8.8 Hz,2H),4.14(s,1H),- 2.78(s,2H);MS m/z:631.5{[M+H]+};Anal.calcd for C44H30N4O:C 83.79,H 4.79,N 8.88;found C 83.59,H 4.82,N 8.84】;其余所用试剂均为分析纯;溶剂使用前均按标准方法干燥纯化。
1.2 合成
(1)1,6-二苯基-1,5-二烯-3,4-二酮(1)的合成
氮气保护,在圆底烧瓶中依次加入2,3-丁二酮 0.4 mL(4.5 mmol),苯甲醛 0.92 mL(9 mmol),哌啶2滴以及甲醇5 mL,搅拌下回流反应24 h(溶液变成深黑色)。置冰箱中冷却析晶,过滤,滤饼用少量冷甲醇洗涤,真空干燥得黄色固体1 247.8 mg,产率 21%,m.p.159 ℃ ~161 ℃;1H NMR δ:7.87(d,J=16.4 Hz,2H),7.67(m,4H),7.49(d,J=16.4 Hz,2H),7.44(m,6H);MS m/z:263.2{[M+H]+};Anal.calcd for C18H14O2:C 82.42,H 5.38;found C 82.26,H 5.40。
(2)2的合成
在单口烧瓶中依次加入1 350 mg(1.33 mmol),对苯二甲醛536 mg(4 mmol),乙酸铵2 g(25.9 mmol)和乙酸10 mL,搅拌下于100℃反应50 min。冷却至室温,析出大量沉淀,过滤,滤饼依次用饱和NaHCO3溶液和蒸馏水洗涤,真空干燥得橙红色固体,经硅胶柱层析[洗脱剂:V(乙酸乙酯)∶V(石油醚)=1∶10]纯化得黄色固体2 290 mg,产率 58%,m.p.249 ℃ ~251 ℃;1H NMR(DMSO-d6)δ:12.75(s,1H),10.06(s,1H),8.37(d,J=8.0 Hz,2H),8.06(d,J=8.0 Hz,2H),7.74 ~7.63(m,6H),7.40 ~7.28(m,8H);MS m/z:377.3{[M+H]+};Anal.calcd for C26H20N2O:C 82.95,H 5.35,N 7.44;found C 82.78,H 5.39,N 7.40。
(3)3的合成
在单口烧瓶中依次加入2 209 mg(0.55 mmol),对二氯苄 300 mg(1.71 mmol),碳酸钾200 mg(1.44 mmol)和无水乙腈10 mL,搅拌下回流反应6 h(TCL跟踪)。冷却至室温,过滤,滤液减压浓缩得黄色固体,经硅胶柱色谱[洗脱剂:A=V(二氯甲烷)∶V(石油醚)=1 ∶10]纯化(收集第二色带)得黄色固体3 334.7 mg,产率65%,m.p.>300 ℃;1H NMR δ:10.02(s,1H),7.89(m,2H),7.76(d,J=8.0 Hz,2H),7.64(d,J=16.0 Hz,1H),7.54(d,J=7.6 Hz,1H),7.46(d,J=8.0 Hz,2H),7.37 ~7.31(m,5H),7.30 ~7.17(m,5H),7.12(d,J=8.4 Hz,2H),6.90(d,J=16.0 Hz,1H),6.75(d,J=16.0 Hz,1H),5.29(s,2H),4.60(s,2H);MS m/z:515.2{[M+H]+};Anal.calcd for C34H27N2OCl:C 79.29,H 5.28,N 5.44;found C 79.08,H 5.30,N 5.42。
(4)5的合成
氮气保护,在圆底烧瓶中依次加入4 72 mg(0.114 mmol),3 440 mg(0.82 mmol),碳酸钾240 mg及DMF 6 mL,搅拌下于80℃(浴温)反应24 h(TLC跟踪)。减压蒸除DMF后经硅胶柱色谱(洗脱剂:A=1∶4)纯化得紫色固体5 38 mg,产率 30%,m.p.>300 ℃;1H NMR δ:10.03(s,1H),8.87 ~8.84(m,8H),8.22 ~8.20(m,6H),8.13(d,J=8.4 Hz,2H),7.93(d,J=8.0 Hz,2H),7.82(d,J=8.0 Hz,2H),7.78 ~7.73(m,9H),7.69 ~7.64(m,3H),7.57(d,J=7.6 Hz,2H),7.38 ~7.20(m,13H),6.96(d,J=16.0 Hz,1H),6.85(d,J=16.0 Hz,1H),5.36(s,4H),- 2.76(s,2H);MS m/z:1 109.8{[M+H]+};Anal.calcd for C78H56N6O2:C 84.45,H 5.09,N 7.58;found C 84.12,H 5.13,N 7.54。
2 结果与讨论
2.1 合成
在1的合成中,为了避免使用柱色谱分离,简化纯化步骤,我们将反应后的混合液放置冰箱中冷冻,使产物直接从反应液中析出来。经过简单的抽滤、洗涤、真空干燥后,经过核磁表征,发现1的纯度足够高(98%),可以直接进行下步反应。

表1 r对2产率的影响*Table 1 Effect of r on the yield of 2
在2的合成中,由于对苯二甲醛含有两个醛基,而两个醛基均可以与1中的二酮基团缩合生成咪唑类化合物。为了提高产率,必须控制对苯二甲醛中仅有一个醛基与1中的二酮基团进行缩合反应。实验中,通过调节反应r[n(对苯二甲醛)∶n(1)]来控制其缩合反应,结果见表1。由表1可见,r=3时,产率达58%;进一步提高r,产率提高不明显。因此,最佳的r=3。
2.2 UV-Vis
图1为3~5的UV-Vis谱图。由图1可见,4和5的UV-Vis光谱具有卟啉化合物的特征吸收,在420 nm左右具有一个强的吸收,为soret吸收带,归属卟啉分子a 1μ(π)-eg(π*)的跃迁。同时,在518 nm,553 nm,590 nm及650 nm左右具有四个弱的吸收带,为Q吸收带,归属卟啉的a 2μ(π)- eg(π*)跃迁产生[10]。除此之外,5 在345 nm左右还具有另一个吸收带,与3的吸收光谱相似,是5中所包含的3取代基团的吸收。因此,根据UV-Vis光谱可以进一步确证,5是由3和4键连而成。

图1 3~5的UV-Vis谱图*Figure 1 UV-Vis spectra of 3 ~5
2.3 5分子中能量转移性能
图2和图3为3~5的荧光发射光谱图。当选用420 nm(卟啉的soret吸收带)激发时,4和5都显示出卟啉的特征荧光发射,即一个主要荧光发射峰在651 nm,另外还有一个荧光发射肩峰在710 nm(图 2)。
为了研究5中取代基团3与4之间的能量转移过程,本文选用345 nm(3的λmax)激发5时,可以在458 nm和651 nm分别观察到3和4的荧光发射峰(图3)。然而,与3的荧光发射光谱相比较,5在458 nm的荧光发射呈现出严重淬灭现象。这个现象表明,在5中,激发取代基团3的能量可能被转移。与此同时,相比较于4的荧光发射,5在651 nm的荧光发射强度大大增强。
综合以上现象表明,在5分子中,通过激发取代基团3,能量可以从基团3转移至卟啉基团4上,并发出卟啉的特征荧光。
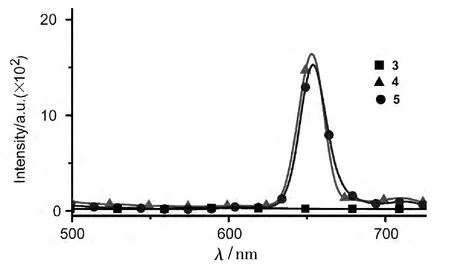
图2 3~5的荧光发射光谱图*Figure 2 Fluorescence emission spectra of 3~5

图3 3~5的荧光发射光谱图*Figure 3 Fluorescence emission spectra of 3~5
3 结论
合成了新化合物4-{4,5-二[(E)-苯乙烯]-1H-咪唑-2-基)苯甲醛(2)。以对二氯苄为连接链,将2与单羟基四苯基卟啉(4)链接起来合成了新化合物 4-{4,5-二[(E)-苯乙烯)-1H-咪唑-2-基)苯甲醛共价键连单羟基四苯基卟啉化合物(5)。
荧光发射光谱研究表明,在5分子中,通过激发取代基团3,能量可以从基团3转移到卟啉基团4上,并发出卟啉的特征荧光。
参考文献
[1]Duan X,Wang J,Pei J.Nanosized π-conjugated molecules based on truxene and porphyrin:Synthesis and high fluorescence quantum yields[J].Org Lett,2005,7(19):4071-4074.
[2]Remón P,Carvalho C P,Baleizão C,et al.Highly efficient singlet-singlet energy transfer in light-harvesting[60,70]fullerene-4-amino-1,8-naphthalimide dyads[J].Chem Phys Chem,2013,14(12):2717 -2724.
[3]Long L,Lin W,Chen B,et al.Construction of a FRET-based ratiometric fluorescent thiol probe[J].Chem Commun,2011,47(3):893 -895.
[4]Zhao X,Yan X,Ma Q,et al.Nonlinear optical and optical limiting properties of graphene hybrids covalently functionalized by phthalocyanine[J].Chem Phys Lett,2013,(577):62 -67.
[5]Xu H J,Mack J,Wu D,et al.Synthesis and properties of fused-ring-expanded porphyrins that were coremodified with group 16 heteroatoms[J].Chem Eur J,2012,18(52):16844 -16867.
[6]Senge M O,Fazekas M,Notaras E G A,et al.Nonlinear optical properties of porphyrins[J].Adv Mater,2007,19(19):2737 -2774.
[7]Zhang M,Li M,Zhao Q,et al.Novel Y-type two-photon active fluorophore:Synthesis and application in fluorescent sensor for cysteine and homocysteine[J].Tetrahedron Lett,2007,48(48):2329 -2333.
[8]Ozturk G,Karakas D,Karadag F,et al.Synthesis and characterization of new Y-shaped fluorophores with an imidazole core[J].J Fluoresc,2012,22(4):1159 -1164.
[9]Adler A D,Longo F R,Finarelli J D,et al.A simplified synthesis for meso-tetraphenylporphyrin[J].J Org Chem,1967,32(2):476 -479.
[10]Wang D J,Zhang J,Shi T,et al.Transition identification of tailed porphyrin-Mn(III)complex in the near-UV and near-IR regions using surface photovoltage spectrum[J].J Photochem Photobiol A,Chem,1996,93(1):21 -25.
