复合光催化剂Cu2(OH)PO4/Ni(OH)2的制备及其光催化性能
2015-04-21于瑞敏陈丽铎
姬 磊,于瑞敏,陈丽铎,姜 震
复合光催化剂Cu2(OH)PO4/Ni(OH)2的
制备及其光催化性能
姬 磊,于瑞敏,陈丽铎,姜 震
(东北石油大学 化学化工学院石油与天然气化工省高校重点实验室,黑龙江 大庆 163318 )
采用水热合成法在Cu2(OH)PO4表面原位沉积Ni(OH)2,制备异质结型的复合光催化剂Cu2(OH)PO4/Ni(OH)2;利用X线粉末衍射仪(XRD)、紫外-可见漫反射光谱仪(UV-Vis-DRS)和扫描电子显微镜(SEM)等,对其相结构、光吸收性能和微观形貌进行表征.结果表明:该复合光催化剂具有良好的紫外光吸收特性,是一类新型的光催化剂.复合光催化剂在紫外光下可以有效降解亚甲基蓝(MB)溶液,当Cu2(OH)PO4与Ni(OH)2的摩尔比为0.2时,Cu2(OH)PO4/Ni(OH)2具有最大催化活性.根据光催化中加入不同活性物种牺牲剂的实验,推测该异质结型材料光催化过程中光生载流子的传输方向及活性物种.Cu2(OH)PO4/Ni(OH)2的催化活性增强主要归结为复合时在两者之间形成有效的异质结,结区的内建电场能够促进光生载流子的分离,同时·OH和h+在光催化降解过程中是主要的活性物种.
Cu2(OH)PO4; Ni(OH)2; 光催化; 异质结; 光催化性能
0 引言
光催化技术具有高效节能和无二次污染等优点,已经成为环境治理和太阳能转化领域的一个重要研究方向[1-3].其中催化剂是提高光催化效率的核心因素,TiO2作为一种常见的光催化剂,虽然具有生物和化学惰性、强氧化能力、低毒和价格低廉等优势,但是也存在一系列问题,如带隙较宽,只能吸收紫外光,对太阳光的利用效率较低;光生电子和空穴的复合率较高,导致其光催化过程量子效率较低等,因而限制它在光催化中的应用[4-6].因此,人们一方面通过对传统半导体光催化剂进行修饰改性,另一方面开发新型半导体光催化剂.Wang H L、Qu Y Q、姬磊等将p型半导体材料与n型半导体材料复合,制得p-n异质结型复合材料,由于在异质结区存在的内建电场能够有效促进光生电子和空穴的分离,从而大大降低两者的复合,使光催化的量子效率得到提高[7-11].
磷酸盐类光催化剂因具有独特的电子结构和优异的光吸收特性而受到人们的关注.其中羟基磷酸铜制备成本低、催化活性高,在工业催化领域是一种重要的苯酚羟基化催化剂,同时在苯乙烯环催化氧化中也表现出良好的催化性能[12-13],而将羟基磷酸铜用于光催化领域的报道还比较少.Cho I S等合成具有纳米3D多层超结构的羟基磷酸铜,在可见光下对亚甲基蓝的脱色性能优于二氧化钛P25和WO3的[14].Wang G等报道羟基磷酸铜在近红外光激发下的光催化活性,它对20 mg/L 的2,4-DCP在6 h内降解接近90%[15].氢氧化镍(Ni(OH)2)的物理和化学性能在锂电池、超级电容器、磁性材料等方面的应用前景[16-18]引起人们的广泛关注,而它在光催化方面的应用甚少,多是作为助催化剂提高光催化性能.Yu J G通过简单的一步沉淀法制备Ni(OH)2-TiO2纳米复合光催化剂,并提高其光催化分解水产氢的活性[19].Cai X Y等合成Ni(OH)2(纳米片)/ZnO(纳米棒) 复合结构,在可见光下对偶氮类染料的光催化降解表明,质量分数为10 % 的Ni(OH)2/ZnO 的光催化活性明显优于纯ZnO的[20].Ran J R 和Chen W等分别采用沉积方法将Ni(OH)2负载到TaON和CdS上,发现它在可见光下光催化分解水的效果明显优于Pt/TaON的[21-22].
文中采用水热合成法制备Cu2(OH)PO4/Ni(OH)2半导体复合光催化材料,并以紫外光下光催化降解染料亚甲基蓝为模型对其性能进行评价.光催化降解实验表明,Cu2(OH)PO4/Ni(OH)2复合材料的光催化性能优于任何一个单体的.笔者在光催化过程中针对不同的活性物种分别加入不同的牺牲剂,分析Cu2(OH)PO4/Ni(OH)2复合光催化剂的催化机理.目前,由这两种半导体制备复合光催化剂的研究还未见报道.
1 实验部分
1.1 主要试剂与仪器
乙酸铜(国药集团化学试剂有限公司生产);磷酸氢二铵(北京化工厂生产);亚甲基蓝(国药集团化学试剂有限公司生产);异丙醇(国药集团化学试剂有限公司生产);甲醇(天津市科密欧化学试剂开发中心生产);对苯醌(上海源叶生物科技有限公司生产).实验用化学试剂均为分析纯,实验用水为膜过滤去离子水.
DMAX-2200型X线衍射仪(日本理学公司生产);ΣIGMA热场发射扫描显微镜(德国Zeiss公司生产);TU-1901双光束紫外可见分光光度计(北京普析通用仪器有限责任公司生产);UV-3010紫外可见分光光度计(日本Hitachi公司生产);LS-55型荧光分光光度计(美国PerkinElmer公司生产).
1.2 实验过程
1.2.1 样品制备
1.2.1.1 Cu2(OH)PO4合成
首先根据Cu∶P(摩尔比)为3∶2称取一定量的 Cu(CH3COO)2和(NH4)2HPO4,将它们分别溶入30 mL蒸馏水中,在常温下磁力搅拌l0 min.将完全溶解的(NH4)2HPO4溶液缓慢滴入Cu(CH3COO)2溶液中并磁力搅拌,立刻生成无定形蓝白色沉淀;然后用CH3COOH(2M) 调节溶液pH=3,在50 ℃温度下磁力搅拌4h.搅拌完毕后,将混合溶液进行超声20 min.将前驱体移取至100 mL聚四氟乙烯内衬的水热反应釜中,置于电热恒温鼓风干燥箱,在100 ℃温度下水热反应4 h,自然冷却至室温并过滤,用乙醇和蒸馏水分别冲洗3次,放入烘干箱,在90 ℃温度下干燥,研磨得到Cu2(OH)PO4.
1.2.1.2 Ni(OH)2合成
称取一定量的Ni(NO3)2·6H2O溶于去离子水,加入浓氨水调节pH至10,磁力搅拌30 min,配成透明的浅绿色溶液.将混合溶液移取至100 mL聚四氟乙烯内衬的水热反应釜中密封,在180 ℃温度下恒温反应36 h,自然冷却至室温.用去离子水洗涤沉淀多次至pH值为中性,放入烘干箱,在80 ℃温度下干燥24 h,得到Ni(OH)2.
1.2.1.3 Cu2(OH)PO4/Ni(OH)2合成
根据Cu∶Ni(掺杂摩尔比)分别为0.1、0.2、0.4、0.8的比例,称取一定量的Cu2(OH)PO4,将它加入硝酸镍溶液,超声震荡10 min并搅拌均匀,其余实验过程同Ni(OH)2的合成,得到不同Cu2(OH)PO4摩尔比的Cu2(OH)PO4/Ni(OH)2复合光催化剂.
1.2.2 催化剂活性评价
采用250 W汞灯为紫外光源,光催化过程中通入循环水使反应体系的温度为25 ℃左右.在反应容器中加入100 mL浓度为1×10-5mol/L的MB溶液和25 mg光催化剂,为了达到吸附—脱附平衡光照前磁力搅拌30 min.打开光源,每隔20 min移取4.0 mL的反应液于离心管,离心沉淀后取上层清液,用可见分光光度计测定它在亚甲基蓝最大吸收波长(λmax=664 nm)处的吸光度.
1.2.3 捕获剂实验
2 结果与讨论
2.1 光催化剂的XRD分析
制备的纯Cu2(OH)PO4、 Ni(OH)2和不同摩尔比的复合材料Cu2(OH)PO4/Ni(OH)2的XRD谱图见图1.由图1可知,Cu2(OH)PO4有较强且窄的衍射峰,表明具有较好的结晶度.Cu2(OH)PO4属于斜方晶系,与标准卡JCPDS NO.83-2264一致.Cu2(OH)PO4特征峰分别对应于(110),(011),(101),(120),(210),(220),(130),(112),(310)等衍射峰.纯Ni(OH)2的衍射峰较宽,晶体结构属于β-Ni(OH)2,为六方晶系,与标准卡JCPDS NO.14-0117一致,每个峰都可以指标化,分别对应于(001),(100),(101),(102),(110),(111)衍射峰,与Chen W和Prathap M U A等的研究结果一致[22-23].随着Cu2(OH)PO4的增加,复合材料的衍射峰变得更加尖锐,表明由Cu2(OH)PO4的增加导致的协同作用有助于表面Ni(OH)2的晶化过程.复合材料中Cu2(OH)PO4的摩尔比从0.1增加到0.4时,并未观察到Cu2(OH)PO4的特征峰,当Cu2(OH)PO4的摩尔比增加到0.8时出现微弱的Cu2(OH)PO4特征峰.这是由于当投入Cu2(OH)PO4后,在其表面原位沉积形成的Ni(OH)2将它包覆在里面,形成核壳结构而导致XRD并未探测到里面的Cu2(OH)PO4,只有当Cu2(OH)PO4的摩尔比足够大时,才能从复合材料的XRD图中观察到其特征峰.
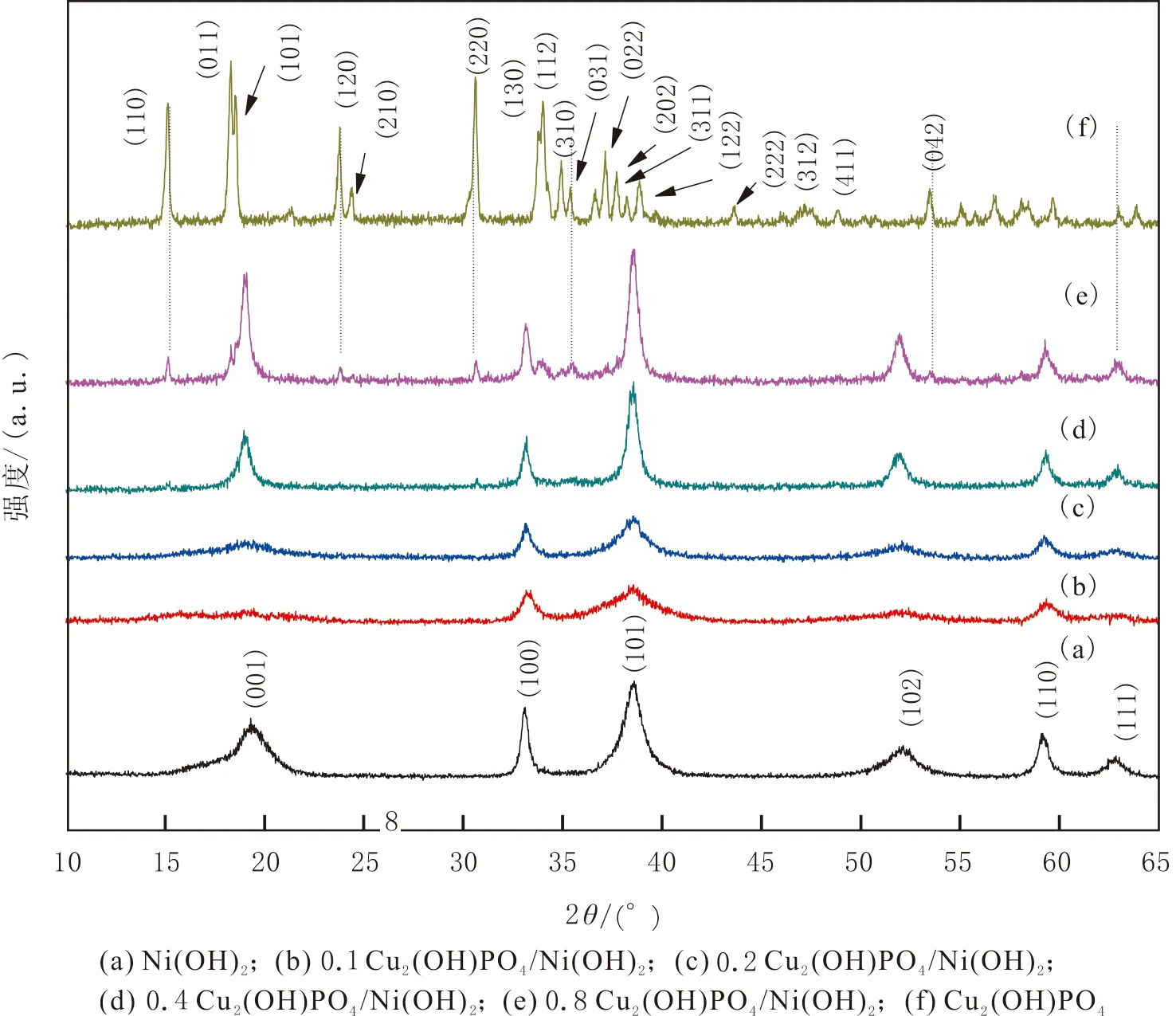
图1 制备样品XRD谱图Fig.1 XRD patterns of the samples
2.2 光催化剂的微观形貌
纯Cu2(OH)PO4、Ni(OH)2和Cu2(OH)PO4/Ni(OH)2异质结构半导体的SEM图见图2.由图2可知,Cu2(OH)PO4为规则的四棱柱状结构,表面光滑且覆有很多细小的Cu2(OH)PO4柱.纯Ni(OH)2为不规则的块状结构,Ni(OH)2的块体表面并不光滑,由细小的纳米片互相交叉而成.由图2(b-c)可知,当在Cu2(OH)PO4表面沉积Ni(OH)2时,复合材料的表面形貌以Ni(OH)2为主,当Cu2(OH)PO4与Ni(OH)2的摩尔比达到0.8时也观察不到Cu2(OH)PO4的特征柱状形貌.这表明所制备的复合材料为Cu2(OH)PO4被Ni(OH)2包覆的结构.由图1可知,制备的复合样品主要以Ni(OH)2的特征衍射峰为主,直到Cu2(OH)PO4的摩尔比达到0.8时才显示特征峰.

图2 制备样品的SEM图Fig.2 SEM images of samples
2.3 光催化剂的光吸收特性
纯Cu2(OH)PO4、Ni(OH)2和Cu2(OH)PO4/Ni(OH)2的紫外—可见漫反射光谱图见图3(a).由图3(a)可知,两种材料在紫外—可见光区显示优异的吸收特性.Ni(OH)2在紫外区有一个非常强的吸收,在可见光区420 nm附近有一个弱吸收带,在可见光区的长波区域也有一定的吸收,甚至延伸到红外光区.
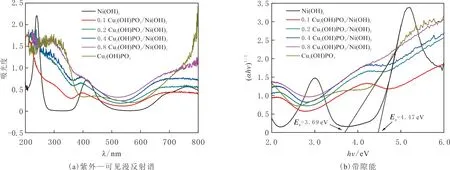
图3 制备样品的紫外—可见漫反射谱和带隙能示意Fig.3 UV-Vis diffuse reflectance spectra and the band gaps (Eg) of different samples
Cu2(OH)PO4也同样在紫外区域存在强的吸收带,在可见光区的长波区域甚至红外光区也有强的吸收.考察两种材料分别在紫外和可见光区的光催化活性,在可见光区的光催化活性均较低,所以重点考察它们在紫外光区的光催化活性.在紫外光区内,Ni(OH)2的吸收带边为272 nm,Cu2(OH)PO4吸收带边扩展到398 nm.随着Cu2(OH)PO4的增加,复合材料Cu2(OH)PO4/Ni(OH)2吸收带边单调红移.计算半导体带隙能的公式:
αhν=A(hν-Eg)n/2,
(1)
式中:α、h、ν、A和Eg分别为吸收系数、普朗克常数、光频率、常数和带隙能.n值由半导体的光学跃迁方式确定,对于Cu2(OH)PO4和Ni(OH)2,n为4.利用(αhν)1/2对(hv)作图得到的Cu2(OH)PO4和Ni(OH)2的带隙能分别为3.69和4.47 eV(见图3(b)).
估算半导体的价带和导带的电势:
EVB=X-Ee+0.5Eg;
(2)
ECB=EVB-Eg,
(3)
式中:X为半导体的电负性,Cu2(OH)PO4和Ni(OH)2值分别为6.38和6.3 eV;Ee为自由电子的氢标电势(约为4.5 eV);EVB和ECB分别为半导体的价带电势和导带电势.经过计算得到Cu2(OH)PO4和Ni(OH)2的EVB分别为3.73和4.04 eV,相应的ECB分别为0.04和-0.44 eV.
2.4 Cu2(OH)PO4/Ni(OH)2的光催化活性
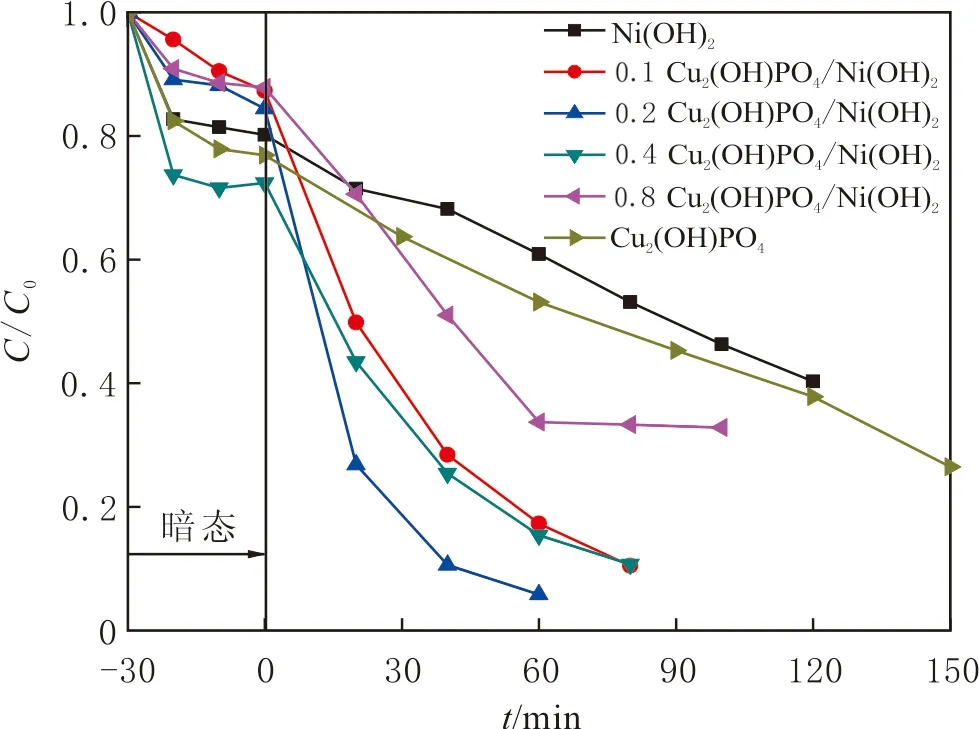
图4 制备样品的暗态吸附及紫外光催化降解MB曲线Fig.4 Dark adsorption and UV light induced photocatalytic degradation of MB over samples
通过紫外光降解水溶液中的亚甲基蓝检测样品的光催化活性,分别给出纯Cu2(OH)PO4、Ni(OH)2和不同摩尔比Cu2(OH)PO4/Ni(OH)2复合光催化材料光催化降解MB曲线(见图4).为了使催化剂和染料达到吸附和脱附平衡,光照前在暗室搅拌30 min.由图4可知,染料与催化剂的吸附和脱附过程在30 min内达到平衡,其中0.2的Cu2(OH)PO4/Ni(OH)2显示最高的光催化活性,60 min内MB几乎完全降解,但吸附能力非常低,表明吸附能力仅仅是决定光催化活性的一个方面,主要因素是材料本身的结构特性.
光催化降解染料的反应属于一级动力学,满足关系式:
(4)

图5 制备样品光催化降解表观速率常数kappFig.5 The kapp of different samples
式中:C0、C分别为反应初始和反应时间为t时MB的浓度;kapp为光催化表观速率常数(min-1).实验得到MB溶液光催化降解的表观反应速率常数kapp见图5.
由图5可知,复合后的样品进行光照后光催化性能均优于纯Cu2(OH)PO4和Ni(OH)2的.当Cu2(OH)PO4摩尔比为0.2时,复合光催化剂的反应速率常数kapp达到最大,远远高于纯Cu2(OH)PO4和Ni(OH)2的,分别为Cu2(OH)PO4和Ni(OH)2的6.7和7.9倍.为了验证两种材料的复合效果,把Cu2(OH)PO4和Ni(OH)2按照摩尔比0.2机械混合得到的样品记为0.2 Cu2(OH)PO4-Ni(OH)2,在相同的实验条件下与0.2 Cu2(OH)PO4/Ni(OH)2进行光催化对比实验,结果见图6.
由图6可知,当把两种单体机械混合后,其光催化效率对于纯样品Cu2(OH)PO4和Ni(OH)2只有微弱提高,而通过化学合成复合的光催化效率有明显提高.这说明制备的复合材料在Cu2(OH)PO4和Ni(OH)2之间形成异质结,其内建电场降低光生电子和空穴的复合,使两者得到更有效的分离,材料的光催化活性大幅提高.

图6 0.2机械混合与复合样品暗态吸附及紫外光催化降解MB曲线及光催化降解表观速率常数Fig.6 Dark adsorption, UV light induced photocatalytic degradation of MB and the kapp of the 20% mechanical mixture and chemical composite
3 光催化机理

图7 不同牺牲剂对样品0.2 Cu2(OH)PO4/Ni(OH)2表观反应速率常数的影响Fig.7 kapp values of 0.2 Cu2(OH)PO4/Ni(OH)2 with different quenchers

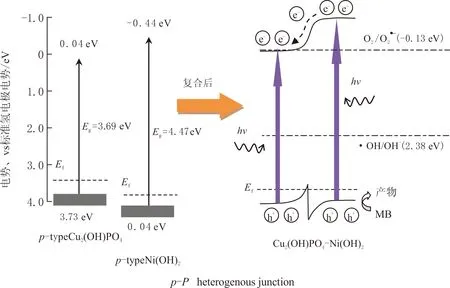
图8 紫外光下Cu2(OH)PO4/Ni3(PO4)2同型异质结构光生载流子传输示意Fig.8 Diagram of the proposed charge separation process of Cu2(OH)PO4/Ni3(PO4)2 heterostructures under UV light irradiation
4 结束语
[1] 陈颖,崔明军,王宝辉,等.光催化氧化降解水中聚丙烯酰胺的可行性研究[J].大庆石油学院学报,2001,25(2):84-86.Chen Ying, Cui Mingjun, Wang Baohui, et al.Study on the photocatalytic oxidation of oily sewage [J].Journal of Daqing Petroleum Institute, 2001,25(2):84-86.
[2] Hoffmann M R, Martin S T, Choi W, et al.Environmental applications of semiconductor photocatalysis [J].Chem Rev, 1995,95:69-96.
[3] Fujishima A, Honda K.Electrochemical photolysis of water at a semiconductor electrode [J].Nature, 1972,238:37-38.
[4] 吴红军,肖同欣,高杨,等.蜂窝状二氧化钛纳米管阵列的制备及光催化性能[J].东北石油大学学报,2013,37(4):93-97.Wu Hongjun, Xiao Tongxin, Gao Yang, et al.Preparation of honeycombed titanium dioxide nanotube arrays and investigation of its photocatalytic activity [J].Journal of Northeast Petroleum University, 2013,37(4):93-97.
[5] Linsebigler A L, Lu G, Yates J T.Photocatalysis on TiO2surfaces: Principles, mechanisms, and selected results [J].Chem Rev, 1995,95:735-758.
[6] 吴红军,高杨,王洋,等.蝶翅状Ag/TiO2NTs的制备及气相光催化性能研究[J].东北石油大学学报,2014,38(4):80-85.Wu Hongjun, Gao Yang, Wang Yang, et al.Study of butterfly-wing shaped Ag/TiO2NTs and gas phase photocatalytic activity [J].Journal of Northeast Petroleum University, 2014,38(4):80-85.
[7] Wang H L, Zhang L S, Chen Z G, et al.Semiconductor heterojunction photocatalysts: Design, construction, and photocatalytic performances [J].Chem Soc Rev, 2014,43:5234-5244.
[8] Qu Y Q, Duan X F.Progress, challenge and perspective of heterogeneous photocatalysts [J].Chem Soc Rev, 2013,42(7):2568-2580.
[9] 姬磊,王浩人,于瑞敏.p-n异质结型光催化剂BiOBr/NaBiO3的制备与可见光催化活性[J].高等学校化学学报,2014,35(10):2170-2176.Ji Lei, Wang Haoren, Yu Ruimin.Preparation, Characterization and visible-light photocatalytic activities ofp-nheterojunction BiOBr/NaBiO3composites [J].Chem.J.Chinese Universities, 2014,35(10):2170-2176.
[10] 姬磊,于瑞敏,王浩人,等.异质型BiOI/NaBiO3光催化剂的合成及其光催化性能[J].无机化学学报,2015,31(3):521-528.Ji Lei, Yu Ruimin, Wang Haoren, et al.Synthesis of heterojunction type BiOI/NaBiO3photocatalyst and enhanced photocatalytic Activities [J].Chinese Journal of Inorganic Chemistry, 2015,31(3):521-528.
[11] 姬磊,于瑞敏,王浩人,等.BiOCl/NaBiO3复合材料的原位合成及光催化性能[J].高等学校化学学报,2015,36(3):551-558.Ji Lei, Yu Ruimin, Wang Haoren, et al.In-situ synthesis of BiOCl/NaBiO3composites and their photocatalytic activities [J].Chinese Journal of Inorganic Chemistry, 2015,36(3):551-558.
[12] Xiao F S, Sun J M, Yu R B, et al.Synthesis and structure of copper hydroxyphosphate and its high catalytic activity in hydroxylation of phenol by H2O2[J].J Catal, 2001,199:273-281.
[13] Meng X J, Lin K, Yang X, et al.Catalytic oxidation of olefins and alcohols by molecular oxygen under air pressure over Cu2(OH)PO4and Cu4O(PO4)2catalysts [J].J Catal, 2003,218:460-463.
[14] Cho I S, Kim D W, Lee S, et al.Synthesis of Cu2(OH)PO4hierarchical superstructures with photocatalytic activity in visible light [J].Adv Funct Mater, 2008,18:2154-2162.
[15] Wang G, Huang B B, Ma X C, et al.Cu2(OH)PO4, a near-infrared-activated photocatalyst [J].Angew Chem Int Ed, 2013,52:4810-4813.
[16] Xu Y H, Feng Q, Kajiyoshi K, et al.Hydrothermal syntheses of layered lithium nickel manganese oxides from mixed layered Ni(OH)2manganese oxides [J].Chem Mater, 2002,14:3844-3851.
[17] Sun Z P, Lu X M.A solid-state reaction route to anchoring Ni(OH)2nanoparticles on reduced graphene oxide sheets for supercapacitors [J].Ind Eng Chem Res, 2012,51:9973-9979.
[18] Lee J W, Ko J M, Kim J D.Hierarchical microspheres based on α-Ni(OH)2nanosheets intercalated with different anions: Synthesis, anion exchange, and effect of intercalated anions on electrochemical capacitance [J].J Phys Chem C, 2011,115:19445-19454.
[19] Yu J G.Enhanced photocatalytic H2-production activity of TiO2by Ni(OH)2cluster modification [J].J Phys Chem C, 2011,115:4953-4958.
[20] Cai X Y, Cai Y, Liu Y J, et al.Photocatalytic degradation properties of Ni(OH)2nanosheets/ZnO nanorods composites for azo dyes under visible-light irradiation [J].Ceramics International, 2014,40:57-65.
[21] Ran J R, Yu J G, Jaroniec M.Ni(OH)2modified CdS nanorods for highly efficient visible-light-driven photocatalytic H2generation [J].Green Chem, 2011,13:2708-2713.
[22] Chen W, Chu M C, Gao L, et al.Ni(OH)2loaded on TaON for enhancing photocatalytic water splittingactivity under visible light irradiation [J].Appl Surf Sci, 2015,324:432-437.
[23] Prathap M U A, Satpati B, Srivastava R.Facile preparation of β-Ni(OH)2-NiCo2O4hybrid nanostructure and its application in the electro-catalyticoxidation of methanol [J].Electrochim Acta, 2014,130:368-380.
[24] 虞丽生.半导体异质结物理[M].2版.北京:科学出版社,2006.Yu Lisheng.Physics of semiconductor heterojunction [M].2nd ed.Beijing: Science Press, 2006.
2015-06-04;编辑:陆雅玲
黑龙江省普通高等学校青年学术骨干支持计划项目(1251G002)
姬 磊(1977- ),女,博士,副教授,主要从事光催化材料的制备、表征及光催化机理方面的研究.
O643.31
A
2095-4107(2015)04-0095-08
DOI 10.3969/j.issn.2095-4107.2015.04.012
