离子色谱法同时测定卷烟主流烟气中氨和烟碱的含量
2015-03-28王永梅张昌壮刘丽竹张玉璞高文全
王永梅,张昌壮,刘丽竹,张玉璞,高文全
(吉林省烟草产品质量监督检验站,长春 130033)
氨是卷烟烟气中一种主要化学成分,对控制卷烟吃味和劲头有重要作用,但过量的氨会刺激人体的呼吸系统。氨既是霍夫曼清单44种烟气有害成分之一,也是我国烟草行业评价卷烟危害性的重要指标[1]。我国烟草行业标准 YC/T 377–2010 采用离子色谱法测定卷烟主流烟气中的氨,但在实际样品测试过程中,铵离子峰存在拖尾现象。马雁军等[2]采用CS16分析柱代替CS12A柱进行测定,实现了实际样品中铵离子与甲胺、乙胺离子峰的真正分离,得到了满意的分析结果。烟碱是烟草中特有的物质之一,卷烟烟气中的烟碱与吸烟成瘾性有重要关系[3]。目前国内外测定烟碱主要采用液相色谱法[4–5]和气相色谱法[6–7],GB/T 23355–2009 采用气相色谱法测定卷烟总粒相物中烟碱的含量。因为烟碱由一个吡啶环和一个氢化吡咯环构成,属二级弱碱,可以捕获两个质子[8–9]。Ayers等[10]采用离子色谱法测定了水中烟碱的含量,利用紫外检测器进行检测。目前还没有采用离子色谱和电导检测器测定烟碱的报道,笔者首次采用离子色谱法同时测定卷烟主流烟气中氨和烟碱的含量,不仅解决了氨测定中峰拖尾的问题,同时为烟碱的测定提供了一种新的参考方法。
1 实验部分
1.1 主要仪器与试剂
离子色谱仪:ICS 5000型,配有自动进样器,电导检测器,阳离子抑制器,美国Dionex公司;
吸烟机:SM 450型,英国Cerulean公司;超纯水器:Synergy UV型,法国Millipore公司;电 子 天 平:BS124S型,感 量 0.1 mg,德 国Sartorius公司;
回旋式振荡器:HY–5型,江苏省金坛市金城国胜实验仪器厂;
盐酸:优级纯,北京化工厂;
铵离子标准溶液:1 000 μg/mL,国防科技工业应用化学一级计量站;
烟碱标准品:20 mg/支,国家烟草质检中心;卷烟样品:市场随机抽样;
实验用水为超纯水(电阻率为18 MΩ·cm)。
1.2 样品处理方法
使用直线型吸烟机,每孔道抽吸4支卷烟,在捕集阱内加入20 mL的10 mmol/L盐酸,按照GB/T 19609规定要求进行抽吸。抽吸完后,将44 mm滤片放入50 mL萃取瓶中,使用四分之一滤片(44 mm)擦拭捕集器,一起置于萃取瓶中,加入20 mL 的 10 mmol/L 盐酸。以 160 r/min振荡萃取30 min。萃取完成后,从捕集阱和萃取瓶中各移取5 mL溶液置于容量瓶中,定容至25 mL,取定容液过0.45 μm的水相滤膜,装入色谱瓶待离子色谱分析。空白样品完全按照前述方法制备,抽吸时卷烟不点燃。
1.3 色谱条件
色谱柱:IonPac CS17阳离子分析柱(250 mm×4 mm,美国Dionex公司),IonPac CG17阳离子保护柱(50 mm×4 mm,美国Dionex公司);抑制电流:74 mA;流速:1.0 mL/min;流动相:梯度洗脱,0~13.5 min,1.5 mmol/L 甲磺酸 –0.5% 乙腈混合溶 液 (99.5∶0.5),13.5~28 min,25 mmol/L甲 磺酸 –0.5% 乙腈 混合 溶 液 (99.5∶0.5),28~30 min,1.5 mmol/L 甲 磺 酸 –0.5% 乙 腈 混 合 溶 液(99.5∶0.5);柱温:40℃;检测器温度:40℃;进样体积:25 μL。
2 结果与讨论
2.1 样品处理方法的优化
2.1.1 烟气捕集效率
为验证主流烟气中氨和烟碱的捕集效率,串联三只捕集瓶,每瓶中加入20 mL的10 mmol/L盐酸,抽吸结束后,分别取三只捕集瓶中溶液,用离子色谱法测定铵和烟碱含量。由于分布在气相中的氨比例很低,而烟碱主要存在于粒相物中[11],因此不经稀释直接对捕集液进行测定,平行测定了3个样品,均只在第一个捕集瓶中有氨检出,含量分别为0.28,0.30,0.27 μg/cig,而烟碱在所有捕集瓶中含量均低于检测限。该实验结果表明,在系统中串接1个捕集瓶能够完全捕集主流烟气气相中的氨和烟碱。
2.1.2 盐酸浓度对萃取效率的影响
使用酸性溶液提取时,萃取液中烟碱存在状态更为稳定[4],而 YC/T 377–2010 中使用盐酸溶液提取主流烟气粒相物中的铵,因此选择盐酸溶液作为铵和烟碱的萃取试剂。分别用浓度为1,5,10,15,20 mmol/L的盐酸溶液进行试验,考察其对氨和烟碱萃取效率的影响,其它条件不变,每种盐酸浓度下平行测定3次,结果见表1。由表1可知,盐酸浓度对烟碱的萃取效率无明显影响,而盐酸浓度从1 mmol/L增大到10 mmol/L时,氨萃取效率呈增大趋势,盐酸浓度进一步增加时,氨萃取效率无明显改善,因此本方法采用10 mmol/L盐酸作为萃取液。2.1.3 萃取时间对萃取效率的影响

表1 不同浓度盐酸对萃取效率的影响
总粒相物中氨和烟碱的萃取一般采用振荡萃取的方式,其含量随萃取时间增大而升高。分别考察了 10,20,30,60,120 min 振荡萃取时间下,氨和烟碱浓度的变化情况,结果见表2。由表2可知,氨和烟碱萃取量随时间增加而升高,但在20 min以后变化趋于平缓,故选择萃取时间为30 min。
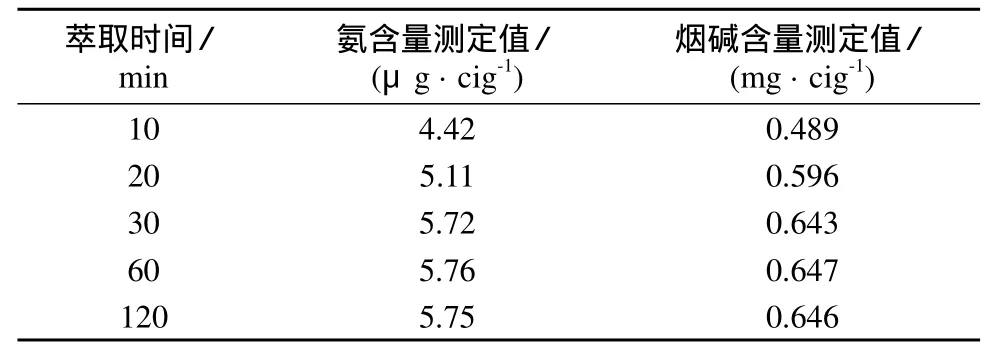
表2 不同萃取时间对萃取效率的影响
2.2 色谱条件优化
2.2.1 色谱柱和淋洗液的选择
卷烟烟气组成成分复杂,常见阳离子钠、钾、钙含量较高且响应灵敏,容易干扰氨和烟碱测定,烷基胺如甲胺、乙胺等干扰铵离子测定。根据文献[12],选择IonPac CS17阳离子分析柱,在甲磺酸梯度淋洗条件下,能有效分离铵、烷基胺、生物碱和碱金属、碱土金属离子。由于铵离子保留较弱,淋洗液浓度较低时分离度较好,烟碱离子保留较强,需要较高的淋洗液浓度,因此选用梯度洗脱,为改善色谱峰形,在淋洗液中添加0.5%乙腈作为基体改进剂,同时乙腈还具有清洗色谱柱的作用。
2.2.2 色谱分离和检测温度
温度对离子色谱分离选择性有明显影响,IonPac CS17阳离子分析柱推荐在较高温度下(40℃)使用。固定淋洗液浓度及淋洗程序,改变柱温和检测温度,进样测定混合标准溶液中铵和烟碱的保留时间、峰面积、峰宽和塔板数。试验结果表明,当检测温度从20℃升高到40℃时,铵和烟碱的保留时间、峰宽和峰面积均有减小的趋势,铵和钠离子的分离度明显增大,烟碱峰的理论塔板数明显增大。这说明升高温度会改善色谱分离情况,但会牺牲目标峰响应灵敏度,因此本实验未对40℃以上情况进行考察,最终选择柱温和检测温度均为40℃条件下进行分离测定。
2.2.3 干扰试验
分别在样品中添加了5.0 μg/mL的Na+,K+,Ca2+,Mg2+,其中Na+在氨之前出峰,K+在烟碱之前出峰,Ca2+和Mg2+均在烟碱之后出峰,均不干扰测定。根据文献[12],在选定的色谱条件下,甲胺、乙胺均在铵离子以后出峰,不影响检测。标准溶液、典型样品溶液色谱图分别见图1、图2。
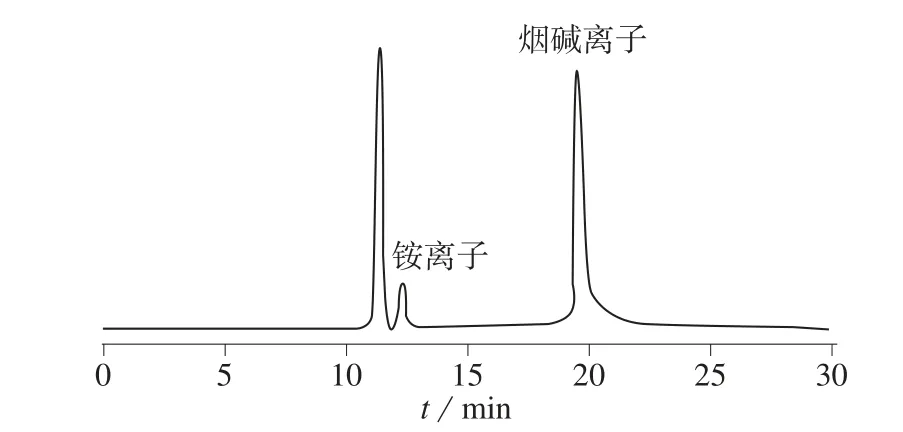
图1 标准溶液离子色谱图
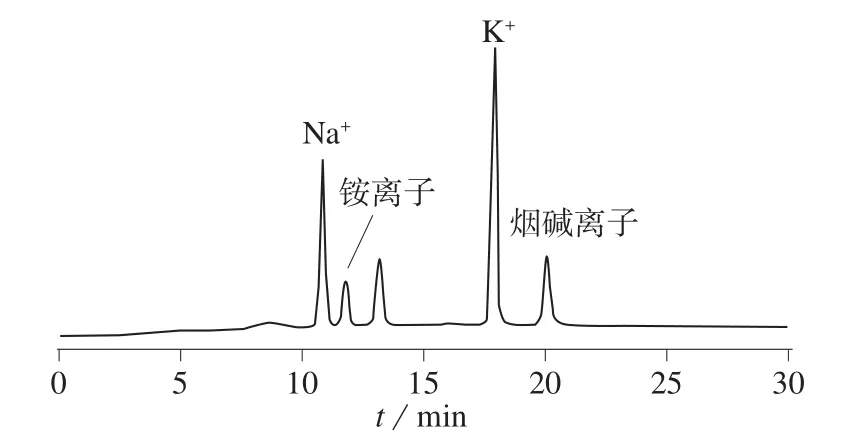
图2 样品溶液离子色谱图
2.3 方法学考察
2.3.1 方法的线性范围、检出限和定量限
铵系列标准溶液的质量浓度分别为0.1,0.3,0.5,0.7,1.0 μg/mL,烟碱系列标准溶液的质量浓度分别为 20,60,100,140,200 μg/mL。用色谱峰面积(Y)对浓度(x,μg/mL)进行线性拟合,结果见表3。依据YC/T377-2010,以浓度最低的标准溶液,重复进样10次,计算测定值的标准偏差,以3倍标准偏差作为方法的检出限、以10倍标准偏差作为方法的定量下限,结果见表3。由表3可知,方法的线性和检出限完全满足卷烟主流烟气中氨和烟碱释放量的检测要求。
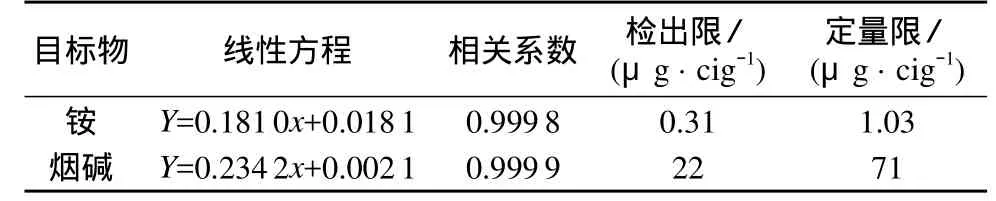
表3 铵、烟碱的线性方程、相关系数和检测限、定量限
2.3.2 方法的回收率
方法的回收试验采用基质加标法,以10 mmol/L HCl做溶剂,配制铵含量分别为0.5,1.0,1.5和烟碱含量分别为60,120,180 μg/mL的混合标准溶液作为加标萃取液,将标样加在样品萃取液中进行回收试验,结果见表4。由表4可知,方法的加标回收率为96.7%~104.9%,说明该方法具有良好的准确度。

表4 方法的加标回收率
2.3.3 精密度试验
按照1.2方法对样品进行前处理,按1.3色谱条件直接在离子色谱仪上进样分析,外标法定量。对典型的卷烟样品溶液重复处理5次,分别进样测定,结果见表5。由表5可知,铵和烟碱相对标准偏差分别为1.86%和2.23%,表明方法具有良好的重现性。

表5 精密度试验结果
2.4 实际样品测试结果
选用10种市售卷烟,涵盖了烤烟型和混合型及不同焦油含量,采用本方法(N)和标准方法(S)同时进行测定,其中,卷烟主流烟气中氨的测定采用YC/T 377–2010标准方法,烟碱的测定采用GB/T 23355–2009标准方法(气相色谱法),测试结果见表6。由表6可知,采用本方法同时测定卷烟主流烟气中氨和烟碱的含量,其测试结果与采用标准方法分别测定氨和烟碱的含量无显著性差异,说明本方法准确、可靠。
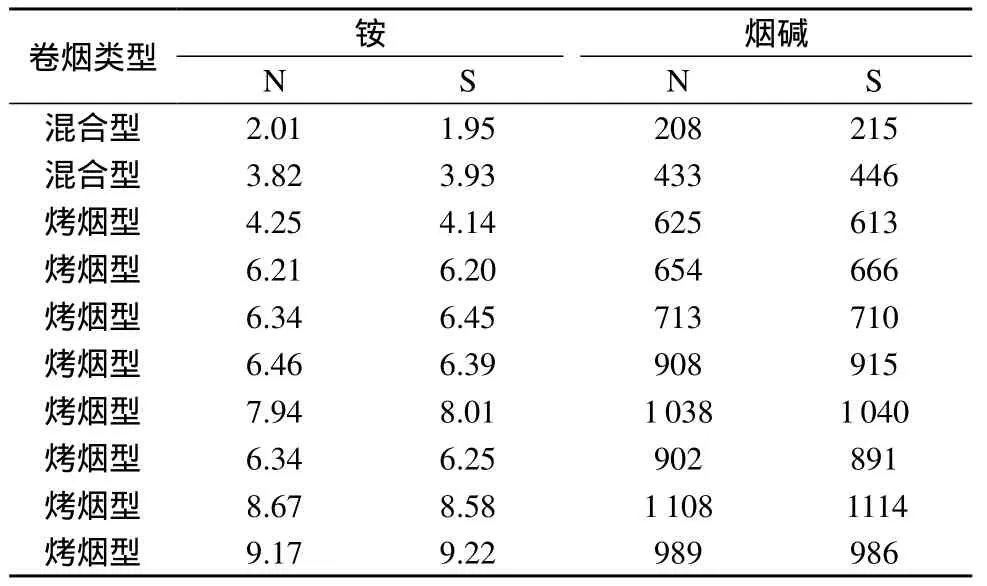
表6 实际样品含量测定结果 μg/cig
3 结语
建立了卷烟主流烟气中铵和烟碱的离子色谱测定方法,相较于标准YC/T 377–2010,在测定主流烟气中氨的含量时,使用CS17阳离子分析柱代替CS12A色谱柱,采用更低的流动相浓度和更高的检测温度,取得了更好的分离效果;相较于传统测定主流烟气中烟碱的方法,该方法检测过程中几乎不使用有机试剂。对市售卷烟样品的测定结果表明,优化的样品前处理方法和检测方法能有效去除干扰。该方法便捷、灵敏、准确可靠,可同时测定多种组分,实用性强。
[1] 谢剑平,刘惠民,朱茂祥,等.卷烟烟气危害性指数研究[J].烟草科技,2009(2): 5–15.
[2] 马雁军,易小丽,李娜,等.改进的离子色谱法用于卷烟主流烟气中氨的测定[J].烟草科技,2012(4): 1–9.
[3] Stein E A,Pankiewicz J,Harsch H H,et al. Nicotine-induced limbic cortical activation in the human brain: a functional MRI study[J]. Am J Psychiatry,1998,155(8): 1 009–1 015.
[4] 黄祝传,朱子高,罗家基,等.用HPLC法测定卷烟总粒相物及烟碱盐中的烟碱含量[J].烟草科技,1997(4): 29–30.
[5] 周一万,陈安良,郝双红,等.反相离子对高效液相色谱法分析混剂中的烟碱研究[J].农药科学与管理,2004,26(7): 6–7.
[6] 罗崇光,莫启武,李杰明.气相色谱/质谱法测定烟用香精和料液中的烟碱含量[J].烟草科技,2012(5): 48–50.
[7] 韩书磊,陈欢,刘彤,等.气相色谱法分析电子烟烟液中主要生物碱含量[J].分析科学学报,2015,31(4): 494–498.
[8] Dixon M,Lambing K,Seeman J I,et a1. On the transfer of nicotine from tobacco to the smoker.A brief review of ammonia and “pH”factors[J]. Beitr Tabakforseh Int,2000,19(2): 103–113.
[9] 吴继忠,戴莉,徐清泉,等.烟碱形态与卷烟烟气粒相物pH的关联性研究[J].湖南农业大学学报:自然科学版,2014,40(3):253–256.
[10] Ayers G P,Selleck P W,Gillett R W,et al. Determination of nicotine in water by gradiention chromatography[J]. Journal of Chromatography A,1998,824(2): 241–245.
[11] Nanette A,Stevens,Michael F Borgerding. GC–AED studies of nicotine fate in a burning cigarette[J]. Anal Chem,1999,71(11):2 179–2 185.
[12] 钟志雄,李攻科,朱炳辉,等.离子色谱法同时测定化妆品中的铵和 6 种烷基胺[J].色谱,2010,28(7): 702–707.
