电解离子水中羟自由基的产生规律
2015-03-24万阳芳李慧颖刘俊果郝建雄刘海杰
万阳芳,李慧颖,刘俊果,郝建雄,*,刘海杰
(1.河北科技大学生物科学与工程学院,河北石家庄 050018;2.河北科技大学化学与制药工程学院,河北石家庄 050018;3.中国农业大学食品科学与营养工程学院,北京 100083)
电解离子水中羟自由基的产生规律
万阳芳1,李慧颖2,刘俊果1,郝建雄1,*,刘海杰3
(1.河北科技大学生物科学与工程学院,河北石家庄 050018;2.河北科技大学化学与制药工程学院,河北石家庄 050018;3.中国农业大学食品科学与营养工程学院,北京 100083)
对不同电解离子水以及次氯酸钠溶液产生羟自由基能力进行了研究,结果表明:当有效氯浓度为17mg/L,pH变化不会对电解离子水的产生羟自由基能力有显著影响;当有效氯浓度为60mg/L时,产生羟自由基能力随着pH升高而升高;微酸电解离子水在0~24h范围内的羟自由基变化不明显,强酸电解离子水在17℃和4℃的贮藏温度下,产生羟自由基的能力均在贮藏时间为5h时达到最大;在不同pH和有效氯浓度范围内,电解离子水产生羟自由基能力均要比次氯酸钠溶液强。
电解离子水,羟自由基,次氯酸钠,生成规律
电解离子水是通过电解稀电解质溶液得到的具有特殊理化性质的功能性水[1],其在医疗[2-4]、食品[1]及农业[5]上的消毒和杀菌效果已经得到广泛应用。近年来在食品工业生产领域中电解离子水的应用主要表现在:果蔬消毒和鲜切产品贮藏[6]、水产肉蛋的杀菌、农药残留[7-8]和污染物降解[9]以及芽苗菜促生长[10]等。
影响电解离子水杀菌能力的因素较多,目前对于其杀菌机理尚未有明确结论,主要有如下几种推测[11]:一是pH,微生物有一定的适宜生存的pH范围,当一定指标的电解离子水超出某一微生物的生存pH范围,必定会对其产生杀灭作用;二是有效氯浓度[12],有效氯包括电解生成的HClO、Cl2、ClO2、ClO-等,能损害细胞膜,还可以穿透衣壳与病毒的核酸其作用;三是氧化还原电位(ORP)[13],好氧性微生物适宜生存的ORP范围是+200~+800mV,厌氧性微生物为-700~+200mV,而制备的电解离子水的ORP值可高达1000mV。另外,活性氧等化学因子[14]也被提出与电解离子水的杀菌作用有关。
近几年,研究者确认了电解离子水中羟自由基的存在,并对其在杀菌应用中的作用进行了研究[15],比较了产生羟自由基能力与次氯酸在杀菌应用中的贡献[16]。但是未从电解离子水微观水环境出发,进一步研究羟自由基在电解离子水中的存在情况,以及它与现在工业中广泛应用的次氯酸钠溶液成分的区别。本实验为探求电解离子水产生羟自由基能力的情况,对不同理化指标的电解离子水和次氯酸钠溶液进行了研究,力求为探寻电解离子水作用机制找到新的方法。
1 材料与方法
1.1 材料与仪器
T6新世纪紫外可见分光光度计 北京普析通用仪器有限责任公司;AR1140型电子天平 上海梅特勒-托利多仪器有限公司;400G-SA纯水机 浙江慈溪电器科技有限公司;PHS-3C型精密pH计 上海仪电科学仪器股份有限公司;实验室自制可调式电解水发生器 主要由电源、电极板和电解槽组成。
1.2 实验方法
1.2.1 电解离子水中有效氯和pH对其产生羟自由基能力的影响 利用实验室自制可调式电解水发生器来制备电解离子水。
通电电压12V,电流10A,添加盐酸1.0mL,氯化钠8g,电解时间10min,电极板距离3cm制备电解水,用稀盐酸调节pH,去离子水调节有效氯浓度,制备1~6号的a组电解离子水各200mL,密封备用。
通电电压24V,电流5A,添加盐酸0.8mL,氯化钠12g,电解时间15min,电极板距离3cm制备电解水,用稀盐酸调节pH,去离子水调节有效氯浓度,制备7~11号的b组电解离子水各200mL,密封备用。
通电电压12V,电流15A,添加盐酸0mL,氯化钠8g,电解时间15min,电极板距离3cm制备电解水,用稀盐酸调节pH,去离子水调节有效氯浓度,制备12~16号的c组电解离子水各200mL,密封备用。
通电电压12V,电流5A,添加盐酸1.0mL,氯化钠12g,电解时间10min,电极板距离3cm制备电解水,用稀盐酸调节pH,去离子水调节有效氯浓度,制备17~21号的d组电解离子水各200mL,密封备用。
近日(8月27日-8月31日),中国化肥批发价格综合指数持稳运行。9月3日中国化肥批发价格综合指数(CFCI)为 2193.41点,环比上涨8.48点,涨幅为0.39%;同比上涨288.24点,涨幅为15.13%;比基期下跌185.46点,跌幅为7.80%。
1.2.2 电解离子水在贮藏过程中产生羟自由基能力的变化 通电电压12V,电流5A,添加盐酸1.0mL,氯化钠12g,电极板距离3cm,电解时间10min制备22号电解水400mL,密封避光备用;选择通电电压24V,电流5A,添加盐酸0.8mL,氯化钠12g,电极板距离3cm,电解时间15min制备23号电解水400mL,密封避光备用。
1.2.3 电解离子水与次氯酸钠溶液产生羟自由基能力的比较 分别取56.8、113.6、170.4、227.2、284、340.8、511.2、681.6、852、1022.4μL次氯酸钠溶液于250mL去离子水中,用稀盐酸调节pH,制备24~33号溶液密封备用。
制备好的电解离子水和次氯酸钠溶液直接用于理化指标测定。有效氯浓度检测采用碘量法[17],pH采用pH计直接测定。
1.2.4 羟自由基生成检测 Fenton反应是最常见的产生羟自由基的化学反应,H2O2的量和Fenton反应产生的·OH量成正比,当给予电子受体后,用griess试剂显色,形成红色物质,其呈色与·OH的多少成正比关系。利用这一比色法原理,显色后在550nm下测定各吸光度值。
按照所采用的羟自由基试剂盒要求,规定每毫升内106个细胞在本反应体系中使反应液中H2O2的浓度增加1mmol/L为一个产生羟自由基能力单位。按照试剂盒中使用说明书中给定的计算公式计算:
产生羟自由基能力(U/mL)=(测定OD值-对照OD值)/(标准OD值-空白OD值)×8.824mmol/L×5
a、b、c、d组电解离子水制备完成后立即进行羟自由基检测。22号和23号指标的电解离子水进行如下处理:各分为两组,每组200mL,一组置于4℃冰箱贮藏,一组置于避光处室温(17℃)下贮藏。在贮藏时间分别为0、1、5、10、24h时进行羟自由基的检测。
实验重复测定3次,结果用平均值表示,处理间的平均数比较用Origin8.0统计软件中的ANOVA法,最小差异显著性水平为0.05。
2 结果与分析
2.1 电解离子水和次氯酸钠溶液的制备
实验用电解离子水和次氯酸钠溶液理化指标见表1。
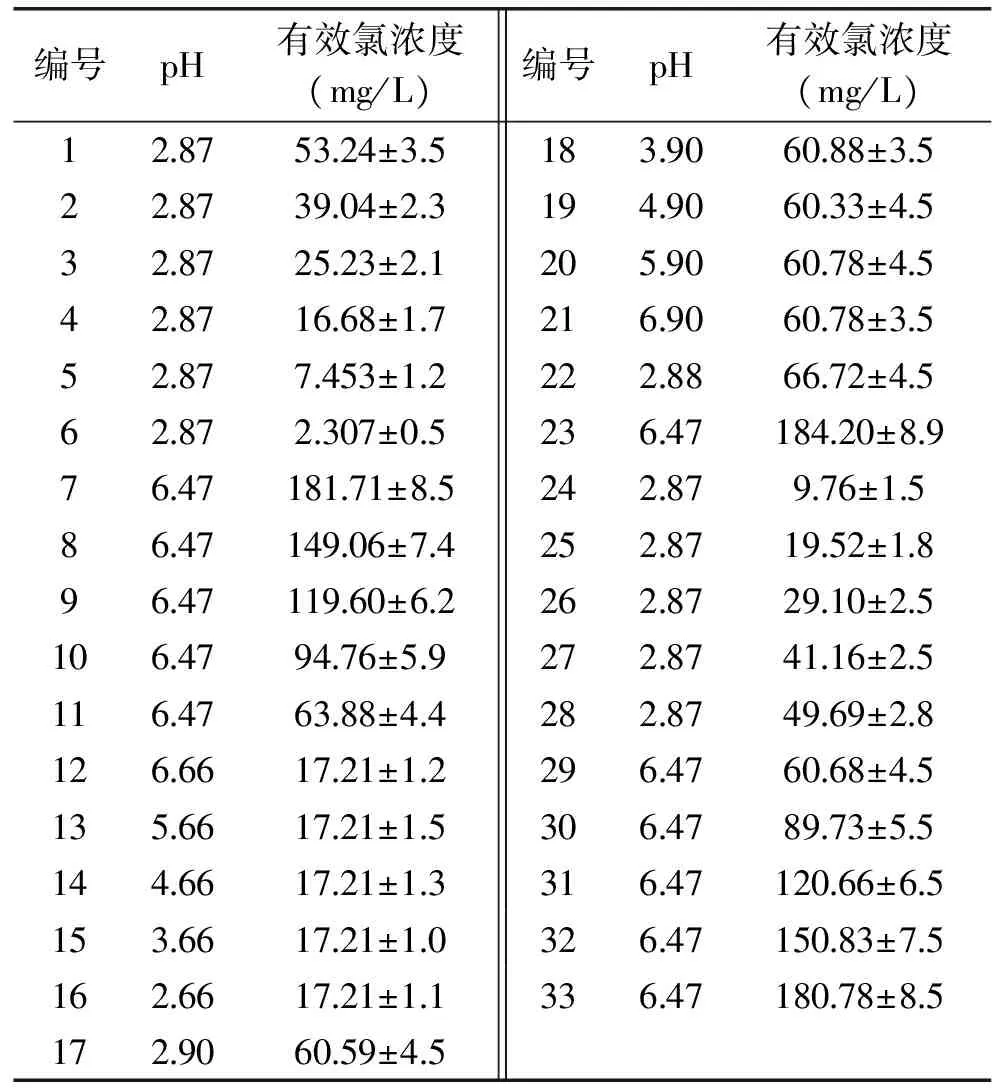
表1 实验用电解离子水和次氯酸钠溶液理化指标Table 1 The physical and chemical indicators ofelectrolyzed water and sodium hypochlorite solutions
注:有效氯浓度均测定3次,数值取平均值。pH由稀盐酸调节而得,为准确值。
2.2 电解离子水中有效氯和pH对其产生羟自由基能力的影响
在一定有效氯浓度下,通过改变pH,得到电解离子水产生羟自由基能力的变化曲线,结果如图1。当有效氯浓度为17mg/L,pH变化不会对电解离子水产生羟自由基能力有显著影响;当有效氯浓度为60mg/L时,产生羟自由基能力随着pH升高而升高(p<0.05)。从整体来看,有效氯浓度17mg/L时电解离子水的产生羟自由基能力要比有效氯浓度为60mg/L时大,且含量更稳定。
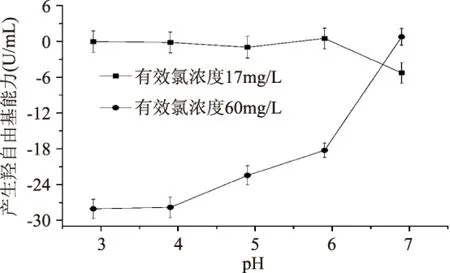
图1 不同pH电解离子水产生羟自由基能力的变化曲线Fig.1 Relation curves of pH and abilitiesof electrolyzed water producing hydroxyl radicals
电解离子水pH固定,改变有效氯浓度,得到有效氯浓度与羟自由基产生能力的关系,如图2所示,A中电解离子水pH为6.47,有效氯浓度从60mg/L增大至180mg/L,羟自由基含量呈下降趋势。图2B中电解离子水pH为2.87,有效氯浓度从2mg/L增大至53mg/L,羟自由基呈先上升后下降的趋势。在高pH、高有效氯浓度范围内,氯的主要存在形式为ClO-,产生羟自由基能力弱,且ClO-浓度越高,羟自由基的产生越少。在低pH,氯的主要存在形式为HClO和Cl2,有效氯在两者之间转换,体系微环境不稳定[15],但总体看来,要比高pH高有效氯浓度的电解离子水产生羟自由基多,可以猜测HClO是产生羟自由基的主要氯形式。
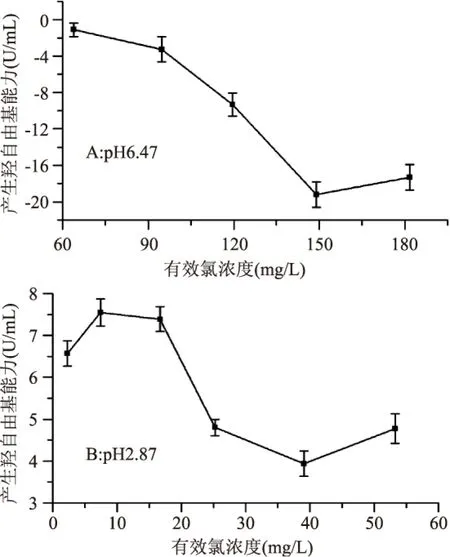
图2 电解离子水中有效氯浓度与产生羟自由基能力大小的关系曲线Fig.2 Relation curves of the available chlorine concentrationand abilities of electrolyzed water producing hydroxyl radicals
2.3 电解离子水在贮藏过程中产生羟自由基能力的变化
研究不同电解离子水在不同贮藏温度下产生羟自由基能力的变化,结果如图3所示。图中A、B分别为贮藏温度为17℃和4℃的实验结果,发现强酸电解离子水的产生羟自由基的能力要大于微酸电解离子水。强酸电解离子水在17℃和4℃的贮藏温度下,产生羟自由基的能力会在贮藏时间为5h时达到最大,且4℃时要比17℃时产生羟自由基能力大,这与李克娟[18]等的研究结果相似;后减小,到24h后仍有羟自由基存在;而微酸电解离子水在0~24h范围内的羟自由基变化不明显,并且一直处于负值。由之前有效氯浓度和pH对其产生羟自由基的影响的结果来看,微酸电解离子水pH6.47,有效氯浓度184mg/L,主要氯形式为ClO-,对羟自由基的产生没有明显的贡献。所以,随着贮藏时间的延长,微酸电解离子水中的羟自由基含量没有明显变化。而强酸电解离子水在0~5h,羟自由基上升至最大值,这可能是因为在电解反应结束后,溶液内各个化学成分需要一定的时间才能达到稳定。在之后的19h内,羟自由基的含量没有明显的减少,有一定的稳定性。

图3 电解离子水贮藏过程中产生羟自由基能力随时间变化曲线Fig.3 Curves of the abilities of electrolyzed water producinghydroxyl radicals during the process of storage as the time extended
2.4 电解离子水与次氯酸钠溶液产生羟自由基能力的比较
通过制备理化指标相同的电解离子水和次氯酸钠溶液,检测其产生羟自由基能力,比较结果如图4。在不同pH和有效氯浓度范围内,电解离子水产生羟自由基能力均要比次氯酸钠溶液强。次氯酸钠溶液中的有效氯主要存在形式为HClO,但其产生羟自由基的能力低于电解离子水,说明羟自由基的产生不仅仅是HClO作用产生的,与电解离子水中的其他活性成分(如O2、Cl2、Cl-、H+、O3)也有关。

图4 电解离子水与次氯酸钠溶液产生羟自由基能力对比曲线Fig.4 Contrast curves of abilities to generate hydroxyl radicalsof electrolyzed water and sodium hypochlorite solution
3 结论
本研究通过对电解离子水产生羟自由基能力的大小、贮藏过程中羟自由基的变化以及与次氯酸钠溶液产生羟自由基能力的考察,初步了解了电解离子水中羟自由基的含量及其变化情况,明确了其与次氯酸钠溶液微环境中羟自由基的不同,可以为探求电解离子水的应用机理找寻更多方法。
[1]Huang Y R,Hung Y C,Hsu S Y,et al. Application of electrolyzed water in the food industry[J]. Food Control,2008,19(4):329-345.
[2]Jiang J X,Wang X F,Yang Y X. Study of oxygen electric water to reduce pharyngolaryngits after general anesthesia operation[J]. Chinese Journal of Nursing,2007,42(10):906-907.
[3]Hu J,Cao J G. Application of Oxidized Electrolytic Water in Operation Room[J]. Chinese Journal of Nosoconmiology,2005,15(1):55-56.
[4]Luo R,Wu L,Zhao S,et al. Study on the effect of preoperative wiping vagina by using electrolyed oxidation water[J]. Nanfang Journal of Nursing,2004,11(9):5-6.
[5]Al-Haq MI,Sugiyama J,Isobe S. Applications of electrolyzed water in agriculture & food industries[J]. Food science and technology research,2005,11(2):135-150.
[6]Koide S,Shitanda D,Note M,et al. Effects of mildly heated,slightly acidic electrolyzed water on the disinfection and physicochemical properties of sliced carrot[J]. Food Control,2011,22(3-4):452-456.
[7]Jianxiong Hao W,Haijie Liu,Tianpeng Chen,et al. Reduction of Pesticide Residues on Fresh Vegetables with Electrolyzed Water Treatment[J]. Journal of Food Science,2011,76:5.
[8]郝建雄,李里特:电生功能水消除蔬菜残留农药的实验研究[J]. 食品工业科技,2006(5):164-166.
[9]Zhang Q,Xiong K,Tatsumi E,et al. Elimination of aflatoxin B1 in peanuts by acidic electrolyzed oxidizing water[J]. Food Control,2012,27(1):16-20.
[10]Rui L,Jianxiong H,Haijie L,et al. Application of electrolyzed functional water on producing mung bean sprouts[J].Food Control,2011,22(8):1311-1315.
[11]高新吴,刘兆辉,李晓林,等. 强酸性电解水的杀菌机理与应用[J]. 中国农学通报,2008,24(7):393-398.
[12]Kim C,Hung Y-C,Brackett RE. Efficacy of electrolyzed oxidizing(EO)and chemically modified water on different types of foodborne pathogens[J]. International Journal of Food Microbiology,2000,61(2-3):199-207.
[13]Kim C,Hung Y-C,Brackett RE. Roles of oxidation-reduction potential in electrolyzed oxidizing and chemically modified water for the inactivation of food-related pathogens[J]. Journal of Food Protection,2000,63(1):19-24.
[14]王文清,陈红梅,张选明,等. 酸性氧化电位水制备和杀菌机理的研究进展[J]. 现代化工,2008(11):24-28.
[15]Hao J,Qiu S,Li H,et al. Roles of hydroxyl radicals in electrolyzed oxidizing water(EOW)for the inactivation of Escherichia coli[J]. International Journal of Food Microbiology,2012,155(3):99-104.
[16]Takayuki Mokudai KN,Taro Kanno,Yoshimi Niwano. Presence of Hydrogen Peroxide,a Source of Hydroxyl Radicals in Acid Electrolyzed Water[J]. Public Library of Science One,2012,7(9):1-8.
[17]张铁垣:化验员手册[M]. 第二版. 北京:中国电力出版社;1996.
[18]李克娟,刘海杰,辰巳英三,等. 离子特性及贮藏条件对强酸性电生功能水理化性质的影响[J]. 食品工业科技,2012(10):138-142.
Forming rules of hydroxyl radicals produced in electrolyzed water
WAN Yang-fang1,LI Hui-ying2,LIU Jun-guo1,HAO Jian-xiong1,*,LIU Hai-jie3
(1.College of Bioscience and Engineering,Hebei University of Science and Technology,Shijiazhuang 050018,China;2.College of Chemical and Pharmaceutical Engineering,Hebei Universityof Science and Technology,Shijiazhuang 050018,China;3.College of Food Science and Nutrition Engineering,China Agricultural University,Beijing 100083,China)
The ability to generate hydroxyl radicals of the different electrolyzed water and the sodium hypochlorite solution in the process of storage was investigated.The results showed that the changes of pH did not affect the ability of electrolyzed water to generate hydroxyl radicals when the available chlorine concentration was 17mg/L. When the available chlorine concentration was 60mg/L,the ability to generate hydroxyl radicals increased with the pH increasing,the hydroxyl radicals in slightly acidic electrolyzed water did not change significantly within 0~24h,the concentration of hydroxyl radicals reached the maximum when the storage time of 5h both at 17℃ and 4℃. At the different pH and the available chlorine concentration,and the capacity of electrolyzed water to produce hydroxyl radicals was stronger than that of sodium hypochlorite solution.
electrolyzed water;hydroxyl radicals;sodium hypochlorite;forming rules
2014-05-14
万阳芳(1989-),女,硕士研究生,主要从事食品加工新技术研究。
*通讯作者:郝建雄(1979-),男,博士,副教授,主要从事农产品贮藏与加工研究。
科技部十二五支撑计划项目(2012BAD29B04-1);国家自然基金项目(31301571);河北省自然基金项目(C2013208163)。
TS251.1
A
1002-0306(2015)05-0049-04
10.13386/j.issn1002-0306.2015.05.001
