基于中国临床证据的前列地尔对DPN患者神经传导速度作用的Meta分析
2015-03-22方朝晖赵进东张文锦
方朝晖,赵进东,丁 雷,刘 剑,杨 雪,杜 雪,张文锦
(安徽中医药大学第一附属医院内分泌科,安徽合肥 230031)
近年来,由于我国人民饮食结构、生活方式较前发生了巨大改变,糖尿病的发病已在我国迅速蔓延,其中成人2型糖尿病发病率高达11.6%[1],成为严重危害人类健康的一类慢性重大疑难疾病,需要多方面共同参与、努力,来防控糖尿的发生。由于糖尿病发病趋于年轻化,从而部分患者的病程将长达40余年,因此伴随糖尿病性周围神经病变(DPN)的发病率也在逐年上升,约50% ~80%的糖尿病患者会伴有DPN。若治疗DPN不及时,往往加重病情,严重影响患者的生存质量,甚至发生肢体坏疽,尤其是下肢更多见,而被迫行截肢手术[2-3],给患者及家庭、社会带来沉重的负担。DPN患者在糖尿病常规降糖基础上,加用前列地尔治疗,可以改善患者临床症状及体征,提高中医证候积分,提高神经传导速度,从而改善患者生存质量。本研究对国内临床上有关前列地尔治疗DPN患者临床疗效的研究报道进行Meta分析,旨在评价前列地尔治疗DPN的疗效,为临床应用该药防治DPN提供最佳的循证医学证据。
1 研究内容及方法
1.1 纳入标准 本研究所观察的病例均来源于从数据库检索到的有关前列地尔防治DPN的随机对照试验(RCT),不论是否采用或不采用盲法;纳入的文献均为中国研究的资料;受发表时间的限制;不受患者年龄、性别、病程的限制。
1.2 排除标准 研究数据明显有误、研究资料无基线数据;非随机对照试验;研究使用的统计方法不正确;无法获得研究全文的试验;治疗组为中药或其他方法联合前列地尔干预的试验;以计数资料表示治疗效果的临床观察;糖尿病以外其他疾病所导致伴发的DPN。
1.3 干预措施与结局指标 对照组给予维生素B1、维生素B12及甲钴胺常规治疗;试验组在对照组基础上加用前列地尔(剂量、剂型、用法、疗程等不限)。结局指标为运动、感觉神经传导速度的变化(正中神经及腓总神经)。
1.4 检索方法 计算机检索中外文数据库:Pubmed数据库、Cochrane图书馆临床对照试验资料库、中国知网期刊全文数据库等相关资料。通过智能检索—人工粗筛—阅读全文的方法获取符合纳入标准及排除标准的临床研究文献。检索词包括“diabetic peripheral neuropathy”,“Alprostadil”、“糖尿病周围神经病变”,“前列地尔”等。检索时限均为从建库至2013年12月。
1.5 文献筛选、资料提取及质量评价 聘请两位评价员,经统一培训后,独立阅读所获得研究的题目和摘要,详尽阅读可能纳入研究的全文,根据以上步骤进行筛选与排除,最终确定是否纳入。按照“文献信息提取表”及“方法学质量评估表”[5]提取和录入资料,提取资料内容包括文献的基本特征(文献作者,文献出处等)、研究类型(随机对照、双盲等)、干预措施、测量指标(神经传导速度)及研究结果等。如遇分歧则通过双方讨论或由第三者讨论协助决定。纳入的文献采用国际通用的Jadad质量记分法进行评分[4]。分别按随机(有随机为1分,具体随机方法加1分);双盲(有双盲为1分,具体双盲方法加1分);不良事件(有不良事件和(或)原因为1分)评估研究质量。总分为5分,分数≥3分为高质量研究;分数为1~2分为低质量研究。
1.6 统计学方法 采用 RevMan系统评价选件5.2版本进行Meta分析。将资料进行综合,首先对纳入的研究进行同质性检验,并根据P值进行效应模型的选择。异质性分析采用χ2检验,P>0.1时不存在异质性,应用固定效应模型进行分析[6];P≤0.1且I2>50%时,认为存在高度异质性,应用随机效应模型进行分析[7];P≤0.1且 I2≤50%时,认为存在低、中度异质性,应用随机效应模型进行分析[7]。连续变量应用标准化均数差(MD)及95%可信区间(95%CI)。

表1 纳入研究文献的一般情况
2 研究结果
2.1 文献检索结果 按照本研究检索方法,最初检索到已发表的45篇中文文献纳入研究。通过阅读初筛文献的题目、摘要后,剔除文献26篇。再仔细阅读初筛文献的全文,因文献无基线资料描述、结局测量指标与研究观察指标完全不同等原因而排除,最终纳入11篇符合纳入标准的文献[8-18]。共纳入935例研究患者,均为基于中国临床证据的RCT。所纳入研究的基本特征见表1。
2.2 纳入研究的方法学质量 纳入本次研究[8-18]
每组的样本量范围是20~90例,约42例,但均未叙述研究样本量的计算方法及说明。5项研究均随机分组,但具体随机方法未提及。无一项研究提及盲法使用的情况,各研究均明确提出组间基线资料相似性良好,并进行了可比性检验。无研究描述依存性分析。按照Cochrane系统评价原则对纳入本研究的方法学进行质量评价,3分4篇,2分6篇,1分1篇。见表1。
2.3 正中神经的运动神经传导速度变化值分析
对纳入研究的11篇文献[8-18]进行统计,异质性分析结果提示纳入的研究文献数据存在明显异质性(P<0.1,I2=88%),应用随机效应模型对文献进行Meta分析,结果提示:前列地尔可提高运动神经传导速度—正中神经[MD= -5.63,95%CI(-6.05,-5.20),P <0.01]。具体内容见图1。
2.4 腓总神经的运动神经传导速度变化值分析
对纳入研究的11篇文献[8-18]进行统计,异质性分析结果显示存在明显异质性(P<0.1,I2=88%),应用随机效应模型对文献进行Meta分析,结果提示:前列地尔可提高运动神经传导速度—腓总神经[MD= - 5.87,95%CI(- 6.31,- 5.43),P <0.01]。具体内容见图2。
2.5 正中神经的感觉神经传导速度变化值分析
对纳入研究的11篇文献[8-18]进行统计,异质性分析结果显示存在明显异质性(P<0.1,I2=80%),应用随机效应模型对文献进行Meta分析,结果显示:前列地尔可提高感觉神经传导速度—正中神经[MD= - 5.51,95%CI(- 5.96,- 5.06),P <0.01]。具体内容见图3。
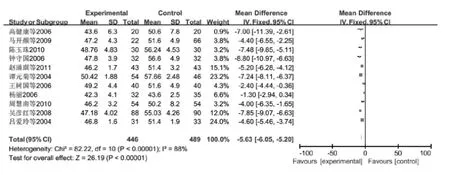
图1 两组患者运动神经传导速度—正中神经变化值分析

图2 两组患者运动神经传导速度—腓总神经变化值分析

图3 两组感觉神经传导速度—正中神经变化值分析
2.6 腓总神经的感觉神经传导速度变化值分析
对纳入的11项研究[8-18]进行分析,异质性分析结果显示存在明显异质性(P<0.1,I2=88%),应用随机效应模型对文献进行Meta分析,结果显示:前列地尔可提高感觉神经传导速度—腓总神经[MD= -4.91,95%CI(-5.35,-4.48),P <0.01]。具体内容见图4。

图4 两组患者感觉神经传导速度—腓总神经变化值分析
3 讨论
糖尿病患者可因葡萄糖氧化受抑制,血液粘度增高、微血管受损等导致神经细胞缺血缺氧,促使神经病变的发生。DPN患者临床症状多以双侧肢体末端出现对称性持续性疼痛、麻木及感觉减退为主,多于夜间加重,给患者带来极大痛苦,严重影响其生活质量[19]。临床治疗DPN的方法较多,如维生素B12、甲钴胺、前列腺素E1、硫辛酸、丹红注射液、加味黄芪桂枝五物汤等。但具有临床循证医学证据能够明显提高神经传导速度的药物尚较少。前列地尔是前列腺素E1以脂微球为载体的一种新型制剂,具有较强的促进血管扩张及抑制血小板聚集的功效,从而改善微循环,改善临床症状及体征,其对DPN患者的治疗有效率日趋备受关注。
在前列地尔治疗DPN的文献中,虽结局指标的选择尚缺乏规范的标准,但本文采用较为公认的神经传导速度作为参照标准,利于本研究的疗效的综合评价。本研究通过 Meta分析的方法,比较了DPN常规降糖和(或)联合营养神经药物治疗与加用前列地尔组与对照组比较,在提高腓总神经、正中神经的运动神经及感觉神经传导速度方面治疗组优于对照组,两组间比较差异有统计学意义(P<0.05)。具体为前列地尔组能进一步提高正中神经及腓神经的运动神经传导速度[MD=-5.63,95%CI(- 6.05,- 5.20),P < 0.01],[MD= - 5.87,95%CI(-6.31,-5.43),P <0.01];提高正中神经及腓神经的感觉神经传导速度[MD=-5.51,95%CI(- 5.96,- 5.06),P < 0.01],[MD=-4.91,95%CI(-5.35,-4.48),P <0.01],进而改善临床症状,提高临床疗效。
前列腺素E的前期研究结论显示其可在一定程度上改善微循环,增加神经血管的血流灌注,触发髓鞘形成及神经轴突再生,修复受损的神经,提高了神经的传导速度[20-21]。前列地尔利用脂微球载体将前列腺E包裹,减少其在肺脏的失活,增强其靶向性,尽可能发挥扩张血管的作用,使血液供应到神经内膜的量增加,抑制血小板凝集,改善周围神经循环及血供,进而促进受损神经纤维的修复,提高神经传导速度,这是其具有确切临床疗效的可能作用机制。同时降低了前列腺素E1对血管的刺激作用,减少不良反应的发生。因此,前列地尔治疗DPN是有效的。本研究纳入的样本量较少,没有多中心、大样本的研究;纳入研究质量不高,均为国内的研究,临床证据等级偏低;疗程较短,缺乏长期随访资料,且未报道失访及退出原因等是本研究的局限性。DPN患者需要长期巩固治疗,而临床上前列地尔却以静脉滴注为主,这就降低了患者的依存性,给临床使用也带来一定的局限性。
[1] Xu Y,Wang L,Jiang H,et al.Prevalence and Control of Diabetes in Chinese Adults[J].JAMA,2013,310(9):948 -958.
[2] 陈灏珠.实用内科学(糖尿病周围神经病变)[M].12版.北京:人民卫生出版社,2005:1030-1032.
[3] 方朝晖,赵进东.芪归糖痛宁颗粒治疗糖尿病周围神经病变临床观察[J].中医药临床杂志,2012,24(2):126 -128.
[4] Jadad AR,Moore RA,Carroll D,et al.Assessing the quality of reports of randomized clinical trials:is blinding necessary?[J].Control Clin Trials,1996,17:1 -12.
[5] Higgins JPT,Altman DG,Sterne JAC,editors.Chapter 8:Assessing risk of bias in included studies.In:Higgins JPT,Green S,editors.Cochrane Handbook for Systematic Reviews of Interventions Version 5.1.0(updated March2011)[M].The Cochrane Collaboration,2011:133 -135.
[6] 陈长生,徐勇勇.第十四讲,如何进行Meta分析[J].中华预防医学杂志,2003,37(2):138 -140.
[7] 孙瑞元,郑青山 主编.数学药理学新论[M].北京:人民卫生出版社,2004:631-666.
[8] 马开颜,李 青.注射用前列地尔治疗糖尿病周围神经病变的疗效观察[J].基层医学论坛,2009,13(8):698 -700.
[9] 赵涌琪,蒋晓江.前列地尔注射液治疗糖尿病周围神经病变临床疗效观察[J].检验医学与临床,2011,8(17):2107-2108.
[10]周慧南,宋志成.前列地尔注射液治疗糖尿病周围神经病变疗效观察[J].中国临床保健杂志,2010,13(2):167 -168.
[11]陈玉珠.前列地尔注射液治疗糖尿病周围神经病变30例[J].福建医药杂志,2010,32(3):137 -138.
[12]杨 丽.前列地尔治疗糖尿病周围神经病的疗效观察[J].锦州医学院学报,2006,27(1):95.
[13]吴彦红,赵 霞.前列地尔治疗糖尿病周围神经病变临床疗效分析[J].中国实用医药,2008,3(35):145 -146.
[14]钟守国.前列地尔治疗糖尿病周围神经病变疗效观察[J].实用全科医学,2006,4(3):353 -354.
[15]谭元菊,安 峥.前列地尔治疗糖尿病性周围神经病变的临床研究[J].中国医院用药评价与分析,2004,4(3):175 -177.
[16]王树国,刘 星.前列地尔治疗糖尿病周围神经病变的临床观察[J].吉林医学,2006,27(7):719-722.
[17]吕爱玲,阮爱兵.前列地尔治疗糖尿病神经病变33例临床观察[J].临床荟萃,2004,19(8):459 -460.
[18]高健康,李育晴.凯时治疗糖尿病神经病变[J].基层医学论坛,2006,10(12):24 -25.
[19]徐 晗,吴 敏.加味白薇煎治疗痛性糖尿病神经病变[J].长春中医药大学学报,2014,30(3):478 -480.
[20]陈晓云,杨庚明,赵义娟,等.前列地尔治疗糖尿病周围神经病变初步探讨[J].新医学,2000,31(9):545 -546.
[21] Shindo H,Tawata M,Inoue M,et al.The effect of prostagiandin E1.Aipha CD on vibratory threshold determinded with the SMC-5 vibrometer in patients with diabetic neuropathy[J].Diabetes Research Clinical Practice,1994,24(3):173 -180.
