一种新型的样品前处理技术
——电膜萃取的发展及应用
2015-03-16孙建楠
孙建楠
(济宁医学院法医学与医学检验学院,山东 济宁 272067)
一种新型的样品前处理技术
——电膜萃取的发展及应用
孙建楠
(济宁医学院法医学与医学检验学院,山东 济宁 272067)

孙建楠,女,汉族,山东省济南人,生于1986年6月。2005年9月考入山东师范大学化学化工与材料科学学院,于2009年7月毕业,获理学学士学位。同年考入中国科学院兰州化学物理研究所分析化学专业硕博连读,师从师彦平研究员和陈娟研究员。在西北特色植物资源院重点实验室学习期间,主要从事基于离子液体的液相微萃取方法的研究与应用。现在济宁医学院工作,任职于法医学与医学检验学院。
样品前处理步骤是整个分析过程中至关重要的环节。电膜萃取作为液相微萃取技术的一名新成员,受到了研究人员的广泛关注。电膜萃取是在液相微萃取的基础上,以电场驱动力代替被动扩散成为萃取主要动力的一种电萃取模式。本文介绍了电膜萃取的常见萃取模式和萃取原理,探讨了影响萃取效率的各个因素,并对电膜萃取方法的优点进行了评述,最后,对电膜萃取的发展趋势进行了展望。
样品前处理技术;液相微萃取;电膜萃取;发展趋势
样品前处理是整个分析过程中占用时间最长和最容易引入方法误差的步骤,因而成为决定分析过程是否成功的至关重要的环节。通过采用合适的样品前处理方法,可以解决目标分子浓度低于仪器检测限、样品基质复杂不适合直接进入仪器检测等问题,以达到改善灵敏度、选择性和精密度的目的。在过去相当长的时间里,研究人员将分析化学的发展重点放到了新型分析仪器的开发上,进而忽视了样品前处理的重要性。近年来,随着分析样品多样化和复杂化的加剧,单纯的仪器分析已无法满足分析过程的要求,研究人员开始将目光投入到样品前处理的发展中,并形成现代样品前处理方法的六大趋势,即简便、快速、微型、自动、经济和安全。在此背景下,研究人员建立、发展了众多新型的微萃取技术,以解决经典手段难以解决的问题,这些种类繁杂的方法总结起来可以分为两大类:固相微萃取(solid phase microextraction,SPME)和液相微萃取(liquid phase microextraction,LPME)。
1 液相微萃取
LPME具有快速、经济的优点,每个萃取过程只需微升级别的溶剂,避免了大量有毒有机试剂的使用,具有较高的富集倍数。从近年来的关于LPME的文献数量的变化趋势可以看出(图 1),自被首次报道至今,针对LPME的研究呈逐年递增的趋势,应用范围更是涉及食品、环境、生物等多个领域。

图1 ISI数据库中2005-2014年关于LPME文章的数目表
LPME有3种萃取模式,其中,中空纤维液相微萃取(hollow fiber liquid phase microextraction,HF-LPME)是非常重要的组成部分。1999年,Pedersen-Bjergaard和Rasmussen研究组首次将中空纤维引入液相微萃取中,建立了HF-LPME。借助中空纤维的作用,萃取剂可以稳定存在于中空纤维壁孔中,分析物首先被萃取到萃取剂形成的支撑液膜(supported liquid membrane,SLM)中,最终富集于中腔的接受相里。当中腔中接受相与SLM溶剂种类相同时,为两相HF-LPME,当接受相为水溶液时,称之为三相HF-LPME。良好的样品净化能力是HF-LPME最突出的优点,这归功于中空纤维的微米级别的壁孔,它可以阻隔环境、生物样品中的大分子物质和杂质颗粒。因此,HF-LPME多被用于复杂基质中痕量物质的萃取。
2 电膜萃取
在HF-LPME中,分析物传质过程是依赖于被动扩散,因此萃取时间和分析物在SLM、水溶液中的分配系数是决定萃取效率的主要因素。但是被动扩散进行的传质是一个相对较慢的过程,因此,HF-LPME的主要缺陷就是萃取时间过长。通常一次完整的HF-LPME过程萃取时间往往长达15~45 min,尤其是在含有蛋白、脂肪、糖类等物质的生物样品中,复杂基质的干扰和络合更是减慢了分析物向SLM的扩散。因此,有必要建立一种快速的萃取方法,以保证大通量的样品被萃取到。
因此,研究人员想到了电场的力量,众所周知,带电离子在电场中可以发生快速的定向迁移,若是带电的分析物可以在电场的作用下穿过SLM实现富集,那萃取时间将会被大大缩短。电膜萃取(electromembrane extraction,EME)就是在此假设上提出的新型样品前处理技术,是液相微萃取与电场结合的新发展。最早关于EME的报道出现于2006年,研究人员将电场引入HF-LPME中,带电的分析物在电场的作用做穿过SLM,最终富集于接受相。随着研究的深入,EME发展出多种萃取形式。与传统的电萃取不同,EME中的液膜是由一层很薄的有机溶剂组成的,避免了大量有机溶剂的使用,提高了传输速度,可以提高萃取效率,而且此液膜的使用,可以避免基质中的杂质穿过,从而具有良好的样品净化能力,可以应用于复杂基质中痕量物质的萃取。
2.1 电膜萃取的萃取模式
2.1.1 基于中空纤维的电膜萃取 基于中空纤维的EME是EME的最早也是最经典的形式,整个萃取装置如图2所示,

图2 基于中空纤维的电膜萃取装置
样品溶液置于萃取容器中,通过调节pH值,使分析物保持在离子状态,将一段中空纤维浸渍于不溶于水的有机溶剂中几秒钟,有机溶剂被固定于中空纤维的壁孔中,形成SLM,接受相注入中空纤维中腔中,一端封口后固定于样品溶液中。一根铂丝电极插入中空纤维内腔中,一根铂丝电极插入样品溶液中。萃取开始后,施加直流电压,带电分子在电场的作用下穿过SLM,进入接受相中。对于带正电的分析物,负极置于中空纤维内腔中,正极固定于样品溶液中,对于带负电的分析物则相反。萃取结束后,关闭电压,以注射器吸取接受相直接进仪器检测。
该装置的核心部分是以多孔的聚丙烯中空纤维为载体的有机溶剂形成的支撑液膜。为了得到尽可能高的萃取效率和选择性,应根据分析物的性质慎重选择形成SLM的有机溶剂。目前SLM的选择没有统一的科学依据,多以实验为准,通过目前研究可知,带有硝基的芳香烃类溶剂,如2-硝基苯辛基醚(2-nitrophenyl octyl ether,NPOE),可用于碱性物质的萃取,而长链烷醇如正辛醇(1-octanol)等可用于酸性物质的萃取。通过选择合适的SLM,带电分析物可以顺利地扩散入SLM,在电压的作用下得到较高的传质效率。对于极性较大的带正电的物质,可以在SLM中加入2-乙基己基磷酸酯(di-(2-ethylhexyl) phosphate,DEHP)等离子对试剂[1],帮助极性物质穿过SLM,实现萃取。
2.1.2 点对点电膜萃取(drop to drop based EME) 在此萃取模式中(如图3)[2]样品溶液与接受相都是微升级别的液滴,二者以一层固定于聚丙烯薄片微孔中的有机溶剂形成的支撑液膜隔开。样品溶液置于一个铝箔制成的容器中,容器直接与电源相连,成为电极,另一电极插入接受相的液滴中,二者形成一个完整的电场。该方法所需的样品溶液体积极小,适合于样品量较小的情况,可以认为是无损检测。但是考虑到样品溶液和接受相的体积相同,该方法无法获得较高的富集倍数,无法实现样品的富集,主要适用于复杂基质中目标物的选择性提取,以去除基质和其他物质的干扰。
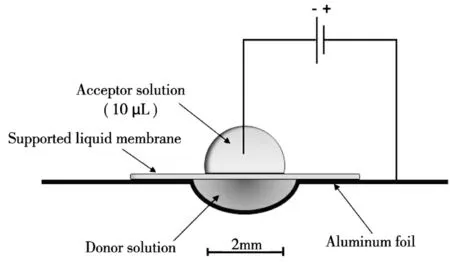
图3 点对点液膜萃取装置图
2.1.3 芯片电膜萃取(microchip based EME) 最近的研究中,EME发展出芯片尺寸的新萃取模式[3-4]。在此萃取模式中(图4),两个具有通道结构的聚甲基丙烯酸酯材质的基片以一层支撑液膜隔开,样品溶液以1~12μL/ min的速度泵入样品通道,接受相或是静止的,或是以1~3 μL/ min速度更换,分析物在电场的作用下,从样品溶液穿越SLM进入接受相。

图4 芯片萃取装置图
与EME其他模式相比,该模式的SLM非常薄,通道短,有利于样品传质,萃取时间更短,萃取效率更高,且易于与分析仪器联用,实现在线测定,实时监测,可用于药物代谢中的活体检测。
2.2 电膜萃取的理论模型
清楚的理论模型可以帮助研究人员有针对性的控制萃取过程,以得到最佳的萃取效果。EME的理论模型[5]是一个包含SLM两侧的电压、离子平衡、绝对温度等因素的Nernst-Planck 方程(1):
Di:带电分析物在SLM中的扩散系数;
h:SLM的厚度;
x:给出相和接受相离子浓度的比值;
Ci,Co:分析物在样品溶液和接受相中的浓度;
zi:分析物的电荷
e:电子电量;
k:玻尔兹曼常数。
方程(1)表明分析物的通量与分析物在SLM中的扩散系数成正比,与SLM的厚度成反比,因此较低黏度的溶剂和较薄的SLM可以提供更好的萃取效率。在EME中,SLM的厚度与载体的厚度一致,因此SLM的种类成为决定萃取效率的主要因素。
方程(1)表明,分析物的通量还与电压的大小成正比,在电压增长到一定水平之前,萃取效率会随着电压的增长而增长。但当电压超过一定限度时,萃取效率受其他因素的限制不会继续升高,在某些情况下,电压过高时,萃取效率反而下降,这是由于电压过高导致的EME装置不稳定的原因。从方程(1)可知,离子平衡和温度也会对离子通量产生影响,但这两个因素都不是决定因素。
2.3 影响电膜萃取效率的因素
2.3.1 支撑液膜的种类 从EME的理论模型可以看出,SLM是影响萃取效率的重要因素,考虑到SLM的厚度是由载体的厚度决定的,对于一个确定模式的实验,载体厚度是固定的,因此SLM的种类成为影响萃取效率的主要因素。但目前尚没有选择SLM的科学依据,经验可知,有机溶剂组成的SLM要具有稳定性和应用性,一般要符合以下四个要求[6-7]:1)有机溶剂应与水不混溶,具有一定的疏水性;2)有机溶剂应具有较低的蒸汽压,保证萃取过程的SLM稳定性;3)有机溶剂应具有一定的偶极矩,具有一定的导电性;4)被分析物在SLM中具有一定的分配系数,可以自由通过SLM。
通过选择合适的SLM种类还可以控制萃取的选择性,一般非极性的溶剂如NPOE和1-octanol组成的SLM可以使小极性或是中等极性的物质通过,极性比较大的物质则被阻隔于SLM之外;在SLM加入DEHP或是TEHP等离子对试剂后[8],大极性的物质可以通过SLM,而小极性和中等极性的物质则被困在SLM中,无法进入接受相实现富集。
2.3.2 萃取电压的大小 在电膜萃取中,带电分析物的定向电迁移是主要传质机理,因此电压的选择成为影响萃取效率的重要因素。电压的选择要以分析物的种类和SLM液膜的种类为依据。根据研究可知,EME中常用的溶剂如NPOE所需的电压一般在上百伏,而1-octanol、ENB和IPNB所需的电压一般在数十伏或是十伏以下。在低电压时,大部分的物质无法进入SLM,只有非极性或是带单电荷的物质可以被萃取,然而当电压增加时,极性较大的多电荷的化合物就可以穿过SLM,实现富集。因此,控制电压的大小也是实现萃取选择性的一个重要条件。
为了保证高萃取效率,萃取电压的大小应控制在合理范围内。电压过小时,分析物的通量较小,萃取效率低;而电压过大时,易产生电解水现象,生成气泡,阻碍传质过程的进行,同时大电压下液膜易流失,造成萃取系统的不稳定,从而影响萃取效率。
2.3.3 样品溶液和接受相的pH值 EME中,分析物在样品溶液和接受相中均应处于离子状态,以便于分析物在电场中的电迁移,因此样品溶液和接受相的pH调节也应以此为准则。一般说来,在碱性物质的萃取中,HCl和HCOOH是常用的酸化剂,同时NaOH常用于离子化酸性物质。从上文所叙述的理论模型中可以看出,萃取效率与离子平衡(x)即样品溶液与接受相离子强度的比值呈反比,因此有时会有接受相的所需的酸碱性大于样品溶液的情况发生,但大部分情况下,二者pH值一致时已经可以提供最佳的萃取效率。
2.3.4 其他影响因素 萃取过程中,升高温度有利于降低SLM的黏度,提高离子的通量,从而改善萃取效率;但是温度过高时,组成SLM的有机溶剂易挥发,体系的电流增大,造成萃取系统的不稳定,电流增大导致的电解现象会产生气泡,阻碍分析物的传质过程。
较短的萃取时间是EME对于传统的HF-LPME的最大改进,对于电迁移来说,不需要考虑分析物在两相间的分配平衡,因此理论上,萃取时间越长,萃取效率越高。但具体到实际应用中,萃取时间过长,萃取效率反而有所下降,这是因为萃取后期接受相中分析物浓度过高,在浓度梯度的作用下会向样品溶液中扩散的影响。
搅拌可以促进分析物在溶液中的扩散作用,更好地与SLM相接触,但在EME中,一来样品溶液的体积通常比较小,例如点对点和芯片EME中,样品溶液的体积在微升级别,无法引入搅拌装置;二来分析物的电迁移速率已经很快,搅拌对其传质速率的帮助很小,鉴于以上两点,EME中通常不需要考虑搅拌对其的影响。
传统的LPME中,盐效应对于萃取效率的改善作用不大,甚至会降低萃取效率。但在EME中,适当质量的盐加入有助于降低整个体系的电阻,使萃取可以在较低电压下进行,促进了带电分析物的电迁移。
2.4 电膜萃取的优点
2.4.1 快速萃取 EME方法提出的最初目的就是为了缩短HF-LPME的萃取时间,而电场成为萃取的主要驱动力也实现了这个目的。研究人员比较了对于同样的分析物——麻黄碱的两种方法在萃取时间上的差异[9]:HF-LPME达到平衡需要25 min,而EME只需要15 min就可以达到相似的萃取效率,证明相比于被动扩散,电迁移的确是一种有效、快速的传质方式。一般说来,一次完整的EME过程所需的时间在5~15 min范围内,而最近报道的一篇动态EME更是将萃取时间缩短到60 s[10]。尽管在此研究中,萃取的回收率仅在12%~22 %,但已经足够对分析物在整个药效浓度范围内进行定量,而方法学的数据也证明了该方法的稳定性和可行性。这表明,EME可以在生物样品中实现快速萃取,在生物分析领域具有良好的应用前景。
2.4.2 有效的样品净化能力 除了较短的萃取时间,良好的样品净化能力也是EME的重要优点。如图5所示[11],电膜萃取后生物样品的色谱图非常干净,基本没有基质峰和杂质峰的干扰。

图5 空白和加标的生物样品EME萃取后电泳图
这主要是归功于EME良好的样品净化和选择萃取能力。首先,多孔的聚丙烯纤维膜常被用作SLM的载体,它本身的微孔结构,可以阻止颗粒物和大分子进入接受相中。其次,由于分隔开样品溶液和接受相的疏水性SLM只允许非极性的分析物通过,因而生物样品中大部分的极性物质则被留在样品溶液中。另外,只有带与萃取电极相反电荷的物质可以在电场的作用下定向迁移入接受相中,所以进入仪器检测的接受相里只含有带同类电荷的非极性物质。因此,载体、SLM和电压3者的协同作用,使EME具有优于HF-LPME的样品净化能力,更适合生物、食品等复杂基质中物质的萃取。
2.4.3 小体积萃取 在小体积的样品中,分析物迁移至SLM的距离很短,有利于传质过程。当样品体积>70 μL时[12],通常选用中空纤维EME,而当样品体积<50 μL时,通常选用点对点或是芯片电膜萃取。
2.4.4 萃取的灵活性 萃取装置的灵活性和通用性是EME的很重要的优点。举例来说,当以NPOE为SLM,负极固定于接受相之中时,可以萃取碱性的非极性化合物;用同一套设备,只要将SLM换为1-octanol,交换电压的方向,就可以萃取酸性非极性化合物;另外,若是在SLM加入离子对试剂,该装置又可以用于极性物质的萃取。
鉴于此,研究者发展了可以同时萃取酸性和碱性物质的双电膜萃取装置(图6)[7]。两个电极均插入中空纤维内腔中,在pH=7的样品溶液中,酸性的双氯芬酸钠带负电在正极富集,带碱性的纳美芬带正电进入负极所在的接受相。

图6 可实现酸碱物质同时萃取的双EME装置图
2.4.5 低消耗和装置简单 EME是微型化的样品前处理技术,对于样品、溶剂的消耗量都很小,这符合绿色化学的要求,对于未来的生物分析具有重要的意义。对于一个典型的EME过程,仅需消耗10~25 μL的有机溶剂来形成SLM[13-14],而接受相和样品溶液均为水溶液,萃取过程所需的电量也很低。目前,尚未有商业化的EME装置,基本为实验室自制,所需的装置价格低廉,易于获得。
2.5 电膜萃取的发展前景
自2006年发展至今,EME已被证明是一种快速、灵活、样品净化能力突出的样品前处理技术。目前发表的关于EME的文章多是针对生物样品中低分子量药物的萃取,在生物分析中具有很好的应用前景。根据微萃取技术发展的总趋势,未来EME的研究可以从以下两个方面考虑:一方面,新种类和专一性的SLM的使用。目前所使用的SLM大部分为有机溶剂组成的液态膜,种类有限,因此可以充分利用新型的溶剂如离子液体特殊的物理化学性质,如低蒸汽压、对于离子态物质的萃取性能和结构可控性,来改善EME目前存在的问题。还可以与纳米材料、分子印迹材料结合,通过纳米材料的吸附系数性能改善萃取效果或是增加萃取的专一性[15]。另一方面,改变外加电源的种类[16]。为了保证目标分子的定向迁移,EME所使用的均为直流电源,但是直流电源在电极附近易形成双电层,阻碍了分析物的迁移,可以使用脉冲电压来击穿双电层,消除阻碍作用。
[1] Petersen N J,Jensen H,Hansen S H,et al.On-chip electro membrane extraction[J].Microfluid Nanofluid,2010,9(4-5):881-888.
[2] Petersen N J,Jensen H,Hansen S H,et al.Drop-to-drop microextraction across a supported liquid membrane by an electrical field under stagnant conditions[J].J Chromatogr A,2009,1216(9):1496-1502.
[3] Petersen N J,Petersen J S,Poulsen N N,et al.On-chip electromembrane extraction for monitoring drug metabolism in real time by electrospray ionization mass spectrometry[J].Analyst,2012,137(14):3321-3327.
[4] Dugstad H B,Petersen N J,Jensen H,et al.Development and characterization of a small electromembrane extraction probe coupled with mass spectrometry for real-time and online monitoring of in vitro drug metabolism[J].Anal Bio Chem,2014,406(2):421-429.
[5] Balchen M,Jensen H,Reubsaet L,et al.Potential-driven peptide extractions across supported liquid membranes:Investigation of principal operational parameters[J].J Sep Sci,2010,33(11):1665-1672.
[6] Davarni S S H,Najarian A M,NOJAVAN S,et al.Electromembrane extraction combined with gas chromatography for quantification of tricyclic antidepressants in human body fluids[J].Anal Chim Acta,2012,725(1):51-56.
[7] Seidi S,Yamini Y,Rezazadeh M,et al.Low-voltage electrically-enhanced microextraction as a novel technique for simultaneous extraction of acidic and basic drugs from biological fluids[J].J Chromatogr A,2012,1243(6) :6-13.
[8] Hasheminasab K S,Fakhari A R.Development and application of carbon nanotubes assisted electromembrane extraction (CNTs/EME) for the determination of buprenorphine as a model of basic drugs from urine samples[J].Anal Chim Acta,2013,767(5) :575-580.
[9] Fotouhi L,Yamini Y,Molaei S,et al.Comparison of conventional hollow fiber based liquid phase microextraction and electromembrane extraction efficiencies for the extraction of ephedrine from biological fluids[J].J Chromatogr A,2011,1218(48):8581-8586.
[10] Eibak L E E,Gjelstad A,Rasmussen K E,et al.Kinetic electro membrane extraction under stagnant conditions-Fast isolation of drugs from untreated human plasma[J].J Chromatogr A,2010,1217(31):5050-5056.
[11] Fakhari A R,Tabani H,Nojavan S,et al.Electromembrane extraction combined with cyclodextrin-modified capillary electrophoresis for the quantification of trimipramine enantiomers[J].ELECTROPHORESIS,2012,33(3):506-515.
[13] Seidi S,Yamini Y,Heydari A,et al.Determination of thebaine in water samples,biological fluids,poppy capsule,and narcotic drugs,using electromembrane extraction followed by high-performance liquid chromatography analysis[J].Anal Chim Acta,2011,701(2):181-188.
[14] Eekandari M,Yamini Y,Fotouhi L,et al.Microextraction of mebendazole across supported liquid membrane forced by pH gradient and electrical field[J].J Phar Biom Anal,2011,54(5):1173-1179.
[15] Strieglerov L,Kuban P,Bocek P.Electromembrane extraction of amino acids from body fluids followed by capillary electrophoresis with capacitively coupled contactless conductivity detection[J].Journal of Chromatography A,2011,1218(37):6248-6255.
[16] DavaraniS S H,Morteza-Najarian A,Nojavan S,et al.Two-phase electromembrane extraction followed by gas chromatography-mass spectrometry analysis[J].J Sep Sci,2013,36(4):736-743.
A new kind of sample preparation technique-the development and application of electromembrane extraction
SUNJiannan
(Institute of Forensic Medicine and Laboratory Medicine, Jining Medical University,Jining 272067, China)
Sample preparation is the key step in a whole analytical procedure. As a new member of liquid phase microextraction (LPME), electromembrane extraction (EME) has accepted widely attention from researchers. EME was proposed on the basis of LPME, and employed electric field as main driving force. This paper introduced the main extraction modes and principle of EME, and discussed the factors which influence the extraction efficiency. At last, the paper reviewed the advantages of EME and looked into the prospect of this method.
Sample preparation; Liquid phase microextraction; Electromembrane extraction; Trend of development
10.3969/j.issn.1000-9760.2015.02.003
O652.6
A
1000-9760(2015)04-086-06
2015-04-14)
