双咪唑鎓杯芳烃类似物的合成、结构表征及其对ATP的识别性能
2015-03-15李宇飞蒋宗林潘云芹
李宇飞,蒋宗林,彭 琼,潘云芹
(西华师范大学化学化工学院,四川 南充 637009)
双咪唑鎓杯芳烃类似物的合成、结构表征及其对ATP的识别性能
李宇飞,蒋宗林,彭 琼,潘云芹
(西华师范大学化学化工学院,四川 南充 637009)
设计合成了两种具有水溶性的双咪唑鎓杯芳烃类似物3和4,经IR、1HNMR、MS谱确定了其结构.采用核磁滴定法,研究了主体化合物3、4对ATP的识别作用;结果表明,其结构更接近于杯芳烃的主体化合物3对ATP分子有显著的识别效果,而4对ATP分子的识别能力较弱.
杯芳烃类似物;咪唑鎓;ATP;分子识别;核磁滴定;Michael加成
早些时候,生物化学家、有机化学家为了从分子水平的角度来研究生物体中的化学问题而提出分子识别的概念.随着科技创新水平的不断提升,人们对研究分子识别机理的认知理念得到了更深层次的升华.随着分子识别机理理念认知的一次次升华,尤其在超分子化学快速发展的背景下,分子识别在化学合成、酶的作用机理、材料科学及信息科学方面的作用变得更加重要[1].
分子识别是指主体(受体)和客体(底物)通过非共价键相互作用而产生特殊效果的过程[2].这些非共价键作用,常见的有:范德华力(包括离子-偶极、偶极-偶 极和偶极-诱导偶极相互作用)、疏水作用、静电作用、氢键等,而分子识别则主要依赖氢键和静电作用[3-6].分子识别的过程中可能会引起主客分子体系电学、光学性质及构象的改变,也可能引起化学性质的改变.这些改变意味着化学信息的储存、传递及处理.利用分子识别过程中这些性质变化,为寻找客体分子的识别探针和化学传感器提供了参考依据.
从2011开始,Kim课题组相继设计并报道了多种带蒽环,萘环,吖啶环的多咪唑鎓环番化合物[7-11],用于对ATP、GTP、UTP等多种核苷酸分子的选择性识别,效果显著;尤其对GTP、ATP选择性效果更佳.我们在此基础之上设计合成了两种双咪唑鎓杯芳烃类似物3和4,与4相比较,杯芳烃类似物3含有酚羟基,其结构更加接近于杯芳烃,二者在识别对ATP分子的识别效果必存在着差异.合成路线如下:
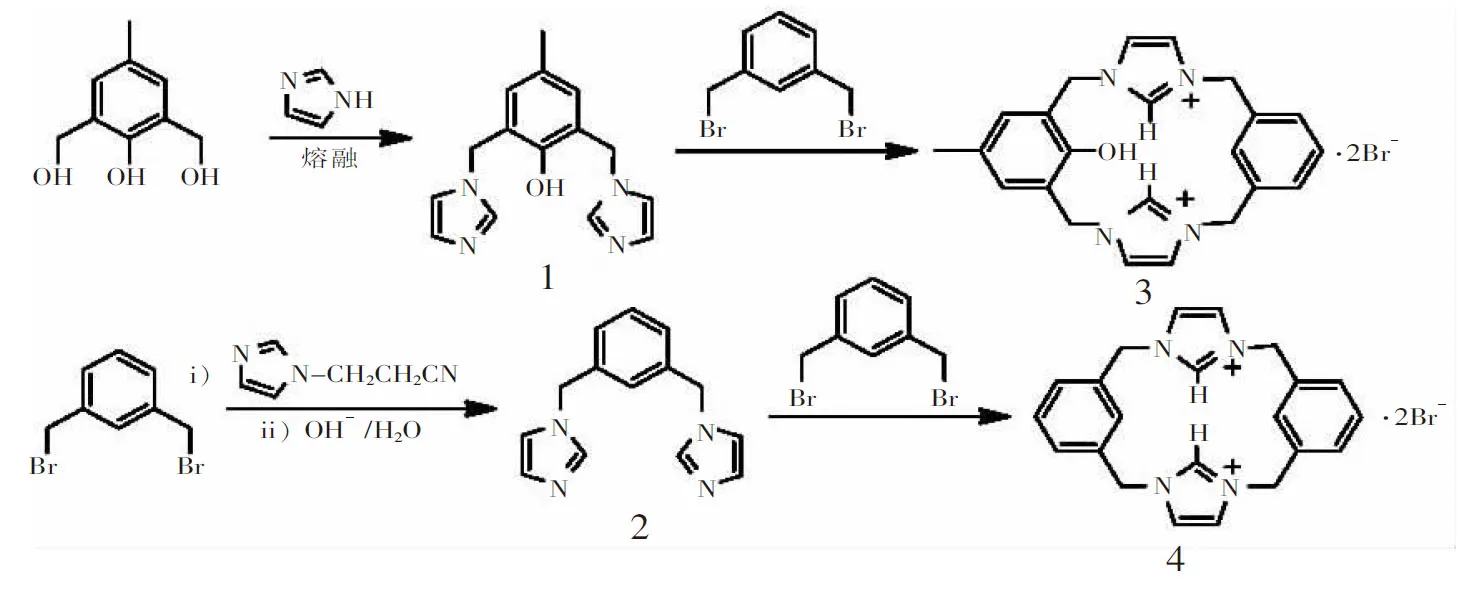
1 实验部分
1.1 主要仪器
XT-4显微熔点测定仪(温度计未校正);360-型傅立叶红外光谱仪,KBr压片;BruckerSF-400 MHz核磁共振仪;Bruker micrOTOF-Q II 质谱仪.
1.2 试 剂
间二溴甲基苯、2,6-二(羟甲基)对甲苯酚参照文献[12,13]合成;氢氧化钠、咪唑、氨水、碳酸氢铵等均为分析纯试剂;ATP为Sigma公司生化试剂;甲醇、乙腈等溶剂按常规方法处理;水为二次重蒸馏水.
1.3 合成实验
1.3.1 2, 6 - 二(1-H咪唑甲基)对甲苯酚1的合成
将5.04 g(30mmoL)2, 6 - 二(羟甲基)对甲苯酚和8.16 g(120mmoL)咪唑加入到25 mL CH3OH中,搅拌至溶解,然后逐渐升温至140℃,蒸出CH3OH及反应生成的水,反应3h后,再升温至150-160℃反应1h,得微黄色液体,冷却后固化;加入适量CH3OH溶解,剧烈搅拌下,将此甲醇溶液缓缓加入到水中,析出大量微黄色固体,滤集固体,乙醇重结晶,得白色晶体1,收率:53%,mp.:188-190℃(文献值[14]:188-191℃).1H NMR(400MHz,CDCl3)δ:7.38(s,2H,Im-2H),6.89(d,J=4.9Hz,4H,Im-4H/5H;2H,Ph-H),5.14(s,4H,-CH2-),2.24(s,3H,Ph-CH3).
1.3.2 1, 3-二(1-H咪唑甲基)苯2的合成
在50 mL的圆底烧瓶中,加入6.80 g(100 mmoL)咪唑、30 mL丙烯腈,于50℃搅拌至反应完全(V氯仿:V甲醇= 9:1),除去过量的丙烯腈,加入50 mL乙腈,于回流状态下滴加13.2g(50mmoL)间二溴甲基苯的30 mL乙腈溶液,搅拌至完全反应(V氯仿:V甲醇= 9:1).蒸出溶剂,加入30 mL H2O至全溶解,再加入8 g NaOH,室温下搅拌至季铵盐消失(TLC:V甲醇:V氨水:V饱和碳酸氢铵溶液=10:2:1),用稀盐酸调pH=9,氯仿萃取,无水硫酸镁干燥,旋干得白色固体2(TLC示纯品:V氯仿:V甲醇= 9:1),收率:95%,mp.:86-88℃(文献值[15]:84-85℃).1H NMR(400MHz,CDCl3)δ:7.55(s,2H,Im-2H),7.37(t,J=7.7Hz,1H,Ph-5H),7.1(d,J= 3.9 Hz,4H,Im-4H/5H),6.93(s,1H,Ph-2H),6.90(s,2H,Ph-4H/6H),5.12(s,4H,-CH2-).
1.3.3 双咪唑鎓杯芳烃类似物3、4的合成
250mL三颈烧瓶中加入10 mL乙腈,于回流条件下等速滴加1.34 g(5mmoL)2, 6 - 二(咪唑甲基)对甲苯酚2的50mL乙腈/甲醇(3:2/V:V)及1.32 g(5mmoL)间二溴甲基苯的50mL乙腈/甲醇(3:2/V:V),滴料时间≧5h.滴加完毕,继续加热,直到产物点不再发生变化(TLC:V甲醇:V氨水:V饱和碳酸氢铵溶液=10:2:1).浓缩反应液,硅胶柱层析分离(洗脱剂:V甲醇:V水:V饱和碳酸氢铵溶液=2:1:1),得白色固体3,收率:43%,mp.:214℃(分解).IR(KBr压片,cm-1):3475,3421,3087,1557,1448,1150,874,740.1H NMR(400MHz,DMSO-d6)δ:9.33(s,1H,OH),8.91(s,2H,Im-2H),7.80(d,J= 6.0 Hz,4H,Im-4H/5H),7.53(s,2H,CH3-Ph-H),7.46(s,3H,Ph-4H/5H/6H),6.75(s,1H,Ph-2H),5.41(s,8H,-CH2-),2.31(s,3H,Ph-CH3).13C NMR(100MHz,DMSO-d6)δ:152.42,137.17,133.93,130.32,129.81,125.39,124.13,123.82,122.92,51.86,49.85,20.51.MS:[M-2Br-] 计算值:372.1939,测定值:372.1930.
类似的方法合成双咪唑鎓杯芳烃类似物4,收率:61%,mp.:255-257℃.IR(KBr压片,cm-1):3417,3145,1555,1492,1141,840,740.1H NMR(400MHz,DMSO-d6)δ:9.45(s,2H,Im-2H),7.85(d,J= 1.4 Hz,4H,Im-4H/5H),7.60(d,J= 7.9 Hz,4H,Ph-4H/6H),7.56-7.47(m,2H,Ph-5H),7.12(s,2H,Ph-2H),5.46(s,8H,-CH2-).13C NMR(100MHz,DMSO-d6)δ:136.76,129.92,129.57,26.33,123.61,52.20.MS:[M-2Br-] 计算值:342.1833.测定值:342.1844.
1.4 杯芳烃类似物3、4对ATP分子的识别
分别配制浓度为10mmoL·L-1的ATP、化合物3、化合物4的D2O溶液各1mL.
取两支直径为5mm的核磁管,各装入相同体积的主体化合物3(10mmoL·L-1)的D2O溶液和ATP(10mmoL·L-1)的D2O溶液,分别测定其核磁共振氢谱(BruckerSF-400MHz核磁共振仪,扫描64次),记录特定质子的初始化学位移.然后把这两支核磁管中的溶液混入到其中一支核磁管中去,这样主体化合物3与ATP的摩尔比为1[简称,3-ATP(1equiv)],混合均匀后静置一段时间,测定其核磁共振氢谱.比较特定质子的化学位移变化情况.相关图谱见图1.
测定化合物4的方法同3,相关图谱见图2.
2 结果与讨论
2.1 酚类化合物的咪唑甲基化
咪唑既是仲胺,又是叔胺.仲胺上的氢使咪唑具有酸性,叔胺氮上的孤对电子使咪唑具有碱性.这种特殊的结构决定了咪唑具有许多种特殊的性质.咪唑,作为一般的酸碱催化功能基和亲核催化功能基,能催化多种有机反应,同时咪唑作为原料参与底物的合成.酚类化合物的咪唑甲基化反应,属于Mannich反应范畴.酚类化合物的直接咪唑甲基化作用,副产物多,分离困难,实验操作不便,合成产率低.采用分步反应,可有效避免副产物的生成,后期纯化过程简单,收率高.室温下酚与甲醛顺利进行羟甲基化反应[13],羟基化的产物与咪唑在熔融状态下高效地得到咪唑甲基化产物[16];TLC跟踪反应进程发现,除了少量酚被氧化,未发现其他诸如聚合物等副产物的生成,且实验操作简便,产率高.该反应机理的研究未见报道,我们推测反应的核心步骤是一经典的Michael加成,反应机理表述如下:
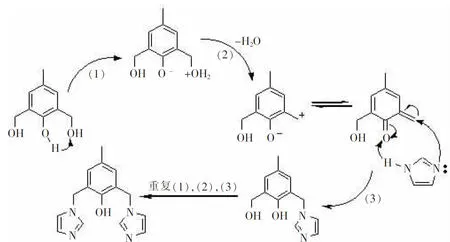
2.2 杯芳烃类似物3、4对ATP的识别
双咪唑鎓杯芳烃类似物3、4对ATP分子核磁滴定的1H谱对比图如下:
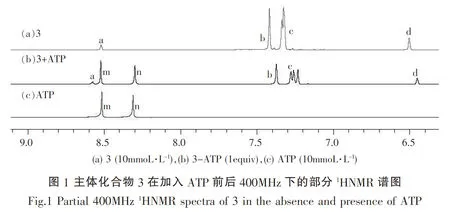
在图1中,在未加入ATP前主体化合物3中各峰的化学位移,δa=8.52,δb= 7.42,δc=7.33,δd=6.50.在加入ATP后,主体化合物3-ATP(1equiv)中各峰的化学位移,δa,=8.58,δb,= 7.37,δc,=7.26,δd,=6.45.比较加入ATP前后,主体化合物3-ATP(1equiv)中咪唑鎓环C-2H的化学位移向低场发生了偏移Δδa=0.06(<0.1),咪唑鎓环C-4H(b)和C-5H(b)的化学位移向高场发生了偏移Δδb=0.05(<0.1),主体化合物3中苯环上的化学位移向高场发生了偏移Δδc=0.07,Δδd=0.05,且主体化合物3中CH3-Ph-2H的化学位移H(c)质子的峰位变宽.加入ATP前后,主体化合物3中各质子的化学位移峰值和峰形的变化较大,说明主体化合物3对ATP的识别能力较强.我们推测主体化合物3对ATP识别不但是通过咪唑鎓环C-2H形成氢键作用,而且主体3整体的类杯芳烃结构也起到了一定的协同作用,增强了对ATP的识别能力.
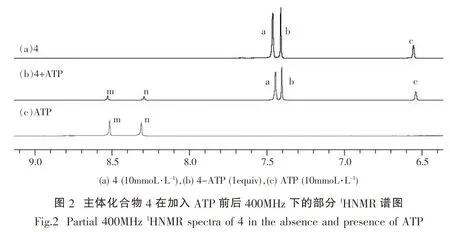
从图2看出,在未加入ATP前主体化合物4中各峰的化学位移,δa=7.46,δb=7.41,δc=6.55.在加入ATP后,主体化合物4-ATP(1equiv)中各峰的化学位移,δa’=7.44,δb’=7.40,δc’=6.54.比较加入ATP前后,主体化合物4-ATP(1equiv)中咪唑鎓环C-2H的化学位移在图谱中没有出现,而咪唑鎓环C-4H(a)和C-5H(a)的化学位移向高场发生了偏移Δδa=0.02(<0.1),主体化合物4中苯环上的化学位移向高场发生了偏移Δδb=0.01,Δδc=0.01.加入ATP前后,主体化合物4中各质子峰的化学位移变化较小,说明主体化合物4对ATP的识别能力较弱.相对于主体3,主体4的类杯芳烃结构性要更差一些,所以主体4对ATP的识别能力较弱.
Ramaiah课题组[17]和Kim课题组[7]分别报道了主体分子能对ATP进行识别,这可能与ATP中糖单元上的多羟基形成氢键作用有关.对比图1、图2,主体化合物3、4对ATP分子识别的差异,与其结构差异密不可分.其共同之处是具有相同个数的咪唑2-H,能与ATP中糖单元上的多羟基能形成氢键作用,实现对ATP进行识别.不同之处在于主体3的结构更接近于杯芳烃,主体3中的酚羟基可与咪唑鎓环2-H协同作用识别ATP,不排除主体3在识别ATP时,酚羟基中的氢原子可能与ATP的多磷酸单元中的氧负离子形成很强的氢键作用的可能,从而增强了对ATP分子的识别性能.
3 结 论
综上所述,本文在Kim课题组用多咪唑鎓环番对核苷酸分子识别的基础之上,在咪唑鎓环番的芳环上引入羟基,其主体化合物的结构完全与杯芳烃类似,与普通的咪唑鎓环番4相比,双咪唑鎓杯芳烃类似物3的结构更接近杯芳烃,对ATP分子识别时,能与ATP中糖单元上的多羟基有效形成氢键作用[7, 17],这一良好效果的取得,是多咪唑鎓环番对核苷酸分子识别的拓展和延续,必将为新型多咪唑鎓环番对核苷酸分子识别提供新的思路和理念.
[1] ZUO C S,QUAN J M,WU Y D.Oxa-Bicyclocalixarenes: A New Cage for Anions via C-H…Anion Hydrogen Bonds and Anion…π Interactions[J].Org. Lett.,2007,9(21):4219-4222.
[2] VINCENT L P,ANN J S,BRAIN R G,et al. Progress in Ingorganic Chemistry [J].1997,45:83-176.
[3] LECLERCQ L,SCHMITZER A R.Dibenzylimidazolium Halides: From Complex Molecular Network in Solid State to Simple Dimer in Solution and in Gas Phase [J].J. Phys. Chem. A.,2008,112(22):4996-5001.
[4] BEER P D,GALE P A.Anion Recognition and Sensing: The State of the Art and Future Perspectives[J].Angew. Chem. Int. Ed. Engl.,2001, 40(3): 486-516.
[5] SCHMIDTCHEN F P,BERGER M.For Recent Reviews of Anion Recognition.Chem [J].Rev.,1997,97,1609-1646.
[6] SCHEERDER J;ENGBERSEN,J. F. J;REINHOUDT,D N Recl,Tray.For Recent Reviews of Anion Recognition [J].Chim. Pays-Bas.,1996,115,307-320.
[7] NISAR A,BAHAREH S,KIM K S. et al.Fluorescent Imidazolium-Based Cyclophane for Detection of Guanosine-5′-Triphosphate and I in Aqueous Solution of Physiological pH[J].Org. Lett.,2011,13(20):5476-5479.
[8] AHMED N.,SHIRINFAR B,KIM K S. et al.A Highly Selective Fluorescent Chemosensor for Guanosine-5′-Triphosphate via Excimer Formation in Aqueous Solution of Physiological pH[J].Chem. Commun.,2012,48(31):2662-2664.
[9] SHIRINFAR B.,PARK Y. S.,KIM K S. et al.Selective Fluorescent Detection of RNA in Living Cells by Using Imidazolium-Based Cyclophane Imidazolium-Based Cyclophane[J].J. Am. Chem. Soc.,2013,135,90-93.
[10] NISAR A,BAHAREH S,KIM K S. et al.Selective Detection of Guanosine-5′-Triphosphate and Iodide by Fluorescent Benzimidazolium-Based Cyclophanes[J].Org. Biomol. Chem.,2013,11,6407-6413.
[11] MUHAMMAD Y,NISAR A,KIM K S. et al.Precise Tuning of Cationic Cyclophanes toward Highly Selective Fluorogenic Recognition of Specific Biophosphate Anions[J].Org. Lett.,2014,16(8):2150-2153.
[12] LI J Y,LIU D,LI Y Q,et al.A High Tg Carbazole-Based Hole-Transporting Material for Organic Light-Emitting Devices [J].Chem. Mater.,2005,17:1208-1212.
[13] GOSWAMI,S;MAITY S;DAS A K,et al.Remarkable ESIPT Induced NIR Emission by A Selective Colorimetric Dibenzimidazole Diimine Sensor for Acetate[J].Tetrahedron Lett.,2013,54(8):5232-5235.
[14] 蒋宗林,肖蓉,苏晓渝,等. 咪唑衍生物的一锅法选择性合成[J].高等学校化学学报.2003,24(1):64-67.
[15] 蒋宗林,鄢家明,刘长路,等.双咪唑的新法合成[J].四川大学学报.1998,34(4):616-618.
[16] YANG,L;LUO,L;JING S Y,et al.Self-assembly from Metal-Organic Vesicles to Globular Networks: Metallogel-Mediated Phenylation of Indole with Phenyl Boronic Acid[J].Chem. Commun.,2010,46(22):3938-3940.
[17] PRAKSH N,MAHESH H,RAMAIAH D.Synthesis of A Novel Cyclic Donor-Acceptor Conjugate of Selective Recognition of ATP[J].Org. Lett.,2005,7(26):5765-5768.
Synthesis, Structural Characterization and Recognition Activities for ATP of Calixarene Analogues Containing Bis-Imidazolium Rings
LI Yu-Fei, JIANG Zong-lin, PENG Qiong, PAN Yun qin
(School of Chemistry and Chemical Engineering,China West Normal University,Nan Chong 637009,China)
Two water-souble Calixarene Analogues Containing Bis-Imidazolium Rings 3, 4 were designed and synthesized.The structures of compounds 3,4 were confirmed by IR,1HNMR and MS spectra.Results showed that host compound 3 had better recognition activities than host compound 4 for ATP by the method of1HNMR tritration,because the structure of compound 3 was closer to Calixarene.
Calixarene analogue;imidazolium;ATP;Molecular Recognition;NMR titration;Michael Addition
1673-5072(2015)01-0036-05
2014-11-25
四川省教育厅自然科学基金重点项目(13ZA0009)
李宇飞(1988-),男,陕西咸阳人,西华师范大学化学化工学院硕士研究生,主要从事酶的化学模拟研究.
蒋宗林(1963-),男,四川达县人,西华师范大学化学化工学院副教授,硕士生导师,主要从事金属蛋白酶的化学模拟及高选择性有机合成研究.
0626.23
B
