HPLC法测定白带丸中芍药苷及盐酸小檗碱的含量
2015-03-14葛洁英
马 帅,葛洁英,周 蓬
(1.淄博市食品药品检验检测中心,山东淄博255086;2.安丘市鲁安药业有限责任公司,山东安丘262100)
HPLC法测定白带丸中芍药苷及盐酸小檗碱的含量
马 帅1,葛洁英2,周 蓬1
(1.淄博市食品药品检验检测中心,山东淄博255086;2.安丘市鲁安药业有限责任公司,山东安丘262100)
目的建立以高效液相色谱法同时测定白带丸中芍药苷及盐酸小檗碱含量的方法。方法 色谱柱为Wondasil C18Superb(4.6 mm×250 mm,5μm);流动相为乙腈-0.3%磷酸溶液,梯度洗脱,流速为1.0 mL·min-1,芍药苷的检测波长为230 nm,盐酸小檗碱的检测波长320 nm。结果芍药苷与盐酸小檗碱分别在0.106 29~2.125 8μg·mL-1(r=0.999 9)与0.060 21~1.204 2μg·mL-1(r=0.999 9)浓度范围内呈良好线性关系;平均回收率为98.45%与100.52%。结论本方法可用于白带丸的质量控制。
白带丸;芍药苷;盐酸小檗碱;高效液相色谱法
白带丸由黄柏(酒炒)、椿皮、白芍、当归、香附5味药组成,有清热、除湿、止带的功效,自1977年以来,一直为《中国药典》所收载。《中国药典》2010年版标准中,其检验项目为HPLC法测定盐酸小檗碱的含量[1]。而方中白芍含有的有效成分芍药苷也可用于该药的质量控制[2]。为了控制白带丸的质量,保证其疗效,采用HPLC法对白带丸中芍药苷、盐酸小檗碱成分同时进行测定。方法学考察结果表明,该方法灵敏度高,重现性好,测定结果准确,样品处理简单。
1 仪器与试药
1.1 仪器 LC-20AT高效液相色谱仪,SPD-20A UV/VIS检测器(日本岛津公司);Mettler AE240电子分析天平(梅特勒-托利多仪器有限公司);KS- 300E超声波清洗机(宁波科生仪器厂)。
1.2 试药 芍药苷对照品(中国食品药品检定研究院,批号:110736-201035)、盐酸小檗碱对照品(中国食品药品检定研究院,批号:110713-200910);样品为白带丸(河北万岁药业有限公司,批号为:130103、130409;山东孔圣堂制药有限公司批号:20806);乙腈为色谱纯,水为超纯水,其余试剂均为分析纯。
2 方法与结果
2.1 色谱条件 Wondasil C18Superb(4.6 mm×250 mm,5μm),流速:1.0 mL·min-1,柱温:40℃,以乙腈为流动相A,0.3%磷酸溶液为流动相B,按梯度洗脱;检测波长0~12 min,230 nm;12~23 min,320 nm;23~35 min,230 nm,结果见表1。。在此色谱条件下,理论板数按芍药苷、盐酸小檗碱计算均不低于4 000。

表1 梯度洗脱顺序
2.2 溶液的制备
2.2.1 对照品溶液的制备 精密称取芍药苷(11.20 mg)、盐酸小檗碱(12.30 mg),加甲醇制成每1 mL分别含芍药苷106.29μg、盐酸小檗碱60.21μg的混合溶液,作为对照品储备液。
2.2.2 供试品溶液的制备 取本品适量,研细,取约0.3 g,精密称定,精密加入盐酸-50%甲醇(1∶100)混合溶液25 mL,称定重量,超声处理30 min(500 W,40 kHz),放冷,用盐酸-50%甲醇(1∶100)混合溶液补足减失的重量,摇匀,滤过,取续滤液,即得[1]。
2.2.3 阴性对照溶液的制备 取处方中除白芍、黄柏外的其他药味,按白带丸制备方法制成阴性样品,按“2.2.2”项下方法操作,制备阴性对照溶液。
2.3 专属性试验 分别精密吸取上述对照品溶液、供试品溶液和阴性对照溶液各10μL,注入液相色谱仪,记录色谱图。在供试品色谱峰与对照品色谱峰相应保留时间的位置上,供试品有相同保留时间的色谱峰,阴性对照溶液无干扰,结果见图1。

图1 白带丸测芍药苷及盐酸小檗碱HPLC图A.对照品;B.样品;C.阴性对照样品 1.芍药苷;2.盐酸小檗碱
2.4 线性关系考察 精密吸取“2.2.1”项下对照品溶液1.0、2.0、5.0、10.0、15.0、20.0μL,注入液相色谱仪,记录峰面积,以对照品进样量为横坐标,峰面积为纵坐标绘制标准曲线,芍药苷回归方程为:Y=1 489 931X+6 014,r=0.999 9;盐酸小檗碱回归方程为:Y=549 986X+14 100,r=0.999 9。结果表明芍药苷在0.106 29~2.125 8μg·mL-1范围内呈良好的线性关系,盐酸小檗碱在0.060 21~1.204 2 μg范围内呈良好的线性关系。
2.5 精密度试验 取“2.2.1”项下对照品溶液10 μL,连续进样5次,结果芍药苷、盐酸小檗碱峰面积的RSD分别为0.26%、0.62%,表明精密度良好。
2.6 重复性试验 取同一批(批号:130103)样品6份,按“2.2.2”项下方法制备供试品溶液,以“2.1”项下色谱条件测定峰面积。结果芍药苷及盐酸小檗碱含量的平均值(n=6)分别为4.38、4.40 mg·g-1,RSD分别为1.5%、1.9%,表明本法重复性良好。
2.7 稳定性试验 取同一供试品溶液,置室温下放置,分别在0、2、4、8、16、24 h各进样10μL,测定芍药苷、盐酸小檗碱色谱峰峰面积RSD分别为0.39%、0.36%,表明供试品溶液在24 h内稳定。
2.8 加样回收试验 取已知含量的本品(批号:130103,芍药苷及盐酸小檗碱含量分别为4.38、4.40 mg·g-1)供试品适量,研细,取约0.1 g,精密称定,置具塞锥形瓶中,共6份,分别精密加入对照品溶液5 mL及盐酸-50%甲醇(1∶100)20 mL,按“2.2.2”项下方法制备,测定芍药苷及盐酸小檗碱的含量,计算平均回收率及RSD值,结果见表2、3。

表2 芍药苷的加样回收结果
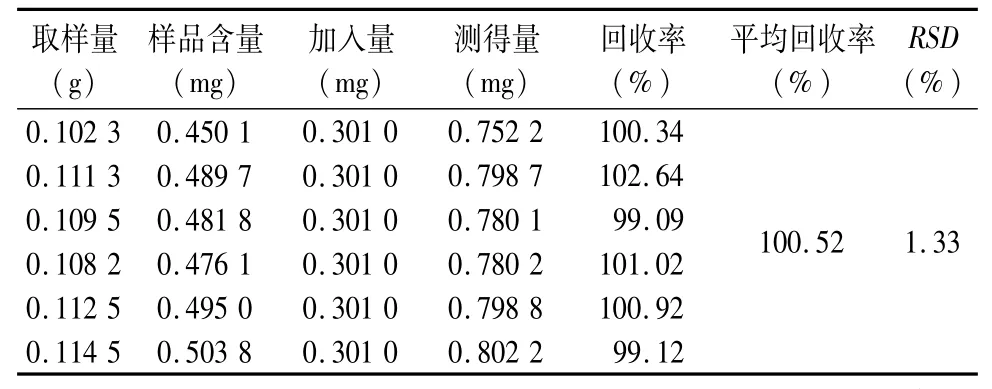
表3 盐酸小檗碱的加样回收结果
2.9 样品测定 取不同批号的样品,分别按“2.2.2”项下方法制备供试品溶液,按“2.1”项下色谱条件进样测定,结果见表4。

表4 样品含量测定结果
3 讨论
3.1 检测波长的选择 芍药苷、盐酸小檗碱分别在230、320 nm处有最大吸收,采用单波长不能兼顾这两种成分的检测,选择双波长检测模式。
3.2 提取溶剂、提取方法及提取时间的选择 比较了超声提取法和加热回流法,两种方法提取效率相当,但超声提取法操作简单;考察了以甲醇,50%甲醇,盐酸-50%甲醇(1∶100)混合溶液为提取溶剂[3~10],结果盐酸-50%甲醇(1∶100)混合溶液提取效果较好;考察了超声提取15、30、45、60 min,实验表明超声提取30 min后,延长提取时间,提取量无明显差别。故确定以盐酸-50%甲醇(1∶100)混合溶液为提取溶剂,超声提取30 min。
3.3 流动相的选择 本试验通过选用不同溶剂系统作为流动相进行试验,分别采用乙腈-水、乙腈-0.3%磷酸溶液等作为流动相[3~10],结果表明,乙腈-0.3%磷酸溶液峰形好,基线较稳定。同时,为解决芍药苷与盐酸小檗碱的分离问题,选择梯度洗脱程序,同时也大大缩短分析时间。因此选择乙腈-0.3%磷酸溶液进行梯度洗脱。
3.4 小结 采用双波长HPLC同时测定白带丸中芍药苷、盐酸小檗碱的含量,灵敏度高,专属性强,重现性好,可用于该制剂质量控制的依据。
[1] 国家药典委员会.中华人民共和国药典2010年版(一部)[S].北京:中国医药科技出版社,2010:655-656.
[2] 邓君丽,梁洪华.HPLC法测定白带丸中芍药苷的含量[J].中国药品标准,2005,6(3):205-206.
[3] 张玲容.HPLC测定白带丸中盐酸小檗碱的含量[J].中华中医药学刊,2011,29(4):905-906.
[4] 师永清,康淑荷,王爱军.HPLC法同时测定黄连双清丸中栀子苷、芍药苷、黄芩苷、盐酸小檗碱和大黄素的含量[J].药物分析杂志,2013,33(9):1612-1616.
[5] 刘峰.HPLC法测定天麻眩晕宁合剂中天麻素和芍药苷的含量[J].药学研究,2014,33(7):386-388.
[6] 吴基威,朱锐金.高效液相色谱法测定茴桂妇炎胶囊中芍药苷的含量[J].中国中医药杂志,2010,17(11):43.
[7] 李启红,杨青军,于绍华.HPLC法测定胃炎康胶囊中芍药苷、盐酸小檗碱及甘草酸的含量[J].中国保健营养,2010,10(1):32-34.
[8] 蔡清宇,张沂,郝特,等.HPLC法测定舒利通颗粒中巴马丁和小檗碱的含量[J].中国实验方剂学杂志,2010,16(2):42-44.
[9] 董长萍,张丹,李生,等.HPLC测定清胃止痛微丸中盐酸小檗碱和芍药苷的含量[J].中国现代中药,2014,16(12):1027-1030.
[10]彭柳,周俊,范开静,等.HPLC法测定金明和胃胶囊中盐酸小檗碱的含量[J].中国现代中药,2013,27(5):66-68.
Determ ination of paeoniflorin and berberine hydrochloride in Baidai Pills by HPLC
MA Shuai1,GE Jie-ying2,ZHOU Peng1
(1.Zibo Institute for Food and Drug Control,Zibo 255086,China;2.Anqiu Luan Pharmaceutical Co.,Ltd.,Anqiu 262100,China)
ObjectiveTo establish an HPLCmethod for the determination of paeoniflorin and berberine hydrochloride in Baidai Pills.M ethodsPaeoniflorin and berberine hydrochloride were separated on Wondasil C18Superb(4.6 mm×250 mm,5μm)column.Themobile phasewas acetonitrile and 0.3%phosphoric acid-solution in gradientmode.The flow rate was 1.0 mL·min-1.The detection wavelength for paeoniflorin was set at 230 nm,and 320 nm for berberine hydrochloride.ResultsThe linear range of paeoniflorin and berberine hydrochloride were 0.106 29~2.125 8μg·mL-1(r=0.999 9)and 0.060 21~1.204 2μg·mL-1(r=0.999 9),and their average recoverieswere98.45%and 100.52%respectively.ConclusionThemethod can be used for the quality control of Baidai Pills.
Baidai Pills;Paeoniflorin;Berberine Hydrochloride;HPLC
R927.2
A
2095-5375(2015)07-0398-003
马帅,女,药师,研究方向:药物分析,E-mail:331425710@qq.com
