腹腔镜辅助胃癌切除术185例报告
2015-03-13蔡丽生蔡铭智陈秋贤沈俊涛方顺勇
蔡丽生 蔡铭智 陈秋贤 沈俊涛 方顺勇
(福建医科大学附属漳州市医院普外二科,漳州 363000)
临床论著·
腹腔镜辅助胃癌切除术185例报告
蔡丽生 蔡铭智 陈秋贤 沈俊涛 方顺勇
(福建医科大学附属漳州市医院普外二科,漳州 363000)
目的 探讨腹腔镜辅助胃癌切除术的安全性及近期效果。 方法 2010年1月~2014年11月,行185例腹腔镜辅助胃癌切除术;腹腔镜下行淋巴清扫,上腹小切口切除标本并行消化道重建。 结果 185例顺利完成腹腔镜辅助胃癌切除手术,围手术期死亡1例。根治性切除(D2)177例,联合脏器切除8例。术后发生外科并发症18例(9.7%),包括腹腔感染10例,切口感染3例,吻合口出血2例,吻合口漏1例,十二指肠残端漏1例,腹腔内大出血1例;非外科并发症11例(5.9%),包括肺炎10例,心肌梗死1例(死亡)。175例(94.6%)术后随访1~59个月,中位数23个月。术后死亡12例,其中10例死于肿瘤复发(均为Ⅲ、Ⅳ期),2例死于其他疾病,3例肿瘤复发带瘤生存。 结论 腹腔镜辅助胃癌切除术安全、可行,手术近期疗效令人满意,远期结果有待进一步观察。
胃癌; 胃切除术; 腹腔镜
随着腹腔镜技术进步及医疗器械的改进,目前腹腔镜胃癌切除手术已经受到多数学者的支持[1]。但是关于进展期胃癌是否适合行腹腔镜手术,及术后远期效果仍有待研究。为进一步研究各期胃癌腹腔镜下根治术的效果,2010年1月~2014年11月我科实施腹腔镜辅助胃癌切除术185例,现报道如下。
1 临床资料与方法
1.1 一般资料
本组185例,男112例,女73例。年龄26~83岁,平均57.9岁。上腹疼痛106例,上消化道出血27例,呕吐、进食后腹胀等幽门梗阻症状18例,进食哽咽感26例,胃镜体检发现25例。均经胃镜检查明确诊断,肿瘤直径0.8~7.5 cm,平均4.6 cm;位于胃底贲门92例,胃体26例,胃窦67例;活检病理均为腺癌,其中溃疡癌变25例,低分化腺癌110例,中分化腺癌21例,高分化腺癌29例;术前TNM分期Ⅰ期23例,Ⅱ期61例,Ⅲ期99例,Ⅳ期2例。贫血76例,血红蛋白65~138 g/L;低白蛋白血症67例,血白蛋白28~43 g/L。35例术前分期为Ⅲ~Ⅳ期患者采用紫杉醇联合奥沙利铂术前辅助化疗3个疗程,CT或MRI检查估计可在腹腔镜辅助下得到R0切除后行手术治疗。
入选标准:胃癌诊断明确;术前影像学评估肿瘤可以完整切除;可耐受腹腔镜手术。
1.2 方法
1.2.1 术前准备 同一般开放胃癌手术,常规放置胃肠减压,麻醉后抽吸胃内可能的积气积液减小胃腔有助于暴露。
1.2.2 术中体位及trocar位置 仰卧位。A点(观察孔10 mm trocar)在脐下缘,进30°腹腔镜;B点(主操作孔12 mm trocar)在左腋前线、肋缘下约2 cm处,按横结肠位置及病人肥胖程度适当调整;C点(术者辅助操作孔5 mm trocar)在左腹直肌外缘平脐上2 cm处;D点(助手辅助操作孔5 mm trocar)在右腹直肌外缘平脐上2 cm处;E点(助手辅助操作孔5 mm trocar)位于右锁骨中线、肋缘下约2 cm处。对于腹腔有手术史或建立气腹困难者,采用开放气腹。
1.2.3 手术方式
(1)腹腔镜下肉眼检查、器械探查,如病灶较小,采用纳米碳胃镜下注射定位及显示淋巴结肿大情况(图1、2)。根据肿瘤具体位置、大小决定手术方式。Ⅰ、Ⅱ、Ⅲ期均采用D2+淋巴清扫术;Ⅳ期根据具体情况处理,如果转移灶能够完全切除则采用D2+淋巴清扫术,如无法完全切除行姑息性胃切除。腹腔镜辅助根治性远端胃及全胃切除术步骤采用黄昌明[2]的方法进行分离;然后取上腹部5~7 cm辅助切口,完成切除肿瘤并重建胃肠道。
(2)胃癌联合脾脏及胰体尾扩大根治术:如肿瘤累及胰腺尾部或脾门淋巴结转移明显,行脾脏及胰体尾切除。显露胰腺下缘,沿胰腺后方间隙分离至上方与胰上间隙相通(图3),把胰体尾部向上牵拉,分离胰腺后方至脾下并切断脾结肠、脾膈韧带,完全游离全胃、胰腺体尾及脾脏(图4),用Endo-GIA腔内直线切割器切断胰体尾部(图5)。
(3)联合其他脏器切除:分离胃周围后,暂不开腹。其中2例合并卵巢种植性转移,探查未发现其他部位转移,行双侧附件及子宫切除术,取下腹辅助孔,行腔镜下双侧附件及子宫切除,然后把标本置于上腹部,上腹辅助切口取出标本,再切除胃肿瘤完成胃肠重建。1例行左肝外侧叶单一转移灶(2 cm)切除,在完成胃周分离后,用超声刀在距离肿瘤边缘约1 cm处分离切除肿瘤。
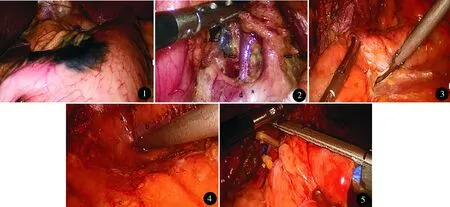
图1 纳米碳标志肿瘤位置 图2 胰腺上沿分离后(a-纳米碳染色淋巴结;b-胃冠状静脉;c-胃左动脉;d-肝总动脉) 图3 胰腺下方切开后腹膜 图4 胰腺后方及上方间隙(a-脾膈韧带;b-脾;c-左肾上腺) 图5 Endo-GIA切断胰体尾部
2 结果
2.1 手术结果
185例在腹腔镜辅助下完成胃癌切除术,其中12例术前纳米碳定位肿瘤位置。淋巴结清扫范围:D2根治术177例,联合脏器切除术8例。术后病理高分化腺癌21例,中分化腺癌45例,低分化腺癌82例,印戒细胞癌37例;TNM分期Ⅰ期28例,Ⅱ期56例,Ⅲ期98例,Ⅳ期3例。各术式手术结果见表1。
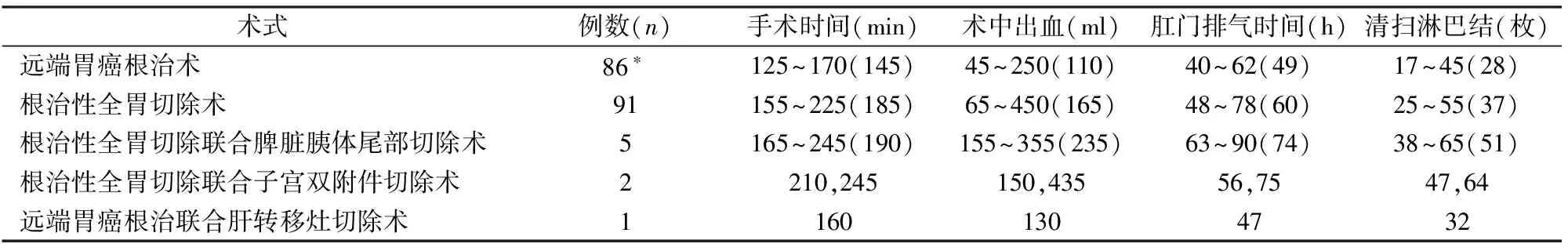
表1 185例腹腔镜辅助胃癌根治术手术情况
*其中1例围手术期死亡
括号内为均数
术后发生外科并发症18例(9.7%),包括:腹腔感染10例,发生在术后48小时以后,腹腔引流液浑浊,细菌培养证实有细菌感染,其中脾窝脓肿2例,脾脏脓肿1例,经抽脓治疗治愈,1例合并胰漏,经引流及抗感染2周后治愈;切口感染3例,经换药后愈合;吻合口出血2例,其中1例术后第6天呕血、休克,胃镜检查证实吻合口一动脉断端出血,使用止血夹夹闭后无再出血,另1例胃管持续引流暗红色血液,心率110次/min,血压95/45 mm Hg,经输血、扩容及生长抑素治疗后治愈;吻合口漏1例,为远端胃癌根治毕罗Ⅰ式吻合,术后第2天右侧腹腔引流管引流出胆汁样液体,造影证实吻合口后壁小漏口,放置肠内营养管营养支持、抗感染等治疗2周后漏口愈合;十二指肠残端漏1例,经引流及抗感染后愈合;腹腔大出血1例,术后2小时腹腔引流出血性液体800 ml,伴血压下降,紧急开腹见胰腺上沿肝总动脉分支出血,缝扎止血成功。
非外科并发症11例,包括肺炎10例,术后2~5天咳嗽、咳痰,胸片证实肺部炎症,细菌培养阳性6例,经抗感染治疗治愈;心肌梗死1例,术前有长期冠心病史,术后6 h胸痛、血压下降,心跳骤停,心电图ST段低平,考虑急性心肌梗死,抢救无效死亡。
2.2 术后随访
术后128例经过5-FU联合奥沙利铂规则化疗8~12个疗程,28例不规则化疗,29例未化疗。175例(94.6%)术后随访1~59个月,中位数23个月(<12个月54例,12~24个月65例,24~36个月21例,>36个月35例)。Ⅰ、Ⅱ期84例均无肿瘤复发。术后死亡12例,其中10例死于肿瘤复发,均为Ⅲ、Ⅳ期,2例死于其他疾病,术后生存时间7~25个月,平均18.5月。3例肿瘤复发带瘤生存。
3 讨论
3.1 腹腔镜胃癌切除的手术适应证
国外学者多数支持胃癌腹腔镜手术仅适用早期胃癌[3,4];根据我国卫生部颁发的《胃癌诊疗规范2011年版》,目前推荐腹腔镜根治性手术选择Ⅰ期病例。本组Ⅰ、Ⅱ期随访过程中均未出现肿瘤复发。对于Ⅲ、Ⅳ期病人是否适合行腹腔镜手术目前尚存争议;多数推荐仅诊断性腹腔镜对进展期病例进行临床分期。近年来,越来越多研究表明[5,6],腹腔镜手术治疗局部进展期胃癌实际上已被普遍接受,并广泛开展。我们早期主要把腹腔镜胃切除手术应用于治疗胃良性疾病和早期胃癌;技术成熟、团队配合熟练后逐渐把腹腔镜用于进展期胃癌甚至晚期肿瘤,手术操作能够遵循开放胃癌根治术原则,同样取得较好的近期效果。
3.2 腹腔镜胃癌联合脏器切除术是否合适
目前关于胃癌根治术联合脾脏及胰体尾部切除切除是存有争议的,2013版《NCCN胃癌临床实践指南》关于胃癌根治术认为T4期肿瘤需要将累及组织整块切除,所以当肿瘤累及脾脏或脾门淋巴结明显有肉眼可见转移时,可以考虑脾切除术;当累及胰、肝脏或部分结肠时也可行扩大切除手术。朱正纲等[7]认为,为了清扫脾门转移淋巴结,可行联合脾脏切除术。是否使用腹腔镜完成联合脏器切除,目前存在争议。我们认为使用腹腔镜辅助下切除胰腺体尾部及脾脏难度并不大,完全可以达到与开放相同的效果,共完成5例胰体尾联合脾脏切除术,5例随访均超过1年,1例腹腔肿瘤种植转移,由于病例数较少,且肿瘤多为晚期,其远期效果有待进一步研究。本组2例卵巢转移,未发现其他部位转移,使用腹腔镜切除双侧附件及子宫,手术过程及术后恢复都比较顺利,2例随访超过1年,未发现肿瘤复发。1例左肝外侧叶单一转移灶,直径2 cm,行胃癌切除同时在腹腔镜下切除左肝转移灶,术后恢复良好,随访18个月,无肿瘤复发。上述病例显示,随着腔镜技术的进步及经验的积累,使用腹腔镜完成良好脏器切除是可行和安全的。
3.3 腹腔镜胃癌切除术重建方式
消化道重建是腹腔镜胃癌手术的另一技术难点,也是比较耗时的手术步骤。消化道重建的方式分为完全腹腔镜下吻合及小切口辅助吻合,多种腹腔镜下吻合方式均取得不错的效果[8]。但我们认为,做上腹辅助小切口切除肿瘤取出标本,再利用该切口完成胃肠道重建,是一种简单、安全且经济的方法,可以减少初学者的学习曲线及降低手术难度。对于远端胃大部切除术后的消化道重建方法,多采用残胃空肠Billroth Ⅱ式吻合,吻合口下方再加空肠侧侧吻合减少胆汁反流性胃炎,建议采用结肠后吻合有助于胃的排空。全胃切除我们多采用结肠后食管空肠“P”襻Roux-en-Y吻合,有助于增强空肠代胃功能及避免“盲襻综合征”。完成器械缝合后,检查吻合情况,吻合口使用可吸收缝线全层缝合加固,减少术后吻合口漏及出血风险。我们采用这样重建和缝合方法取得较满意结果。
3.4 手术并发症的发生与预防
防治腹腔镜胃癌根治术后并发症关系到病人安全及术者信心的培养。有经验的外科医师行腹腔镜胃癌根治术发生的并发症低于开放手术组[9]。在确保胃癌手术根治性的前提下,减少术后并发症的发生,一直是国内外学者关注的热点[10]。本组手术发生的并发症与亚洲其他学者报道胃癌根治术后并发症发生率基本相同[11]。随着手术例数的逐年递增,术中和术后并发症发生率逐年下降[12]。我们认为,初期开展胃癌手术时,应该做好充分准备,术者应该具有良好的胃癌开腹手术及腹腔镜手术经验;选择合适病例,最好在有经验的腹腔镜胃癌手术医师带领下完成,每次手术前应该反复与助手研究其他患者手术视频探讨手术方案,做好术中发生意外并发症的预案;手术过程中应该遵循胃癌根治术的原则,每个手术步骤不马虎,避免在视野不清的情况下盲目操作,手术难度应循序渐进,合理使用超声刀,避免止血不彻底伤及重要血管;完成重建后应详细检查吻合口及胃周各血管的处理情况,必要时适当提升血压检查是否有出血;术中出现出血等意外情况时不要慌张,应合理使用各种止血技术,多数能在腹腔镜下控制住出血;如果在腔镜阶段处理不满意,应记录,待开放吻合后再次检查。
本回顾性分析显示,腹腔镜辅助胃癌根治性切除术是可行和安全的,有开放胃癌根治术经验的外科医师,通过经验的积累,循序渐进开展该手术,可以减少手术的并发症,提高手术的安全性。
1 许燕常,李志雄,林文霖.腹腔镜辅助与开腹胃癌D2根治术的对比研究.中国微创外科杂志,2013,13(6):485-488.
2 黄昌明,王家镔,郑朝辉,等.腹腔镜辅助胃远端癌淋巴结清扫术近期疗效.中华胃肠外科杂志,2009,12(6):584-587.
3 Ohtain H,Tamamori Y,Noguchi AK,et al.A meta-analysis of randomized controlled trials that compared laparoscopy-assisted and open distal gastrectomy for early gastric cancer.J Gastreintest Surg,2010,14(6):958-964.
4 Kitano S,Shiraishi N,Uyama I,et al.A multicenter study on oncologic outcome of laparoscopic gastrectomy for early cancer in Japan.Ann Surg,2007,245(1):68-72.
5 Fujita J,Kurokawa Y,Sugimoto T,et al.Survival benefit of bursectomy in patients with resectable gastric cancer: interim analysis results of a randomized controlled trial.Gastric Cancer,2012,15(1):42-48.
6 黄昌明.局部进展期胃上部癌腹腔镜淋巴结清扫的评价与策略.第三军医大学学报,2013,35(18):1896-1898.
7 朱正纲.扩大根治术在胃癌外科治疗中的临床意义.中华胃肠外科杂志,2006,9(1):11-12.
8 Kanaya S,Kawamura Y,Kawada H,et al.The delta-shaped anastomosis in laparoscopic distal gastrectomy:analysis of the initial 100 consecutive procedures of intracorporeal gastmduodenostomy.Gastric Cancer,2011,14(4):365-371.
9 Kim HH,Hyung WJ,Cho GS,et al.Morbidity and mortality of laparoscopic gastrectomy versus open gastrectomy for gastric cancer:an interim report-a phase Ⅲ multicenter,prospective,randomized Trial (KLASS Trial).Ann Surg,2010,251(3):417-420.
10 李 栋,周旭坤,李 平.腹腔镜进展期胃癌根治术66例报告.中国微创外科杂志,2011,11(9):773-775.
11 Huscher CG,Mingoli A,Sgarzini G,et al.Laparoscopic versus open subtotal gastrectomy for distal gastric cancer: five-year results of a randomized prospective trial.Ann Surg,2005,241(2):232-236.
12 Etch T,Inomata M,Shiraishi N,et al.Revisional surgery after gastrectomy for gastric cancel:review of the literature.Surg Laparosc Endosc Percutan Tech,2010,20(5):332-337.
(修回日期:2015-06-22)
(责任编辑:王惠群)
Laparoscopic-assisted Gastrectomy for Gastric Cancer:a Report of 185 Cases
CaiLisheng,CaiMingzhi,ChenQiuxian,etal.
DepartmentofGeneralSurgery,ZhangzhouAffiliatedHospitalofFujianMedicalUniversity,Zhangzhou363000,China
Correspondingauthor:CaiLisheng,E-mail:cailisheng@medmail.com.cn
Objective To evaluate the feasibility and safety of laparoscopic-assisted gastrectomy for gastric cancer. Methods From January 2010 to November 2014, laparoscopic gastrectomy was performed in 185 cases of gastric cancer. After resecting the stomach and involved lymph nodes by laparoscopy, we removed the samples and reconstructed the digestive tract by short abdominal incision. Results Laparoscopic procedure was completed successfully in all the 185 patients, and one patient died of myocardial infarction during perioperative period. Among the 185 cases, 177 received radical gastrectomy and 8 underwent extended radical operation. The incidence of surgical complications was 9.7% (18/185), including 10 cases of abdominal infection, 3 cases of wound infection, 2 cases of anastomotic bleeding, 1 case of anastomotic leakage, 1 case of duodenal stump leakage, and 1 case of abdominal bleeding. The incidence of non-surgical complications was 5.9% (11/185), including 10 cases of pulmonary infection and 1 case of myocardial infarction (dead). After the surgery, 175 patients (94.6%) were followed up for 1-59 months (median, 23 months). Twelve patients with Ⅲ/Ⅳ stage tumor died of cancer recurrence, and 2 patients died of other disease. Three patients with tumor recurrence survived. Conclusions Laparoscopic-assisted gastrectomy is feasible and safe for patients with gastric cancer. The short-term outcomes of the procedure is favorable, but the long-term outcomes remains uncertain.
Gastric cancer; Gastrectomy; Laparoscopy
福建医科大学漳州市医院院内基金项目(201204)
,E-mail:cailisheng@medmail.com.cn
R735.2
A
1009-6604(2015)09-0789-04
10.3969/j.issn.1009-6604.2015.09.006
2014-12-11)
