OrVil系统行胸腹腔镜联合Ivor-Lewis食管癌根治术临床分析
2015-03-12张旭刚李维青李志田
张旭刚,李维青,李志田,戈 烽
(首都医科大学附属北京世纪坛医院胸外科,北京100038)
随着腔镜技术的发展,许多临床中心报道了微创食管癌手术的安全性及有效性[1-2]。但他们多数采用颈部吻合,而腔镜下胃食管胸内吻合技术操作复杂,一直是胸外科医师挑战的难点。OrVil新型经口置入钉砧头技术能简化腔镜下消化道重建的操作步骤并缩短手术时间,从而简化了胸腹腔镜联合Ivor-Lewis食管癌切除术。本科从2010年3月至2013年5月应用OrVil系统施行胸腹腔镜联合Ivor-Lewis食管癌切除术共30例,效果良好,现报道如下。
1 资料与方法
1.1 一般资料 选择食管癌患者30例,术前均行胸部和腹部CT扫描、锁骨上及腹部彩超、电子胃镜、上消化道造影和胃镜活检,术前诊断明确。患者的一般资料见表1。
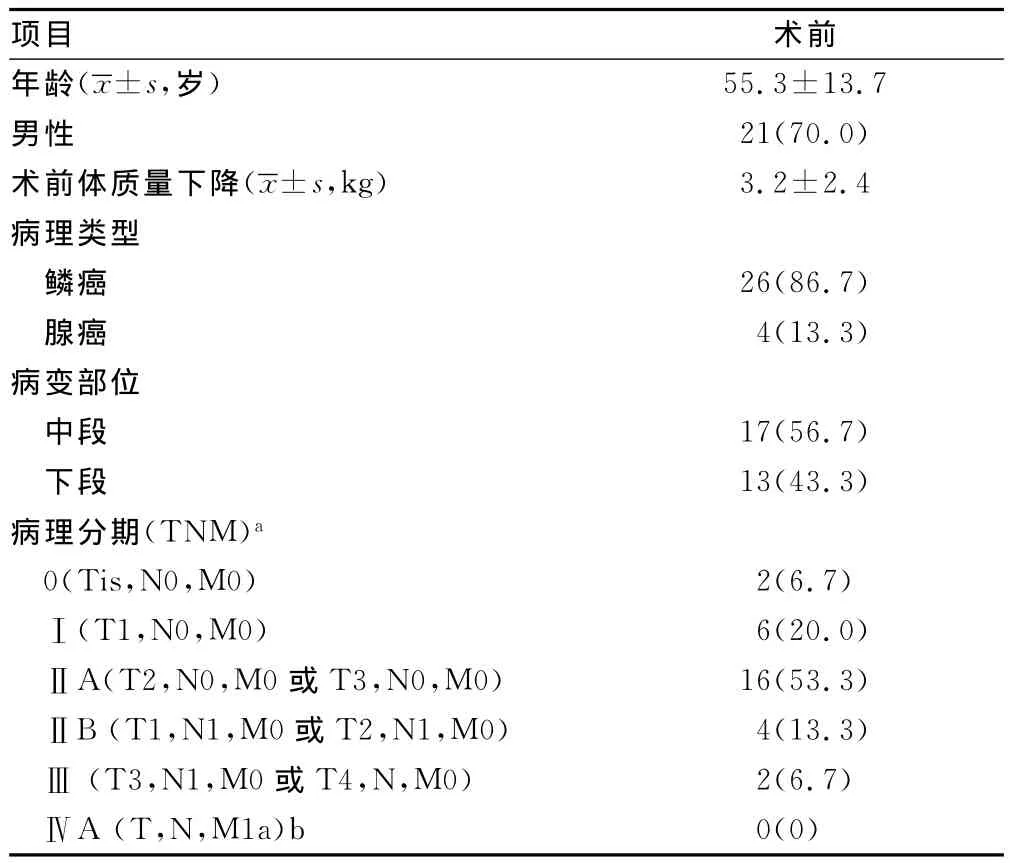
表1 患者的一般资料[n(%)]
1.2 方法
1.2.1 腹部手术 全身麻醉,患者取仰卧A字位。腹部5个戳卡:脐上为观察孔(10mm);右锁中线脐上水平(12mm)和左腋前线肋弓下缘(12mm)分别为主操作孔和副操作孔;左侧锁骨中线外侧肋缘下(5mm)和剑突下偏右侧(5mm)为助手辅助操作孔。建立人工气腹(压力15cm H2O)。用结扎速(ligaSure)距胃网膜右血管弓2cm切开胃结肠韧带,离断胃脾、胃膈韧带直至贲门左侧,切断胃网膜左动脉及胃短动脉。牵拉肝左叶,切开小网膜,游离肝胃韧带,将胃向上方翻起,在胰腺上缘游离胃左血管,清除胃左动脉旁淋巴结,胃左血管用Hem-o-lock夹闭后切断。应用Endo-GIA沿胃底大弯侧至胃角小弯侧水平连线制作管状胃。游离胃后壁及胃底。显露两侧膈肌脚并切断部分右侧膈肌脚,扩大食管裂孔,可将部分食管下段拽入腹腔。检查腹腔无活动性出血后,关闭腹腔切口。
1.2.2 胸部手术 患者转为左侧卧位。胸部观察孔位于右侧腋中线第7肋间,腋后线第8肋间做主操作孔,长约3cm(可进2根手指),听诊三角处设副操作孔(10mm),腋前线第4肋间为助手操作孔(10mm)。探查胸腔及食管病变,切开纵隔胸膜,切断下肺韧带,切开食管裂孔处胸膜,悬吊食管,结扎速环周游离下段食管。游离奇静脉弓,切断奇静脉,游离胸段食管,清扫周围淋巴结。距肿瘤上缘约5cm处用Endo-GIA切断闭合食管。经口放置OrVil吻合器钉砧头,经食管残端切口穿出。向上将胃体牵至胸腔,置入25mm端端吻合器机身,将大弯侧后壁与食管残端吻合,用Endo-GIA闭合胃前壁切口,胃壁浆肌层包埋。观察吻合口完整严密,放置胸腔引流管,关闭胸部操作孔。
1.2.3 观察指标 (1)手术有效性:手术时间、术中出血量、淋巴结清扫数目、输血比例、术后进流食时间。(2)手术安全性:中转开胸或开腹率、吻合口瘘、乳糜胸、胃排空障碍及二次手术发生率。(3)依据手术日期先后顺序,分为早期组和后期组,各15例,比较两组手术时间、术中出血量、清扫淋巴结数及中转开胸率。
1.3 统计学处理 应用SPSS 17.0统计软件对数据进行分析,计量资料符合正态分布、方差齐的数据用±s表示,组间比较采用t检验,计数资料用率表示,组间比较采用χ2检验,检验水准α=0.05,以P<0.05为差异有统计学意义。
2 结果
2.1 手术相关观察指标 见表2。
2.2 两组临床指标比较 后期组与早期组比较,其手术时间与术中出血量均明显减少,差异有统计学意义(P<0.05)。
2.3 随访情况 术后随访2~36个月,平均19.4个月,采用门诊定期复查或电话随访方式进行随访,其中1例(T2N0M0ⅡA期)患者于术后15个月出现颈部淋巴结转移,行颈部淋巴结清扫;1例(T3N1M0Ⅲ期)于术后10个月出现纵隔淋巴结肿大,行放疗治疗;1例于术后20个月出现吻合口复发,给予保守维持治疗;1例于术后29个月死亡。见表3。

表2 手术结果指标[n(%)]

表3 早、晚期手术临床指标比较
3 讨论
腔镜下消化道重建技术是全腔镜食管癌根治术的核心技术。由于腔镜下放置吻合器的钉砧头和制作荷包十分困难,且容易造成食管黏膜损伤,因此全腔镜吻合技术一直是手术的难点[3]。而微创食管癌切除术的Meta分析表明,胸、腹腔镜联合术式在某些方面优于传统术式[4]。
3.1 OrVil系统的应用 OrVil系统是一种一体化的经口钉砧头放置装置,倾斜钉砧头经胃管的引导容易通过口腔及食管上段,当钉砧头与吻合器器身对合后则会自动回复其功能位置。该法能简化钉砧头置入过程,避免腔镜下荷包缝合,从而缩短手术时间,吻合简单易行[5]。适用于食管中、下段肿瘤,肿瘤上缘距胸廓入口超过5cm的患者。2008年,Nguyen等[6]首次报道了采用OrVil技术进行胸、腹腔镜联合完全腔镜下食管癌根治术。2009年,OrVil系统进入中国,本科自2010年采用OrVil技术完成胸、腹腔镜联合完全腔镜下食管癌根治术。目前,已经使用这项技术完成手术30例,现将使用OrVil的注意事项总结如下:(1)放置时先用石蜡油润滑引导胃管和钉砧头;(2)使患者头部尽量后仰,钉砧头光面朝向硬腭一侧,松开气管插管气囊,方便钉砧头顺利通过上段食管;(3)多选择胃管顶起部位切开食管残端,切口不宜过大,直径约3mm,此时放置胃管的助手要持续向腔内推送,切忌暴力,直至胃管顶出;(4)钉砧头与吻合器对合时,须用腔镜抓钳夹持住钉砧头的白色部分,不可放松,保证对合确实,避免钉砧头退回食管残端内。
3.2 手术并发症 食管癌术后吻合口瘘是食管癌术后最常见、最严重的并发症之一。吻合口瘘治疗难度大、病死率高,尤其是胸腔内吻合口瘘,病死率在50%以上[7]。本组研究吻合口瘘发生率6.7%,与国外同类报道相近[8-9]。预防吻合口瘘的发生应注意:(1)保护血运。术中要减少对胃壁的牵拉、揉捏;必须保留胃网膜右血管,因其是管状胃主要血供来源;游离食管及清扫上纵隔淋巴结时应注意保留食管残端血供。(2)降低吻合口张力。将胃体游离至幽门部,使吻合时不存在张力,也不能扭曲;用大网膜对吻合口环行包埋,预防吻合口瘘的发生[10];术中将胃管送入胸胃内,术后保持胃肠减压通畅,防止因胃排空障碍或急性胃扩张导致吻合口瘘;为了避免复张肺的推挤或胃体悬挂于胸腔导致吻合口张力过大撕裂,可将胸、胃在纵隔内进行妥善固定以减少张力。(3)熟练掌握吻合器的正确使用方法。吻合时要确认钉座与吻合器之间无周围组织夹入,激发后退出时要缓慢旋转退出,防止撕裂吻合口。此外,术后管理不善,如低蛋白血症、患者术后痰多等,均增加吻合口瘘的概率。吻合口狭窄严重影响患者的生活质量,患者常有不同程度的吞咽困难,需要胃镜扩张。国外报道吻合口狭窄发生率8.7%~55.0%[11-12],本组30例患者,吻合口狭窄发生率16.7%。吻合口狭窄原因包括:吻合时周围组织内卷,胃和食管黏膜未能良好对合;组织受机械压迫愈合后易形成瘢痕;患者术后长期进流食,使吻合口未能有效扩张;吻合口处受到胃酸反流或碱反流,导致纤维瘢痕增生;术后吻合口瘘;术后放射线损伤;吻合口处肿瘤复发或转移的淋巴结外部压迫使食管狭窄等。
3.3 学习曲线 腔镜技术的应用有其不可避免的局限性。外科医生需重新适应新视野下的器械操作,且需要医生同时掌握胸腔镜及腹腔镜手术技巧,这个过程存在学习曲线。Osugi等[13]报道胸腔镜食管癌切除术经34例手术实践操作后,才能达到稳定状态。Song等[14]做了胸、腹腔镜治疗食管癌学习曲线的研究,但是由于只有28例患者,未能给出明确的学习曲线;陈焕文等[15]报道有经验医师完成胸、腹腔镜食管癌切除术的学习曲线大约为20例。本组30例患者均由同一术者完成,术者具有丰富的胸腔镜手术经验,且早在2007年开展胸腔镜食管癌根治行颈部吻合,积累了胸腔镜游离食管的经验。本研究表明:开展约15例后,手术时间明显缩短,术中出血量也明显下降,差异有统计学意义,提示技术达到相对稳定成熟状态。但对于缺乏胸腔镜手术经验的医师,15例可能偏少。
总之,应用OrVil系统行胸腹腔镜联合Ivor-Lewis食管癌根治术,是一种安全可靠的全腔镜下消化道重建辅助系统。由于这种技术新,手术操作难度和手术费用高,随访时间短及淋巴结未确认清扫是否彻底等原因,其远期效果还有待于多中心、大样本的研究进一步证实。
[1] Nguyen NT,Follette DM,Lemoine PH,et al.Minimally invasive Ivor Lewis esophagectomy[J].Ann Thorac Surg,2001,72(2):593-596.
[2] Braghetto I,Csendes A,Cardemil G,et al.Open transthoracic or transhiatal esophagectomy versus minimally invasive esophagectomy in terms of morbidity,mortality and survival[J].Surg Endosc,2006,20(11):1681-1686.
[3] Pennathur A,Awais O,Luketich JD.Technique of minimally invasive Ivor Lewis esophagectomy[J].Ann Thorac Surg,2010,89(6):S2159-2162.
[4] Biere SS,Cuesta MA,Van Der Peet DL.Minimally invasive versus open esophagectomy for cancer:a systematic review and meta-analysis[J].Minerva Chir,2009,64(2):121-133.
[5] Jaroszewski DE,Williams DG,Fleischer DE,et al.An early experience using the technique of transoral OrVil EEA stapler for minimally invasive transthoracic esophagectomy[J].Ann Thorac Surg,2011,92(5):1862-1869.
[6] Nguyen TN,Hinojosa MW,Smith BR,et al.Thoracoscopic construction of an intrathoracic esophagogastric anastomosis using a circular stapler:transoral placement of the anvil[J].Ann Thorac Surg,2008,86(3):989-992.
[7] Shiozaki H,Imamoto H,Shigeoka H,et al.Minimally invasive esophagectomy with 10cm thoracotomy assisted thoracoscopy for the thoracic esophageal cancer[J].Gan To Kagaku Ryoho,2003,30(7):923-928.
[8] Law S.Minimally invasive techniques for oesophageal cancer surgery[J].Best Pract Res Clin Gastroenterol,2006,20(5):925-940.
[9] Blewett CJ,Miller JD,Young JE,et al.Anastomotic leaks after esophagectomy for esophageal cancer:a comparison of thoracic and cervical anastomoses[J].Ann Thorac Cardiovasc Surg,2001,7(2):75-78.
[10] 陈正海.带蒂大网膜在食管癌贲门癌手术中的应用体会[J].吉林医学,2010,31(25):4367-4368.
[11] Blackmon SH,Correa AM,Wynn B,et al.Propensitymatched analysis of three techniques for intrathoracic esophagogastric anastomosis[J].Ann Thorac Surg,2007,83(5):1805-1813.
[12] Kondra J,Ong SR,Clifton J,et al.A change in clinical practice:apartially stapled cervical esophagogastric anastomosis reduces morbidity and improves functional outcome after esophagectomy for cancer[J].Dis Esophagus,2008,21(5):422-429.
[13] Osugi H,Takemura M,Higashino M,et al.Learning curve of video-assisted thoracoscopic esophagectomy and extensive lymphadenectomy for squamous cell cancer of the thoracic esophagus and results[J].Surg Endosc,2003,17(3):515-519.
[14] Song SY,Na KJ,Oh SG,et al.Learning curves of minimally invasive esophageal cancer surgery[J].Eur J Cardiothorac Surg,2009,35(4):689-693.
[15] 陈焕文,杜铭,吴庆琛,等.胸、腹腔镜食管癌切除术学习曲线分析[J].第三军医大学学报,2012,34(12):1237-1239.
