Nano-Au/复合壳聚糖@纳米碳修饰金电极检测亚硝酸盐
2015-03-11韩瑞芳曹艳萍王若珩张凌燕
韩瑞芳,曹艳萍,王若珩,张凌燕
(1.西北政法大学公安学院,陕西西安710063)
(2.西南政法大学刑事侦查学院,重庆401120)
0 引言
壳聚糖是天然生物高分子甲壳素的衍生物,具有无毒且可以成膜等许多优良性质,而该分子中含有丰富的氨基,其与纳米金之间有很强的亲和力,故被广泛用于传感器中制备电极[1]。
亚硝酸盐是肉制品及其它食品加工过程中常用的一种食品添加剂。此外,在泡菜及不新鲜的食物中也容易出现亚硝酸盐。食品中亚硝酸盐含量超过国家标准,就会导致食物中毒。由于亚硝酸对人体的危害,其检测受到全世界的重视。近些年来,国内外研究工作者利用电流型传感器对其进行检测的报道明显增多。国外主要选用特异性亚硝酸盐还原酶,Silveira.C.M 小组[2]为其代表,他们选用多媒体细胞色素c 和亚硝酸还原酶[3-6],Almeida.M.G 小组、Davis.J.J 小组等[7-8]用含铜型亚硝酸盐还原酶,C.C.Rosa 小组[9]则用细胞色素cd1 亚硝酸盐还原酶[10-11]作为亚硝酸盐特异性识别元素。国内的研究则主要集中在用非特异性蛋白如血红蛋白[12]、肌红蛋白[13-14]或细胞色素c[15]作为生物识别元素检测亚硝酸盐,而西南大学的袁若小组[16]则利用镧–多壁纳米碳管等具有催化性能的纳米材料作为识别元素检测亚硝酸盐,该传感器由于无酶或蛋白质,传感器稳定性显著提高。
该文采用带丰富氨基的壳聚糖(CS)分散纳米碳(Nano-C)后将其滴加于电极上,利用其氨基吸附纳米金(Nano-Au),从而制备了无生物物质标记且无电子媒介体的亚硝酸盐传感器:(1)该传感器制备及反应过程中无电子媒介体,故无电子媒介体渗漏、富集等不良问题,进一步提高了电极稳定性;(2) 该传感器在反应过程中无生物物质,显著提高了电极的使用寿命;(3) 该传感器制备简单,成本低廉。
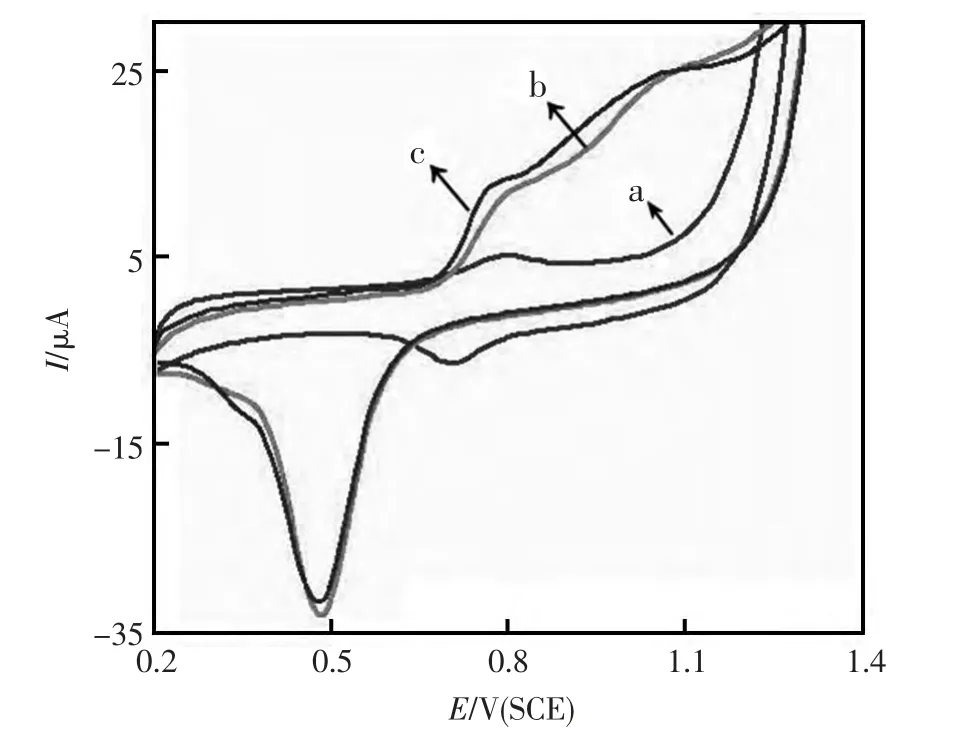
图1 电极修饰过程表征图:(a)裸金电极;(b)CS@Nano-C 修饰的金电极;(c)Nano-Au/CS@Nano-C 修饰的金电极,测试底液0.25 mol/L PBS(pH6.0)+25 μmol/L NO2-Fig.1 CV at a:(a)Au electrode,(b)CS@Nano-C modified Au electrode,(c)Nano-Au/CS@Nano-C modified Au electrode in PBS and NO2-
1 实验部分
1.1 仪器与试剂
壳聚糖、氯金酸(Sigma 公司),纳米碳(北京德科岛金科技有限公司);柠檬酸三钠(四川化学试剂厂)。实验用水为二次蒸馏水。
CHI660A型电化学工作站(上海辰华仪器公司) 三电极系统:Nano-Au/复合壳聚糖@ 纳米碳(Nano-Au/CS@ Nano-C) 修饰金电极为工作电极,饱和甘汞电极为参比电极,铂丝电极为对电极,0.25 mol/L PBS溶液(pH6.0)为测试底液。
1.2 免疫传感器的制备
取1 mg 壳聚糖和1 mL mol/L 醋酸溶液混合,对其超声2 h 后,然后取1mg 纳米碳加入4 mL 上述壳聚糖溶液中,超声分散4 h 后得到均匀分散的黑色悬浊液。在已预处理的金电极(Φ=4.0 mm)表面滴加8 μL CS@Nano-C,在室温条件下让其自然干燥,待完全风干后置入Nano-Au(4℃,8 h) 制的Nano-Au/CS@Nano-C 修饰电极,水洗后置于4℃冰箱中保存待用。
2 结果与讨论
2.1 电极自组装过程的电化学表征
以不同修饰状态的电极为工作电极,于0.25 mol/L PBS(pH6.0)测试底液中含25 μmol/L NO2-在0.2~1.2V 范围内进行循环伏安测定,所得循环伏安曲线如图1所示。图1a 是裸金电极的循环伏安曲线图,图1b 是CS@Nano-C 修饰金电极的循环伏安,由于Nano-C 催化性能,电极峰电流明显增大。当CS@Nano-C 修饰电极吸附Nano-Au后,由于纳米金具有良好的导电性,能促进电子的传递,故峰电流值继续增大(图1c)。
2.2 NO2-在Nano-Au/CS@Nano-C 修饰电极上的电化学行为
图2考查了Nano-Au/CS@ Nano-C 修饰电极对NO2-的电催化还原能力。当NO2-浓度分别是0 mol/L,0.9×10-4mol/L,4.0×10-4mol/L时,从图2a到图2c,可看出Nano-Au/CS@Nano-C 电极的氧化峰电流显著增加,这证明Nano-Au/CS@Nano-C 对NO2-有良好的电化学行为。
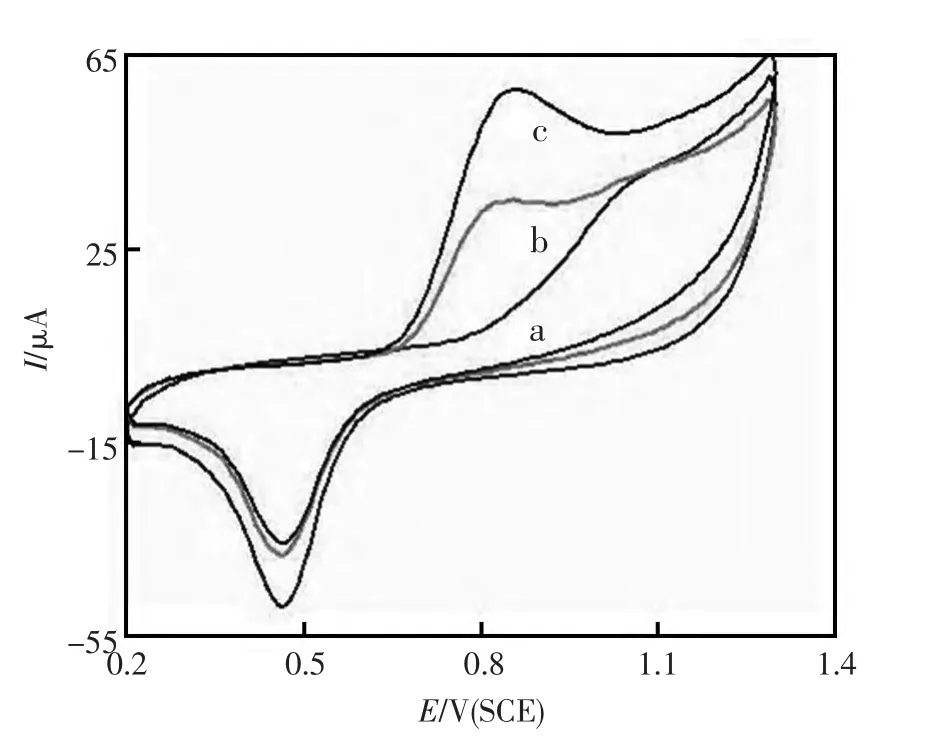
图2 Nano-Au/CS@Nano-C 修饰电极在0.25 mol/L PBS(pH6.0)中含不同NO2-的CV 响应:(a)0 mol/L,(b)0.9×10-4 mol/L,(c)4.0×10-4 mol/LFig.2 CV response of Nano-Au/CS@Nano-C modified Au electrode in PBS at various NO2-concentrations:(a)0 mol/L,(b)0.9×10-4 mol/L,(c)4.0×10-4 mol/L
2.3 实验条件优化
图3比较了CS@ Nano-C 与Nano-Au/CS@Nano-C 不同修饰电极对NO2-响应的影响。由图可见,与CS@Nano-C 修饰电极相比,Nano-Au/CS@ Nano-C 电极对NO2-响应最好,故选择Nano-Au/CS@Nano-C 电极为工作电极。
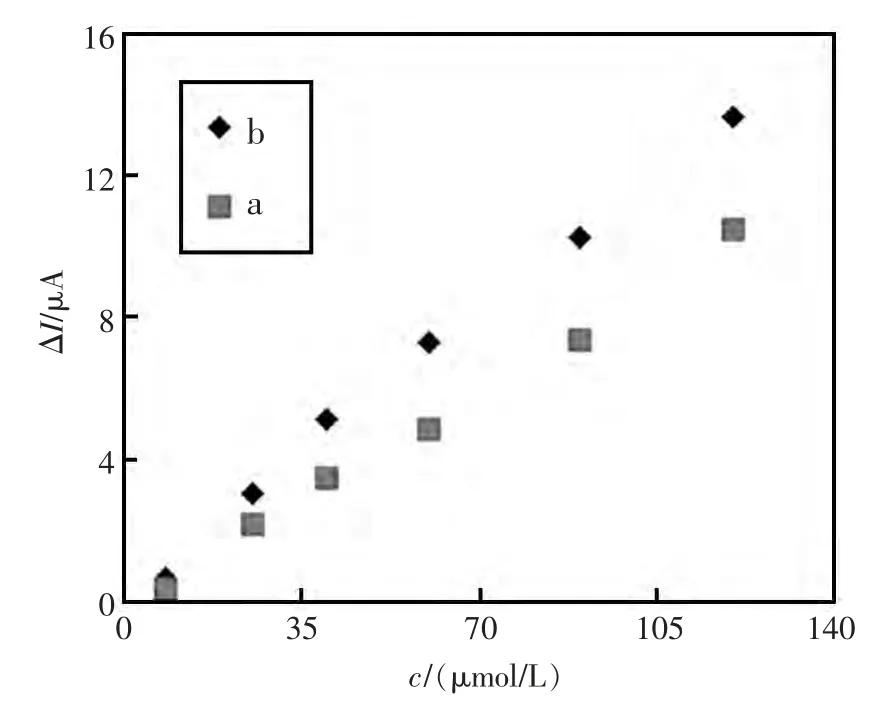
图3 不同修饰电极在0.25 mol/L PBS(pH6.0)中对NO2-的电流响应:(a)CS@Nano-C 修饰电极;(b)Nano-Au/CS@Nano-C 修饰电极Fig.3 Current response of different electrode in PBS:(a)CS@Nano-C modified Au electrode,(b)Nano-Au/CS@Nano-C modified Au electrode
实验比较了滴加Nano-C 量对电极的影响,发现若Nano-C 量过多时与电极结合不牢,Nano-C 膜易脱落,而当Nano-C 量过少,工作电极灵敏度降低。此外,用于分散Nano-C时CS 的浓度也会对电极带来很大影响,当加入Nano-C 中CS 的浓度过大时,将严重阻碍电子传递,降低响应;而当加入Nano-C 中CS 的浓度较少时,又不利于CS@Nano-C 膜的稳定。因此,实验中Nano-C 在CS 中的含量为0.25 mg/L。
pH 对Nano-Au/CS@Nano-C 电极催化反应及其活性有重要影响。该次实验在酸性及中性环境内检测了Nano-Au/CS@ Nano-C 电极的电流响应,由图4可知,当pH为6.0时,该修饰电极对NO2-催化效果最佳;当pH为4.0时,该修饰电极对NO2-催化效果最差。其可能的原因是CS 在酸性条件下不稳定,易溶于水,而当电极置于中性环境内时,电极反应缺少相应的质子,故电催化变困难,电极的电流响应降低。
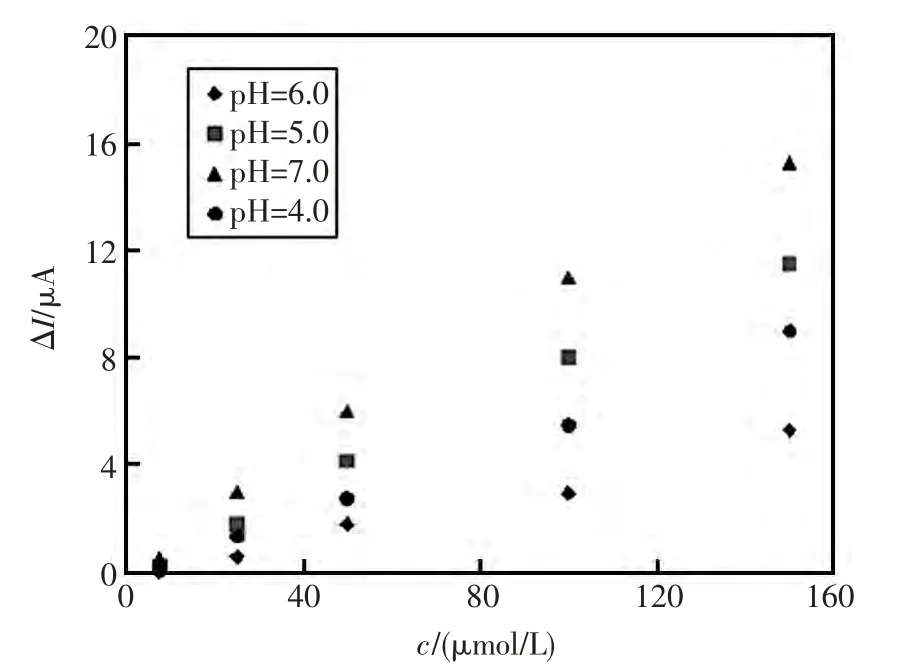
图4 Nano-Au/CS@Nano-C 修饰电极在不同pH 测试底液中对NO2-的电流响应Fig.4 Current response of Nano-Au/CS@Nano-C electrode in different pH
Nano-Au/CS@ Nano-C 修饰电极对NO2-有良好催化性能,在优化条件下,其在NO2-浓度为8.0×10-6~2.0×10-4mol/L 范围内有线性响应(图5),线性方程y =0.1146x + 0.409,检测下线2.7×10-6mol/L(S/N=3),这是因为纳米碳有较好的催化性能,而Nano-Au 能促进电子传递,二者协同作用,故电极灵敏度提高。
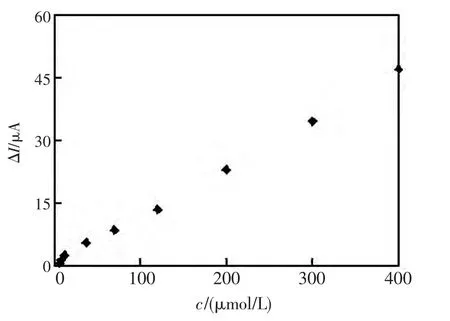
图5 Nano-Au/CS@Nano-C 修饰电极在0.25 mol/L PBS(pH6.0)中的动力学响应曲线Fig.5 Current response response of Nano-Au/CS@Nano-C modified Au electrode in PBS at various NO2-concentrations
2.4 电极的稳定性、重现性、干扰实验
为了考察该修饰电极的稳定性,将Nano-Au/CS@Nano-C 电极置于不含NO2-的测试底液中连续循环扫描100 圈后,其电流响应信号仍能保持初始信号的97.2%,这证明由于该修饰电极无电子媒介体,电极稳定性显著提高。此外,壳聚糖的网状结构将纳米碳稳固于电极上,其氨基与Nano-Au 强烈的吸附作用又增加了Nano-Au 的稳定性。为了考察该修饰电极的寿命,将该电极置于2~8℃冰箱中放置10 d,在放置期间歇性使用,其响应信号稍有变化,但变化量没有超过初始信号的2.2%。同时制备4 支电极,分别在NO2-浓度为50 μmol/L NO2-下对其进行测定,4 支电极其响应电流的相对标准偏差RSD<4.0%,表明该修饰电极具有良好的重现性。
NO2-在pH6.0 PBS 中,其峰电位在0.8 V,抗坏血酸及多巴胺峰电位分别在0.2 V、1.1 V,而过氧化氢峰电位在-0.7 V。因此,上述常见物质均不会对NO2-的检测产生干扰。
2.5 回收测定
以0.25 mol/L PBS(pH6.0)为测试底液,把标准NO2-配制成不同浓度的待测品,将该工作电极置于待测样品溶液中各测定3次,测定其电流响应变化值,结果列于表1,该工作电极的回收率从98.0%~103.5%。

表1 该电极的回收结果(n=3)Tab.1 Recovery of the prepared biosensor(n=3)
3 结论
该文以壳聚糖分散的纳米碳为基底结合纳米金,利用Nano-Au/CS@Nano-C 的直接电催化作用制备了具有催化性能的纳米材料作为识别元素检测亚硝酸盐的传感器。该传感器具有制备简单、灵敏度高、稳定性好、无外加毒性物质,且无电子媒介体渗漏、富集等消极问题。
[1]Yang W Y,Zhou X,Zheng N,et al.Electrochemical biosensors utilizing the electron transfer of hemoglobin immobilized on cobalt-substituted ferrite nanoparticles–chitosan film [J].Electrochim.Acta,2011,56:6588-6592.
[2]Silveira C M,Gomes S P,Araújo A N,et al.An efficient non-mediated amperometric biosensor for nitrite determination[J].Biosens.Bioelectron.,2010,25:2026-2032.
[3]Almeida M G,Silveira C M,Moura J J G.Biosensing nitrite using the system nitrite redutase/Nafion/methyl viologen—Avoltammetric study [J].Biosens.Bioelectron.,2007,22:2485-2492.
[4]Chen H,Mousty C,Cosnier S,et al.Highly sensitive nitrite biosensor based on the electrical wiring of nitrite reductase by [ZnCr-AQS]LDH [J].Electrochem.Commun.,2007,9:2241-2246.
[5]Silva S,Cosnier S,Almeida M G,et al.An efficient poly(pyrrole–viologen)-nitrite reductase biosensor for the mediated detection of nitrite [J].Electrochem.Commun.,2004,6:404-408.
[6]Zhang Z,Xia S,Leonard D,et al.A novel nitrite biosensor based on conductometric electrode modified with cytochrome c nitrite reductase composite membrane [J].Biosens.Bioelectron.,2009,24:1574-1579.
[7]Astier Y,Canters G W,Davis J J,et al.Sensing Nitrite through a Pseudoazurin – Nitrite Reductase Electron Transfer Relay [J].ChemPhysChem,2005,6:1114-1120.
[8]Serra A S,Jorge S R,Silveira C M,et al.Cooperative use of cytochrome cd nitrite reductase and its redox partner cytochrome c to improve the selectivity of nitrite biosensing[J].Anal.Chim.Acta,2011,693:41-46.
[9]Rosa C C,Cruz H J,Vidal M,et al.Oliva.Optical biosensor based on nitrite reductase immobilised in controlled pore glass [J].Biosens.Bioelectron.,2002,17:45-52.
[10]Ferretti S,Lee S K,MacCraith B D,et al.Optical biosensing of nitrite ions using cytochrome cd1 nitrite reductase encapsulated in a sol–gel matrix [J].Analyst,2000,125:1993-1999.
[11]Strehlitz B,Gründiig B,Schumacher W,et al.A Nitrite Sensor Based on a Highly Sensitive Nitrite Reductase Mediator-Coupled Amperometric Detection [J].Anal.Chem.,1996,68:807-816.
[12]Ding Y,Wang Y,Li B,et al.Electrospun hemoglobin microbelts based biosensor for sensitive detection of hydrogen peroxide and nitrite [J].Biosens.Bioelectron.,2010,25:2009-2015.
[13]Zhu W L,Zhou Y,Zhang J R.Direct electrochemistry and electrocatalysis of myoglobin based on silica-coated gold nanorods/room temperature ionic liquid/silica sol–gel composite film[J].Talanta,2009,80:224-230.
[14]Sun W,Li X,Wang Y,et al.Electrochemistry of myoglobin in Nafion and multi-walled carbon nanotubes modified carbon ionic liquid electrode [J].Bioelectrochemistry,2009,75:170-175.
[15]Chen Q,Shiyun A,Zhu X,et al.A nitrite biosensor based on the immobilization of Cytochrome c on multi-walled carbon nanotubes–PAMAM–chitosan nanocomposite modified glass carbon electrode [J].Biosens.Bioelectron.,2009,24:2991-2996.
[16]Zhang W,Yuan R,Chai Y Q,et al.A simple strategy based on lanthanum – multiwalled carbon nanotube nanocomposites for simultaneous determination of ascorbic acid,dopamine,uric acid and nitrite[J].Sensor.Actuat.B,2012,166-167:601-607.
