黄连羊肝丸中小檗碱百分含量测定
2015-03-10杨新宇徐蓓蕾
杨新宇,徐蓓蕾,2,沈 芸
(1.哈尔滨商业大学 生命科学与环境科学研究中心,哈尔滨 150076;2 哈尔滨商业大学 药学院,哈尔滨 150076)
黄连羊肝丸中小檗碱百分含量测定
杨新宇1,徐蓓蕾1,2,沈 芸1
(1.哈尔滨商业大学 生命科学与环境科学研究中心,哈尔滨 150076;2 哈尔滨商业大学 药学院,哈尔滨 150076)
考察不同厂家黄连羊肝丸中小檗碱百分含量,比较不同厂家黄连羊肝丸的质量.主要通过高效液相色谱法(HPLC),对不同厂家的黄连羊肝丸中主要成分小檗碱进行百分含量测定,高效液相色谱法测定盐酸小檗碱的回归方程为:Y= 37.643X+0.987 4,r= 0.999 3,线性关系良好.测定结果显示,以小檗碱百分含量计,百分含量最高为“赤峰天奇制药有限责任公司(水蜜丸)”,为0.23%;百分含量最低为“北京同仁堂股份有限公司同仁堂制药厂(蜜丸)”,为0.11%.不同厂家的黄连羊肝丸由于制作工艺不同,原材料差异,导致药品质量存在差异,但均在药典规定范围内,不影响产品使用.高效液相色谱法应用于中成药的百分含量测定具有简便、灵敏度高、重复性好等优势,可以为黄连羊肝丸质量标准制定奠定基础.
黄连羊肝丸;盐酸小檗碱;超声提取;高效液相色谱法;百分含量测定
黄连羊肝丸具有泻火明目的作用,多用于肝火旺盛,目赤肿痛,视物昏暗,羞明流泪,胬肉攀睛[1-2].黄连是黄连羊肝丸的君药,其主要成分为小檗碱,小檗碱以盐酸盐的形式存在于植物之中,故又叫盐酸小檗碱,均为黄色结晶体[3-5].市面上中成药黄连羊肝丸的种类繁多,为保证用药安全有效,采用超声提取的方法,对不同厂家黄连羊肝丸中小檗碱进行提取分离.以盐酸小檗碱为对照品,通过高效液相色谱法[6-8],测定不同厂家黄连羊肝丸中小檗碱的百分含量,为黄连羊肝丸的质量标准制定提供了科学依据.
1 材料与方法
1.1 药品与试剂
盐酸小檗碱标准品(四川维克奇对照品有限公司);黄连羊肝丸1(北京同仁堂股份有限公司同仁堂制药厂 蜜丸,批号2013178);黄连羊肝丸2(北京同仁堂股份有限公司同仁堂制药厂 蜜丸,批号2013439);黄连羊肝丸3(赤峰天奇制药有限责任公司 蜜丸,批号20120922);黄连羊肝丸4(赤峰天奇制药有限责任公司 水蜜丸,批号20120507);黄连羊肝丸5(赤峰丹龙药业有限公司 水蜜丸,批号20120838);黄连羊肝丸6(药都制药集团股份有限公司 蜜丸,130101).甲醇(色谱纯,天津市启邦化工产品销售有限公司);乙腈(色谱纯,Fisher公司);水(娃哈哈纯净水).
1.2 仪器与设备
Thermo u3000高效液相色谱仪(戴安公司);分析天平(上海器械厂)KS-600D超声清洗机(宁波科生仪器厂).
1.3 标准溶液的制备
精密称量5.2 mg盐酸小檗碱于50 mL烧杯中,用甲醇溶液溶解,将溶解后的溶液用甲醇定容到10 mL容量瓶中,得到0.5 mg/mL盐酸小檗碱溶液;用移液管精密吸取上一步配得的0.5 mg/mL盐酸小檗碱溶液,分别取0.02、0.04、0.1、0.2、1、2、5 mL,分别用甲醇稀释定容到10 mL容量瓶中,即得到7个呈梯度浓度的盐酸小檗碱对照品溶液,质量浓度分别为:0.001、0.002、0.005、0.01、0.05、0.1、0.25 mg/mL.
1.4 试样的处理
取质量差异项下的不同厂家黄连羊肝丸(1-6)(取药量详见表1),剪碎,混匀,分别取约0.5 g,精密称定,置具塞锥形瓶中,精密加甲醇溶液25 mL,密塞,称定质量,摇匀,浸泡过夜,超声处理(功率250 W,频率50 kHz)40 min,放冷,再称定质量,用甲醇溶液补足减失的质量,摇匀,过滤,取续滤液作为供试品溶液.即得6份供试品溶液.
表1 不同厂家黄连羊肝丸取药量

药品取药量/g黄连羊肝丸10.5258黄连羊肝丸20.5139黄连羊肝丸30.5111黄连羊肝丸40.4968黄连羊肝丸50.5065黄连羊肝丸60.5172
1.5 高效液相色谱条件
色谱柱:Agilent C18(150 mm×5 μm); 流动相:乙腈:KH2PO4(0.02 mol/L)(35∶65)流速1 mL/min;检测波长:345 nm;进样量:10 μL;柱温:室温.
1.6 进样
将供试品和对照品溶液分别注入高效液相色谱仪,进样量10 μL,在最佳的色谱条件下进行HPLC分析,并记录数据.
2 结果与讨论
2.1 标准曲线绘制结果
依1.5项下色谱条件测定,得出标准品峰面积测定结果.
以对照品进样量(μg)为横坐标,峰面积值为纵坐标,做回归曲线见图1.计算求得回归方程见公式:Y= 37.643X+0.987 4,r= 0.999 3.

图1 盐酸小檗碱标准曲线
2.2 精密度试验
取上述同一批盐酸小檗碱标准品配成标准溶液,每次取10 μL,重复进样5次,分别测得5个峰面积,得出其RSD值为1.54%,表明精密度良好.
2.3 重复性试验
取同一批样品6份,照上述方法溶解、测定,得RSD值为0.88%.表明重复性良好.
2.4 回收率试验
精密称取同法测定的已知百分含量为2.5的样品6份,精密加入盐酸小檗碱对照品2.5 mg,依法测定,别计算其回收率,求得平均回收率为102.7%,RSD值为1.52%.
2.5 不同厂家黄连羊肝丸小檗碱百分含量测定结果
依1.5项下色谱条件测定,得出色谱图.从色谱图中可以看出,与对照品比较,所有供试品都在盐酸小檗碱峰处有明显的对应峰出现.对照品及不同厂家黄连羊肝丸中盐酸小檗碱色谱图见图2.
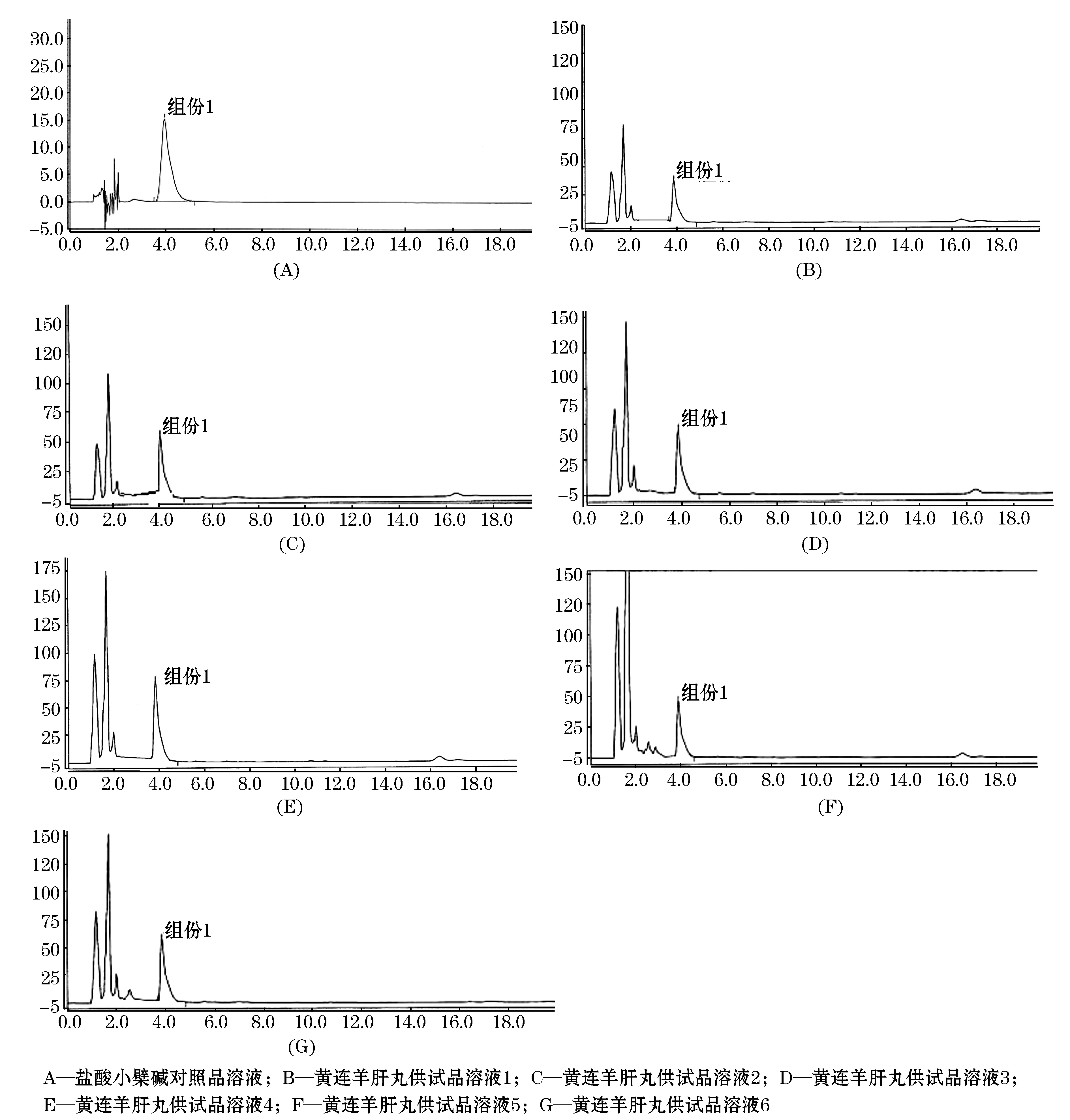
图2 盐酸小檗碱高效液相色谱图
根据其峰面积,再由2.1项下得出的回归方程,可以计算出不同厂家黄连羊肝丸中盐酸小檗碱百分含量.具体百分含量测定结果见表2.
表2 供试品百分含量测定结果

样品样品1样品2样品3样品4样品5样品6峰面积8.95712.84610.99018.79410.32014.120百分含量/%0.110.160.130.230.160.17
根据《中国药典》2010版规定,每丸(含9 g)黄连羊肝丸含盐酸小檗碱的量不得低于6.3 mg.即百分含量不得低于0.07%.
根据以上所得供试品百分含量测定结果,对比药典标准,做出图3供试品百分含量与药典标准比较.从图3 中可以清晰看出,实验中所用所有供试品都符合药典规定,为合格产品.在合格的基础上,产品质量有所差异,但并无较大差异.

图3 供试品百分含量与药典标准比较
3 讨 论
实验数据表明,不同厂家黄连羊肝丸中小檗碱百分含量在合格的基础上有所差异,原因可能是多方面的:其一,黄连羊肝丸是由多味中药组成的复方中药丸剂,其药物成分多且复杂,因此影响测定因素较多且互有干扰;其二,实验过程中由于仪器、设备的问题或是人为因素造成的误差.方中药味较多,其效用是靠多种成分共同作用而成,本实验只测定不同厂家黄连羊肝丸中小檗碱的百分含量,一种成分的百分含量测定不足以说明药品的内在质量[9],本实验中还可加入对黄芩苷进行了百分含量测定,从而达到全面控制药品质量的目的[10].本文参照药典提取方法,采用甲醇等溶剂进行了萃取,可将多余繁杂的水溶性成分除去,以达到分离、纯化目标物的目的.并选用超声波提取方法,可以缩短提取时间,同时还不破坏有效物质化学结构,比冷浸法、渗漉法、蒸馏法等提取方法,操作简便.实验中加入了精密度实验、重复性试验和回收率方
法学的验证,以提高实验的准确性并对本实验中的测定方法进行评估[11-12].
[1] 国家药典委员会. 中华人民共和国药典(一部)[M]. 北京: 中国医药科技出版社, 2010.1068-1069.
[2] 张贵君. 中药鉴定学[M]. 北京: 北京科学出版社, 2009.84-87.
[3] YI P, LU F E, XU L J,etal. Berberine reverses free-fatty-acid-induced insulin resistance in 3T3-L1 adipocytes through targeting IKKβ[J]. World J Gastroenterol, 2008, 14(6): 876-883.
[4] 徐西强. 盐酸小檗碱治疗骨肉瘤的作用及其机制[D]. 武汉: 华中科技大学, 2012.
[5] IKEMOTO S, SUGIMUKA K, YOSHIDA N,etal. Antitum or effects of scutellariae radix and its components baicalein, baicalin, and wogonia on bladder cancer cell lines [J].Urology, 2010, 55(6): 951.
[6] 李红星, 王金平, 陈建英, 等. 高效液相色谱法在药物分析中的应用概述[J].重庆中草药研究, 2010, 23(02): 38-39.
[7] 刘建新, 张同宝. 高效液相色谱法在中药指纹图谱中的研究与现状分析[J].华章, 2011, 17(35): 366.
[8] MICHAL, SRBEK J, R DL S,etal. Identification, characterization, synthesis and HPLC quantification of new process-related impurities and degradation products in retigabine [J].Journal of Pharmaceutical and Biomedical Analysis, 2014, 42(01): 1016.
[9] 刘征辉, 叶挺祥, 赵洪芝, 等. 黄连羊肝片质量标准研究[J].中成药, 2009, 31(08): 3-6.
[10] 吴 阳. 黄连羊肝丸质量标准的研究[D]. 锦州: 辽宁医学院, 2011.
[11] WANG D F, XU Q L, ZUO D,etal. Determination of Berberine Hydrochloride in Shihu Yeguang pillss by HPLC[J].Medicinal Plant,2010, 8(1): 74-75, 78.
[12] 沈 芸,徐蓓蕾,杨新宇.黄莲功效药对配伍中盐酸小檗碱质量分数测定[J].哈滨滨商业大学学报:自然科学版,2015,31(2):155-158.
Determination of berberine in Huanglian Yanggan pills
YANG Xin-yu1, XU Bei-lei1,2, SHEN Yun1
(1. Research Center on Life Sciences and Environmental Sciences, Harbin University of Commerce, Harbin 150076, China; 2. School of Pharmacy, Harbin University of Commerce, Harbin 150076, China)
To investigate determination of berberine in Huanglian Yanggan pills from different manufacturers, the qualities of Huanglian Yanggan pills from different manufacturers were compared. High performance liquid chromatography (HPLC) was used to determine the content of berberine which is the main components of Huanglian Yanggan pills that came from different manufacturers. By high performance liquid chromatography, a regression equation of berberine hydrochloride:Y=37.643X+0.987 4,r=0.999 3 was obtained which had a good linear relationship. All samples were in line with Pharmacopoeia requirements of berberine. Huanglian Yanggan pills from Tianqi Chifeng Pharmaceutical Co., Ltd. (water pill) had the highest content of berberine, 0.23%,while from Beijing Tong Ren Tang Pharmaceutical Co., Ltd. (pill) had the lowest content of berberine,0.11%. The different production process and raw materials led to the different quality of Huanglian Yanggan pills from different manufacturers, but all were within the range specified in the Pharmacopoeia. The method of high performance liquid chromatography (HPLC) was rapid, sensitive, simple and highly reproducible in determination of the content of Chinese patent medicines, and capable to lay a foundation to establish the quality standards of Huanglian Yanggan pills.
Huanglian Yanggan pills; berberine hydrochloride; ultrasonic extraction; HPLC; ddetermination.
2014-12-13.
哈尔滨商业大学研究生创新科研项目(YJSCX2014-322HSD);黑龙江省博士后基金资助项目(LBH-Z13121);哈尔滨商业大学科研启动基金资助项目(13DL024)
杨新宇(1991-),男,硕士,研究方向:抗肿瘤药物研究.
徐蓓蕾(1983-),女,博士,教师,研究方向:抗肿瘤药物研究.
R286
A
1672-0946(2015)03-0267-04
