HPSEC法测定注射用头孢噻肟钠他唑巴坦钠(6∶1)中高分子聚合物的含量Δ
2015-03-09李三红王永庆戴云志南京大学医学院附属口腔医院南京10008南京医科大学第一附属医院南京10008南京优科生物医药有限公司南京10009
董 静,李三红,王永庆,戴云志(1.南京大学医学院附属口腔医院,南京 10008;.南京医科大学第一附属医院,南京 10008;.南京优科生物医药有限公司,南京 10009)
注射用头孢噻肟钠他唑巴坦钠(6∶1)是一种新型抗菌药物复方制剂。原卫生部全国细菌耐药监测网(基础网)的调查结果显示[1-3],头孢噻肟的耐药率逐年增高,并且革兰阴性菌耐药问题在第三代头孢菌素类药物中以头孢噻肟最为严重。头孢噻肟的主要耐药机制是细菌产生的β-内酰胺酶对其水解灭活,而他唑巴坦对β-内酰胺酶有抑制作用,二者联用可抑制细菌耐药性、发挥协同抗菌作用。该复方制剂临床上主要用于产β-内酰胺酶耐药菌感染的治疗。
与其他半合成的β-内酰胺类抗菌药物一样,注射用头孢噻肟钠他唑巴坦钠(6∶1)在生产和贮存过程中也会形成头孢噻肟高分子聚合物,在临床使用中可能会引发速发型过敏反应[4-5],因此控制其含量非常必要。2010年版《中国药典》收载了头孢噻肟钠中高分子聚合物检查项,采用的是以葡聚糖凝胶G-10为填充剂的凝胶色谱柱[6]。但近年来,随着分析技术的不断发展,高效分子排阻色谱(HPSEC)法逐渐成熟。该法测定抗菌药物中高分子杂质时更为准确、灵敏,且操作简便,因此其应用也越来越广泛。本试验建立了使用TSK-GEL G2000SWXL 凝胶色谱柱的HPSEC 法,用于测定注射用头孢噻肟钠他唑巴坦钠(6∶1)中高分子聚合物的含量,现报道如下。
1 材料
LC-20A 型高效液相色谱(HPLC 仪),包含真空在线脱气机、四元泵、自动进样器、柱温箱、SPD-20A 检测器和LCsolution 化学工作站(日本岛津公司);MS205DU 型电子天平(瑞士Mettler-Toledo公司)。
注射用头孢噻肟钠他唑巴坦钠(6∶1)(南京优科生物医药有限公司,规格:1.17 g,批号:20120401、20120402、20120403);头孢噻肟、他唑巴坦对照品(中国食品药品检定研究院,批号:130483-200303、130511-200402,纯度:90.6%、99.1%);磷酸氢二钠、磷酸二氢钠和磷酸等均为分析纯,水为纯净水。
2 方法与结果
2.1 色谱条件
色谱柱:TSK-GEL G2000SWXL 凝胶色谱柱(30 cm×7.8 mm,5 μm);流动相:0.01 mol/L磷酸盐缓冲液[0.01 mol/L磷酸氢二钠-0.01 mol/L磷酸二氢钠(61∶39,V/V),用0.1 mol/L磷酸调节pH 至7.0];流速:1.0 ml/min;检测波长:254 nm;进样量:10 μl;柱温:25 ℃。
2.2 溶液的制备
头孢噻肟对照品溶液:取头孢噻肟对照品适量,精密称定,加水溶解并定量稀释制成每1 ml 中约含头孢噻肟170 μg的溶液,即得。
他唑巴坦对照品溶液:取他唑巴坦对照品适量,精密称定,加水溶解并定量稀释制成每1 ml中约含他唑巴坦10 μg的溶液,即得。
供试品溶液:取注射用头孢噻肟钠他唑巴坦钠(6∶1)适量,精密称定,加水溶解并定量稀释成每1 ml中约含头孢噻肟1.0 mg的溶液,即得。
空白溶剂:流动相。
2.3 专属性考察
分别取空白溶剂、他唑巴坦对照品溶液、头孢噻肟对照品溶液和供试品溶液各适量,按“2.1”项下色谱条件进样测定,记录色谱,详见图1。由图1可知,主峰相邻高分子聚合物峰保留时间为9.600 min,其与主峰分离度为3.472;他唑巴坦、空白溶剂及其他杂质均不干扰本品中高分子聚合物的测定。
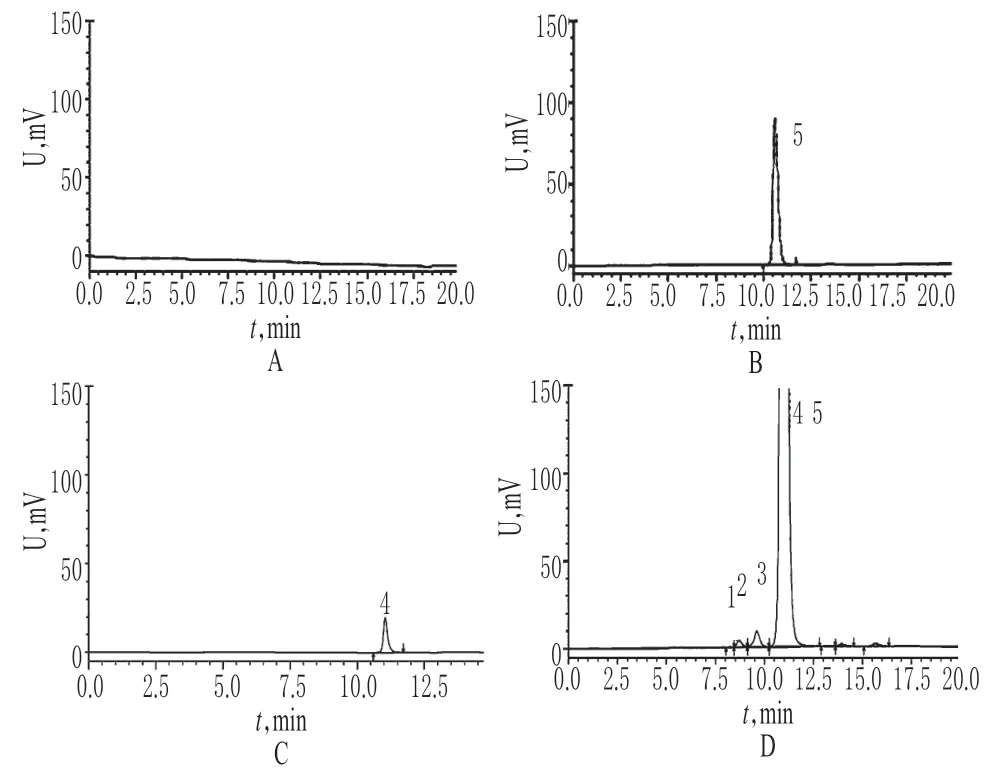
图1 高效分子排阻色谱图A.空白溶剂;B.他唑巴坦对照品;C.头孢噻肟对照品;D.供试品溶液;1.聚合物-1;2.聚合物-2;3.聚合物-3;4.头孢噻肟;5.他唑巴坦Fig 1 HPSEC chromatogramsA.blank solvent;B.reference substance of tazobactam;C.reference substance of cefotaxime;D.solution of test sample;1.polymer-1;2.polymer-2;3.polymer-3;4.cefotaxime;5.tazobactam
2.4 线性关系考察
取头孢噻肟对照品约11 mg,精密称定,置于100 ml 量瓶中,加流动相溶解并稀释至刻度,摇匀,精密量取1 ml,置于50 ml 量瓶中,加流动相定容,摇匀。分别精密量取上述溶液1、10、20、40、50、60、80、100 μl注入HPLC仪进样,记录色谱。以进样量(x,ng)为横坐标、峰面积(y)为纵坐标进行线性回归,得头孢噻肟回归方程y=2 075x-477.2(r=0.999 9)。结果表明,头孢噻肟进样量在2.3~226.4 ng范围内与其峰面积呈良好的线性关系。
2.5 检测限、定量限考察
取“2.2”项下头孢噻肟对照品溶液适量,加流动相逐级稀释后,按“2.1”项下色谱条件进样测定,以信噪比为10 计算头孢噻肟的定量限为0.45 ng,以信噪比为3计算头孢噻肟的检测限为0.14 ng。
2.6 精密度试验
取“2.2”项下头孢噻肟对照品溶液适量,按“2.1”项下色谱条件重复进样5 次,记录峰面积。结果,头孢噻肟峰面积的RSD为0.14%(n=5),表明仪器精密度良好。
2.7 稳定性试验
取注射用头孢噻肟钠他唑巴坦钠(6∶1)(批号:20120401)适量(约相当于头孢噻肟10 mg),精密称定,置于10 ml 量瓶中,加流动相溶解并定容,摇匀,分别于25 ℃下放置0、1、2、3、4、5、6 h 时按“2.1”项下色谱条件进样,记录峰面积。结果,高分子聚合物峰面积随着时间延长而增加,头孢噻肟峰面积的RSD为12.17%(n=7),表明供试品溶液不稳定,不宜长时间放置,应临用新配。
2.8 重复性试验
取注射用头孢噻肟钠他唑巴坦钠(6∶1)(批号:20120401)适量(约相当于头孢噻肟10 mg),共6份,精密称定,分别置于10 ml量瓶中,加流动相溶解并定容,摇匀,按“2.1”项下色谱条件进样测定高分子聚合物的含量。结果,高分子聚合物平均含量为1.05%,RSD为0.79%(n=6),表明本方法重复性较好。
2.9 耐用性考察
本试验分别考察了采用不同柱温、流速、波长、pH、流动相盐浓度对注射用头孢噻肟钠他唑巴坦钠(6∶1)(批号:20120401)中高分子聚合物含量测定的影响,结果见表1(注:分离度1指聚合物-1峰与聚合物-2峰之间的分离度;分离度2指聚合物-2峰与聚合物-3峰之间的分离度;分离度3指聚合物-3峰与相邻主峰之间的分离度)。由表1可知,上述因素在一定范围内变化对高分子聚合物峰之间以及高分子聚合物峰与主峰之间的分离度影响不大,均符合2010年版《中国药典》(二部)附录ⅤD HPLC法的要求,说明本方法的耐用性良好。
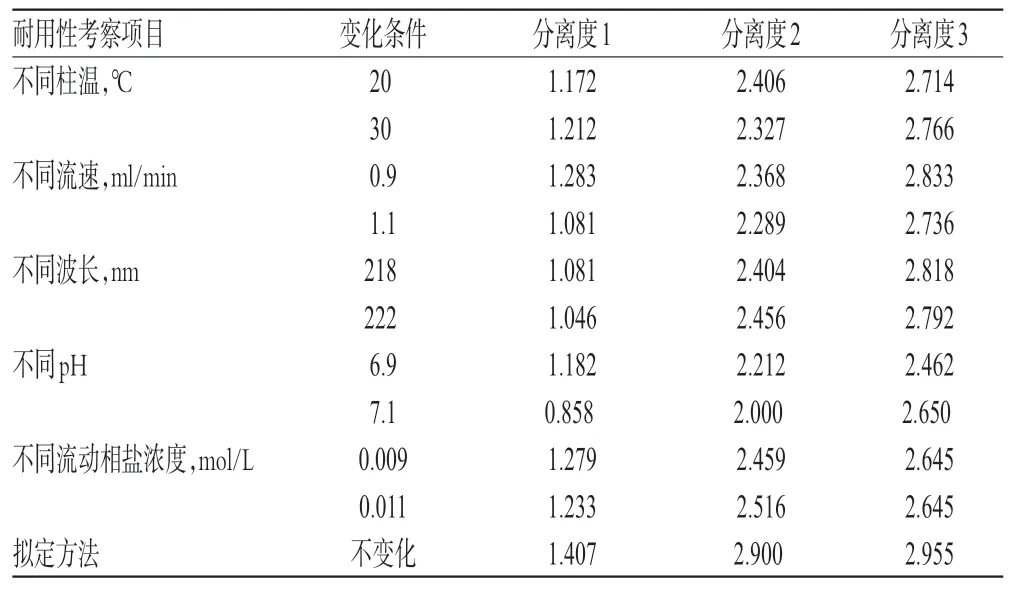
表1 耐用性试验结果Tab 1 Results of durability test
2.10 样品中聚合物的含量测定
取3 批样品各适量,分别按“2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,计算高分子聚合物含量,并且同采用2010年版《中国药典》收载的G-10法测定的高分子聚合物的含量进行比较,结果见表2。

表2 样品中聚合物的含量测定结果(n=3,%)Tab 2 Results of contents determination of polymer in samples(n=3,%)
3 讨论
3.1 HPSEC法与G-10法的比较
抗菌药物中的高分子聚合物系指其中分子量大于药物本身的杂质的总称,其分子量一般在1 000~5 000 Da,个别可达10 000 Da左右。由于高分子聚合物具有高度不均一性和不确定性,无法制备出具有固定含量的对照品,现行版《美国药典》未收载相关测定方法。2010年版《中国药典》收载的以自身对照外标法定量测定β-内酰胺类抗菌药物中高分子聚合物的方法,通过两种流动相的转换,以药品自身对照品取代高分子聚合物对照品对其中的高分子聚合物进行检测,为相关研究指出了一个新的方向。
本试验曾根据2010 年版《中国药典》头孢噻肟钠项下规定,采用以葡聚糖凝胶G-10 为填充剂的凝胶色谱柱对注射用头孢噻肟钠他唑巴坦钠(6∶1)中的高分子聚合物的含量进行测定。结果表明,该色谱柱的柱效低(柱效仅1 000 左右),进样浓度高(20 mg/ml),峰形拖尾,分析时间长(一个样品需要2 h 左右),分离效果差(所有高分子聚合物为一个峰,且该峰与主峰未能达到基线分离),导致高分子聚合物的检出量非常低。而采用以TSK-GEL G2000SWXL为填充剂的凝胶色谱柱进行测定,柱效高(上万),分析时间短(一个样品仅需要20 min),分离效果好(高分子聚合物峰与主峰能达到基线分离)。故高分子聚合物的检出量更高,更适合于测定注射用头孢噻肟钠他唑巴坦钠(6∶1)中聚合物的含量。
3.2 流动相的选择
在酸性和碱性条件下头孢噻肟均可发生聚合反应[7],因此测定时应选择pH 为中性的流动相系统。本试验参照2010 年版《中国药典》中头孢菌素类抗菌药物高分子聚合物测定方法,选用0.01 mol/L磷酸盐缓冲液(pH 7.0)为流动相,发现高分子聚合物与样品能达到基线分离。同时,本试验还进行了流动相的耐用性试验,微调磷酸盐缓冲盐的浓度,分别用0.009 mol/L 磷酸盐缓冲液(pH 7.0)和0.011 mol/L 磷酸盐缓冲液(pH 7.0)进行考察,发现微调流动相盐浓度对分离度和柱效均无明显影响,说明以0.01 mol/L 磷酸盐缓冲液(pH 7.0)为流动相的耐用性良好。因此,最终选择0.01 mol/L 磷酸盐缓冲液(pH 7.0)为流动相。
3.3 测定波长的选择
注射用头孢噻肟钠他唑巴坦钠(6∶1)中高分子聚合物主要是由头孢噻肟聚合而成,由于难以获得高分子聚合物对照品,而高分子聚合物是由单体聚合而成,所以本试验参考2010年版《中国药典》头孢噻肟钠中高分子聚合物检查项下的检测波长,选择254 nm为测定波长。在此波长下,他唑巴坦及其他杂质均不干扰该复方制剂中高分子聚合物的测定。
3.4 对照品的选择和准确度的考察
由于头孢噻肟高分子聚合物是由头孢噻肟单体分子通过分子间的氢键、静电相互作用、疏水相互作用而形成的,未破坏其分子结构,也未改变其化学性质,头孢噻肟高分子聚合物和头孢噻肟单体分子具有相似的色谱行为,因此可以用头孢噻肟作为对照品,来测定头孢噻肟高分子聚合物的含量。
由于无法获得头孢噻肟高分子聚合物的对照品,因此无法进行加样回收率试验,并且本制剂中不含任何辅料,也无需进行回收率试验。本研究重复性试验中连续测定了6 份供试品中高分子聚合物的含量,其RSD为0.79%,说明本方法的重复性较好;另外,通过考察不同柱温、流速、波长、pH、流动相盐浓度对供试品中高分子聚合物含量测定的影响,结果表明上述因素在一定范围内变化对高分子聚合物峰之间以及高分子聚合物峰与主峰之间的分离度影响不大,说明本方法耐用性较好。由此说明本方法测定注射用头孢噻肟钠他唑巴坦钠(6∶1)中高分子聚合物的含量的准确度较好。
综上所述,本方法操作简单、专属性强、灵敏度高,可用于注射用头孢噻肟钠他唑巴坦钠(6∶1)中高分子聚合物的含量测定。
[1]刘根焰,童明庆,梅亚宁,等.Mohnarin 2009年度报告:青壮年(14~65岁)来源菌株耐药监测[J].中国临床药理学杂志,2011,27(7):508.
[2]梅亚宁,童明庆.2010 年度卫生部全国细菌耐药监测网报告:青壮年来源菌株耐药监测结果[J].中华医院感染学杂志,2012,22(1):44.
[3]梅亚宁,童明庆.2011 年度卫生部全国细菌耐药监测网报告:成年患者分离菌的耐药监测[J].中国临床药理学杂志,2014,30(2):94.
[4]金少鸿,胡昌勤.β-内酰胺类抗生素过敏反应研究进展[J].中国新药杂志,1994,3(4):38.
[5]霍秀敏.β-内酰胺类抗生素高分子杂质的研究[J].药品评价,2005,2(5):324.
[6]国家药典委员会.中华人民共和国药典:二部[S].2010年版.北京:中国医药科技出版社,2010:217-218.
[7]胡昌勤,金少鸿,孙学兰.头孢菌素结构和其聚合反应关系的探讨:Ⅰ.结构对反应类型的影响[J].中国抗生素杂志,1991,16(1):25.
