噻唑烷二酮类药物对非酒精性脂肪性肝病的治疗作用
2015-03-07霍光同,梁成宵,周维均等
噻唑烷二酮类药物对非酒精性脂肪性肝病的治疗作用
作者单位:610041 成都,成都军区空军司令部门诊部(霍光同,梁成宵,顾明忠);解放军77113部队卫生队(周维均);四川省疾病预防控制中心(兰莹);解放军452医院急诊科(任婷婷,苟仲勇)
霍光同,梁成宵,周维均,兰莹,顾明忠,任婷婷,苟仲勇
[关键词]噻唑烷二酮;非酒精性脂肪性肝病;治疗
代谢综合征、肥胖及胰岛素抵抗已经成为了世界性的健康问题,虽然非酒精性脂肪性肝病(NAFLD)的病因未完全清楚,但它与代谢综合征之间的关系是相当密切的。基于这种联系,人们开展了大量胰岛素增敏剂噻唑烷二酮类药物(TZDs)治疗肝脏脂肪蓄积的临床研究。TZDs可影响胰岛素敏感组织中的糖、脂代谢,从而通过一些中间步骤来调控肝脏脂肪的含量。现就此做一综述。
1NAFLD的发病机制
在以非酒精导致的、肝内脂质沉积为主要表现的慢性肝病中,NAFLD是最常见的疾病,它包括了以下两种情况,从轻到重分别为: (1)以肝脏内单纯甘油三酯蓄积为特征的非酒精性单纯性脂肪肝;(2)由肝内脂肪蓄积导致的炎症及损伤为主要特征的非酒精性脂肪性肝炎。NAFLD可导致肝硬化、失代偿性的肝疾病甚至肝癌。在西方国家,NAFLD的患病率达到了30%以上,在亚太地区各国也有5%~30%的患病率。越来越多的证据显示,NAFLD与胰岛素抵抗、肥胖、Ⅱ型糖尿病、高血压、高脂血症等代谢综合征的关系是相当密切的,在如此强的相关性下,有人把NAFLD看作是全身性代谢综合征在肝脏的表现。一项时间跨度为4年的回顾性研究提示,NAFLD是糖尿病的一个独立危险因素,在肥胖成人、糖尿病患者和高脂血症患者中,NAFLD的患病率分别为80%~90%、30%~50%和90%[1],故对NAFLD的控制显得十分重要。然而,在NAFLD的治疗中,仍然缺乏有效的手段。关于NAFLD的病因,现普遍接受的是“二次打击学说”,其中的“第一次打击”是指由于胰岛素抵抗和肥胖,肝细胞内蓄积了过多的游离脂肪酸(FFAs)和甘油三酯; “第二次打击”是指随之而来的氧化应激、脂质过氧化、线粒体功能障碍、炎症介质释放等一系列病理生理变化,这些因素是导致非酒精性单纯性脂肪肝进展为非酒精性脂肪性肝炎和纤维化的主要因素。胰岛素抵抗是指原本对胰岛素敏感的肌肉、脂肪等组织对胰岛素的感受能力下降、葡萄糖摄取能力降低,胰岛素抵抗可增加脂肪组织的脂质分解并输出入血,导致循环中的FFAs含量增多,而肝脏则是FFAs输入并最终到达的器官。肝脏中增加的FFAs可损伤肝细胞的脂质氧化系统,从而引起肝脏的脂质沉积。
2TZDs对NAFLD的治疗
NAFLD最主要的治疗手段是饮食控制及生活习惯的改善,包括减肥、低能量摄入、日常运动等,通过减少摄入增加消耗的方式来使其得到控制。但对于一些不能严格执行一般治疗的人群,以及作为一般治疗的辅助,甚或是对于一些严重的NAFLD患者,则有必要进行药物治疗。鉴于NAFLD与糖、脂代谢密切相关,增加胰岛素敏感性的药物TZDs是最有治疗价值的药物之一。
2.1关于TZDs治疗NAFLD的临床研究胰岛素增敏剂可直接或间接通过调控肝脏脂质代谢的稳态,从而达到治疗NAFLD的效果。TZDs类药物是一种为人熟知的胰岛素增敏剂。罗格列酮和吡格列酮可增加2型糖尿病中高胰岛素血症患者的外周组织血糖摄取能力及全身组织的胰岛素敏感性[2-3]。同时TZDs也可改善禁食时的FFAs水平及肝脏脂质蓄积[4-5]。表1列举了TZDs对2型糖尿病患者肝脏脂质蓄积的研究,然而TZDs降低肝脏脂质含量的效应与剂量和给药时间之间没有明显的联系。在使用罗格列酮治疗NAFLD时,用4 mg或8 mg的剂量分别可使肝脏脂质含量分别下降38%[6]和30%[7]/51%[2];而同样使用8 mg的剂量治疗4、6、8个月时,肝脏脂质含量分别下降30%[7]/51%[2]、15%[8]、46%[4]。使用45 mg/d的吡格列酮治疗NAFLD时,在改善胰岛素抵抗的同时,也可观察到肝脏脂肪蓄积程度的改善[3-5,9-10]。而且TZDs减少肝脏脂质蓄积的效应与患者的体重无关[3-5,7,10]。还有一些临床试验发现,TZDs可防止NAFLD时氧化应激增加、脂质过氧化、前炎症因子释放等后续事件的发生,减少了进展为非酒精性脂肪性肝炎(NASH)的可能性。表2列举了TZDs在治疗NASH时对肝脏代谢和组织学指标的改善情况。在罗格列酮[11-13]和吡格列酮[14-16]的治疗下,可改善转氨酶水平、肝脂质含量和脂肪变性、气球样变等组织学特征。从表1和表2中可以看出,TZDs不仅可降低肝脏的脂质含量,而且可以改善肝组织的损伤。但在得出确切结论前,仍需要进行更多的研究来证实长期TZDs对肝损伤和NASH的治疗作用。
2.2TZDs的副作用尽管TZDs可从多个角度治疗NAFLD,但同时也有一些副作用,从一定程度上限制了TZDs在临床的应用,如因严重的肝毒性而被迫下市的曲格列酮。所幸的是,其他格列酮类的药物如罗格列酮和吡格列酮均无产生肝功能障碍症状的副作用。
水肿是TZDs最常见的副作用,Berlie等[17]进行的Meta分析也发现TZDs与水肿成正相关,其原因与肾脏排钠功能和小肠绒毛离子转运状态改变、造成血容量增加及液体潴留有关,但TZDs引起的水肿并不严重,且使用利尿剂可以预防和快速改善水肿。但TZDs与心衰之间有强相关性,在一项Teleo分析中发现,在使用TZDs 2.2年的患者中,每50人就有1人发生心衰[18],基于此原因,美国心脏协会和美国糖尿病协会不推荐有高心脏病风险的患者使用TZDs。而且,TZDs治疗可通过增加骨髓中脂肪生成,使骨密度降低,增加骨折的风险。TZDs可使患者体重增加,这是糖尿病的一个危险因素,但TZDs引起的肥胖与胰岛素敏感性增加无关,而与皮下脂肪组织堆积和脂肪重新分布有关。
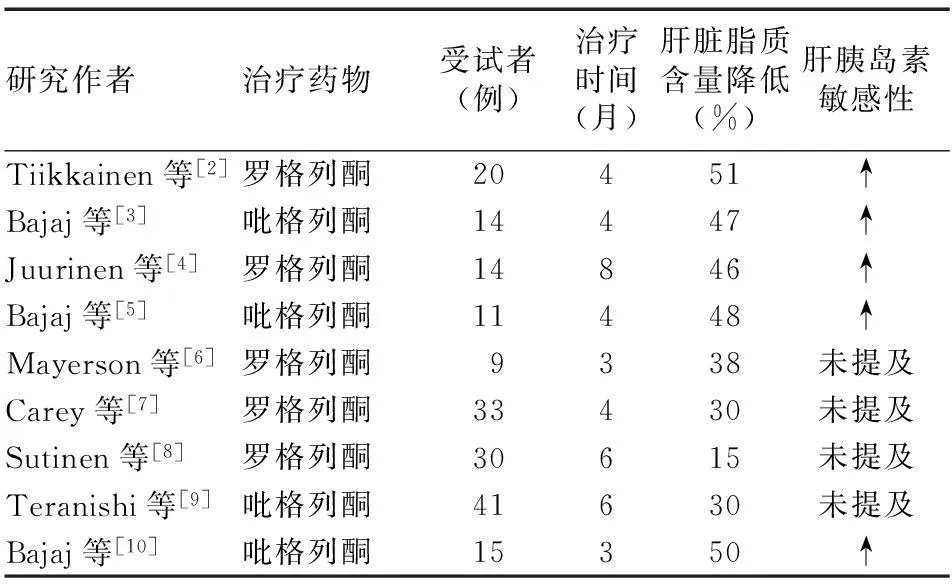
表1 TZDs治疗2型糖尿病患者对肝脂质蓄积的改善情况
2.3TZDs治疗NAFLD的可能机制TZDs是过氧化酶体增殖物激活受体γ(PPARγ)的激动剂,而PPARγ是调控糖脂代谢的重要受体。PPARγ受TZDs激活后,可降低脂肪分解,增加脂肪组织中脂肪酸摄取和储存能力,导致脂肪组织的体积和重量上升,TZDs对脂肪组织的效应可防止肝脏等胰岛素敏感组织FFA脂毒性的损伤。
TZDs不仅可减少脂肪因子的产生,也能减少TNF-α等前炎症因子的产生,而TNF-α是与肝脏脂肪变性和纤维化密切相关的。脂联素是一种可以抑制炎症的脂肪因子,在对患有Ⅱ型糖尿病的动物和人的研究中,发现TZDs可上调脂联素的合成,脂联素可通过活化AMPK来促进脂肪酸氧化分解,更可通过调控乙酰辅酶A羧化酶、PGC-1α来减少脂质蓄积。因此,脂联素可能是TZDs减少肝脏脂肪蓄积的途径之一。
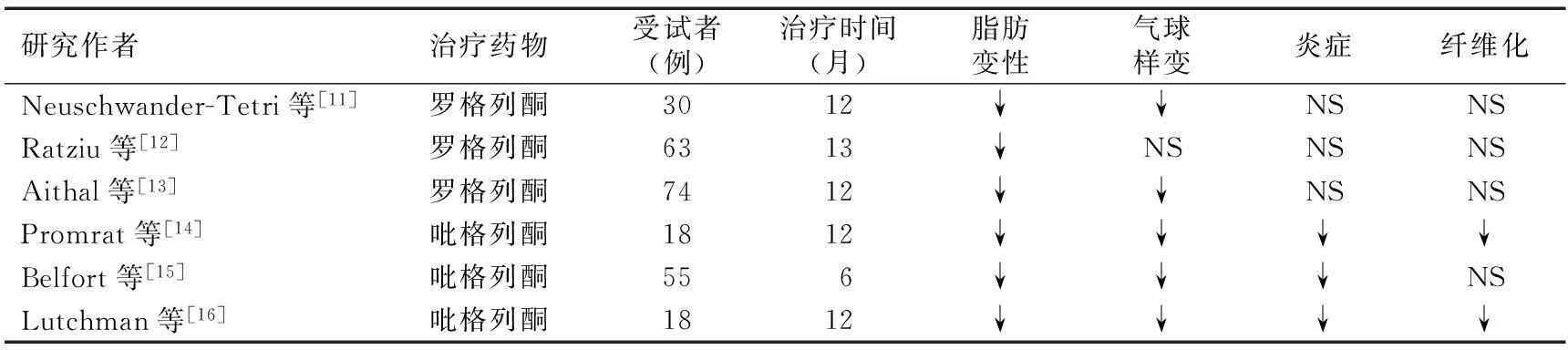
表2 TZDs对NASH治疗效果的部分临床研究
注:无显著改善(NS)
3展望
肝脏脂肪变性是饮食、代谢系统、脂肪组织、肝脏等多因素相互作用的结果,但它确切的病因仍未阐明。所以目前尚未有可以专门针对NAFLD进行治疗的药物。鉴于肝脏脂质沉积和代谢系统的相关性,人们把目光放在以TZDs为代表的胰岛素增敏剂上,希望它能够成为一个治疗突破口。TZDs可通过调控肝脏中脂联素等一些代谢相关的基因表达而改善NAFLD。但TZDs的治疗可能同时带来一些副作用,故有必要研发新的、特异的PPARγ激动剂来改善这种情况。现有MBX-102、INT131等对PPARγ有高亲和力的药物出现,但远未进入临床应用阶段,故要寻找对NAFLD治疗效果明确的药物,仍需进行进行大量动物及临床研究来观察长期疗效。
【参考文献】
[1]Bellentani S,Scaglioni F,Marino M,et al.Epidemiology of non-alcoholic fatty liver disease[J].Dig Dis,2010,28:155-161.
[2]Tiikkainen M,Häakkinen AM,Korsheninnikova E,et al.Effects of rosiglitazone and metformin on liver fat content,hepatic insulin resistance,insulin clearance,and gene expression in adipose tissue in patients with type 2 diabetes[J].Diabetes,2004,53:2169-2176.
[3]Bajaj M,Suraamornkul S,Pratipanawatr T,et al.Pioglitazone reduces hepatic fat content and augments splanchnic glucose uptake in patients with type 2 diabetes[J].Diabetes,2003,52:1364-1370.
[4]Juurinen L,Kotronen A,Graner M,et al.Rosiglitazone reduces liver fat and insulin requirements and improves hepatic insulin sensitivity and glycemic control in patients with type 2 diabetes requiring high insulin doses[J].J Clin Endocrinol Metab,2008,93:118-124.
[5]Bajaj M,Suraamornkul S,Piper P,et al.Decreased plasma adipo-nectin concentrations are closely related to hepatic fat content and hepatic insulin resistance in pioglitazonetreated type 2 diabetic patients[J].J Clin Endocrinol Metab,2004,89:200-206.
[6]Mayerson AB,Hundal RS,Dufour S,et al.The effects of rosiglitazone on insulin sensitivity,lipolysis,and hepatic and skeletal muscle triglyceride content in patients with type 2 diabetes[J].Diabetes,2002,51:797-802.
[7]Carey DG,Cowin GJ,Galloway GJ,et al.Effect of rosiglitazone on insulin sensitivity and body composition in Type 2 diabetic patients[J].Obes Res,2002,10:1008-1015.
[8]Sutinen J,Hakkinen A,Westerbacka J,et al.Rosiglitazone in the treatment of HAART-associated lipodystrophy-a randomized double-blind placebo-controlled study[J].Antivir Ther,2003,8:199-208.
[9]Teranishi T,Ohara T,Maeda K,et al.Effects of pioglitazone and metformin on intracellular lipid content in liver and skeletal muscle of individuals with type 2 diabetes mellitus[J].Metabolism,2007,56:1418-1424.
[10]Bajaj M,Suraamornkul S,Hardies L,et al.Effects of peroxisome proliferator-activated receptor(PPAR)-a and PPAR-c agonists on glucose and lipid metabolism in patients with type 2 diabetes mellitus[J].Diabetologia,2007,50:1723-1731.
[11]Neuschwander-Tetri BA,Brunt EM,Wehmeier KR,et al.Improved nonalcoholic steatohepatitis after 48 weeks of treatment with the PPAR-gamma ligand rosiglitazone[J].Hepatology,2003,38:1008-1017.
[12]Ratziu V,Giral P,Jacqueminet S,et al.Rosiglitazone for nonalcoholic steatohepatitis:one-year results of the randomized placebo-controlled Fatty Liver Improvement with Rosiglitazone Therapy(FLIRT)Trial[J].Gastroenterology,2008,135:100-110.
[13]Aithal GP,Thomas JA,Kaye PV,et al.Randomized,placebo cont-rolled trial of pioglitazone in nondiabetic subjects with nonalcoholic steatohepatitis[J].Gastroenterology,2008,135:1176-1184.
[14]Promrat K,Lutchman G,Uwaifo GI,et al.A pilot study of pioglitazone treatment for nonalcoholic steatohepatitis[J].Hepatology,2004,39:188-196.
[15]Belfort R,Harrison SA,Brown K,et al.A placebo-controlled trial of pioglitazone in subjects with nonalcoholic steatohepatitis[J].N Engl J Med,2006,355:2297-2307.
[16]Lutchman G,Promrat K,Kleiner DE,et al.Changes in serum adipo-kine levels during pioglitazone treatment for nonalcoholic steatohepatitis:relationship to histological improvement[J].Clin Gastroenterol Hepatol,2006,4:1048-1052.
[17]Berlie HD,Kalus JS,Jaber LA.Thiazolidinediones and the risk of edema:a meta-analysis[J].Diabetes Res Clin Pract,2007,76:279-289.
[18]Singh S,Loke YK,Furberg CD.Thiazolidinediones and heart failure:a teleo-analysis[J].Diabetes Care,2007,30:2148-2153.
(收稿日期:2014-12-05)
文章编号1004-0188(2015)03-0336-03
doi:10.3969/j.issn.1004-0188.2015.03.043
中图分类号R 575.29
文献标识码A
通讯作者:苟仲勇,E-mail:1106808684@qq.com
