羟基磷灰石及氟掺杂对的吸附性能研究
2015-03-03李永鹏张红平林晓艳
李永鹏 张红平 林晓艳
(西南科技大学生物质材料教育部工程研究中心 四川绵阳 621010)
李永鹏 张红平 林晓艳
(西南科技大学生物质材料教育部工程研究中心 四川绵阳 621010)
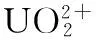
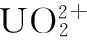
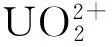
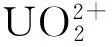
1 实验
1.1 材料与仪器
四水硝酸钙,磷酸氢二铵,氨水,氟化钠,盐酸,偶氮胂III(分析纯,成都科龙化工试剂厂),硝酸氧铀酰(湖北楚盛威化工有限公司)。
恒温震荡培养箱(上海鸿都电子科技有限公司);氟离子选择性电极(上海仪电科学仪器股份有限公司);X射线衍射分析仪(PANalytical Corporation;2θ测试角度3°~ 80°,Cu靶 Kα1);傅立叶变换红外光谱仪(PerkinElmer Instrument Corporation;测试范围4 000~400 cm-1);X射线光电子能谱仪(Kratos Corporation;Al Kα激发源);同步热分析仪(TA Instrument Corporation;空气气氛,升温速率10 ℃/min);原子吸收分光光度计(PerkinElmer Instrument Corporation;测定波长422.7 nm);紫外-可见分光光度计(Shimadzu Corporation;测定波长650 nm)
1.2 羟基磷灰石、氟掺杂羟基磷灰石制备
25 ℃下,将2.952 g四水硝酸钙和0.99 g磷酸氢二铵分别溶于去离子水中配成0.5 mol/L的溶液A和0.3 mol/L的溶液B,通过不同的F-/Ca2+(摩尔比)来控制氟掺杂量,分别取0 g,0.063 g和 0.157 5 g的氟化钠(即F-/Ca2+摩尔的比分别为0,3/25和3/10)加入上述溶液B中,搅拌至完全溶解后,将B的混合液以5 mL/min的速度均匀滴加入A溶液中,以500 r/min 的速度机械搅拌,通过添加氨水调节溶液的pH值为10。溶液B滴加完后,继续搅拌2 h,然后在25 ℃下陈化24 h,移除陈化后的上清液,离心洗涤白色沉淀,冷冻干燥后得到白色粉末样品[9]。采用氟离子电极表征了FHA中F的含量,样品的命名及其氟含量如表1所示。

表1 HA,FHA93和FHA200样品及其氟的含量Table 1 The HA,FHA93 and FHA200 specimens prepared and their fluorine contents
1.3 耐酸性实验
称取0.1 g的HA,FHA粉末分别加入到50 mL pH值3~7的醋酸溶液中,25 ℃下振荡2 d使其达到溶解平衡,过滤得到澄清溶液,通过原子吸收分光光度计测定溶液中的钙离子浓度。
1.4 吸附实验
(1)
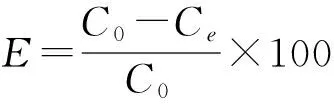
(2)
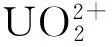
2 结果与讨论
2.1 红外光谱分析
HA,FHA93和FHA200的红外光谱图如图1(a)所示,图中清楚呈现了磷灰石的光谱特征。471cm-1,565cm-1和603cm-1处对应O-P-O的弯曲振动峰;962cm-1处的吸收峰对应P-O的对称伸缩振动;1 039cm-1和1 093cm-1处为P-O的不对称伸缩振动峰[11]。630cm-1处的吸收峰对应羟基的摆动振动峰,随着F-的掺入量提高,OH-逐渐被F-取代,导致羟基的摆动振动峰逐渐减弱[12]。根据MahmoudAzami的报道,随着HA晶格中氟含量的提高,603cm-1处的峰强度相对于565cm-1处的峰强度在逐渐增强[13]。在3 300~3 600cm-1和1 641cm-1处较宽的扩散峰可能是晶格中水的吸收峰。
2.2XRD分析
图1(b)所示为HA,FHA93和FHA200的XRD图谱分析。由图可知,随着氟掺杂量的增加,衍射峰逐渐变得尖锐且强度增强,因此氟掺杂有利于提高晶体结晶性。同时可看到,与HA相比,FHA93和FHA200的(211)晶面所对应的衍射峰向右方向偏移,说明F-取代了HA中的OH-。由于F-离子半径较OH-离子半径小,HA晶格畸变,引起晶胞参数a和b (a=b)减小,导致衍射峰位置偏移。根据文献报道,F-对HA晶格中的晶胞参数c值不会产生影响[14]。
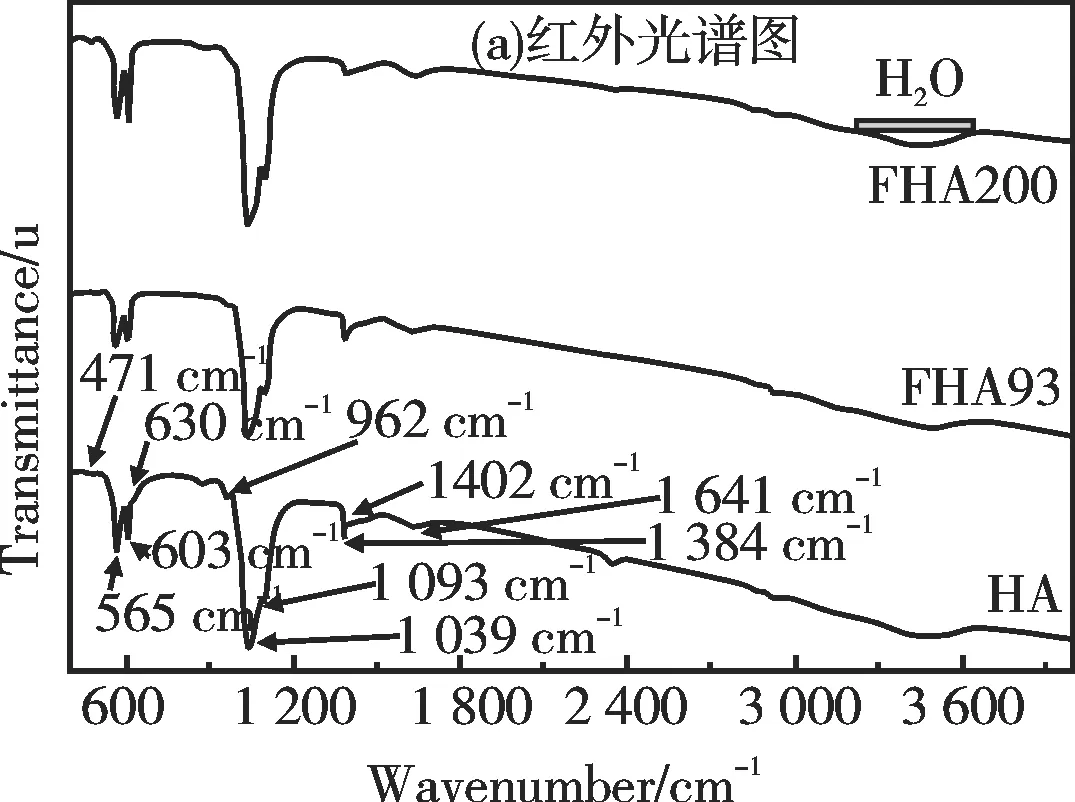
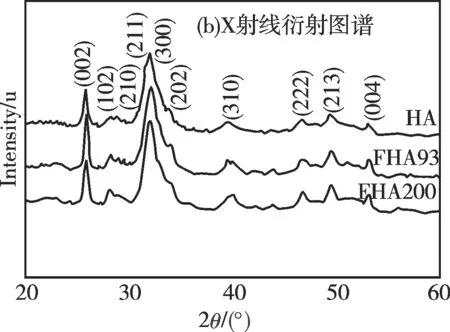
图1 HA,FHA93和FHA200的红外光谱图和X射线衍射图谱Fig. 1 FT-IR spectra and XRD patterns of HA, FHA93 and FHA200
2.3 热稳定性分析
采用热失重分析了HA,FHA93和FHA200 样品的热稳定性,如图2(a)所示,在50~100 ℃时,3个样品出现快速失重,可能是样品中附带的一些水分失去所致。在100 ℃以上,HA一直保持较快的失重速率,而FHA93和FHA200的失重逐渐趋于稳定。从室温到1 000 ℃,HA的失重百分比明显大于FHA93和FHA200,即HA(失重11.10%)> FHA93(失重8.35%)> FHA200(失重6.60%)。
为进一步研究HA的热稳定性,对HA,FHA93和FHA200进行1 200 ℃焙烧2 h处理,图2(b)是焙烧处理后的XRD分析图,从图2(b)可以看到,经过焙烧处理后的HA出现了杂相β-TCP,可能是HA高温下失去了羟基而分解成磷酸三钙,因而高温下焙烧的HA稳定性较差。在相同焙烧温度下,FHA93和FHA200未发现β-TCP衍射峰,说明掺入的F-提高了HA的热稳定性[8]。强电负性的氟很容易与羟基中的氢原子结合,从而产生键能更强的氢键,所以在焙烧过程中FHA的OH-很难失去,进而提高了氟掺杂羟基磷灰石的热稳定性。
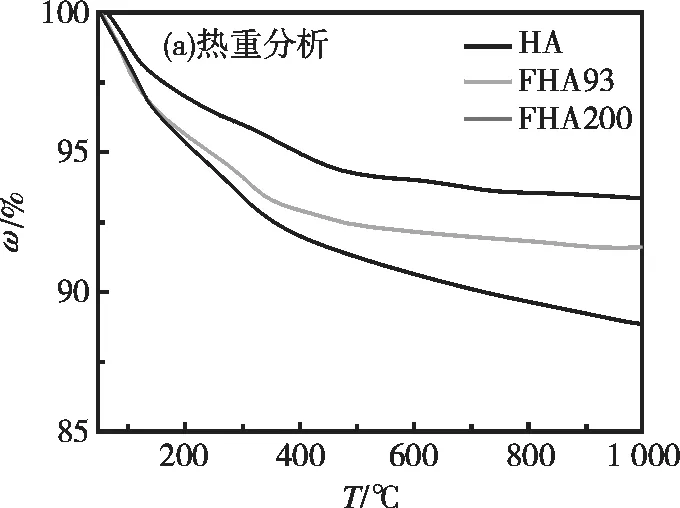
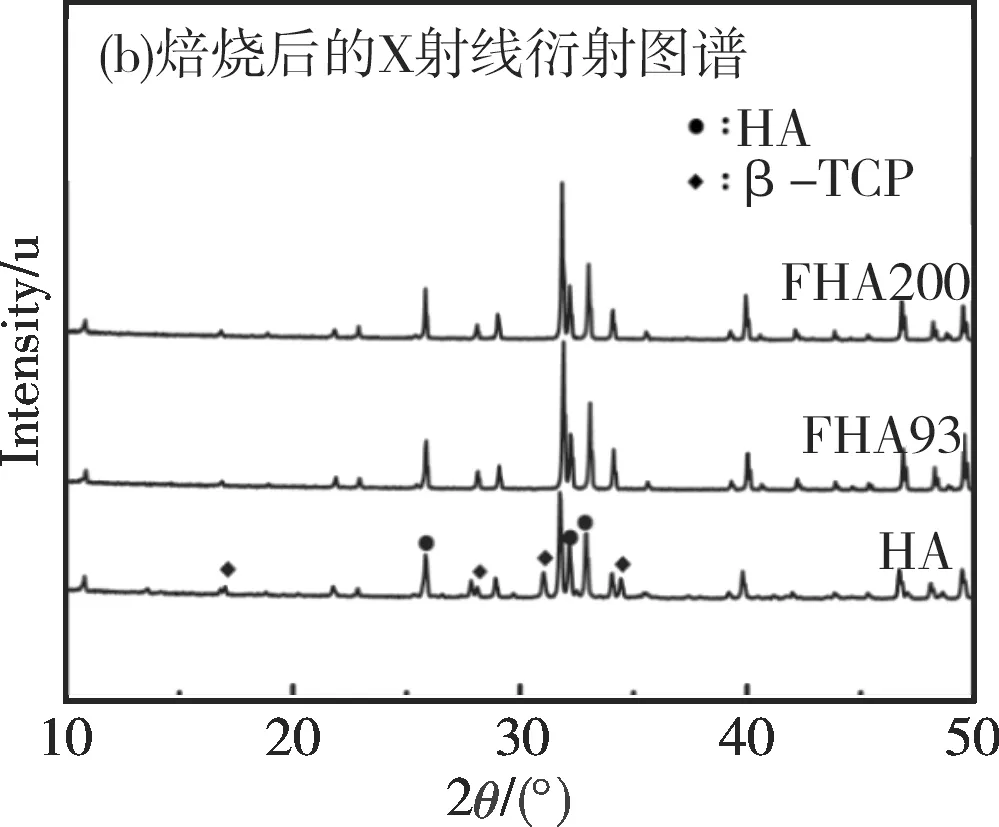
图2 HA,FHA93和FHA200的热重分析和焙烧后的X射线衍射图谱Fig. 2 TGA analysis and XRD patterns of HA, FHA93 and FHA200 samples of samples after calcination
2.4 耐酸性分析
图3所示为HA,FHA93和FHA200经过不同pH值的酸液处理2 d后的Ca2+离子浓度曲线图。由图3可知,氟掺杂羟基磷灰石所释放的Ca2+离子浓度都较HA的小,特别是在pH值为3时,FHA200所释放的Ca2+离子浓度比HA和FHA93的少近0.08 mM,因此,引入F-改善了HA的耐酸性。HA和FHA在酸性环境中分别产生如下反应:
Ca10(PO4)6(OH)2+2H+→
(3)
Ca10(PO4)6(OH)xF2-x+xH+→
(4)
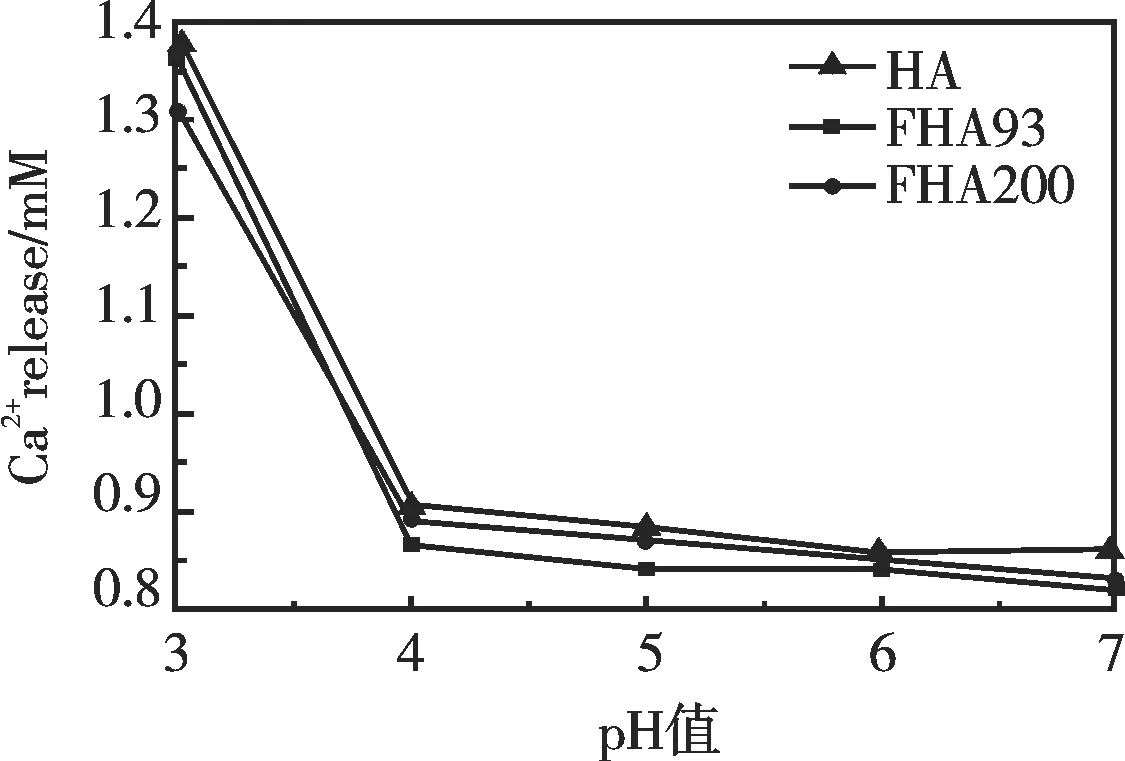
图3 HA,FHA93和FHA200在稀酸溶液中Ca2+的释放行为Fig. 3 The release behavior of Ca2+ from HA, FHA93 and FHA200 in dilute acid solution
由于掺氟羟基磷灰石的晶体结构比羟基磷灰石更加紧密,导致掺氟羟基磷灰石的溶解度比羟基磷灰石小,所以反应(4)进行的程度比反应(3)慢[15]。
2.5 XPS分析
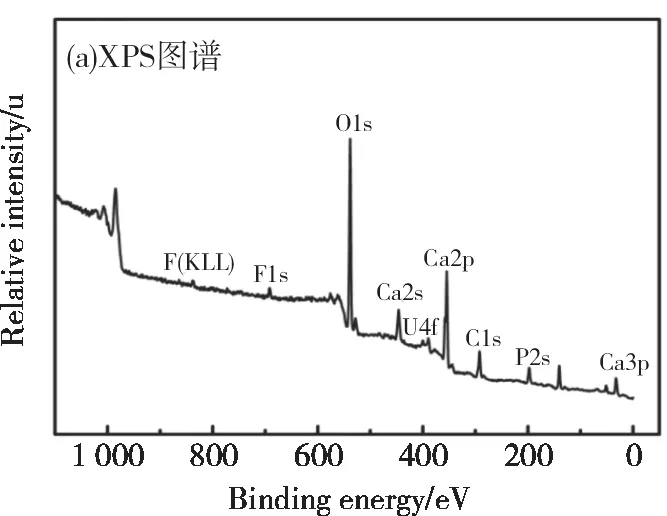
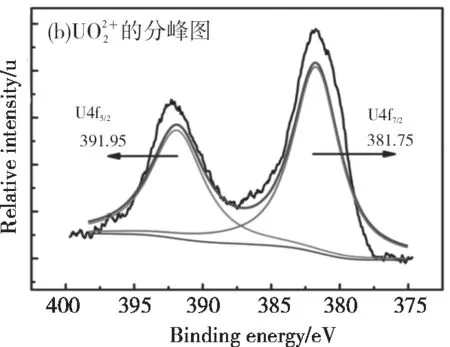
2.6 影响吸附的因素和吸附特性
2.6.1 溶液酸碱性因素
2.6.2 初始溶液浓度因素
2.6.3 吸附时间因素
如图5(c)所示,吸附时间在1 h以内时,HA,FHA93和FHA200的吸附量均随着时间的变化而迅速增加,在1~12 h内,吸附量呈缓慢增加的趋势,12 h后完全达到饱和吸附状态。尤其是FHA93在1 h的吸附量达到饱和吸附量的98%,这种优势比HA和FHA200更加明显。
2.6.4 吸附热力学研究
吸附过程中相关的热力学函数值用方程(5)-(7)进行拟合计算[17]。
ΔG0=ΔH0-TΔS0
(5)
(6)
(7)
式中R是理想气体常数,数值是8.314(J/mol K);T是反应的温度(K);Kd是热力学平衡常数;ΔG0是反应时的吉布斯自由能变(kJ·mol-1);ΔH0是焓变(kJ·mol-1);ΔS0是熵变(J·mol-1·K-1)。ΔH0和ΔS0可以根据拟合后直线的斜率和截距计算出来。
拟合后得到的数据图如图5(d)所示,ΔH0的数值是正值,说明吸附过程是吸热的。ΔS0的数值大于零,说明在吸附过程中固液界面的混乱度增加了。ΔG0的数值小于零,表明吸附过程是自发进行的,同时随着温度的升高,ΔG0的数值变得更小,这也说明升高温度对吸附过程是有利的。
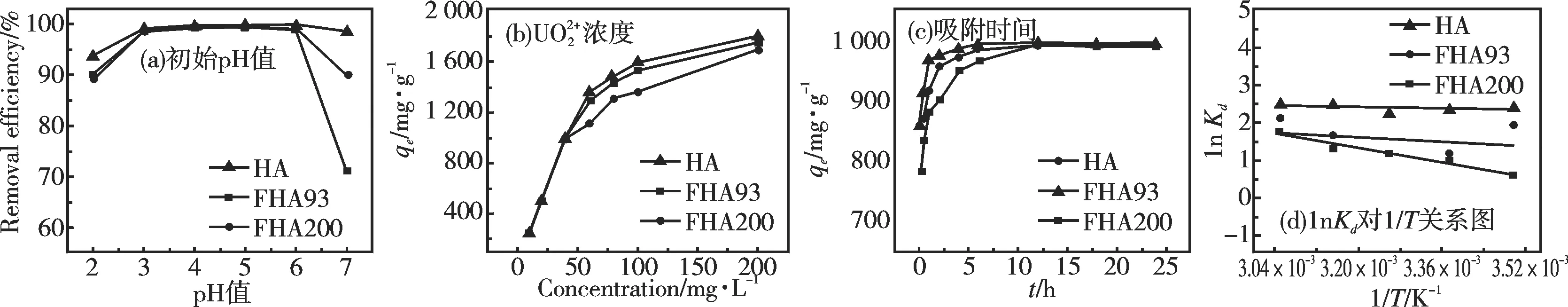
2.6.5 等温吸附模型及吸附动力学研究
用Langmuir(8)和Freundlich(9)方程对吸附数据进行拟合[17]:
(8)
(9)
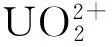
(10)
公式(10)中,当RL=0时为不可逆吸附;0
采用准一级动力学(11)和准二级动力学(12)对吸附数据进行拟合[17]:
1n(qe-qt)=1nqe-k1t
(11)
(12)
qe和qt分别是平衡时的吸附量和t(min)时刻的吸附量(mg/g);t是吸附的时间(min);k1为准一级动力学模型的吸附速率常数(min-1);k2为准二级动力学模型的吸附速率常数(g/mg·min)。
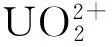
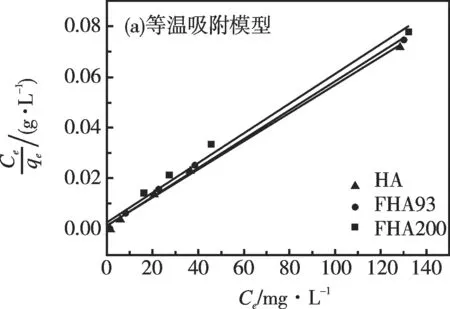
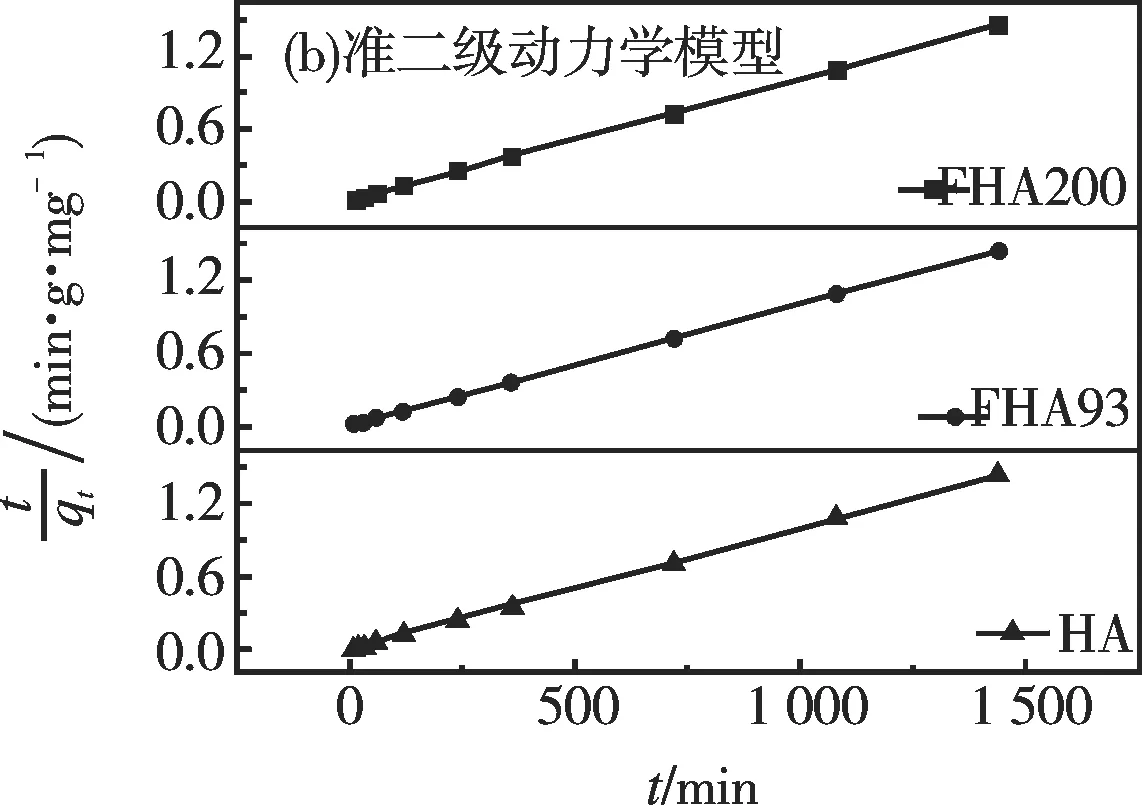
图6 Langmuir 等温吸附模型和准二级动力学模型Fig. 6 Langmuir adsorption isotherms model and pseudo-second-order model
3 结论
[1] WANG G H,LIU J S,WANG X G,et al.Adsorption of uranium(VI) from aqueous solution onto cross-linked chitosan[J].Journal of Hazardous Materials,2009,168(2):1053-1058.
[2] WANG G H,WANG X G,CHAI X J,et al.Adsorption of uranium (VI) from aqueous solution on calcined and acid- activated kaolin[J].Applied Clay Science,2010,47(3-4):448-451.
[3] DONAT R.The removal of uranium (VI) from aqueous solutions onto natural sepiolite[J].The Journal of Chemical Thermodynamics,2009,41(7):829-835.
[4] SADAT-SHOJAI M,KHORASANI M T,DINPANAH -KHOSHDARGI E,et al.Synthesis methods for nanosized hydroxyapatite with diverse structures[J].Acta Biomater,2013,9(8):7591-7621.
[5] THAKUR P,MOORE R C,CHOPPIN G R.Sorption of U(VI) species on hydroxyapatite[J].Radiochimica Acta,2005,93(7):385-391.
[6] CHATTANATHAN S A,CLEMENT T P,KANEL S R,et al.Remediation of uranium-contaminated groundwater by sorption onto hydroxyapatite derived from catfish bones[J].Water,Air & Soil Pollution,2013,224(2):1 -9.
[7] 杨国华,黄统琳,姚忠亮,等.吸附剂的应用研究现状和进展[J].化学工程与装备,2009,(6):84-88.
[8] CHEN Y,MIAO X G.Thermal and chemical stability of fluorohydroxyapatite ceramics with different fluorine contents[J].Biomaterials,2005,26(11):1205-1210.
[9] ESLAMI H,SOLATI-HASHJIN M,TAHRIRI M.Synthesis and characterization of nanocrystalline fluorinated hydroxyapatite powder by modified wet -chemical process[J].Journal of Ceramic Processing Research,2008,9(3) :224 -229.
[10] ULUSOY U,AKKAYA R.Adsorptive features of polyacrylamide- apatite composite for Pb2 +,UO2 +2 and Th4 +[J].Journal of Hazardous Materials,2009,163(1):98 -108.
[11] FATHI M H,ZAHRANI E M.Fabrication and characterization of fluoridated hydroxyapatite nanopowders via mechanical alloying[J].Journal of Alloys and Compounds,2009,475(1):408-414.
[12] BIANCO A,CACCITOTTI I,LOMBARDI M,et al.F -substituted hydroxyapatite nanopowders: Thermal stability,sintering behaviour and mechanical properties[J].Ceramics International,2010,36(1):313-322.
[13] AZAMI M,JALILIFIROOZINEZHAD S,MOZAFARI M,et al. Synthesis and solubility of calcium fluoride/hydroxy-fluorapatite nanocrystals for dental applications[J]. Ceramics International,2011,37(6):2007-2014.
[14] LU Z Z,WANG H,ZENG J,et al. Dynamic crystal-growth process observed during hydrothermal coarsening of nanocrystalline hydroxyfluorapatite[J]. Journal of Crystal Growth,2009,311(23-24):4791-4798.
[15] 赵朝霞,翁文剑,曲海波,等. 含氟羟基磷灰石薄膜的溶胶-凝胶制备和溶解特性研究[J]. 材料科学工程学报,2005,23(2):226-229.
[16] CHENG K,ZHANG S,WENG W J. The F content in sol-gel derived FHA coatings: an XPS study[J]. Surface and Coatings Technology,2005,198(1-3):237-241.
[17] TAN L C,WANG Y L,LIU Q,et al. Enhanced adsorption of uranium (VI) using a three-dimensional layered double hydroxide/graphene hybrid material[J]. Chemical Engineering Journal,2014,259(1):752-760.
[18] ILAIYARAJA P,DEB A,SIVASUBRAMANIAN K,et al. Adsorption of uranium from aqueous solution by PAMAM dendron functionalized styrene divinylbenzene[J]. Journal of Hazardous Materials,2013,250:155-166.
The Effect of Hydroxyapatite and Fluorine-Substituted on the Adsorption of
LI Yong-peng, ZHANG Hong-ping, LIN Xiao-yan
(EngineeringReaearchCenterofBiomassMaterials,MinistryofEducation,SouthwestUniversityofScienceandTechnology,Mianyang621010,Sichuan,China)
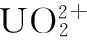
2015-02-11
国家自然科学基金青年基金(31300793)。
李永鹏(1990—),男,硕士研究生。通讯作者:张红平(1982—),男,博士,研究方向为材料表面界面。E-mail:zhp1006@126.com
X703
A
1671-8755(2015)02-0001-06
