水溶性 β-NaY(Gd)F4∶Yb3+/Er3+纳米棒的水热合成及生物偶联
2015-03-02孙振刚华瑞年
肇 欣,孙振刚,张 伟,华瑞年*
(1.辽宁师范大学化学化工学院,辽宁大连 116029;2.大连民族学院生命科学学院,辽宁大连 116600)
1 引 言
自从上世纪90年代以来,由于化学、物理和材料在纳米领域的快速发展,导致了“纳米科学和纳米科技”这一新兴学科的出现。作为21世纪的关键性技术,纳米技术涉及到多学科交叉的研究领域。在这一领域中,尤其是高质量的单分散无机纳米晶对形貌和比表面积的性质依赖,以及这一性质在光学、催化、生物传感和数据存储上的应用已经得到了极大的发展。稀土离子独特的4f电子结构使稀土纳米材料具有很多独特的性质。稀土上转换发光纳米材料(Upconversion nanoparticles,UCNPs)已成为当前发光学领域的研究热点[1-2]。
稀土掺杂氟化物上转换纳米发光材料具有毒性小、自荧光背景低、发射峰窄、化学性质稳定等特点,在红外光光催化、光动力学治疗、荧光探针和生物医学等领域具有广阔的应用前景[3-7]。传统的荧光探针(如有机颜料)由于采用短波激发光源和相对较高的荧光漂白速率,因而具有较高的背景荧光并只能用于短时间内的成像[8]。与传统发光标记物相比,UCNPs具有化学稳定性好、毒性低、发光强度高和Stokes位移大等优点。另外,UCNPs的激发光为红外光,不会损伤生物体也不会激发出背景荧光,信噪比高,非常有利于活体生物成像[9-11]。NaYF4是近年来发现的一种理想的上转换基质材料,具有较低的声子能量,能降低多声子弛豫率,提高上转换发光效率,稀土氟化物β-NaYF4被公认为是一种优质的上转换发光材料[12-14]。2010 年,喻学峰等[15]合成了一系列大半径稀土离子(La3+、Ce3+、Pr3+、Nd3+、Sm3+、Eu3+和Gd3+等)掺杂的水溶性六方相NaYF4纳米棒,六方相 NaYF4∶(Yb,Er)/La 和 NaYF4∶(Yb,Er)/Ce纳米棒表现出比立方相更高的上转换荧光效率。在目前报道的所有 UCNPs中,NaYF4∶Yb,Er/Tm的上转换效率是最高的。可以用于生物检测的上转换荧光标记物也主要是 Yb/Er和Yb/Tm共掺杂的NaYF4纳米粒子。NaYF4属于多晶型的复合稀土氟化物,具有亚稳相——立方相(α-NaYF4)和稳定相——六方相(β-NaYF4)两种晶体结构。六方相 NaYF4∶Yb,Er/Tm相对于其立方相材料,上转换发光效率要高一个数量级。
本文利用一步水热法合成出氨基表面修饰、单分散性好、尺寸小、发光性能优异的水溶性β-NaY(Gd)F4∶Yb3+/Er3+上转换纳米棒,用X射线粉末衍射仪(XRD)、扫描电子显微镜 (SEM)、透射电子显微镜(TEM)和荧光光谱(PL)等手段对制备的样品进行了表征,并通过戊二醛法将BSA生物分子与所制备的β-NaY(Gd)F4∶Yb3+/Er3+上转换纳米棒成功偶联。
2 实 验
2.1 试剂
分析纯氯化钠(NaCl)、无水乙醇(C2H5OH)、氟化铵(NH4F)、聚乙烯亚胺(PEI)、牛血清蛋白(BSA)、戊二醛(25%,质量分数)、磷酸(H3PO4)、考马斯亮蓝(G-250)、磷酸氢二钠Na2HPO4·12H2O和磷酸二氢钠 NaH2PO4·12H2O等均购于天津科密欧化学试剂有限公司。Y2O3(99.99%)、Gd2O3(99.99%)、Yb2O3(99.99%)和 Er2O3(99.99%)均购于上海第二化学试剂厂。氯化钆(GdCl3·6H2O)、氯化镱(YbCl3·6H2O)、氯化钇(YCl3·6H2O)和氯化铒 (ErCl3·6H2O)均为自制,即将相应的稀土氧化物溶于6 mol/L HCl中,重结晶4次获得。
2.2 β-NaY(Gd)F4∶Yb3+/Er3+纳米棒的制备
称取0.058 4 g NaCl(1 mmol)、0.115 2 g YCl3·6H2O(0.38 mmol)、0.077 5 g YbCl3·6H2O(0.20 mmol)、0.007 63 g ErCl3·6H2O(0.02 mmol)和0.148 6 g GdCl3·6H2O(0.40 mmol)溶于10 mL去离子水中得到溶液A,再称取0.296 0 g NH4F(8 mmol)溶于10.0 mL去离子水中得到溶液B,量取10mL质量浓度为0.05 g/mL的PEI溶液和30 mL无水乙醇混合在50 mL烧杯中得到溶液C。在不断搅拌下,将溶液C缓慢滴加到溶液A中。搅拌30 min后,再将溶液B缓慢滴加到其中,10 min内完成滴加,再缓慢匀速搅拌20 min。将上述溶液倒入100 mL不锈钢反应釜,放在烘箱中,温度调至200℃,加热8 h后,关闭烘箱,取出反应釜,自然冷却至室温。将产物在9 000 r/min的转速下离心10 min,用无水乙醇洗涤4次,获得的沉淀在80℃下干燥,得到的白色粉末即为表面有氨基修饰的水溶性β-NaY0.38Gd0.4F4∶20%Yb3+,2%Er3+纳米棒。
2.3 β-NaY(Gd)F4∶Yb3+/Er3+与 BSA 偶联产物的制备
准确称取10 mg所制备的 β-NaY(Gd)F4∶Yb3+/Er3+纳米棒溶解在2.0 mL去离子水中,超声分散30 min后,在3 000 r/min的转速下离心,上清液倒出以备后续实验中使用。将有少量沉淀的离心管放入烘箱中,干燥后称其质量,用于计算溶解于水中的样品的质量。将1 mg的BSA加入到上清液中,在室温下搅拌2 h后,再将0.10 mL戊二醛(25%,质量分数)滴加到上述溶液中,在室温下缓慢搅拌5 h。将产物在9 000 r/min的转速下离心,并用磷酸缓冲溶液(10 mmol/L,pH=7.4)洗涤3次,最后定容在2.0 m L的磷酸缓冲溶液中。
2.4 实验仪器
日本岛津公司产XRD-6000型X射线粉末衍射仪,铜靶(λ=0.154 06 nm);日本日立公司产S-4800型场发射扫描电子显微镜;日本电子公司JEM-2010型透射电子显微镜;日本Horiba公司产SZ-100-Z型激光粒度分析仪;日本日立公司F-4600型荧光光谱仪;日本岛津UV-2450紫外光谱仪;上海美谱达仪器有限公司产UV-6100紫外-可见分光光度计。摩尔分数为40%条件下制得的β-NaY(Gd)F4∶Yb3+/Er3+纳米棒样品的粉末X射线衍射(XRD)谱。从图中可以看出,β-NaY(Gd)F4∶Yb3+/Er3+纳米棒的衍射峰与β-NaYF4的标准卡片完全一致,没有出现其他杂质峰,表明产物物相纯净、结晶良好。在该反应条件下,如果不引入大半径的Gd3+,产物为 α-NaYF4和 β-NaYF4混相产物;随着Gd3+离子掺杂量的增大(至Gd3+的摩尔分数到30%),仍得不到纯相的 β-NaYF4(产物为 β-NaYF4和少量的α-NaYF4)。该实验结果表明,当引入一定量大半径的Gd3+后,在较短的反应时间内,有利于α-NaYF4向β-NaYF4相转变,并最终获得纯相的β-NaYF4纳米棒。
3 结果与讨论
3.1 物相结构分析
图1为反应温度200℃、反应时间8 h、Gd3+

图1 β-NaY(Gd)F4∶Yb3+/Er3+纳米棒的XRD谱Fig.1 XRD pattern ofβ-NaY(Gd)F4∶Yb3+/Er3+nanorods
3.2 形貌分析
在室温下,通过扫描电子显微镜和透射电子显微镜对合成的β-NaY(Gd)F4∶Yb3+/Er3+纳米棒的形貌进行了观测,如图2所示。
从图2可以看出,β-NaY(Gd)F4∶Yb3+/Er3+样品的形貌为规则的实心六棱柱型纳米棒,截面粒径平均约为40 nm,平均长度约为210 nm。偶联BSA后的β-NaY(Gd)F4∶Yb3+/Er3+表面覆盖了一层物质,因此形貌发生了变化,但粒径大小没有发生明显改变。
3.3 荧光光谱分析
图3是在980 nm激发下的β-NaY(Gd)F4∶Yb3+/Er3+纳米棒的上转换发光光谱。谱图显示了4个明显的发射带,发射中心位于407,529,546,660 nm,分别对应于2H9/2→4I15/2、2H11/2→4I15/2、4S3/2→4I15/2和4F9/2→4I15/2跃迁。图 4 是 β-NaY(Gd)F4∶Yb3+/Er3+纳米棒的上转换发光机理图。Er3+的基态能级是4I15/2,当用980 nm的红外激光器激发样品时,电子跃迁至4I11/2能级,Yb3+发生2F7/2→2F5/2跃迁,激发到2F5/2能级的电子通过声子参与的非共振能量转移把能量转到Er3+的4I11/2能级上。Er3+可吸收第2个光子或吸收邻近已处于2F5/2能级的电子的能量,再次跃迁至2H11/2和4S3/2能级,返回基态能级4I15/2时分别发出529 nm和546 nm的绿光;另有一部分到达4S3/2能级的电子经无辐射跃迁至4F9/2能级,由4F9/2能级返回基态时发出660 nm的红光。

图2 样品 β-NaY(Gd)F4∶Yb3+/Er3+的SEM 照片(a)和透射电镜照片(c),β-NaY(Gd)F4∶Yb3+/Er3+偶联BSA后的SEM照片(b)及β-NaY(Gd)F4∶Yb3+/Er3+的粒径分析图(d)。Fig.2 SEM image(a)and TEM image(c)ofβ-NaY(Gd)F4∶Yb3+/Er3+,SEM image(b)ofβ-NaY(Gd)F4∶Yb3+/Er3+conjugated with BSA,and particle size distribution ofβ-NaY(Gd)F4∶Yb3+/Er3+(d).

图4 β-NaYF4∶Yb3+/Er3+的上转换发光机理图Fig.4 Upconversion luminescence mechanism diagram ofβ-NaYF4∶Yb3+/Er3+

图3 样品 β-NaY(Gd)F4∶Yb3+/Er3+的荧光谱 (λex=980 nm)Fig.3 Fluorescent spectrum ofβ-NaY(Gd)F4∶Yb3+/Er3+(λex=980 nm)
3.4 紫外光谱分析
作为有机功能分子,聚乙烯亚胺(PEI)被选作修饰β-NaY(Gd)F4∶Yb3+/Er3+纳米棒表面的有机功能分子。因PEI结构中含有氨基,并且可进一步与BSA偶联。PEI修饰的β-NaY(Gd)F4∶Yb3+/Er3+纳米棒能够很好地分散在水溶液中(溶解度约为1 mg/mL),其表面氨基的存在非常适合于生物和生物医学应用。图5的紫外-可见吸收光谱进一步证实了 β-NaY(Gd)F4∶Yb3+/Er3+纳米棒样品已与BSA成功偶联。在BSA的紫外标准光谱中,位于276 nm和208 nm的峰被指认为BSA中的色氨酸残基和肽键的吸收峰。在 β-NaY(Gd)F4∶Yb3+/Er3+@PEI-BSA 的紫外光谱中也可以观察到276 nm和208 nm处的吸收峰,然而在 β-NaY(Gd)F4∶Yb3+/Er3+@PEI的紫外光谱中却没有出现这两个吸收峰。这一实验结果初步证实了BSA与β-NaY(Gd)F4∶Yb3+/Er3+@PEI纳米棒的成功偶联。
3.5 考马斯亮蓝法定量分析蛋白含量
用布拉德福德试剂(100 mg的考马斯亮蓝G-250在50 mL的95%乙醇中溶解,然后加入120 mL的85%磷酸,用水稀释至1.0 L)与BSA发生颜色反应,进一步定量地验证 BSA是否与 β-NaY(Gd)F4∶Yb3+/Er3+@PEI纳米棒偶联。考马斯亮蓝G-250是一种甲基取代的三苯基甲烷,分子中含磺酸基的蓝色染料,在465 nm处有最大的吸收值。因此,布拉德福德试剂能吸收465 nm可见光,布拉德福德试剂与BSA蛋白结合物可以吸收595 nm可见光,其吸光度值与蛋白质含量成正比。这种变化通过紫外光谱分析法可以用来量化样品中BSA蛋白的含量。
首先,配制BSA的标准溶液,浓度分别为0,0.02,0.04,0.06,0.08,0.10 mg/mL 的 BSA 溶液各1.00 mL。然后,向上面的BSA溶液中分别加入5.00 mL的布拉德福德试剂。2 min后,用布拉德福德试剂-BSA偶联物的蛋白质溶液在595 nm处进行吸光度的测定,测定的值依次为0,0.145,0.294,0.403,0.565,0.652。最后得到在0.0 ~0.1 mg/mL浓度范围内的吸光度与BSA的浓度的线性关系,如图6所示。回归方程可以表示如下:
Y=6.6129X+0.0125,(R2=0.995 1), (1)式中,X为BSA浓度,Y为吸光度。经测定,样品β-NaY(Gd)F4∶Yb3+/Er3+@PEI-BSA 的吸光度为0.127,根据蛋白质标准曲线计算出β-NaY(Gd)F4∶Yb3+/Er3+@PEI表面的BSA偶联率为1.73%(含BSA 0.017 3 mg/mL)。这个结果进一步表明,BSA 与 β-NaY(Gd)F4∶Yb3+/Er3+@PEI纳米粒子偶联成功。
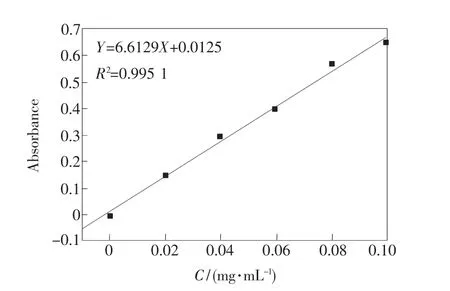
图6 在595 nm吸收波长下,BSA的浓度与吸光度的关系曲线。Fig.6 Linear relationship between the concentration of BSA and absorbance at595 nm
4 结 论
以聚乙烯亚胺(PEI)为表面活性剂,采用水热法,在Gd3+的摩尔分数为40%、反应温度为200℃、时间为8 h的条件下制得了纯相的β-NaY(Gd)F4∶Yb3+/Er3+纳米棒。纳米棒的平均截面粒径约为40 nm,平均长度约为210 nm。偶联BSA后的β-NaY(Gd)F4∶Yb3+/Er3+表面覆盖了一层物质,因此形貌发生了变化,但粒径大小没有发生明显改变。当用980 nm波长激发样品后,β-NaY(Gd)F4∶Yb3+/Er3+纳米棒的上转换光谱中出现了4个明显的发射带,发射中心位于 407,529,546,660 nm,分别对应于2H9/2→4I15/2、2H11/2→4I15/2、4S3/2→4I15/2和4F9/2→4I15/2跃迁。采用戊二醛法,使得蛋白(BSA)上的氨基与 β-NaY(Gd)F4∶Yb3+/Er3+纳米棒表面的氨基牢固地键合在一起,并通过紫外光谱分析和考马斯亮蓝法证明了β-NaY(Gd)F4∶Yb3+/Er3+纳米棒与 BSA偶联成功。根据考马斯亮蓝法算出 β-NaY(Gd)F4∶Yb3+/Er3+纳米棒与 BSA的偶联率为1.73%(0.017 3 mg/mL)。该研究为将 β-NaY(Gd)F4∶Yb3+/Er3+纳米棒应用于生物分子分析、细胞标记及成像提供了实验参考。
[1]Li C X,Lin J.Rare earth fluoride nano-/microcrystals:Synthesis,surfacemodification and application[J].J.Mater.Chem.,2010,20:6831-6847.
[2]Shen J,Sun LD,Yan CH.Luminescent rare earth nanomaterials for bioprobe applications[J].Dalton Trans.,2008(42):5687-5697.
[3]Qin W P,Zhang D S,Zhao D,etal.Near-infrared photocatalysis based on YF3∶Yb3+,Tm3+/TiO2core/shell nanoparticles[J].Chem.Commun.,2010,46(13):2304-2306.
[4]Zhang P,SteelantW,Kumar M,et al.Versatile photosensitizers for photodynamic therapy at infrared excitation[J].J.Am.Chem.Soc.,2007,129(15):4526-4527.
[5]Chatterjee D K,Rufaihah A J,Zhang Y.Upconversion fluorescence imaging of cells and small animals using lanthanide doped nanocrystals[J].Biomaterials,2008,29(7):937-943.
[6]Wang L Y,Yan R X,Huo Z Y,et al.Fluorescence resonant energy transfer biosensor based on upconversion-luminescent nanoparticles[J].Angew.Chem.Int.Ed.,2005,44(37):6054-6057.
[7]Zhang P,SteelantW,Kumar M,et al.Versatile photosensitizers for photodynamic therapy at infrared excitation[J].J.Am.Chem.Soc.,2007,129(15):4526-4527.
[8]Song W Y,Shi F,Qin W P,etal.Synthesis and characterization of small size,water soluble,and intense ultravioletupconversion emission ofβ-NaYF4∶Yb,Tm nanocrystals[J].Chin.J.Lumin.(发光学报),2012,33(7):688-692(in Chinese).
[9]Nyk M,Kumar R,Ohulchanskyy T Y,et al.High contrastin vitroandin vivophotoluminescence bioimaging using near infrared to near infrared up-conversion in Tm3+and Yb3+doped fluoride nanophosphors[J].Nano Lett.,2008,8(11):3834-3838.
[10]Wang M,Mi C C,Wang W X,et al.Immunolabeling and NIR-excited fluorescent imaging of HeLa cells by using NaYF4∶Yb,Er upconversion nanoparticles[J].ACSNano.,2009,3(6):1580-1586.
[11]Yang T S,Sun Y,Liu Q,etal.Cubic sub-20 nm NaLuF4-based upconversion nanophosphors for high-contrastbioimaging in different animal species[J].Biomaterial,2012,33(14):3733-3742.
[12]Wang F,Liu X G.Upconversion multicolor fine-tuning:Visible to near-infrared emission from lanthanide-doped NaYF4nanoparticles[J].J.Am.Chem.Soc.,2008,130(17):5642-5643.
[13]Wang F,Wang J,Liu X G.Direct evidence of a surface quenching effect on size-dependent luminescence of upconversion nanoparticles[J].Angew.Chem.Int.Ed.,2010,49(41):7456-7460.
[14]Boyer JC,Cuccia L A,Capobianco JA.Synthesis of colloidal upconverting NaYF4∶Er3+/Yb3+and Tm3+/Yb3+monodisperse nanocrystals[J].Nano Lett.,2007,7(3):847-852.
[15]Yu X F,LiM,Xie M Y,et al.Dopant-controlled synthesis ofwater-soluble hexagonal NaYF4nanorods with efficient upconversion fluorescence formulticolor bioimaging[J].Nano Res.,2010,3(1):51-60.

肇欣 (1989-),女,辽宁沈阳人,硕士研究生,2012年于辽东学院获得学士学位,主要从事稀土发光材料的合成与光谱性质方面的研究。
E-mail:737547805@qq.com

华瑞年 (1965-),男,吉林九台人,教授,2003年于东北师范大学获得博士学位,主要从事稀土发光材料的合成、光谱性质及生物利用方面的研究。
E-mail:rnhua@dlnu.edu.cn

孙振刚 (1963-),男,黑龙江肇源人,教授,2000年于东北师范大学获得博士学位,主要从事新型金属有机膦酸盐配位聚合物的设计合成、结构表征和性能的研究。
E-mail:szg188@163.com
