Fahr病1例报道及文献复习
2015-02-27顾正天严婷婷
顾正天 严婷婷
(淮安市第二人民医院ICU 淮安 223002)
Fahr病为散发或家族性的自发性基底神经节钙化,可导致多种神经、精神、认知等功能异常。目前本病并不罕见。我们接诊1例该病患者,表现为偏侧肢体感觉、运动异常。该患者经神经营养剂及钙离子拮抗剂等治疗后好转,现报道如下。
1 病例
患者,女,66岁,汉族,已婚,江苏省高淳县人。因“右侧肢体活动障碍1 d伴麻木”入院。患者入院前一天晚间在无明显诱因下突然出现右侧肢体麻木、活动无力,患腿不能行走,但患手尚能持物。当时无头晕、胸闷、心慌,无口角歪斜、口齿不清,自行服1粒阿司匹林肠溶胶囊。第二日未见好转,至我院门诊就诊,查头颅CT示:双侧小脑半球、基底节区、侧脑室旁、放射冠区对称性钙化灶(图1)。为进一步诊治,门诊拟Fahr病收入病房。患者发病以来无头痛、意识及情绪改变,无畏寒发热,大小便正常。病因、既往史:有高血压病史,否认发作前有前驱感染、中毒等病史,否认有甲状旁腺功能异常等代谢性疾病病史,否认有手足抽搐发作史,否认癫痫及使用抗癫痫药物史,余无相关病史。个人史及家族史均无特殊。入院后查体全身体格检查未见明显异常。神经系统专科检查见:意识清楚、精神可;双瞳孔大等圆,直径约2.5 mm,对光反射灵敏;右上肢肌力4级,右下肢肌力3级;四肢肌张力不高;右上肢痛觉稍减退。
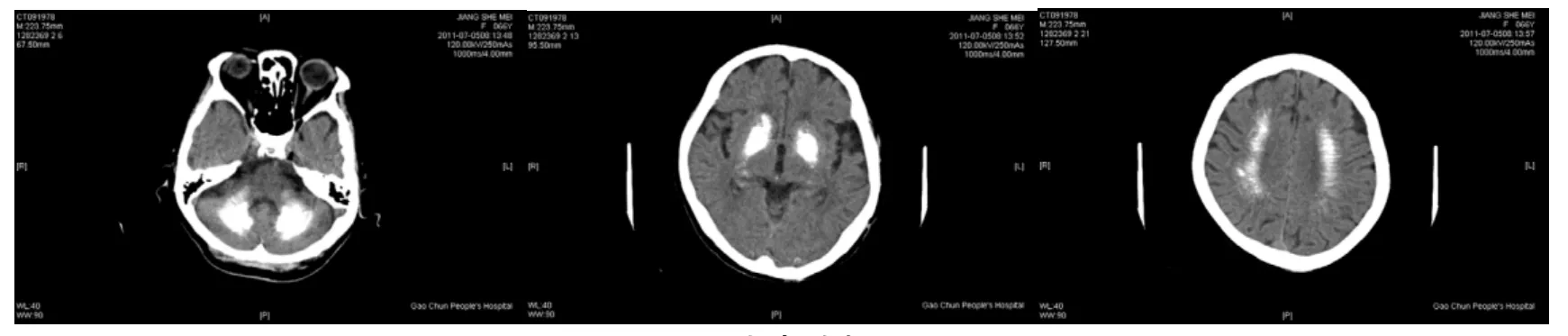
图1 患者头颅CT
入院辅助检查:血清甲状旁腺激素53.3 pg/ml,血钙2.54 mmol/L,血磷1.05 mmol/L,肾功能正常,24 h尿钙正常,血常规各指标正常,国际标准化比值1.1;甲状腺彩超示甲状腺右叶回声结节,甲状腺左叶下方低回声结节(考虑淋巴结);颈部血管彩超示双侧颈动脉硬化伴双侧颈总动脉膨大,颈部动脉斑块形成。心脏彩超示EF 0.60,动脉硬化,左室舒张功能减退,微量主动脉瓣返流、中度二尖瓣返流,中度肺动脉高压伴中度三尖瓣返流;头颅MRI示(图2)两侧小脑齿状核、苍白球见不规则异常信号,但T1WI、T2WI及 FLAIR序列基本未显示CT所见的钙化灶。入院后给予复合维生素B片口服,每天3次,1粒/次,甲钴胺针0.5 mg 静脉注射,每天1次,氟桂利嗪胶囊(西比灵)10 mg睡前口服,胞磷胆碱750 mg静脉滴注,活血化瘀药疏血通针6 ml静脉滴注,每天1次,另外积极治疗高血压等其他疾病。治疗2周后,患者病情逐渐趋于好转、稳定,神经系统异常体征基本消失后出院。出院后一直使用复合维生素B片及甲钴胺维持治疗。3年后随访示患者病情恢复良好,无肢体无力、麻木等发作,无精神、行为异常,查体示认知功能正常,无幻觉,无颅神经功能异常,右下肢轻瘫实验阳性,余四肢肌力及四肢肌张力无异常,无感觉异常,无共济失调等,日常生活评定量表(ADL)评分满分(100分)。
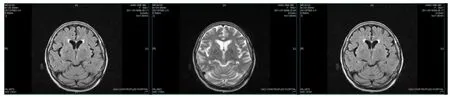
图2 患者头颅MRI
2 讨论及文献复习
Fahr病,又称自发性基底节钙化,最早由Karl在1930年报道,是指散发或家族性的自发性基底神经节钙化,可导致多种神经、精神异常;也可继发于其他疾病。沉积物常集中于壳核、尾状核、内囊、齿状核、丘脑、小脑以及大脑白质,其中基底节区及齿状核受累最常见。本病的症状表现常为非特异性,以神经心理改变及运动障碍为主。神经心理改变主要有:认知损害、抑郁、幻觉、妄想、躁狂、焦虑、精神分裂样精神病及人格改变等。其他临床症状包括:帕金森样症状、共济失调、头痛、痫性发作、眩晕、卒中样症状、体位性低血压、震颤、吞咽困难、构音障碍及轻瘫等。但最常见的首发表现为锥体外系症状。本病常发病于40~60岁之间,儿童起病者亦有少量报道。本例患者为66岁女性,首发症状为偏侧肢体活动障碍,并伴有麻木感,符合卒中样症状的表现,与上述文献报道相符。
尽管相对较为少见,Fahr病有家族性发病的报道[1]。家族性及散发病均以染色体显性遗传为主[2],故遗传因素在本病的发病中占有举足轻重的作用。而且,本病也有继发于小儿麻痹症后期综合征的报道[3];亦可伴发假性甲状旁腺功能减退症[4]及甲状旁腺功能亢进[5],这些疾病均可导致钙磷代谢异常;还有报道M蛋白血症可导致本病[6],而M蛋白血症常为多发性骨髓瘤、巨球蛋白血症等疾病的表现,这些疾病也常存在钙磷代谢的异常。另外,低钙血症可加重本病,并使本病所引起的癫痫对抗癫痫药物不敏感[7]。以上证据表明,本病与钙磷代谢异常关系密切,低钙、高磷可诱导、加重本病,但其具体作用机制仍不明。Sava等[8]报道1例合并慢性淋巴细胞性甲状腺炎的病例,患者死亡后尸检病理改变包括微血管壁钙化、颅内受累区域的小血管及中等血管钙化、慢性淋巴细胞性甲状腺炎改变及纤维脂肪组织取代甲状旁腺组织。另外,Sbai等[9]报道了本病继发于细菌性脑膜炎,Fahr病的上述病理变化及其继发细菌感染的特点提示本病还可能与感染性及非感染性炎症反应,特别是淋巴细胞介导的慢性炎症反应有关。
如前所述,Fahr病的表现为非特异性,最常见的表现为锥体外系症状,如步态异常[4]、小脑性共济失调[10]等;还有癫痫发作、困倦、失语[6]等表现;本病还可表现为行为异常[11]、短暂性意识丧失[12]甚至引起猝死[13];本病也可引起精神损害,如神经性厌食[14]、视幻觉、被害妄想[15]等;另外,Markesber[16]报道了与肌无力、身材矮小症、神经性耳聋轻度周围神经损伤及神经源性膀胱合并存在的Fahr病,其母存在小柳原田综合征,提示本病也可能是遗传性疾病的一系列表现之一。
1971年,Moskowitz等[17]制定本病的诊断标准:①影像上有对称性双侧基底节钙化;②无假性甲状旁腺功能减退现象;③血清钙、磷均正常;④肾小管对甲状旁腺激素反应功能正常;⑤无感染、中毒代谢等原因。本例患者根据其临床表现及辅助检查结果,符合上述标准。如前所述,本例患者无相关家族史,故考虑为散发病例。
本病目前缺乏有效的根治方法,主要为对症、支持治疗。如改善脑供血、营养神经等,癫痫发作给予抗癫痫治疗等。Casamassima等[18]报道了1例电休克治疗Fahr病引起的双相精神障碍,取得可观的疗效,但本治疗方法缺乏大样本研究,其疗效及不良反应尚需更多的研究证实。青霉胺等螯合物与抗氧化剂、钙拮抗剂(如氟桂利嗪)等联用可能改善症状,本例患者使用氟桂利嗪后效果良好,但同样缺乏大样本、多中心的研究资料证实。
值得一提的是,目前诊断本病首选方法为头颅CT检查,其表现为双侧基本对称的钙化斑,较为典型。而在MRI上由于钙化常表现为等信号或稍低、稍高信号,小的病灶更是不易察觉,故对本病的诊断存在缺陷[19]。而且,诊断本病须排除内分泌及代谢性疾病[9]等所致的继发性发病。
[1] Kotan D, Aygul R. Familial Fahr disease in a Turkish family[J]. South Med J, 2009, 102(1): 85-86.
[2] Mufaddel AA, Al-Hassani GA. Familial idiopathic basal ganglia calcification (Fahr’s disease) [J]. Neurosciences,2014, 19(3): 171-177.
[3] Oliveira MF, Oliveira JR. A comorbid case of familial Idiopathic Basal Ganglia Calcification (“Fahr’s Disease”)associated with post-polio syndrome[J]. J Neuropsychiatry Clin Neurosci, 2012, 24(2): E14-E15.
[4] Ferroir JP, Haymann JP, Giannesini C, et al. Epilepsia and Fahr syndrome revealing pseudohypoparathyroidism[J]. Rev Neurol , 2014, 170(1): 51-53.
[5] Rharrabti S, Darouich I, Benbrahim M, et al. A confusional syndrome revealing a Fahr syndrome with hyperparathyroidism[J]. Pan Afr Med J, 2013, 29(14): 123.
[6] Hategan A, Parthasarathi U, Losier B, et al. Fahrtype calcification and neuropsychiatric symptoms with M-proteinemia[J]. J Neuropsychiatry Clin Neurosci, 2011,23(4): E9-E10.
[7] Hmami F, Chaouki S, Benmiloud S, et al. Seizures revealing phosphocalcic metabolism abnormalities[J]. Rev Neurol,2014, 170(6-7): 440-444.
[8] Sava A, Dumitrescu G, Haba D, et al. The Fahr syndrome and the chronic lymphocytic thyroiditis[J]. Rom J Morphol Embryol, 2013, 54(1): 195-200.
[9] Sbai H, Smail L, Hamdani S, et al. Fahr syndrome discovered following a bacterial meningitis[J]. Rev Med Interne, 2008,29(5): 412-414.
[10] Rafik R, Hachimi M, Ouarssani A, et al. Cerebellar ataxia:A rare revelation of Fahr syndrome[J]. Arch Pediatr, 2012,19(11): 1258-1259.
[11] Hoque MA, Siddiqui MR, Arafat Y, et al. Fahr’s disease: a very rare cause of epilepsy[J]. Mymensingh Med J, 2010,19(1): 127-129.
[12] Simone O, Tortorella C, Antonaci G, et al. An unusual case of transient loss of consciousness: the Fahr’s syndrome[J].Recenti Prog Med, 2008, 99(2): 93-96.
[13] Unkrig S, Gullotta F, Madea B. Morbus Fahr--considerations on a case of sudden death[J]. Forensic Sci Int, 2011, 204(1-3):e12-e15.
[14] Jager CM, Hoekstra M, Nijsten MW, et al. Metabolic and neurologic sequelae in a patient with long-standing anorexia nervosa who presented with septic shock and deep hypoglycemia[J]. Int J Eat Disord, 2011, 44(8): 756-759.
[15] Shirahama M, Akiyoshi J, Ishitobi Y, et al. A young woman with visual hallucinations, delusions of persecution and a history of performing arson with possible three-generation Fahr disease[J]. Acta Psychiatr Scand, 2010, 121(1): 75-77.
[16] Markesbery WR. Lactic acidemia, mitochondrial myopathy,and basal ganglia calcification[J]. Neurology, 1979, 29(7):1057-1060.
[17] Moskowitz MA, Winickoff RN, Heinz ER. Familial calcification of the basal ganglions: a metabolic and genetic study[J]. N Engl J Med, 1971, 285(2): 72-77.
[18] Casamassima F, Lattanzi L, Perlis RH, et al. Efficacy of electroconvulsive therapy in Fahr disease associated with bipolar psychotic disorder: a case report[J]. J ECT, 2009,25(3): 213-215.
[19] Kozic D, Todorovic-Djilas L, Semnic R, et al. MR imaging -an unreliable and potentially misleading diagnostic modality in patients with intracerebral calcium depositions. Case report[J]. Neuro Endocrinol Lett, 2009, 30(5): 553-557.
