氨基磺酸催化合成丙烯酸苄酯工艺优化及动力学研究
2015-02-27李学坤李稳宏潘柳依邓寒霜
李学坤,李稳宏,常 远,潘柳依,邓寒霜
(1.西北大学 化工学院, 陕西 西安 710069;2.西安文理学院 化学与化学工程学院, 陕西 西安 710065)
·化学与化学工程·
氨基磺酸催化合成丙烯酸苄酯工艺优化及动力学研究
李学坤1,2,李稳宏1,常 远1,潘柳依1,邓寒霜1
(1.西北大学 化工学院, 陕西 西安 710069;2.西安文理学院 化学与化学工程学院, 陕西 西安 710065)
优化丙烯酸苄酯合成工艺并建立其合成反应动力学。采用氨基磺酸为催化剂、甲苯为携水剂、对苯二酚为阻聚剂,应用响应面法对合成工艺条件进行优化,并对产品表征分析。优化结果为:催化剂用量为反应物总质量的2.74%,酸醇物质的量比1.37∶1,反应时间2.63h。丙烯酸苄酯最高收率可达到88.4%;该条件下反应属于二级不可逆反应,反应活化能为40.4kJ/mol,指前因子为3.418×103L/(mol·min)。该工艺研究预测结果与实验数值吻合,具有催化剂可重复利用,后处理操作简便、收率高,废水产生量少的特点,易于工业化生产。
氨基磺酸;催化剂;酯化;丙烯酸苄酯;响应面法;动力学
丙烯酸酯类化合物用途广泛,可以被用来合成许多有机化工产品、香料产品、合成树脂以及UV光固化材料的稀释单体,应用于油墨、涂料、黏合剂等新领域。传统丙烯酸酯的合成,采用浓硫酸等液体强酸作为催化剂,存在设备腐蚀严重、废水污染、催化剂难以回收利用、产物色泽差等问题[1]。近几年,该类反应催化剂研究不断发展,在强酸性离子交换树脂、杂多酸和固体超强酸等方面取得了很多成果,但由于催化剂制备工艺复杂,造成成本偏高,使其应用受到一定的限制[2]。氨基磺酸为价廉易得、性质稳定的有机酸,易溶于水和强极性溶剂,低温下不溶于低极性或非极性溶剂。以其为催化剂,反应结束后只需简单过滤洗涤即可再生回收利用,因此被作为一种绿色催化剂广泛应用于酯化与酯交换、羟基与羰基的保护、Beckmann重排及环醚开环等多种类型有机合成反应中[3-4]。丙烯酸苄酯又称丙烯酸苯甲醇酯,是丙烯酸酯中一类重要的化合物。熊英莹等采NaHSO4·H2O为催化剂进行了丙烯酸苄酯合成反应[5],收率良好;侯学振、王丹菊等采用对甲苯磺酸为催化剂研究了丙烯酸苄酯的合成工艺[6-7],最佳收率分别为83%和88%。上述工艺研究均未考虑催化剂的回收和利用,在一定程度上存在生产费用较高、后处理废水量大等问题。本文以氨基磺酸为催化剂,以丙烯酸和苯甲醇为原料、甲苯为携水剂、对苯二酚为阻聚剂进行了绿色酯化反应,并对合成工艺过程进行了优化,同时对氨基磺酸催化反应的动力学进行了研究,以期为工业生产提供技术支持。
1 实 验
1.1 试剂及仪器
苯甲醇,丙烯酸,对苯二酚,甲苯,氨基磺酸,分析纯,阿拉丁试剂(上海)有限公司。
DF-101S集热式磁力搅拌器,水浴控温精度为±0.5℃,上海百申仪器设备有限公司;WLB-21精密水银温度计,分度值0.1℃,量程100~150℃,常州盛之源仪器仪表有限公司;D8型红外光谱仪,NICOLET公司;气相色谱GC-2060,上海瑞敏仪器有限公司。
1.2 实验方法
1.2.1 合成过程 丙烯酸苄酯合成路线如下。
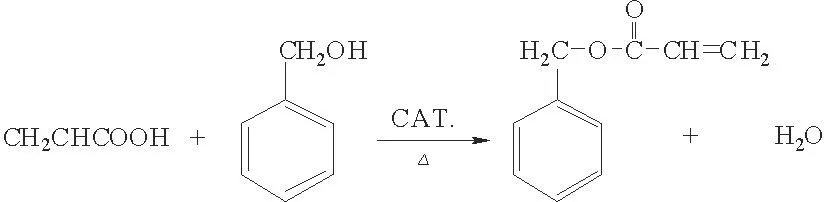
在250mL三口烧瓶中加入21.6 g新蒸丙烯酸,27.04g苯甲醇,加入0.486g氨基磺酸(占酸醇总质量的1%,下同),阻聚剂对苯二酚0.243 2g(占酸醇总质量0.5%),携水剂甲苯23mL(占酸醇总质量的40%),加热回流反应。待分水器中水层体积不再增加停止反应,降温至室温。氨基磺酸固态沉析出,回收催化剂重复利用。反应液进行减压蒸馏,回收未反应的丙烯酸,收集98~110℃/3.3kPa下馏分。再经碳酸钠溶液和饱和食盐水进行洗涤,无水硫酸钠干燥后得到产品。由实际产量和理论产量计算收率,进行产品折光率及红外图谱检测分析。
1.2.2 分析方法 根据国标GB/T 17530.4-1998《工业丙烯酸酯酸度的测定》方法来测定样品酸值。采用GC 2060气相色谱仪分析,氢火焰离子化检测器FID,载气高纯氮气,OV-17型毛细管柱(30m×0.53mm×1.0μm),检测器温度350℃,气化室温度350℃。升温程序:70℃(2min)→110℃(0min)→260℃(2min),一阶升温速度10℃/min,二阶升温速度30℃/min。采用面积归一法对苯甲醇进行含量分析;产品溴化钾压片法进行IR测定,光谱扫描范围为500cm-1~3 400cm-1,分辨率为0.2cm-1,信噪比为35 000∶1,波数精度为0.01cm-1,吸收精度为0.1%T。
2 结果与讨论
2.1 丙烯酸苄酯合成工艺优化
实验中加入了大量携水剂甲苯(占酸醇总质量的40%),甲苯与水汽化共沸,导致实际反应体系温度会随时间在118~125℃小范围内出现波动,较难准确控制。因此,实际反应中设定油浴加热温度维持恒定在130℃不变。在大量预实验基础上,选择对丙烯酸苄酯合成影响较显著的3个因素,即催化剂用量、酸醇物质的量比和反应时间进行响应面优化实验,设计了3因素3水平响应面优化实验,见表1。
响应面中心组合实验结果见表2,方差分析见表3。
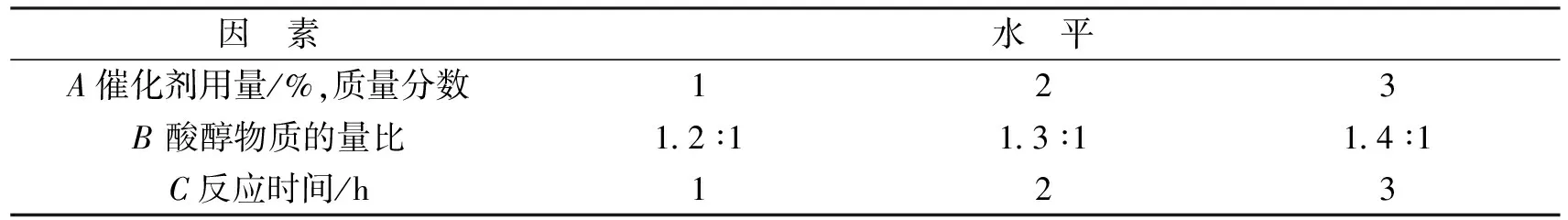
表1 丙烯酸苄酯合成因素水平表Tab.1 Levels and factors of catalyst
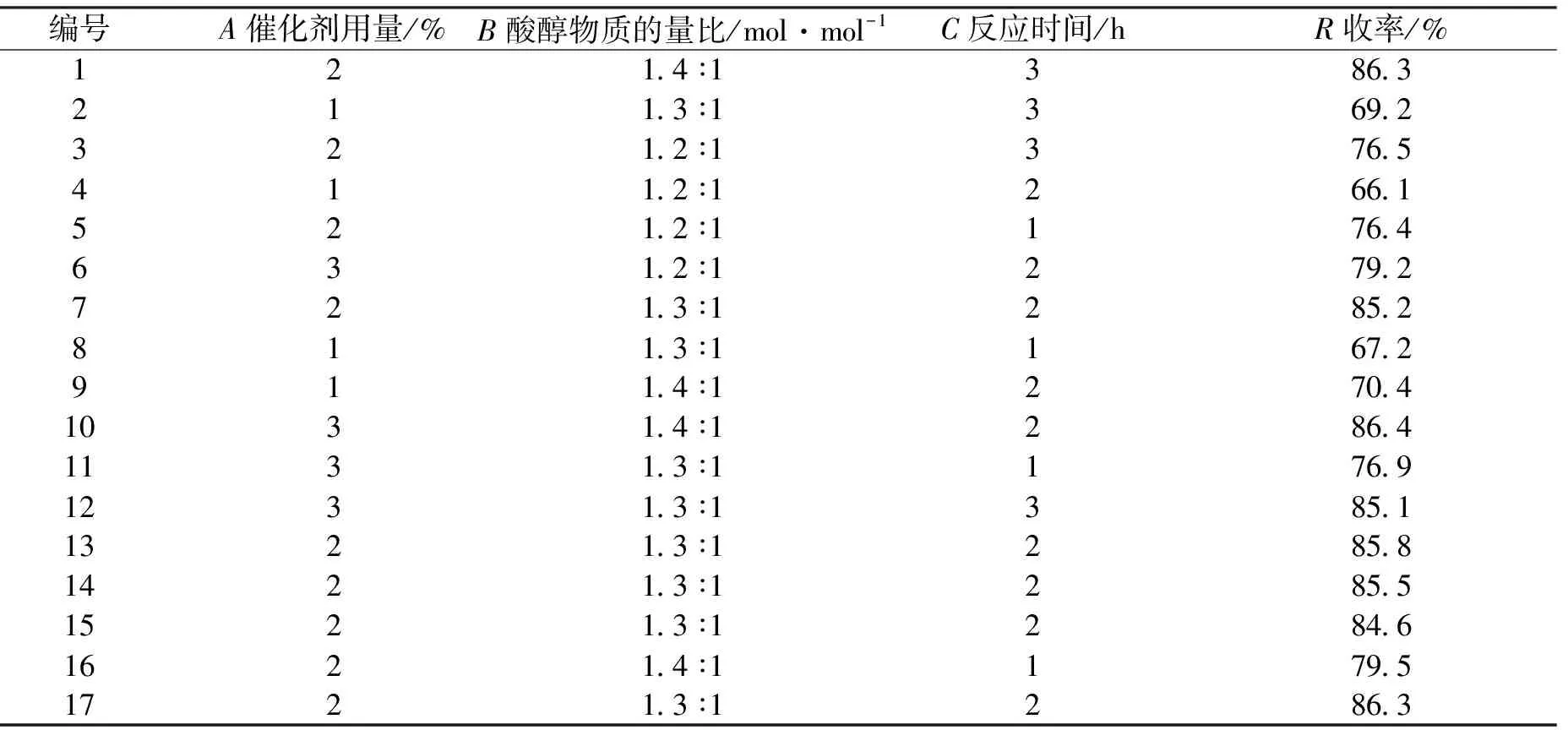
表2 响应面试验结果Tab.2 The scheme and the results of response surface method experimental design
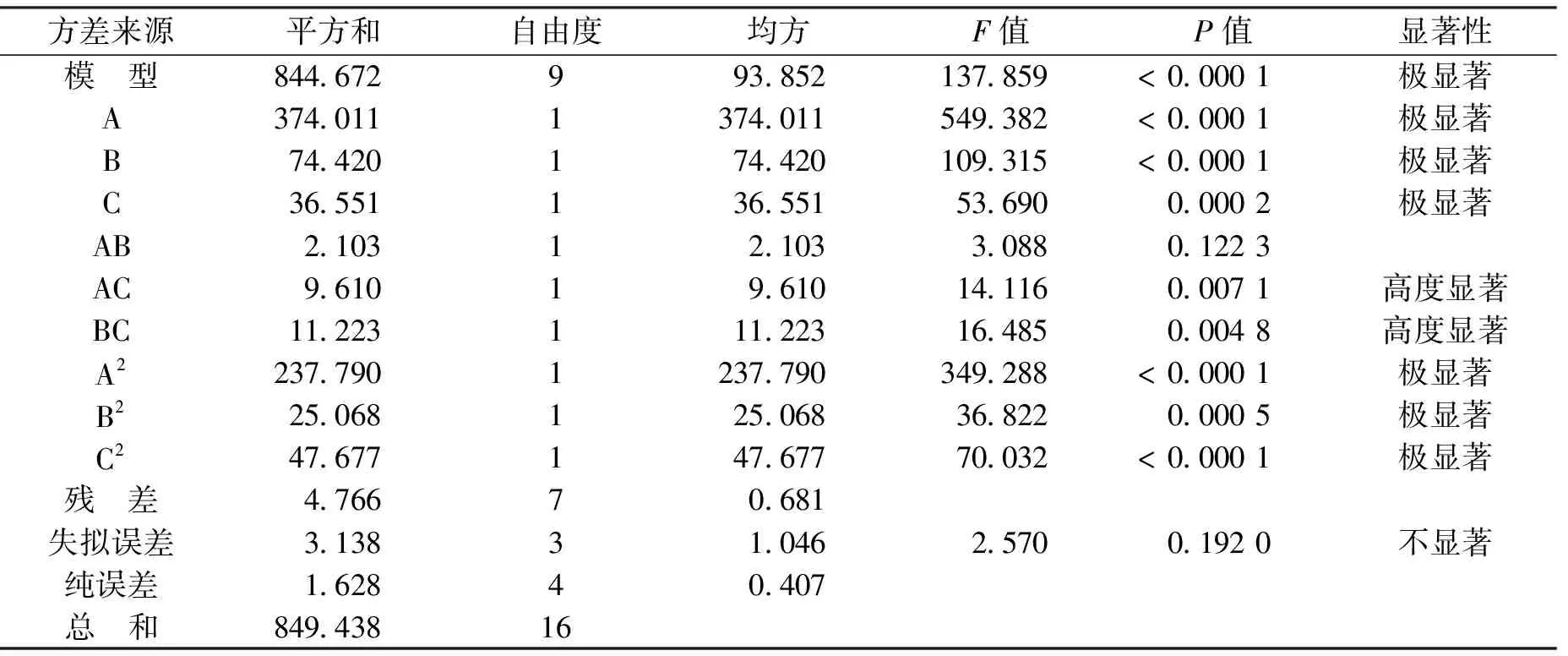
表3 响应面实验方差分析表Tab.3 Analysis of variance by response surface method experimental design
由表3可知,丙烯酸苄酯反应模型的F值=137.89>F0. 01(9,7)=6.71,显著性水平P值<0.000 1,说明该模型是极显著的,即用该模型来分析各因素对丙烯酸苄酯收化率的影响是合理的。失拟项F=2.56
对二次回归方程的响应面分析结果见图1。
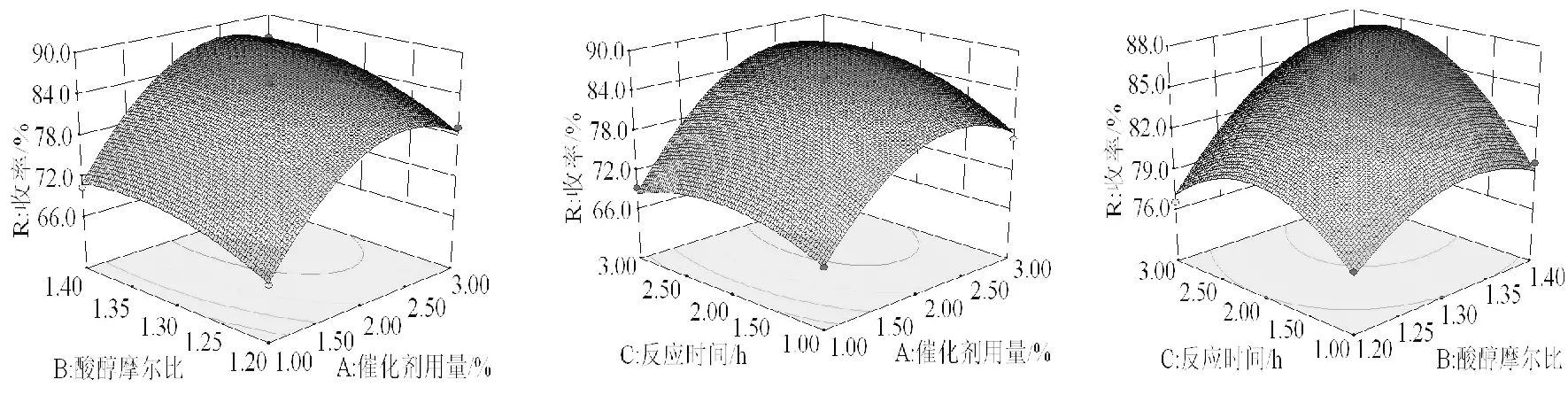
图1 因素催化剂用量、酸醇物质的量比和反应时间对丙烯酸苄酯合成收率影响的响应曲面图Fig.1 Response surface plots for the synthesis conditions (the amount of catalyst, the ratio of acid to alcohol and reaction time) on the esterification rate of the benzyl acrylate
由图1可看出,催化剂用量影响最为显著,表现为收率随其变化明显,曲面陡峭。收率因素影响大小依次为:催化剂用量、酸醇物质的量比和反应时间,与表3中结果一致。对比图1和表2数据,催化剂用量较少时,反应体系中催化酸活性中心少,反应速度较低;当催化剂增加后,由于活性中心的增加而加快反应速率,氨基磺酸在110~130℃反应体系中有一定的溶解度;当催化剂增大到一定程度后由于部分氨基磺酸成固态存在于瓶底,未形成均相催化体系反而对催化效率无明显影响。从经济角度出发,存在一个最优的催化剂浓度。酸醇比增大,有利于提高苯甲醇的转化率,提高产品的收率。但是,丙烯酸用量的增加到一定程度后,由于丙烯酸在高温自聚形成低聚物,增加了反应体系的黏度,导致产品颜色加深,丙烯酸损耗增大,加大了后处理的难度。因此,产品收率反而有所降低。在响应曲面表现为,收率随酸醇比先增大后降低趋势;随着反应时间的增加,丙烯酸和苯甲醇的转化率增加,产品收率增大;当时间增加到一定程度后,由于丙烯酸自聚等副反应发生,收率降低,同样在响应曲面上表现为收率随时间的延长先增加后降低的趋势。
经软件对各因素回归拟合后,得到回归方程:
R=85.48+6.84A+3.05B+2.14C+0.72AB+1.55AC+1.68BC-7.52A2-2.44B2-3.36C2。
根据所得到的模型,可预测在稳定状态下的最大收率为88.4%,优化条件为:催化剂用量2.74%、酸醇物质的量比1.37∶1和反应时间2.63h。采用上述优化条件进行丙烯酸苄酯的合成,共进行了3次平行实验,收率分别为87.1%,88.4%和87.6%,平均收率为87.7%,与预测值接近,且均高于探索实验。
2.2 催化剂重复使用性能实验
为验证催化剂氨基磺酸的重复利用性能,在优化反应条件下,将过滤催化剂用甲苯洗涤后,进行重复性实验,结果见表4。

表4 催化剂重复性实验Tab.4 Repeatability experiments of catalyst
由表4可知,该催化剂多次重复使用后产品收率有所下降,9次重复实验后,丙烯酸苄酯收率仍高达83.4 %,表明催化剂重复利用性良好。活性降低,可能是由于催化剂与反应液分离时损失或残余少量产品覆盖催化剂部分活性中心,使得催化剂与反应物的接触面积减少,降低了其催化活性。
2.3 丙烯酸苄酯检测分析
产品经过纯化后,用阿贝折射仪、IR及气相色谱对其折光率、结构和含量进行分析,由阿贝折射仪测得产品在25℃下折光率为1.518 6,与文献值1.518 0接近[7]。采用GC 2060型气相色谱进行定量分析,丙烯酸苄酯停留时间为8.2min左右,由面积归一法测得其含量为98.73%,达到了工业产品要求。采用溴化钾薄膜压片法测得丙烯酸苄酯的IR谱图见图2。
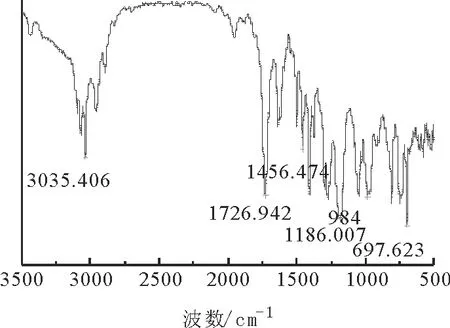
图2 丙烯酸苄酯的IR测定Fig.2 IR figure of benzyl acrylate
由图2可知,产物在3 035cm-1出现明显特征峰,该峰为芳香烃和烯烃CHCH的伸缩振动特征峰。1 726 cm-1特征峰为CO伸缩振动特征峰。1 186 cm-1为化合物红外指纹区特征峰,该峰为C—O—C弯曲振动峰,为酯类化合物的特征峰,在1 456 cm-1处及附近、697 cm-1处及附近都有明显吸收峰,该类峰为苯环的特征吸收峰,同时通过对比萨特勒(Sadtler)红外光谱库证明合成产物为丙烯酸苄酯。
2.4 反应动力学
由于在实验条件下,携水剂甲苯将反应生成的水及时分离出去,有效抑制了逆反应的进行,假设带出反应器水的体积与反应系统总体积相比可以忽略,即认为该反应为恒容不可逆反应,根据幂函数型动力学关系[8]有:
(1)
式(1)中:-dCA/dt为丙烯酸消耗速率;CA,CB分
别为丙烯酸和苯甲醇在t时刻的浓度。假定反应级数α=β=1,并定义丙烯酸和苯甲醇初始浓度CA0和CB0,n为醇酸物质的量比,XA为丙烯酸的转化率,将式(1)积分并整理得:
(2)
式(2)中:C为积分余项。令积分式(2)左侧为积分值I,在醇酸物质的量比1∶1.3条件下,测得温度分别在383.15K,393.15K和403.15K下不同时刻的丙烯酸转化率数据,将其带入式(2)中,以积分值I对时间t作图。如果线性相关性较好,说明假设反应级数正确,否则重新假定反应级数。实验中不断调整油浴加热温度,控制实际反应在规定温度下,测得转化率XA及计算积分值I见表5,拟合线性关系见图3。
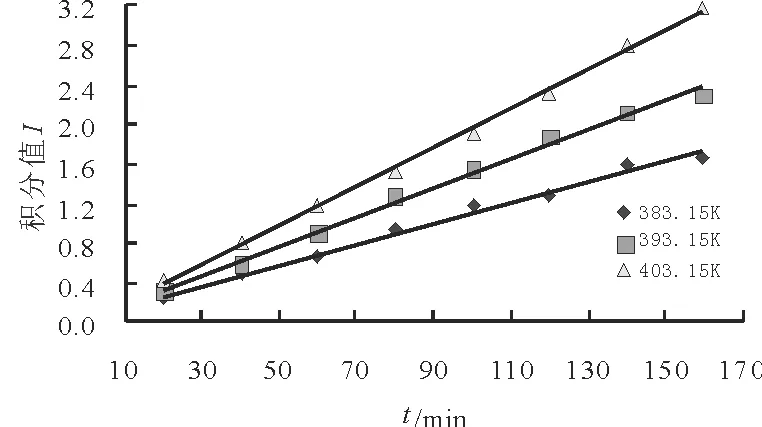
图3 不同温度下积分值I与时间t拟合关系图Fig.3 The fitting curve of I and t at different temperature
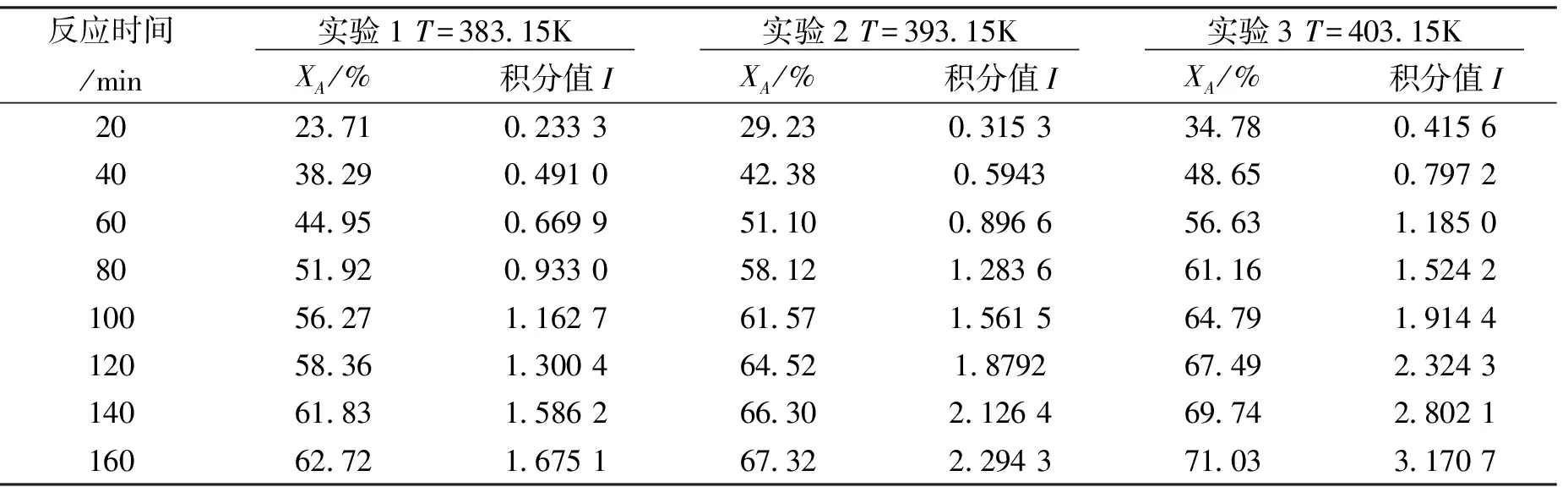
表5 各个反应温度下不同时间的转化率XA及积分值ITab.5 Experimental results of conversion at different temperature and time
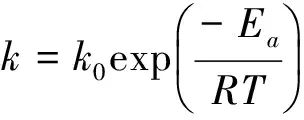
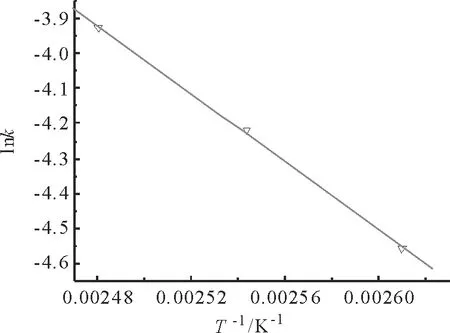
图4 速度常数与反应温度的拟合关系图Fig.4 The relationship of reaction rate constant and temperature
可以得出,拟合方程为lnk=-4 861.7T-1+8.136 8,相关系数R为0.998,线性关系良好。由求Arrhenius关系式求得反应活化能Ea为40.4kJ/mol,指前因子k0为3.418×103L/(mol·min)。该反应活化能较高,温度对反应速度的有一定程度的影响,考察的温度范围内反应适于在较高温度下进行,属于动力学控制过程。然而,较高的反应温度会引起丙烯酸自身及合成产品的聚合,导致副反应增加和能耗增加。因此,需要从产品收率和能耗角度综合考虑选择合理温度。
为了验证求得的动力学模型的可靠性,在响应面优化最佳工艺条件下进行实验。严格控制实际反应温度为125℃,反应每隔一段时间取样求丙烯酸的转化率,并将其与上述所得该酯化反应的动力学方程计算得到的转化率数值进行比较。计算相对误差R,所得结果见表6。
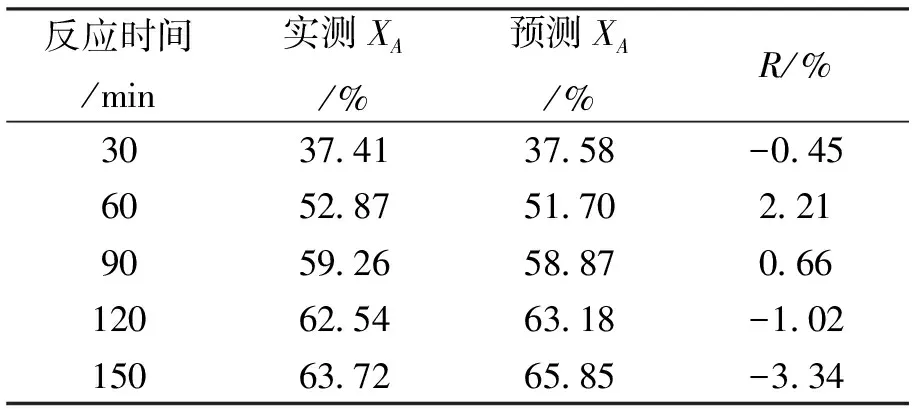
表6 398.15K时动力学模型计算所得转化率与实际测得的转化率比较Tab.6 Comparison of the kinetics model calculated and the actual measured conversion rate at 398.15K
可以得出,由动力学模型计算所得转化率与实际测得的转化率之间的相对误差绝对值小于3.4%。这说明预测值与实际值相差不大,求得的动力学模型预测的结果与实验真实结果能够很好地吻合。
3 结 论
1)得到了氨基磺酸催化合成丙烯酸苄酯的工艺路线,应用响应面法优化了合成条件:催化剂用量为反应物总质量的2.74%,酸醇物质的量比1.37∶1,反应时间2.63h,甲苯加入量40%(质量分数),对苯二酚加入量为反应物总质量0.5%(质量分数),反应温度在118~125℃。粗产品经减压经蒸馏回收甲苯、丙烯酸,再经碳酸氢钠、氯化钠洗涤和无水硫酸钠干燥得到产品,丙烯酸苄酯最高收率可达到88.4%。
2)建立了110~130℃间丙烯酸苄酯合成动力学模型,该反应属于不可逆二级反应,活化能为40.4kJ/mol,指前因子为3.418×103L/(mol·min),预测值与实际检测结果吻合度良好。
3)该工艺路线与文献报道的路线相比,催化剂氨基磺酸可回收重复使用,降低了废水产生量,工艺操作简便,易于工业化生产。
[1] JAKUBOWSKI W, JUHARI A,BEST A, et al. Comparison of thermomechanical properties of statistical,gradient and block copolymers of isobornyl acrylate and n-butyl acrylate with various acrylate homopolymers[J]. Polymer,2008,49(6):1567-1578.
[2] 黄庆华,陈明,白雄雄,等. 氨基磺酸/浓硫酸协同催化合成羧酸乙酯[J].化学研究与应用,2014,26(2):277-280.
[3] WANG Bo. Sulfamic Acid: A very useful catalyst [J]. Synlett, 2005,8:1342-1343.
[4] 卢跃东, 夏敏. 氨基磺酸催化剂在有机合成中的应用[J].合成化学,2007,15(2):123-130.
[5] 熊英莹. 丙烯酸酯合成工艺研究[J].山西化工,2007,27(2):22-23.
[6] 侯学振.几种丙烯酸酯的合成及其对假酱油中胱氨酸的检测研究[D].长沙:中南大学,2012.
[7] 王丹菊. 丙烯酸苯甲醇酯合成条件的研究[J].广州化工,2009,37(2):145-146.
[8] 刘勇,杨浩,陈蔚萍,等. 强酸性阳离子交换树脂催化合成乙酸异辛酯动力学[J].石油化工,2013,42(6):620-623.
(编 辑陈镱文)
Process optimization and reaction kinetics study of benzyl acrylate catalyzed by sulfamic acid
LI Xue-kun1,2, LI Wen-hong1, CHANG Yuan1, PAN Liu-yi1, DENG Han-shuang1
(1.School of Chemical Engineering, Northwest University, Xi′an 710069, China; 2.School of Chemistry & Chemical Engineering, Xi′an University of Arts and Sciences, Xi′an 710065, China)
The process for synthesis of benzyl acrylate and its reaction kinetics was optimized and discussed. The benzyl acrylate was synthesized taking sulfamic acid as catalyst, methylbenzene as water-carrying agent and hydroquinone as polymerization inhibitor. The factors, such as the amount of catalyst, the molar ratio of acid to alcohol and reaction time, were optimized by the response surface method (RSM). The product was characterized by infrared spectroscopy and refraction analysis method. The optimal synthesis conditions of benzyl acrylate were as follows: catalyst concentration 2.74% (w, relative to the total mass of reactants), n(acrylic acid):n(benzyl alcohol)1.37∶1 and reaction time 2.63h. The yield of benzyl acrylate could be up to 88.4%. The reaction can be considered as a second-order irreversible reaction with activation energy 40.4kJ/mol and pre-exponential factors 3.418×103L/(mol·min). The experiment result shows an acceptable agreement with the predicted result. The process with catalyst repeatedly used, easy to operate, high yield and less waste water can be applied to industrial production.
sulfamic acid; catalyst;esterification; benzyl acrylate; response surface method; kinetics
2014-04-18
陕西省科技统筹创新工程计划基金资助项目(2011KTCL01-15);2012年度陕西省工程中心科研基金资助项目(2011ZDGC-XX)
李学坤,男,山东德州人,博士生,从事基础化工工艺及相关研究。
李稳宏,男,陕西西安人,西北大学博士生导师,从事有机化工及天然产物分离纯化研究。
TQ351.4,TQ013.2
:ADOI:10.16152/j.cnki.xdxbzr.2015-03-016
