塑料电镀中的敏化活化一步法
2015-02-18孙永泰
孙永泰
(辽宁省辽中县水利化工设备厂,辽宁辽中,110200)
塑料电镀中的敏化活化一步法
孙永泰
(辽宁省辽中县水利化工设备厂,辽宁辽中,110200)
通过生产实践,对塑料电镀工艺的敏化、活化分步法改为一步法,从而缩短了工艺流程,提高了一次成品合格率,取得了一定经济效益。
塑料电镀、敏化、活化、工艺流程
1 概述
塑料电镀技术在近30多年已发展成为一种极有价值的技术,由于镀层与基体的结合力好,抗蚀性能比以钢铁为基体的镀层强,并且耐热、耐磨性能也能满足设计要求,因此,应用越来越广。选择符合标准的塑料材料(目前电镀所用的大多是电镀型ABS塑料),按照规定的注塑方法加工成型,然后再依次分别进行机械粗化、化学粗化、敏化、活化、化学镀铜或化学镀镍、电镀厚铜、电镀光亮铜、电镀光亮镍、电镀装饰铬。这是塑料电镀自1 9 6 2年投入工业化生产以来,一直普遍采用的工艺方法。这一方法虽然比较“成熟”,但质量欠佳,一次合格率严重受到加工过程,尤其是敏化、活化工序操作技术的影响。敏化、活化的目的,是为了使制品表面形成一层均匀的、连续的、有贵金属构成的催化“中心”,这种呈胶状微粒的贵金属;在化学镀铜或化学镀镍时具有“诱导”作用。但是在生产过程中很难保证这层催化中心的均匀性和连续性,因而极易形成化学镀层的缺陷。我们在参阅了有关资料后,将敏化、活化合并成一步进行,从而提高了产品的一次合格率。在工件进行化学粗化、清洗后,其主要工艺过程如下: 浸胶体钯溶液→解胶→化学镀铜或化学镀镍→电镀光亮铜→电镀光亮镍→电镀装饰铬。
2、电镀工艺
2.1 化学粗化
2.2 粗化液的配方:
组成:
硫酸 (d = l.84) 600ml ;
铬酐 CrO320g ;
水 400 m1
工艺条件:
温度 (℃) 70~75;
时间,(min) 3~7
以上组分皆为l L溶液中的含量。
2.3 粗化液的配制:首先将计算量铬酐溶于少量水中,在不断搅拌下缓慢加入计算量硫酸,然后用水释至规定体积,冷却到工艺范围后即可。不要把铬酐倒入硫酸中,因为这样溶解难以进行。此外,对粗化液的成分含量要注意调整。
3 浸胶体钯溶液
3.1 胶体钯敏化活化机理:胶体钯的胶团是双层结构。把塑料件浸入胶体钯敏化活化液中时,制品表面首先吸附Sn2+,被吸附的Sn2+再吸附Cl-,形成{n S n2+·2(n-x)C 1-}吸附层,在这个吸附层外,又形成2xC1-层,成为扩散层,其形式如下:
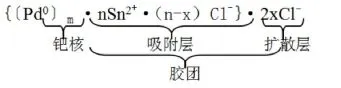
m、n、x与Sn2+/Pd2+(为Sn2+个数与Pd2-个数之比)及HCl的含量有关。
在盐酸水溶液中,当Sn2+/Pd2+<2时,先生成[Pd Sn2]6+,即:Pd2++2 Sn2+→[PdSn2]6+
这是第一中间产物。其内部发生氧化还原反应而生成Pd0,即: [Pd Sn2]6+→pdo+Sn4++Sn2+
当Sn2+/Pd2+>2时,因有过量的Sn2+存在,故可生成更稳定的[PdSn]14+,即:
[PdSn2]6++4 Sn2+→[PdSn6]l4+这是第二中间产物。其内部发生氧化还原反应P d0,即: [PdSn6]l4+→Pdo+Sn4++5Sn2+
所以;随着Sn2+/Pd2+的增加,生成物的稳定性便提高了,因此,Sn2+/Pd2+要大于2。但过大时,会使胶团微粒过大,因而降低吸附效果,减少催化中心的数量,以致于影响镀层与基体的结合力。
3.2 胶体钯溶液的配方:
甲液组分:
氯化钯(pbCl2) 1 g ;
氯化亚锡(SnCl2·2H2O) 2.53g
蒸馏水 200ml ;
盐酸 (d=1.14) 100ml
乙液组分:氯化亚锡(SnCl2·2H2O) 75g;
锡酸钠 (Na2SnO3·3H2O) 7g
盐酸 (d=1.14) 200ml
工艺条件:
温度(℃)20左右
时间(min)10~20
3.3 胶体钯配制及配制时反应机理:
3.3.l 胶体钯配制:
(1)甲液配制: 将固体二氯化钯溶于l00ml盐酸和200ml蒸馏水的混合液中,在30±2℃的条件下,加入固体氯化亚锡,并在不断搅拌下反应12min。
(2)乙液配制:将固体氯化亚锡加到200ml盐酸中,搅拌至完全溶解,再加锡酸钠,制成白色乳浊液。
(3)混合:将配制好的乙液在不断搅拌下,慢慢倒入甲液中,稀至1 L, 便得到深褐色的敏化活化液。在40~45℃下保温3h,以提高其活性,并延长其使用寿命。
3.3.2 胶体钯配制的反应机理:在盐酸水溶液中,Pd2+和Sn2+进行反应,其最后有金属钯微粒生成,钯微粒吸附溶液中过量的Sn2+,以胶态形式存在。一般反应可以用下列方程式表示:nSn2+(过量)+Pd2+→Sn4++Pd0[(n-1)Sn2+]
但实际上其反应机理是比较复杂的。有研究认为,整个过程与Sn2+的过量程度、
Sn2+/pd2+、溶液的pH值、配制时的反应条件等多种因素有关。
3.4 .操作过程中应注意的事项:
3.4.1 避免Cr6+的带入。
因Cr6++Sn2+→Sn4++Cr3+,而影响溶液稳定性。
3.4.2 空气中的氧会使Sn2+氧化成Sn4+,而加速溶液的分解,因此在配制和使用溶液时,不要将大量空气带入溶液,以避免Sn2+被氧化。溶液不用时要加盖。
3.4.3 避免水的带入。为此,可将制件在下述的溶液中“预浸”1~3min:
氯化亚锡SnCI2·2H2O 40g/1; 盐酸(d=1.14) HC1 100ml/1
制件预浸后把水尽量滤干,直接进入胶体钯活化液。
3.4.4 发现分层现象时,及时加入1 0~20g/L氯化亚锡溶液,可使分层消失。
3.4.5 敏化活化时温度不要低于1 5℃,否则,活化效果不佳。采用水套加温,避免用蒸汽直接加温。
3.4.6 在采用这种敏化活化工艺后,进行化学镀镍的效果不如化学镀铜的效果好,这种差异随着敏化活化溶液的使用程度而越来越大。所以新配液可先作化学镀镍的活化液,再作化学镀铜活化液使用。
3.4.7 当氯化钯含量小于0.lg/L时会失去敏化活化作用,故应予及时补充。
3.4.8 使用时,要保持Sn2+过量和足够的酸度。为此,可定期添加亚锡盐和盐酸,或添加新配制而尚未稀释的浓溶液。
4 解胶
4.1 解胶原理:
经过胶体钯溶液处理过的塑料件,其表面吸附一层胶体钯的颗粒夕经解胶处理后夕胶体钯外面的锡离子被溶解面去掉,从而将钯裸露出来。这些裸露出来的钯核在化学镀时起催化作用。见图l
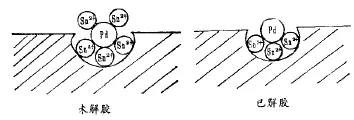
图1 解胶原理图
4.2 配方
组分与工艺条件如下:
盐酸(d =1·1 4) 80~l00ml;
温度(℃) 30~40 ;
时间(rain.) 2.5~5
5 化学镀铜和化学镀镍
5.1 化学镀机理
经过活化后的镀件,表面形成一层催化活性中心,当浸入化学镀液时,这些催化中心成为化学镀的“结晶核”。镀液中的金属离子首先在“结晶核”的周围开始还原成金属,然后逐渐扩大,形成虽然很薄(一般只有0.1~1.5 μm),但是连续的金属薄层为非金属电镀创造了条件。
5.2 化学镀铜:
5.2.1 配方和工艺:
甲液组分:
硫酸铜(CuSO4·5H2O) 14g ;
酒石酸钾钠(NaKC4H4O6) 44.5g
碳酸钠(Na2CO3) 4.2g ;
氢氧化钠(NaOH) 9g ;
一氯化镍(NiC12·6H2O) 4g
乙液组分:甲醛(CHCO36%~40%) 51 ml ;
工艺条件: pH 12.5;
温度 室温 ;
时间(min) 20~30
5.2.2 溶液的配制:
(1)先用适量的水把酒石酸钾钠、氢氧化钠、碳酸钠分别溶解夕必要时可加温到50~60℃,然后混合成一种溶液。再用适量的水分别将硫酸铜、氯化镍溶解夕然后混合成另一种溶液。最后将这两种溶液混合,即得甲液。
(2)使用时往甲液中加入规定量的甲醛并稀释至规定体积即可。(如甲醛混浊或有白色胶状物,系甲醛发生自聚,应过滤)。
5.2.3 影响化学镀铜速度的主要因素及溶液的维护:
(1)溶液中各成分的主要作用
硫酸铜:提供氧化剂Cu2+。酒石酸钾钠:是使铜呈溶解的络合状态而存在,防止Cu2+在碱性介质中产生氢氧化铜的沉淀, 起络合剂的作用,同时还可控制溶液中二价铜离子的浓度,起缓冲剂的作用。氢氧化钠:提供了所需的碱性环境。碳酸钠:保证较快的沉积速度,氢氧化钠消耗后,提供OH-。氯化镍:使镀层细致光滑,又会降低铜的还原速度。
(2).溶液的pH值
提高溶液的pH值,铜的沉积速度加快,同时也加快了氧化亚铜(Cu2O)生成的反应速度(见图2)。
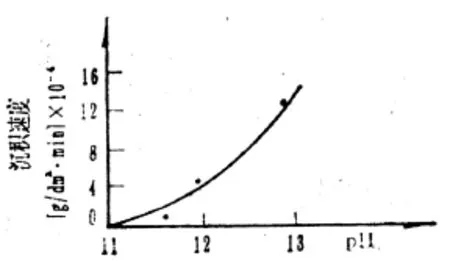
图2 pH值对沉积速度的影响
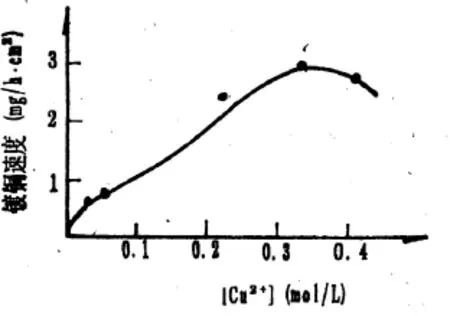
图3 [Cu2+]对化学镀铜速度的影响
当溶液温度升高时,沉铜速度加快,易于生成氧化亚铜。溶液的分解加快,所得的化学镀铜层疏松粗糙、结合力下降。若温度过低,则沉铜速度太慢(见图4),有时有局部沉不上铜的情况。所以温度一般控制在17~30℃。
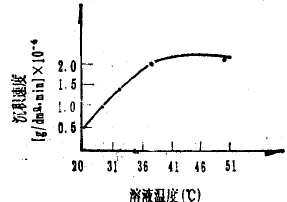
图4 温度对沉积速度的影响
(5)防止金属钯微粒的带入,影响溶液的稳定性。所以在胶体钯活化后,应清洗干净。
(6)搅拌溶液
沉铜过程中应不断搅拌溶液。这有两个好处,其一是使沉铜过程中产生的氧化亚铜微粒有可能重新氧化成二价铜离子,提高了溶液的稳定性,反应为:
2Cu2O+O2+8H+→4Cu2++4H2O
其二是搅拌可以使沉铜过程中产生并附着在塑料件表面的细微氢气泡迅速离开镀件,从而减少镀层起泡的可能性,提高了结合力。
5.3 化学镀镍:
5.3.1 配方和工艺:
组分:
硫酸镍(NiSO4·7H2O) 20g ;
次亚磷酸钠(NaH2PO2·H2O 30 g
柠檬酸钠(Na3C6H4O7·2H2O) 10g ;
氯化铵(NH4C1) 30g
工艺条件:
pH8.5~9.5 ;
温度(℃) 35~45;
时间(m i n) 5~1 0
5.3.2 溶液的配制:
(1)以适量的水分别将硫酸镍、氯化铵、柠檬酸钠溶解,然后混合成一种溶液。(2)用另一容器,以适量的水将次亚磷酸钠溶解,然后将上述两种溶液混合均匀。使用前以浓氨水调整pH值至所需范围(可用广泛pH试纸测量),加水至规定体积。
5.3.3 溶液的维护:
(1)如不用,最好用硫酸(1+1)把p H调整到溶液呈现绿色,以防分解,下次用时,再用氨水调整即可。
(2)与化学镀铜一样,在胶体钯活化后,应清洗干净,以防钯带入溶液中,影响溶液的稳定性。
(3)经常过滤槽液,以免金属或沉淀对溶液稳定性的影响。溶液使用一段时间后,HPO-→HPO2-,
222从而形成NiHPO2沉淀析出,而影响沉积速度。这时可加FeCl3,形成羟基亚磷酸-氢铁的碱式复盐沉淀.{Na2[Fe2(OH)(HPO3)2]·2H2O},过滤除去即可。
(4)溶液温度不可长期维持在50℃以上; 同时酸度不可保持pH为8.5~9.5之间。否则,溶液不稳定。
6 常规电镀
塑料件在化学镀之后即可进行常规电镀。一般原则是:塑料件化学镀之后,电镀酸性光亮铜,再电镀光亮镍, 然后电镀装饰铬或其它金属层。关于常规电镀方法,采用的是下列工艺。
6.1 酸性光亮镀铜:
组分与工艺条件:
硫酸铜(CuSO4·5H2O) 180~2 20g;
硫酸(d=1.8 4) 50~70 g ;
氯离子0.0 1~0.03g ;
K G-1添加剂 3~5 g;
阴极电流密度Dk1~8 A/dm2;
阳极电流密度DA为阴极电流密度的1/3 ;阳极材料 含磷0.1%~0.3%铜板;
阴极移动 18~21次/分;
阳极行程 ≈10cm ;
温度(℃) 8~35;
时间(min) 视需要而定,通常l0min。
6.2 光亮镀镍:
组分和工艺条件:硫酸镍(NiSO4·7H2O) 3 0 0~3 5 0 g ; 氯化钠(N a C l) 1 5~2 0 g;
硼酸(H3BO3) 30~35g;
791光亮剂 5ml;
糖精(C6H4COSO2NH) 0.5~1g;
十二烷基硫酸钠 0.l~0.2g;
温度(℃) 4 5~5 5;
电流密度 2~3A/dm2;
pH 4~5 ;
时间 30min或视需要而定。
6.3. 镀装饰铬:
组分和工艺条件:
铬酐 280~350g;
硫酸 (d=1.8 4)2.8~3.5g;
三价铬离子 3~5g;
温度(℃) 48~55;
阴极电流密度Dk1 5~25A/dm2;时间 3min或视需而定。
7 结论
经过实验,使用如下工艺流程来对ABS塑料进行电镀:ABS塑料制品→消除应力→去油→胶体钯活化→还原或称解胶→化学镀铜或化学镀镍→(闪镀铜或闪镀镍)→酸性光亮镀铜→光亮镀镍→镀装饰铬→烘干或凉干。
实验结果表明,使用胶体钯活化液所得镀件,在光洁度、结合力等方面,不亚于敏化活化分步进行的情况。就经济效益而言,胶体钯活化液与敏化活化分步进行所需溶液相比,稳定性稍好,维护、使用都较方便。尽管一次性投资较大,但从整体角度而言,使用胶体钯溶液更为合算。所需工序大大简化(敏化活化分步进行大约29道工序,使用胶体钯活化液,至少可减少7—8道工序),时间相对缩短,提高了成品的一次合格率。
[1]电镀手册〔M〕.国防工业部出版社(1997.10).
[2]伍学高,塑料电镀技术〔M〕. 四川科技出版社。
[3]赵山泉,塑料电镀的结合力影响因素与工艺改进,新疆工学院学报[J]. 2(1 0),4 5(1 9 9 9)。
[4] 严钦元、方景礼,塑料电镀[J].重庆出版社(1997.7)。
[5]曾华梁、吴仲达等,电镀工艺手册 [M]. 机械工业出版社(1996.4)。
[6]孙大粱、张玉华等译,镀镍和镀铬新技术,[M].科学文献出版社(1992.6)。
In plastic galvanization sensitization activation one-stage process
Sun Yongtai
( Liaoning Province Liaozhong County water conservation chemical industry plantl Liaoning Liaozhong 110200)
through the production practice, to the plastic galvanization craft's sensitization, the activation method of fractional steps changes the one-stage process, thus reduced the technical process, raised an end product qualified rate, has obtained the certainly economic efficiency.
plastic galvanization Sensitization activation Technical process
孙永泰(1972~),男,满族,毕业于沈阳化工学院化工系工艺专业,高级工程师。
