肾癌术后肾上腺孤立转移灶的外科治疗方式比较:18例经验报告
2015-02-13刘佳虞巍杜鹏何群金杰周利群韩文科杨勇
刘佳,虞巍,杜鹏,何群,金杰,周利群,韩文科,杨勇
(1.北京大学肿瘤医院暨北京市肿瘤防治研究所泌尿外科,恶性肿瘤发病机制及转化研究教育部重点实验室,北京 100142;2.北京大学第一医院泌尿外科,北京大学泌尿外科研究所,北京 100034)
肾癌术后肾上腺孤立转移灶的外科治疗方式比较:18例经验报告
刘佳1,虞巍2,杜鹏1,何群2,金杰2,周利群2,韩文科2,杨勇1
(1.北京大学肿瘤医院暨北京市肿瘤防治研究所泌尿外科,恶性肿瘤发病机制及转化研究教育部重点实验室,北京 100142;2.北京大学第一医院泌尿外科,北京大学泌尿外科研究所,北京 100034)
目的探讨肾癌术后肾上腺孤立转移灶的不同外科手术方式的优缺点。方法收集并分析2003至2013年北京大学第一医院泌尿外科和北京大学肿瘤医院泌尿外科收治的肾癌术后肾上腺孤立转移灶行肾上腺切除术的患者共18例,比较不同手术的差异。结果9例肾癌术后同侧肾上腺转移患者中,经腹腹腔镜组的术中失血均值明显较少(1 300 mL vs 304 mL)。9例对侧转移患者中,腹膜后镜组禁食时间[(1.4±0.8)h vs(4.0±1.4)h,P=0.036]和住院日[(4.5±1.2)d vs(7.0±4.5)d,P=0.041]较短。而经腹腹腔镜与腹膜后镜切除组相比,后者的平均禁食时间和平均住院日明显较短。结论肾癌术后肾上腺鼓励转移灶的手术方式可以选择开放、经腹腹腔镜和腹膜后镜手术。其中对于同侧肾上腺转移的患者,经腹腹腔镜具有出血量少的趋势,而对侧肾上腺转移的患者,腹膜后镜比开放手术具有禁食时间和住院时间较短的优势。
肾癌;转移;肾上腺;腹腔镜;肾上腺切除
肾癌是泌尿系统常见肿瘤,早期手术治疗效果较好。但部分患者术后仍出现局部复发或转移,而放化疗对转移性肾癌的疗效欠佳。随着靶向治疗的出现,转移性肾癌患者的预后获得一定改善,但手术治疗在转移性肾癌中仍具有重要作用。研究显示,对于肾癌切除术后出现孤立性转移灶或者肾癌伴发孤立性转移的患者,转移灶完全切除后其5年生存率能达到44%,而不完全切除5年生存率仅为14%[1]。肾癌转移多发生于肺、骨、肝脏和胰腺,肾上腺转移仅占1.9%~7.1%[2],转移后行肾上腺切除术可以延长患者生命[3]。
自1992年[4]首次报道腹腔镜肾上腺切除术(laparoscopic adrenlectomy,LA)后,这种微创手术已经成为肾上腺良性肿瘤切除的标准方式。相对于传统的开放肾上腺切除术(open adrenalectomy,OA)来说,LA具有创伤小、恢复快等优点。但对于肾癌术后肾上腺孤立转移灶,由于肿瘤侵润导致粘连等情况,LA手术难度较单纯肾上腺腺瘤大,手术并发症风险也相对较高。目前,国内对于肾癌术后肾上腺孤立转移灶手术方式的比较研究尚缺乏,因此,本研究回顾性分析了北京大学泌尿外科研究所和北京大学肿瘤医院近十年来收治的肾癌术后肾上腺转移的患者,对比不同手术方式的优缺点。
1 材料与方法
1.1 临床资料
2003年至2013年,北京大学泌尿外科研究所和北京大学肿瘤医院共收治肾癌术后肾上腺孤立转移灶的患者18例,其中男性13例(72.2%),女性5例(18.8%);年龄37~74岁,平均(57±10)岁。所有患者原发均为肾透明细胞癌且行肾癌根治性切除术(其中5例开放性肾根治性切除术,13例腹膜后镜肾癌根治术),转移灶诊断时间为肾癌根治术后2~132个月,平均(38±36)月;肾上腺转移灶位于左侧10例,右侧8例;肾癌同侧肾上腺转移9例,对侧肾上腺转移9例。手术方式:由于肾癌根治术后,同侧肾上腺转移灶的手术时存在腹膜后粘连的问题,在同侧转移9例患者中,有4例患者行经腹腔入路的开放性肾上腺切除(transperitoneal open adrenlectomy,TOA),另5例患者行经腹腔入路的腹腔镜肾上腺切除(transperitoneal laparoscopic adrenlectomy,TLA);9例对侧转移患者中,2例患者行TOA,另外7例采取腹膜后入路的腹腔镜肾上腺切除(retroperitoneal laparoscopic adrenlectomy,RLA)。18例患者的具体临床病理资料见表1。
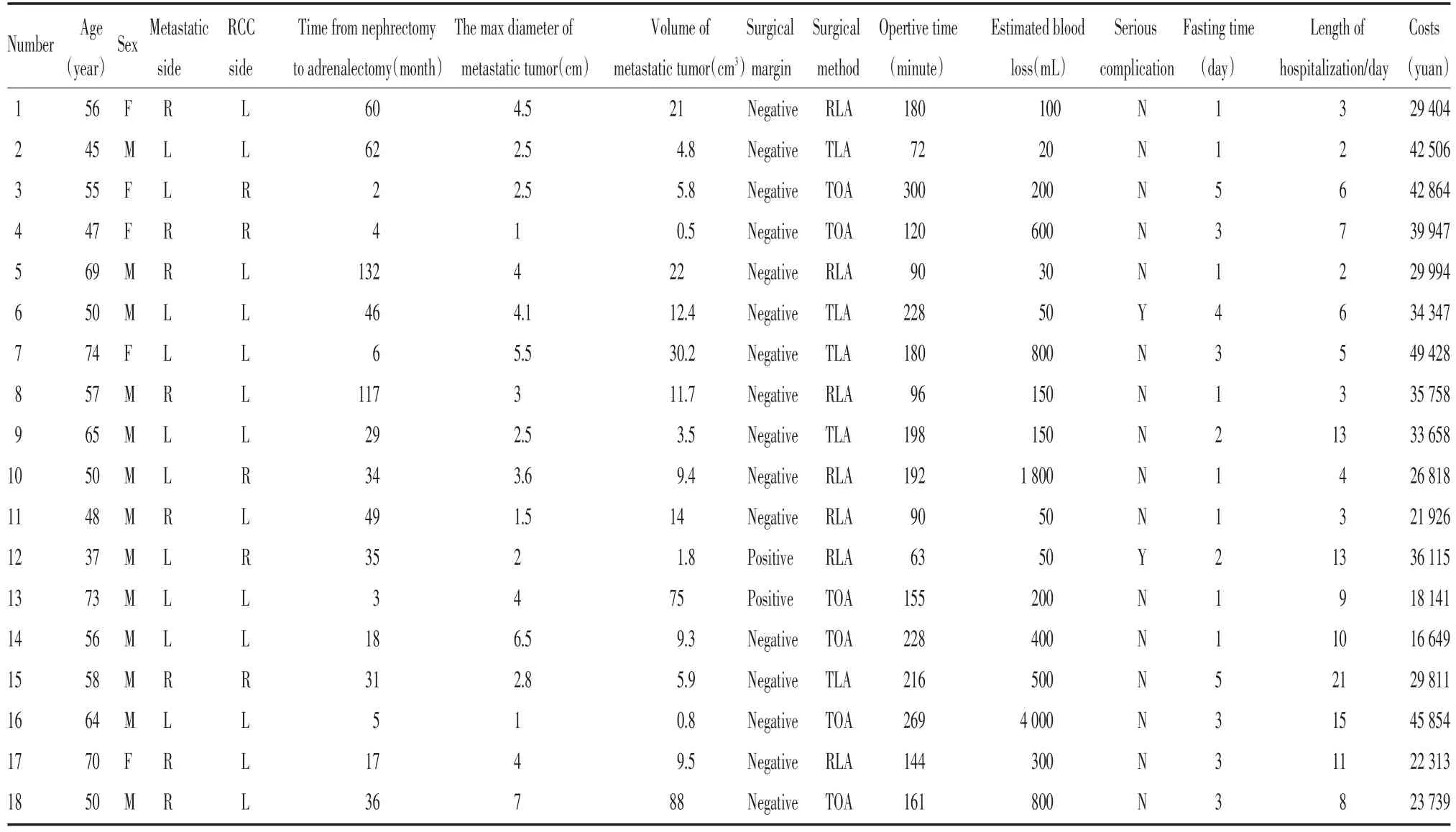
表1 患者特征及资料Tab.1 Patients’characteristics and results
1.2 统计学方法
采用SPSS 16.0统计软件,将连续变量用Mann-Whitney’s U检验进行非参数检验;分类比较采用χ2检验,P<0.05为差异有统计意义。
2 结果
18例病理标本肿瘤平均最大径为(3.4±1.7)cm,根据椭圆形公式估测肿瘤平均体积为(18.1±25)cm3。有2例(11.1%)患者术后切缘阳性,其中1例为RLA,1例为OA。平均手术时间(166±67)min;术中平均出血量(566±962)mL。1例TLA患者二次手术止血,另1例OA患者因术后肾上腺危象入SICU治疗(对侧肾上腺在进行肾癌根治时已切除)。术后患者平均禁食时间为(2.3±1.4)d;平均住院日(7.8±5.2)d。
由于肾癌根治术后,进行同侧肾上腺转移灶切除时存在局部粘连的问题,因此,我们将9例同侧肾上腺转移与9例对侧肾上腺转移患者分别进行分析(表2)。同侧肾上腺转移的患者中,4例TOA与5例TLA患者相比,2组在肿瘤体积、外科切缘、术中出血、手术时间、并发症、术后禁食时间、平均住院日方面均无显著差异(P>0.05);但经腹腹腔镜组的术中失血均值明显较少(1 300 mL vs 304 mL)。在对侧肾上腺转移患者中,2例TOA与7例RLA患者相比,2组在肿瘤体积、外科切缘、术中出血、手术时间、并发症方面无统计学差异(P>0.05);而在术后禁食时间(P=0.036)和平均住院日(P=0.041)上,2者差异显著,RLA组优于OA组。此外,对5例TLA和7例RLA对比分析发现,2亚组的上诉各项指标均无统计学意义(P>0.05);但RLA组的术后禁食时间和住院日均值明显较短(3.0 d vs 1.4 d和9.4 d vs 4.5 d)。
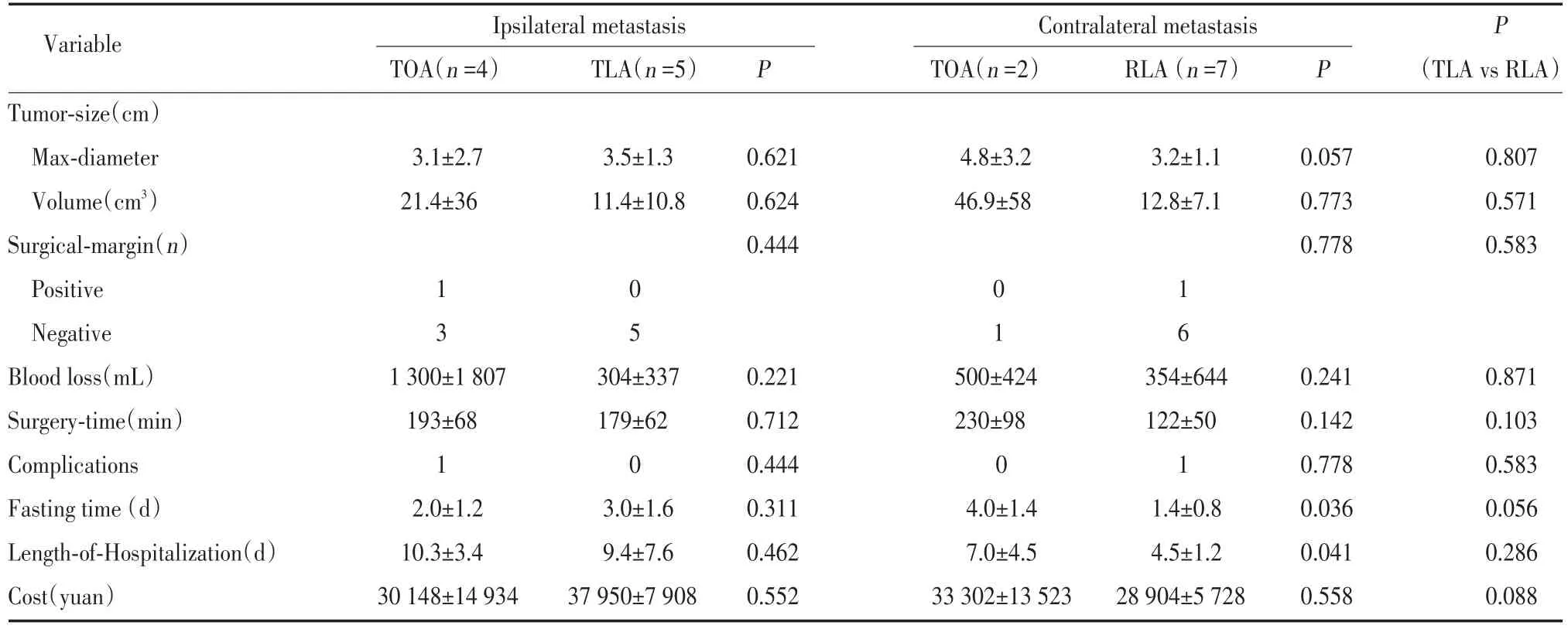
表2 肾癌肾上腺转移患者的统计数据Tab.2 Descriptive statistics for all adrenal metastases of renal cell carcinoma
3 讨论
近年来,随着分子靶向药物的使用,转移性肾细胞癌(metastatic renal cell carcinoma,mRCC)的治疗效果有所提高,但肿瘤中位生存率仍小于2年,完全缓解的病例罕见[5]。已有研究[3]显示,肾癌术后肾上腺转移灶切除可明显延长患者生命,文献报道[6]其中位生存时间能达到84个月。目前国内关于LA治疗肾癌术后肾上腺转移的报道比较少见。
与传统OA相比,LA手术创伤小,术后恢复快已是不争事实,且术后能更早接受系统靶向治疗从而获益[5]。以往对于恶性肾上腺肿瘤特别是转移性肿瘤,LA的应用饱有争议。已有研究[7]发现,相较于肾上腺原发恶性肿瘤,肾上腺转移癌LA术后的局部复发和操作腔道种植发生率非常低。这可能是因为肾上腺转移癌多位于腺体中央,质地均匀常有坚韧包膜,术中小心操作不宜发生瘤体破裂[8]。欧洲1项多中心研究收集了317例肾上腺转移肿瘤患者资料,146例LA与171例OA相比,1、2、3、5年生存率及肿瘤复发率均无统计学差异[6]。本组18例患者中,LA组和OA组的肿瘤切缘和术后并发症发生率均无统计学差异。1例LA切缘阳性,其肿瘤最大径为4.2 cm;另1例OA切缘阳性,系肿瘤侵犯腔静脉壁,术中切除部分血管壁并修补。术后2例并发症,1例LA术后出血,经二次手术止血后病情平稳出院;另1例因肾癌根治术同时切除同侧肾上腺,对侧转移时行OA,术后出现肾上腺危象入SICU。
LA有经腹腔和腹膜后2种方式,既往未行同侧肾脏手术的患者2种方式效果相近。Rubinstein等[9]比较了25例RLA和32例TLA病例,发现2组在平均手术时间(P=0.64)、出血量(P=0.92)、住院日(P= 0.56)以及并发症发生率(P=0.58)方面均无显著差异。Marangos等[10]认为肿瘤侵犯大血管是LA的禁忌症。对于肾癌术后同侧肾上腺转移的患者,采用TLA可以避免重新游离已经粘连的腹膜后间隙。本组9例肾癌术后同侧转移病例,OA组与TLA组在肿瘤体积、外科切缘、术中出血、手术时间、并发症、术后禁食时间、平均住院日和住院费用方面均无显著差异(P>0.05)。OA组中有1例患者,术中出血为4 000 mL,这主要与粘连较重有关,但与OA组相比,TLA在出血量上有相对较少的趋势(2组均值为1 300 mL vs 304 mL),这可能与TLA手术视野放大,血管处理较为仔细相关。因此,对于肾癌术后同侧肾上腺转移的患者,采用TLA手术时,需要丰富的腹腔镜操作经验。
对于肾癌术后的对侧肾上腺转移灶,由于对侧腹膜后既往未行手术,RLA仍为较好选择。本组9例对侧转移病例,OA组2例,RLA组7例;OA组与RLA组在肿瘤体积、外科切缘、术中出血、手术时间、并发症和住院费用方面差异并不明显(P>0.05);而在术后禁食时间(P=0.036)和平均住院日(P=0.041)上,RLA组明显优于OA组。与TLA相比,RLA对肠道影响较小,术后患者恢复更快[9]。亚组分析发现,5例TLA与7例RLA相比,虽然各项指标之间无显著差异(P>0.05),但RLA组在术后禁食时间和住院日均值上具有一定优势的趋势(3.0 d vs 1.4 d和9.4 d vs 4.5 d),这可能与TLA术中二氧化碳和出血刺激腹膜,影响肠道功能有关;2列数据总体并未体现出统计学差异,可能与病例数较少及个体差异较大有关。
对于手术方式,选择合适的患者至关重要,除了腹腔镜本身的禁忌证之外,肿瘤的大小以及肿瘤与血管的关系是手术方式选择的重要决定因素。本单位的数据分析2组患者肿瘤体积差距不明显,但回顾原始资料我们发现,2例最大径>5 cm的肿瘤均采取了TOA的方式。此外,术者的经验也很重要,术中应小心操作避免肿瘤破裂种植。对于肾癌术后同侧转移的患者,我们推荐TLA;而对侧转移则可行RLA,这种方式术后患者恢复更快。
腹腔镜手术在我国泌尿外科领域已广泛开展,随着技术的成熟,一些原来的手术禁忌证也逐渐转变为手术适应证。本研究结果提示:在合理选择患者的基础上,LA是治疗肾癌肾上腺孤立转移灶的一种安全可行的方式。
[1]Kavolius JP,Mastorakos DP,Pavlovich C,et al.Resection of metastatic renal cell carcinoma[J].J Clin Oncol,1998,16(6):2261-2266.
[2]Su JR,Zhu DJ,Liang W,et al.Investigation on the indication of ipsilateral adrenalectomy in radical nephrectomy:a meta-analysis[J]. Chin Med J(Engl),2012,125(21):3885-3890.
[3]Antonelli A,Cozzoli A,Simeone C,et al.Surgical treatment of adrenal metastasis from renal cell carcinoma:a single-centre experience of 45 patients[J].BJU Int,2006,97(3):505-508.
[4]Gagner M,Lacroix A,Bolte E.Laparoscopic adrenalectomy in Cushing′s syndrome and pheochromocytoma[J].N Engl J Med,1992,327(14):1033.
[5]Heng DY,Xie W,Regan MM,et al.Prognostic factors for overall survival in patients with metastatic renal cell carcinoma treated with vascular endothelial growth factor-targeted agents:results from a large,multicenter study[J].J Clin Oncol,2009,27(34):5794-5799.
[6]Moreno P,de la Quintana Basarrate A,Musholt TJ,et al.Adrenalectomy for solid tumor metastases:results of a multicenter European study[J].Surgery,2013,154(6):1215-1222,1223.
[7]Strong VE,D′Angelica M,Tang L,et al.Laparoscopic adrenalectomy for isolated adrenal metastasis[J].Ann Surg Oncol,2007,14(12):3392-3400.
[8]Duh QY.Laparoscopic adrenalectomy for isolated adrenal metastasis:the right thing to do and the right way to do it[J].Ann Surg Oncol,2007,14(12):3288-3289.
[9]Rubinstein M,Gill IS,Aron M,et al.Prospective,randomized comparison of transperitoneal versus retroperitoneal laparoscopic adrenalectomy[J].J Urol,2005,174(2):442-445.
[10]Marangos IP,Kazaryan AM,Rosseland AR,et al.Should we use laparoscopic adrenalectomy for metastases?Scandinavian multicenter study[J].J Surg Oncol,2009,100(1):43-47.
(编辑 裘孝琦)
Comparison of Different Surgical Treatments for Solitary Adrenal Metastasis Following Nephrectomy in Patients with Renal Cell Carcinoma:18 Cases Report
LIUJia1,YUWei2,DU Peng1,HE Qun2,JINJie2,ZHOU Li-qun2,HANWen-ke2,YANGYong1
(1.Key laboratory of Carcinogenesis and Translational Research of Ministry of Education,Department of Urology,Peking University Cancer Hospital&Institute,Beijing 100142,China;2.Department of Urology,Peking University First Hospital,Institute of Urology,Peking University,Beijing 100034,China)
ObjectiveTo investigate the feasibility and outcomes of different surgical treatments for adrenal metastasis after previous radical nephrectomy for patients with renal cell carcinoma.MethodsA total of 18 adrenal solitary metastasis of renal cell carcinoma were identified from database of two institutions between 2003 and 2013.Clinical and pathologic data were collected and analyzed.ResultsOf9 patients who had ipsilateral metastasis of the renal tumor,the estimated blood loss were obviously fewer in the transperitoneal LA group.Of 9 cases who had contralateral metastasis of the renal tumor,the fasting time[(1.4±0.8)h vs(4.0±1.4)h,P=0.036]and length of hospital stay[(4.5±1.2)d vs(7.0±4.5)d,P= 0.041]were obviously fewer in the retroperitoneal LA group.The averages of the fasting time and length of hospital stay in the retroperitoneal LA group were obviously smaller than in the transperitoneal LA group.ConclusionLA for treatment of renal cell carcinoma metastasis is technically feasible in selected patients.Transperitoneal and retroperitoneal LA can be respectively recommended as an appropriate approach for isolated adrenal metastases of ipsilateral and contralateral renal cell carcinoma after nephrectomy.
renal cell carcinoma;adrenal;metastases;laparoscopy;adrenalectomy
R737.11
A
0258-4646(2015)12-1125-04
刘佳(1984-),男,主治医师,博士.
虞巍,E-mail:yuweif@126.com
2015-03-04
网络出版时间:
