地西他滨治疗骨髓增生异常综合征的疗效分析
2015-01-25初晓丽
初晓丽
中国医科大学附属盛京医院,辽宁沈阳 110000
骨髓增生异常综合征是一组起源于多能造血干细胞的恶性克隆性疾病[1],以骨髓无效造血、长期的进行性难治性外周血细胞减少、造血功能衰竭等为主要特征表现,有向急性髓系白血病转化的风险,各年段均可发病,但中老年发病率较高,是对人类健康造成严重威胁的疾病之一[2]。临床多用免疫抑制剂、造血生长因子、诱导分化剂、雄激素等药物进行治疗,但均未收到理想的治疗效果,治愈患者所占的比例较低[3]。本研究收集来我院就诊的骨髓增生异常综合征患者32例并用地西他滨治疗,效果较好,现报道如下。
1 资料与方法
1.1 一般资料
回顾性分析2012年5月~2015年5月我院收治的中、高危骨髓增生异常综合征患者63例,所有患者均符合《血液病诊断与疗效标准》中骨髓增生异常综合征的诊断标准[4],并经过骨髓穿刺、骨髓活检及骨髓细胞染色分析确诊。男41例,女22例,年龄37~72岁,平均(59.6±10.4)岁,病程3d~47个月,平均(1.9±0.4)个月。IPSS危险分组中危Ⅰ22例,中危Ⅱ26例,高危15例。按照治疗方法将患者分为两组,研究组32例,对照组31例,两组患者在性别、年龄、病程、骨髓增生程度等一般资料方面比较差异无统计学意义(P>0.05),具有可比性。
1.2 方法
两组在治疗期间均用相同的对症支持治疗。研究组用地西他滨[(齐鲁制药(海南)有限公司,H20140051]治疗,使用剂量为15~20mg/(m2·d),1次/d,静脉滴注5d,每次1h。对照组用传统的HA方案治疗:三尖杉酯碱及阿糖胞苷。三尖杉酯碱(H)使用剂量2~4mg/d,阿糖胞苷(A)使用剂量100~200mg/d,静脉滴注7d;治疗期间对外周白细胞进行监测,当水平低于4×109/L时给予G-CSF,剂量为300μg/d,当高于4×109/L水平时停止使用,两组患者在治疗期间均同时进行营养支持、止吐治疗。两组均治疗3个月。
1.3 观察指标
临床疗效:将临床疗效分为完全缓解、部分缓解、血液学改善、无效四个等级,患者符合下述标准:Hb高于110g/L、中性粒细胞急速(ANC)不低于1.5×109/L、血小板(PLT)不低于100×109/L且持续时间不低于8周。完全缓解为治疗后患者情况达到上述标准且临床中无病态造血者;部分缓解为患者治疗后符合上述标准但临床中存在持续病态造血者;血液学改善为未输血情况下Hb明显升高,且升高程度介于10 ~ 20g/L范围内或红细胞输注减少程度不低于50%者。总有效率=(完全缓解+部分缓解+血液学改善)/总例数×100%[5]。不良反应发生率:记录治疗后两组中出现骨髓抑制、感染、恶心、发热、肝功能异常等各项不良反应的患者例数,计算各组不良反应总发生率。
1.4 统计学方法
用SPSS17.0统计软件分析,计数资料用率(%)表示,两组比较用x2检验,检验水准α=0.05,以P<0.05为差异有统计学意义。
2 结果
2.1 两组临床疗效比较
研究组总有效率与对照组比较,差异无统计学意义(P>0.05),具体见表1。
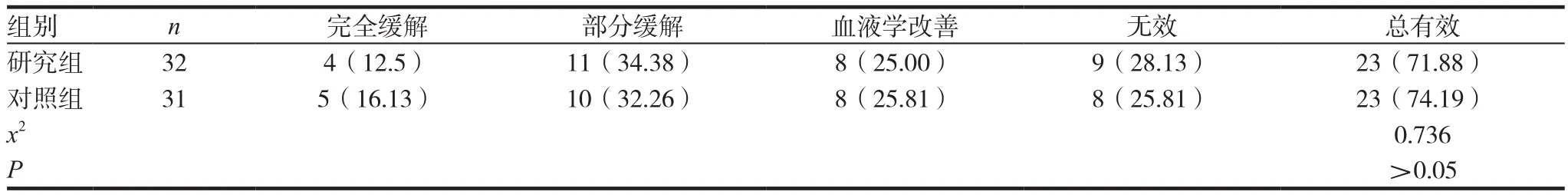
表1 两组临床疗效比较[n(%)]
2.2 两组不良反应发生率比较
研究组不良反应总发生率与对照组比较明显较低,两组差异有统计学意义(P<0.05),见表2。不良反应均较轻微给予对症处理后好转。

表2 两组不良反应发生率比较
3 讨论
骨髓增生异常综合征为获得性干细胞疾病,临床表现多样,从单纯性中度贫血至白血病等,病程也长短不等,短则数月,长则多年,该病可发生于肿瘤的放(化)疗后,接触有毒或能导致突变的物质,但大部分的骨髓增生异常综合征为原因不明确的原发性疾病。目前尚无有效的方法治疗,预后不佳[6-8]。骨髓增生异常综合征患者多用对症支持治疗,根据IPSS评分对患者疾病程度进行评定,低危及中危-1患者、中危-2及高危患者分别给予包括免疫抑制剂、细胞因子、去甲基化药物等在内的低强度治疗;包括造血干细胞移植、去甲基化药物、化疗等措施在内的高强度治疗,但均未收到理想的疗效[9-10]。骨髓增生异常综合征患者中老年人占大部分,该病呈现慢性临床过程,由于部分制剂有较大毒副作用,在高龄骨髓增生异常综合征患者中难以使用,患者出现感染、出血、铁负荷过大或转化为白血病[11-12]。
地西他滨为5-氮杂-2'-脱氧胞嘧啶核苷,是一种胞苷的脱氧核苷类似物,属于可阻止DNA的甲基化过程的特异的DNA甲基转移酶抑制剂,该药最早作为一种抗癌药物应用于临床,但由于使用的剂量较大时会发生严重的骨髓抑制,使其在临床的应用受到了一定程度的限制[13]。近年来,在骨髓增生异常综合征的治疗方面应用效果较好,谢伟成等[14]用地西他滨治疗高危骨髓增生异常综合征患者,发现地西他滨治疗组的总有效率达到72.7%,不良反应发生率为27.3%,证实地西他滨治疗骨髓增生异常综合征的有效性及安全性。地西他滨剂量较高时有细胞毒性作用,剂量较低时可诱导肿瘤细胞分化[15],可使甲基转移酶失活,有去甲基化作用,主要是通过使DNA甲基转移酶受到抑制而使基因组中局部高甲基化CpG岛发生去甲基化,从而使抑癌基因重新表达,诱导肿瘤细胞向正常细胞分化或诱导肿瘤细胞凋亡,达到抗肿瘤的效果[16-17]。
本次研究结果表明,研究组总有效率与对照组比较差异无统计学意义(P>0.05)。不良反应总发生率与对照组比较明显较低,两组差异有统计学意义(P<0.05)。结果说明地西他滨治疗骨髓增生异常综合征的疗效与HA方案相近,但不良反应总发生率较低,有较高的安全性,但由于本次研究样本量较少,地西他滨治疗骨髓增生异常综合征的远期疗效还需要加大样本深入研究。
[1] 张信国.地西他滨联合预激方案治疗老年骨髓增生异常综合征临床研究[J].基层医学论坛,2015,19(3):334-335.
[2] 党惠兵.沙立度胺和环孢素A联合亚砷酸治疗骨髓增生异常综合征的38例分析[J].重庆医学,2014,43(14):1791-1793.
[3] 吴骁,杨光.氨磷汀治疗骨髓增生异常综合征的临床分析 [J].现代实用医学,2015,27(1):54-55.
[4] 张之南,沈悌.血液病诊断及疗效标准[M].第3版,北京:科学出版社,1999:157-163.
[5] Trotti A,Byhardt R,Stetz J,et al.Common toxicity criteria:version 2.0 an improved reference for grading the acute effects of cancer treatment:impact on radiotherapy[J].Int J Radiat Oncol Biol Phys,2000,47(1):13-47.
[6] 梁月娜,黎少玲.三氧化二砷与沙利度胺联合应用治疗骨髓增生异常综合征的疗效分析[J].医学理论与实践,2013,26(17):2312-2313.
[7] 郭智,刘晓东,谭晓华,等.氨磷汀治疗骨髓增生异常综合征临床观察[J].现代中西医结合杂志,2009,18(27):3312-3313.
[8] 杨明.小剂量阿糖胞苷治疗骨髓增生异常综合征的效果分析 [J].中外医学研究,2014,12(20):152-153.
[9] 于奇宁,常新东,刘先桃,等.地西他滨联合CAG方案治疗高危骨髓增生异常综合征疗效观察[J].疑难病杂志,2013,12(5):357-359.
[10] 杨杰,彭志刚.中医药治疗骨髓增生异常综合征的研究进展 [J].临床内科杂志,2014,31(3):162-163.
[11] 隋潇徽,周慧,刘新,等.CAG方案治疗中高危骨髓增生异常综合征的临床观察[J].中华肿瘤防治杂志,2008,15(21):1666-1668.
[12] 卢学春,朱宏丽,姚善谦,等.氨磷汀联合重组人红细胞生成素治疗高龄骨髓增生异常综合征近期疗效观察[J].中国实验血液学杂志,2005,13(3):440-442.
[13] 李娜,侯丽虹.去甲基化药物地西他滨治疗血液系统恶性肿瘤的研究进展[J].中国医药科学,2014,4(6):44-49.
[14] 谢伟成,程淑琴,林翠芳,等.地西他滨治疗骨髓增生异常综合征的临床疗效研究[J].临床和实验医学杂志,2014,13(11):877-880.
[15] 胡通林,郑智茵,刘文宾.地西他滨联合HA方案治疗难治性急性髓细胞性白血病疗效观察[J].临床内科杂志,2013,30(9):640-641.
[16] 方宝枝,何广胜,吴德沛,等,地西他滨治疗成人急性髓细胞白血病的临床观察[J].肿瘤,2011,31(11):1022-1025.
[17] 凌琳,吴华,冯付超,等.地西他滨治疗恶性血液系统疾病的研究进展[J].肿瘤药学,2015,5(1):14-20.
