CuO/ZnO复合纳米材料的合成及其催化烯烃环氧化性能研究
2015-01-12王建凤
朱 婕,王建凤,陈 伟
(浙江省碳材料技术研究重点实验室,温州大学化学与材料工程学院,浙江 温州 325027)
研究与开发
CuO/ZnO复合纳米材料的合成及其催化烯烃环氧化性能研究
朱 婕,王建凤,陈 伟
(浙江省碳材料技术研究重点实验室,温州大学化学与材料工程学院,浙江 温州 325027)
以醋酸锌和硝酸铜为原料通过离子共沉淀法一步合成了(CuxZn1-x)(OH)m(CO3)n固溶体,并选择在500℃条件下煅烧得到CuO/ZnO复合纳米晶体。采用扫描电镜和EDS-Mapping等进行表征,分析材料的形貌和组成,证明晶体为疏松结构的小球,且铜元素和锌元素均匀地分散其中。另外,把得到的样品应用于环辛烯氧化中,发现当Cu2+∶Zn2+=3时的催化活性最高。
离子共沉淀法;CuO/ZnO;复合纳米晶体;环辛烯氧化
尺寸和结构可控的过渡金属氧化物在材料合成领域已经引起了广泛的关注[1-10]。其中,过渡金属氧化物CuO和Cu2O等由于具有低能带隙(Eg=1.2eV)而具有反应温度低、转化率高、催化剂易分离等优点,目前已经被广泛应用到催化[11]、传感[12-13]、电极材料[14]和锂电池[15-16]等领域。同时,在CO、NO和类似乙醇的有机挥发性化学物质的氧化中也发挥了极好的作用[17],且C-N耦合反应用氧化铜作催化剂也具有极高的活性。目前,人们已开发出各种方法来制备不同尺寸和形貌的铜氧化物纳米材料,如溶胶-凝胶法、水热法、溶剂热法、气相沉积法等。
纳米粒子因具有特殊表面与界面效应,从而表现出比块状催化剂更加优异的催化活性。然而,在工业应用中,我们常将固体颗粒分散在液体中,由于纳米颗粒的小尺寸使其表面存在大量的不饱和键,表面活性很大,再加上一些外在的条件如高温,使纳米粒子在使用过程中往往存在很多共同的缺陷,如易发生团聚而导致材料粒径变大、表面能减小而失去纳米材料的特性[18],特别是在催化燃烧等一类的高温反应中。因此,在纳米催化剂的研究中,设法提高纳米材料的稳定性,防止或减慢纳米粒子间的团聚现象,是今后研究的一个重点[19]。
本文利用离子共沉淀法合成出了CuO/ZnO复合纳米晶体,使铜锌2种元素均匀分散在晶体球中,这样不仅增加了铜纳米粒子的分散性,使粒子与粒子之间分离开,减轻反应中的团聚;且小球本身的孔道结构使反应物更容易到达催化剂表面,从而加速了催化反应的进行。
1 实验部分
1.1 主要试剂
二水乙酸锌(AR)、三水硝酸铜(AR)、碳酸氢铵(AR)、聚乙烯吡咯烷酮(K-30),cis-Cyclooctene(95% stab),叔丁基过氧化氢,(70% aq.soin),联苯,GR,乙腈,HPLC(≥99.9%),高纯水。
1.2 CuO/ZnO复合结构纳米材料的合成
首先称取0.93288g醋酸锌和0.1812g硝酸铜于100mL烧杯中,加入15mL蒸馏水,强力搅拌使之溶解,得到溶液1。另外,称取0.7906g碳酸氢铵于100mL烧杯中,加入15mL去离子水,搅拌使之溶解,得到溶液2。然后把溶液1逐滴滴加到溶液2中,待滴加完毕,加入0.1g PVP,继续搅拌10min,使三者充分混匀。然后,将溶液转移到50mL聚四氟高压反应釜中,120℃条件下反应10h。待高压釜冷却至室温,把产物离心分离,用乙醇和水的混合液洗涤沉淀3~5次,得到的样品在50℃下真空干燥。
把得到的固体粉末于马弗炉中500℃条件下煅烧2h,即得到铜锌比为0.276378∶1的CuO/ZnO样
品粉末。其余3个比例的合成方法均一致。
1.3 CuO/ZnO催化环辛烯氧化性能的研究
我们用环辛烯作为烯烃氧化反应的原料。固定催化剂中氧化铜的含量为10mg,分别将不同比例的催化剂和1mmol联苯、1mmol环辛烯、10mL乙腈加入到50mL圆底烧瓶中,超声数分钟使催化剂分散在溶液中,然后将反应固定在带有回流管的油浴锅中,70℃回流反应,5min后,加入50μL TBHP,开始计时。每隔一段时间取样,用丙酮稀释后离心分离,取上层清液使用气相色谱仪进行定量,分析测试溶液中反应物和产物的比。
1.4 分析方法
采用Nova NanoSEM 200型扫描电镜和FEI Tecnai G2 F20 S-Twin型透射电镜对材料的形貌特征进行观察。采用Bruker D8 Advance型X射线粉末衍射仪、透射电镜的EDS-Mapping、电感耦合等离子体发射光谱仪(ICP-OES)联合ASAP 2020 HD88型比表面仪分析材料的组成和结构。
2 结果和讨论
图1为加入不同量的醋酸锌和硝酸铜后得到的样品的扫描电镜图。图1(a)为加入0.93288g醋酸锌和0.1812g硝酸铜得到的样品,图1(b)为 加入0.87804g醋酸锌和0.2416g硝酸铜的样品, 图1(c)为加入0.8232g醋酸锌和0.302g硝酸铜的样品,图1(d)为加入0.65853g醋酸锌和0.4832g硝酸铜的样品。从图1(a)中可以看出,得到的样品为尺寸均一的晶体球,有轻微的团聚现象。插图为该样品在高倍镜下观察到的图像,从图中可以看出,晶体球的形貌呈草团状。其余3个样品的形貌和尺寸与此差不多,但是,观察图1(c)发现,加入0.8232g醋酸锌和0.302g硝酸铜得到的样品的分散性较好。
聚乙烯吡咯烷酮(PVP)是一种既溶于水又能溶于大部分有机溶剂的中性表面活性剂。因为能与很多物质发生络合而常被用在纳米合成反应中来调节生成的纳米晶体的尺寸大小和形貌的均一性。图2为加入0.87804g醋酸锌和0.2416g硝酸铜所得到的样品的TG-DTA图。从热重图可以看出,当温度升到200℃左右时,出现一个很小的失重台阶,在图上表现不是很明显。这个过程为材料表面吸附的水分的脱除。而在200~375℃之间为一个主要的失重带,这个过程为物质中CO和OH-的分解,并且在DTA图中有一个对应的放热峰。说明物质的分解发生在253℃左右。而在350℃以后还有一个失重台阶,应该为PVP的分解。同时,对应DTA图中,在354℃左右时出现一个吸热峰,说明在354℃时可能出现了晶型的转变。

图1 加入不同的铜锌量所得到的样品的扫描电镜
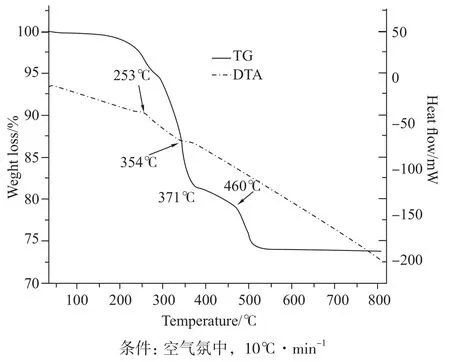
图2 干燥后样品的TG-DTA曲线
将样品于50℃条件下干燥,把得到的固体粉末置于马弗炉中,1℃·min-1的升温速度由室温升到500℃并保持2h。把焙烧后的样品用扫描电镜观察(图3),可以看出4个铜锌比例不同的样品在焙烧前后尺寸和形貌基本不变,结构仍然很完整。为了了解煅烧后样品的物相组成,我们将其进行了XRD分析,结果见图4。分析图谱发现,样品中均含有2种成分,所有的衍射峰都归属于CuO(JCPDS 48-1548)和ZnO (JCPDS 36-1451)。因此,可以确定4个样品在500℃条件下煅烧2h后,均可得到结晶度
较好的CuO/ZnO复合纳米晶体。

图3 500℃条件下煅烧后得到的样品的扫描电镜图

图4 加入不同铜锌量的样品在500℃条件下煅烧后的样品的XRD图
图5为加入4.25mmol醋酸锌、0.75mmol硝酸铜所得的CuO/ZnO样品中单个球形结构的扫描透射图和元素分布图(氧元素、铜元素和锌元素),我们从中挑选了尺寸较小的球以方便观察。从图5中我们可以看出,样品经500℃焙烧后,结构仍然很完整。且从元素分布图(EDS-Mapping)中观察到铜、锌、氧3种元素均匀地分散在小球中。由此证明,我们通过离子共沉淀法制得的CuO/ZnO复合纳米晶体,铜锌元素有极好的分散性。
图6为 CuO/ZnO(加 入4.25mmol醋 酸 锌、0.75mmol硝酸铜所得样品)样品的N2吸脱附曲线和孔径分布图;图7为 CuO/ZnO(加入3.75mmol醋酸锌、1.25mmol硝酸铜所得样品)样品的N2吸脱附曲线和孔径分布图;图8为CuO/ZnO(加入4.25mmol醋酸锌、0.75mmol硝酸铜所得样品)样品的N2吸脱附曲线和孔径分布图;图9为 CuO/ZnO(加入3mmol醋酸锌、2mmol硝酸铜所得样品)样品的N2吸脱附曲线和孔径分布图。分析图谱可得4个样品的吸脱附曲线几乎一致,均属于Ⅲ型吸附等温线,并且我们可以从图中观察到脱附等温线具有迟滞环,相对压力在0.9以上时曲线基本呈线性上升,这应
该是发生了表面吸附。从脱附曲线形成的迟滞环来看,高压端吸附量大,属于第三类回滞环。样品孔径类型属于片状粒子堆积形成的狭缝孔。同时我们采用BJH(Barrett-Joiner-Halenda)模型计算出了孔径分析曲线,从图6中观察得到材料的平均孔径约为12.6nm,属于标准的介孔(10~50nm左右的孔)结构材料。图7与此一致。图8中材料的孔径尺寸不一,主要集中在9.3nm和15.2nm附近两个范围内,也是介孔材料。而图9中材料的尺寸分布则主要集中在7.6nm附近,属于小介孔材料的范畴。这些与吸脱附曲线相一致。由以上这些数据可以得出,随着铜锌比例的增加,合成的CuO/ZnO复合结构纳米材料的孔径逐渐减小,而孔径太小将不利于反应物到达材料的内部,因此可能导致催化效率有所下降。
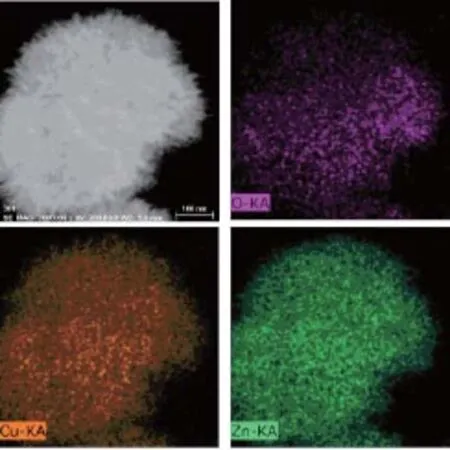
图5 CuO/ZnO(加入4.25mmol醋酸锌、0.75mmol硝酸铜所得样品)样品单个球形结构的扫描透射图和元素分布图 (氧元素、铜元素和锌元素)
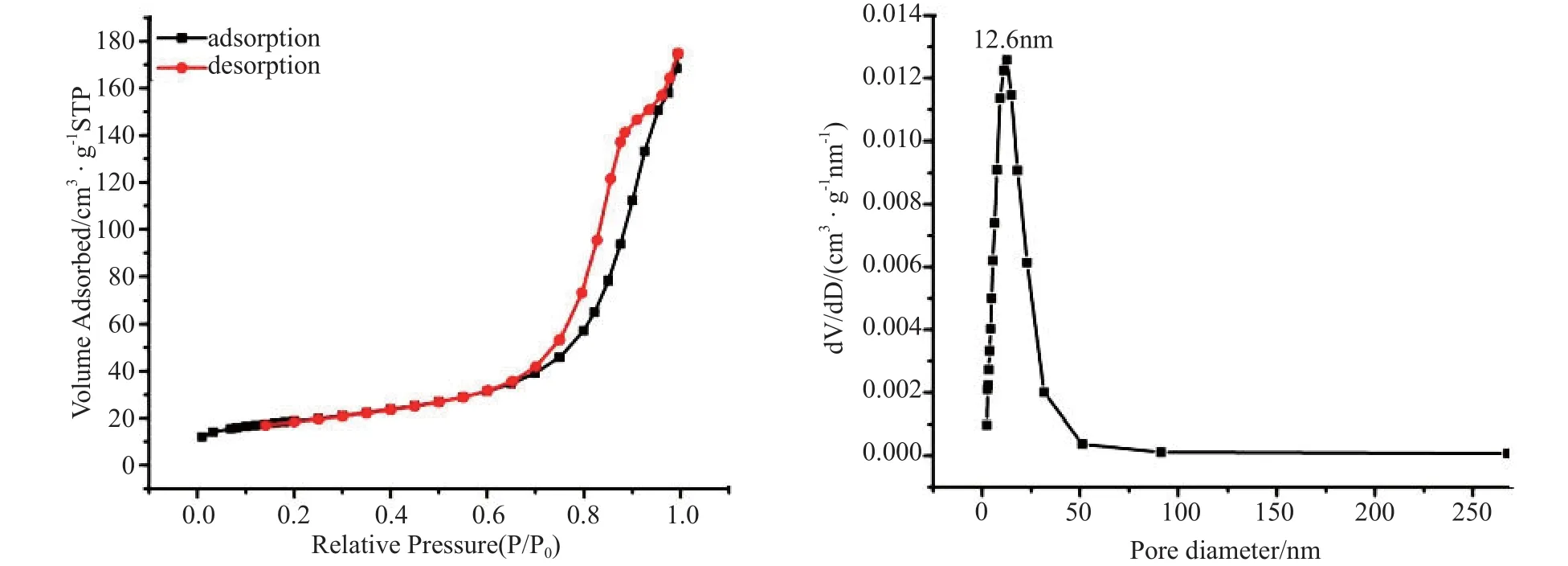
图6 CuO/ZnO(加入4.25mmol醋酸锌、0.75mmol硝酸铜所得样品)样品的N2吸脱附曲线和孔径分布图

图7 CuO/ZnO(加入4mmol醋酸锌、1mmol硝酸铜所得样品)样品的N2吸脱附曲线和孔径分布图

图8 CuO/ZnO(加入3.75mmol醋酸锌、1.25mmol硝酸铜所得样品)样品的N2吸脱附曲线和孔径分布图
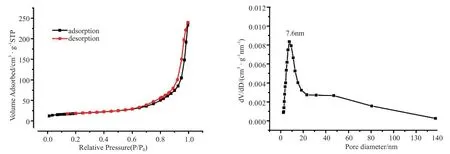
图9 CuO/ZnO(加入3mmol醋酸锌、2mmol硝酸铜所得样品)样品的N2吸脱附曲线和孔径分布图
为了确定4个样品中铜锌元素的确定比例,我们将样品用浓硝酸溶解后定容,得到合适浓度的4种溶液。利用ICP进行定量测量,计算得到4个样品中的铜锌两种元素的摩尔比并列于表1。
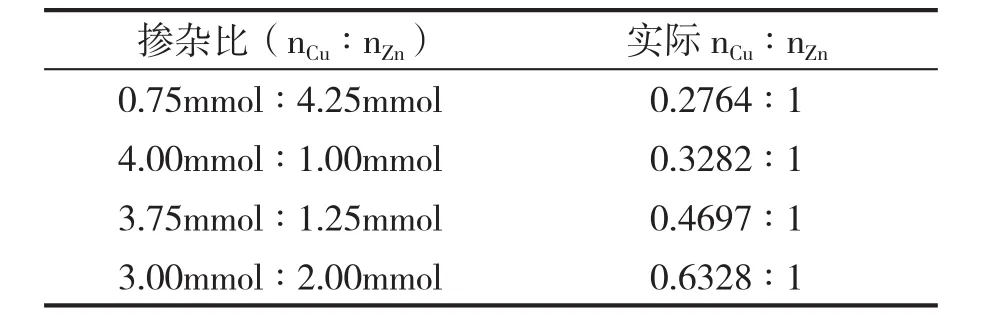
表1 4种样品中铜锌元素的加入的量比和实际所含铜锌元素的比例
为了研究离子共沉淀法合成出的CuO/ZnO复合结构纳米球的催化性能,我们把所制得的样品应用于环辛烯氧化中,并作了下列探究。
图10为含铜锌比例不同的CuO/ZnO催化剂催化环辛烯氧化的转化率随时间的变化图。从图中我们可以看出,分析比较铜锌比为0.2764∶1、0.3282∶1、0.4697∶1的样品图谱,随着含铜量的增加,环辛烯转化的速率和转化率不断提高,而当铜元素比例增加到0.6328∶1时,转化率和开始时的转化速率开始有所下降。这与我们前面的猜测相一致。当铜锌比例增加到0.6328∶1时,制得的CuO/ZnO纳米晶体由于孔道太小,阻碍了反应物与催化剂的结合速度和接触面积,因此催化效率反而有所降低。
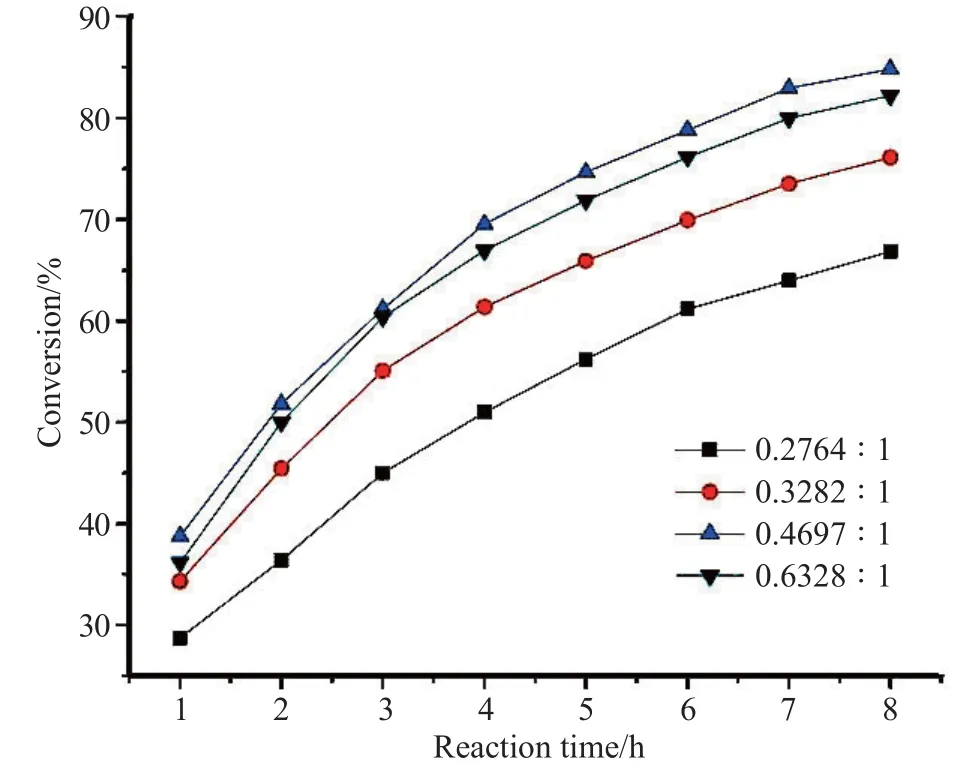
图10 含铜锌比例不同的CuO/ZnO催化剂催化环辛烯氧化的转化率随时间的变化
分析图11中的铜锌元素比为0.4697∶1的CuO/ ZnO催化剂的循环性能测试图发现,该比例的催化剂在催化环辛烯氧化的过程中有着很好的稳定性,在重复使用5次后,8h反应环辛烯氧化的转化率降低很少。这也在循环使用5次后的样品的扫描电镜图中得到验证。观察图11中的扫描电镜图,发现使用5次CuO/ZnO纳米晶体球只有部分结构发生轻微的破裂,其他的基本保持完好。因此,说明我们通过离子共沉淀法制备出的CuO/ZnO纳米晶体球在催化氧化环辛烯中有着很高的转化率和稳定性。

图11 铜锌比为0.3282∶1的CuO/ZnO纳米复合晶体球的循环性能测试和使用5次后样品的扫描电镜图
3 小结
我们通过离子共沉淀法一步制得了CuO/ZnO纳米晶体球的前驱体(CuxZn1-x)(OH)m(CO3)n,并在500℃煅烧后得到结晶度较好的CuO/ZnO晶体球结构。通过扫描电镜表征,发现晶体为草团状的球形结构。EDS-Mapping图表征发现铜元素和锌元素均的分散在该球形晶体结构中,且该催化剂在环辛烯氧化中表现了很高的转化率和稳定性。在连续使用5次后,催化剂的形貌基本保持不变。
[1] Ni, Y., Mi, K., Cheng, C., Xia, J., Ma, X., Hong, J.Urchinlike Ni-P microstructures: facile synthesis, properties and application in the fast removal of heavy-metal ions[J].Chem.Commun., 2011, 47(20): 5891-5893.
[2] Sun Shaodong, Zhang Xiaozhe, Sun Yuexia, Zhang Jie, Yang Shengchun, Song Xiaoping, Yang Zhimao.A facile strategy for the synthesis of hierarchical CuO nanourchins and their application as non-enzymatic glucose sensors[J].RSC Adv., 2013, 3(33): 13712-13719.
[3] Zhang, J., Liu, J., Peng, Q., Wang, X., Li, Y.Nearly Monodisperse Cu2O and CuO Nanospheres: Preparation and Applications for Sensitive Gas Sensors[J].Chem.Mater., 2006, 18(4):867-871.
[4] Xiao H.-M., Fu S.-Y., Zhu L.-P., Li Y.-Q., Yang, G.Controlled Synthesis and Characterization of CuO Nanostructures through a Facile Hydrothermal Route in the Presence of Sodium Citrate[J].Eur.J.Inorg.Chem., 2007, 2007(14):1966-1971.
[5] Xu Y., Chen D., Jiao X.Fabrication of CuO pricky microspheres with tunable size by a simple solution route[J].J.Phys.Chem.B., 2005, 109(68):13561-13566.
[6] Gao X.P., Bao J.L., Pan G.L., Zhu H.Y., Huang P.X., Wu F., Song D.Y.Preparation and Electrochemical Performance of Polycrystalline and Single Crystalline CuO Nanorods as Anode Materials for Li Ion Battery[J].J.Phys.Chem.B., 2004, 108(18): 5547-5551.
[7] Liu B., Zeng H.C.Mesoscale Organization of CuO Nanoribbons: Formation of “Dandelions” [J].J.Am.Chem.Soc., 2004, 126(26): 8124-8125.
[8] Yu H., Yu J., Liu S., Mann S.Template-free Hydrothermal Synthesis of CuO/Cu2O Composite Hollow Microspheres[J].Chem.Mater., 2007, 19(17): 4327-4334.
[9] Wang X., Xi G., Xiong S., Liu Y., Xi B., Yu W., Qian Y.A One-Pot Approach to Hierarchically Nanoporous Titania Hollow Microspheres with High Photocatalytic Activity[J].Cryst.Growth Des., 2008(3):930-934.
[10] U Y., Chen D., Jiao X., Xue K.Synthesis of chrysalis-like CuO nanocrystals and their catalytic activity in the thermal decomposition of ammonium perchlorate[J].J.Chem.Sci., 2009, 121(6): 1077-1081.
[11] Zhao Y., Zhu J.-J., Hong J.-M., Bian N., Chen H.-Y.Microwave-Induced Polyol-Process Synthesis of Copper and Copper Oxide Nanocrystals with Controllable Morphology[J].Eur.J.Inorg.Chem., 2004(20): 4072-4080.
[12] Kuo C.-H., Yang Y.-C., Gwo S., et al.Facet-Dependent and Au Nanocryst al-Enhanced Electrical and Photocatalytic Properties of Au-Cu2O Core-Shell
Heterostructures [J].J.Am.Chem.Soc., 2011, 133(4): 1052-1057.
[13] Choi J., Jun Y., Yeon S., et al, Biocom patible Heterostructured Nanoparticles for Multimodal Biological Detection [J].J.Am.Chem.Soc., 2006, 128 (50):15982-15983.
[14] Wang Dingsheng, Li Yadong.One-Pot Protocol for Au-Based Hybrid Magnetic Nanostructures via a Noble-Metal-Induced Reduction Process [J].Commun, 2010, 132(18):6280-6281.
[15] Ge J.P., Zhang Q., Zhang T., et al, Porous Silica Protected Core-Satellite Nanocomposite Catalysts: Controllable Reactivity, High Stab ility and Magnetic Recyclability [J].Angew.Chem.Int.Ed., 2008, 47(46): 8924-8929.
[16] Kim S., Fisher B., Eisler H.J., et al, Type-II Quantum Dots: CdTe/CdSe(Core/Shell) and CdSe/ZnTe(Core/SheⅡ) Heterostructures [J].J.Am.Chem.Soc., 2003, 125(38): 11466-11467.
[17] Wu M.K., Ashburn J.R., Torng C.J., Hor P.H., Meng R.L.,Gao L., Huang Z.J., Wang Y.Q., Chu C.W.Superconductivity at 93 K in a new mixed-phase Y-Ba-Cu-O compound system at ambient pressure[J].Phys.Rev.Lett., 1987, 58(9): 908-910.
[18] Liu Y., Fu Q.Stephanopoulos; M, F, Preferential oxidation of CO in H2over CuO-CeO2catalysts[J].Catal.Today, 2004(93/95):241-246.
[19] M.Lakshmi Kantam, Jagjit Yadav, Soumi Laha,Bojja Sreedhar , Shailendra Jha Kantam.N-Arylation of Heterocycles with Activated Chloro-and Fluoroarenes using Nanocrystalline Copper(Ⅱ ) Oxide[J].Adv.Synth.Catal., 2007, 349(11/12):1938-1942.
Synthesis of CuO/ZnO Composite Nanospheres and Efficient Olefin Epoxidation Catalytic Performance Study
ZHU Jie, WANG Jian-feng, CHEN Wei
(Key Laboratory of Carbon Materials of Zhejiang Province, College of Chemistry and Material Engineering, Wenzhou University, Wenzhou 325027, China)
In this paper, CuO/ZnO nanocomposite with spheric structure was prepared by calcinating the (CuxZn1-x)(OH)m(CO3)nprecursor at 500℃, which was obtained from the coprecipitation of Cu2+and Zn2+.Scanning electron microscope (SEM) and EDSMapping were used to analyse the morphology and structure of the materials.It was proved that the composite nanomaterials were of loose sphere structure, and copper and zinc evenly dispersed in these spheres.In addition, the sample with a [Cu]/[Zn] ratio of 3∶1 had the highest catalytic activity in cyclooctene oxidation.
ion coprecipitation; CuO/ZnO; composite nanocrystal; cyclooctene oxidation
O 643.36
A
1671-9905(2015)02-00-
国家自然科学基金项目(21101119)
朱婕(1989-),女,硕士,研究方向:催化新材料,E-mail:854219297@qq.com
2014-11-11
