杨树叶粉末对水中氨氮的吸附性能研究
2015-01-12荆肇乾杨凯华董向芸
何 瑞,荆肇乾,杨凯华,茅 尖,董向芸,陈 硕
(南京林业大学土木工程学院,江苏 南京 210037)
杨树叶粉末对水中氨氮的吸附性能研究
何 瑞,荆肇乾,杨凯华,茅 尖,董向芸,陈 硕
(南京林业大学土木工程学院,江苏 南京 210037)
采用干燥的杨树叶粉末,探讨其对水中氨氮的吸附性能。结果表明,pH变化对氨氮吸附效果影响较小;相同氨氮初始浓度条件下,随着投加量增加,单位质量杨树叶粉末对氨氮的吸附量明显减少;初始氨氮浓度越大,单位吸附量也越大。杨树叶粉末对氨氮的吸附遵循 Langmuir及Freundlich等温吸附模型。
杨树叶;氨氮;吸附;等温线
氮磷营养盐是导致水体富营养化[1-5]的主要因素,是目前水污染防治的关键控制因子。近几年中国环境状况公报显示,我国主要湖(库)富营养化问题严重,国家主要监控的湖(库)中超过IV类水质的达到70%以上,太湖、滇池为劣V类水质;7大水系总体为中度污染,且均存在氨氮指标较高的问题。从全国范围来看,主要水体的污染不仅没有从根本上控制,而且还存在逐年加重的趋势。能否有效地控制点源和面源氮素污染[6],已经成为遏制目前水体污染加剧形势的关键所在。
杨树是一个生长迅速、适应性广的优良树种,在人工林种植中占有重要地位[7],是我国数量最多的树木之一,作为落叶树种每年有大量的杨树落叶废弃而没有得到较好的利用。通过研究杨树落叶对氨氮的去除效果,探索能否利用杨树落叶提升滨水林区含氮污染物的削减效果,具有重要应用价值。
1 材料与方法
1.1 实验材料
杨树叶粉末。来自山东某杨树林区落叶经自然干燥碾碎后的粉末。
模拟氨氮废水:准确称取3.819g于105℃条件下干燥2h的无水氯化铵,溶于水,配制成氨氮质量浓度为1000mg·L-1的标准储备液。吸取该储备液100.00mL于1000mL容量瓶中,用去离子水定容至刻度,摇匀,即得氨氮质量浓度为100mg·L-1的模拟废水。其他质量浓度配制方法相同。
苯酚钠溶液(阴暗处保存5d内可用):量取5mol·L-1的NaOH 55mL注入烧杯,加入25g苯酚,溶解冷却后加入6mL丙酮,加蒸馏水至200mL。
次氯酸钠溶液(可保存7d):按市售次氯酸钠:蒸馏水=1∶4稀释即可。
L6紫外可见分光光度计,FA2004B 1‰电子天平,CHA-SA 气浴恒温振荡器,HH-6数显恒温水浴锅,GZX-9140MBE电热鼓风干燥箱,PHB-4 便携式pH计,温度计,50 mL具塞比色管,10mm玻璃比色皿。
1.3 实验方法
1.3.1 杨树叶粉末吸附氨氮的测定方法
氨氮的测定采用苯酚钠分光光度法[8]。按式(1)计算氨氮去除率R,按式(2)计算杨树叶粉末的吸附量q。


式中:C0为吸附前氨氮溶液的质量浓度,mg·L-1;C为吸附后氨氮溶液的质量浓度,mg·L-1; q为氨氮的吸附量,mg·g-1;V为氨氮溶液体积,mL;m为吸附剂干重,g。
1.3.2 吸附影响因素实验
在不同pH、氨氮初始浓度及杨树叶粉末投加量条件下,对杨树叶粉末吸附氨氮效果进行实验研究,探讨杨树叶粉末吸附氨氮的操作参数。
该护坡工程模袋采用国内某公司生产的模袋;细骨料采用当地产砂;粗骨料采用当地产碎石,规格为5~20 mm,级配为5~10 mm的占30%,10~20 mm的占70%;选用P.O42.5水泥;外加剂选用某高新材料有限责任公司生产的外加剂;掺和料采用当地某电厂Ⅱ级粉煤灰。
1.3.3 吸附等温线研究
配制初始质量浓度分别为6、10、15、20、30、40、50mg·L-1的氨氮溶液置于250mL锥形瓶中,然后分别投加40g·L-1杨树叶,加塞后在45℃下恒温振荡至吸附平衡(5h),过滤后用苯酚钠分光光度法测定滤液中氨氮浓度。实验结果利用Langumuir及Freundlich等温吸附模型进行拟合。
2 结果与讨论
2.1 氨氮初始浓度对吸附的影响
在杨树叶用量均为40g·L-1、pH=6.93、震荡温度45℃、震荡时间1h的条件下,在2~100mg·L-1范围内,调整氨氮初始浓度,研究初始浓度对吸附过程的影响,结果如图1所示。
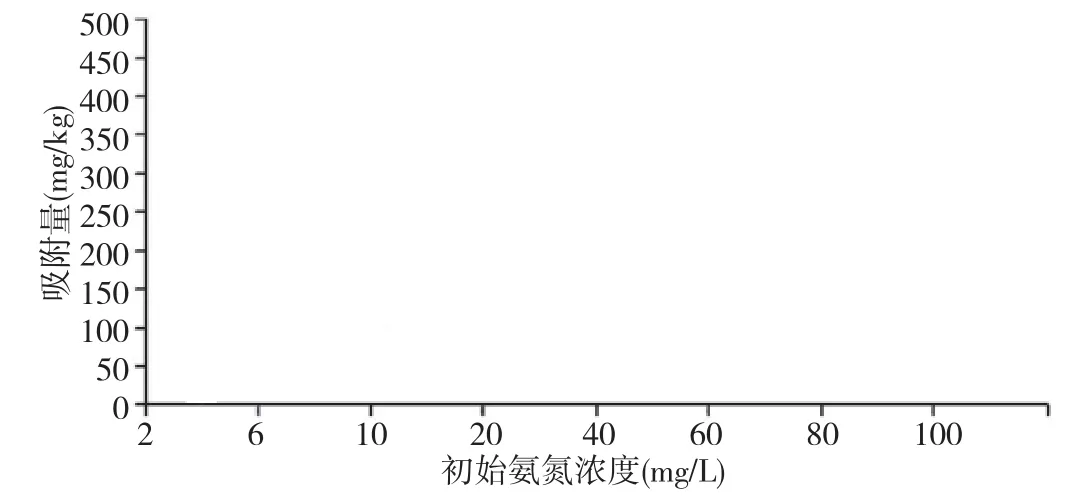
图1 初始氨氮浓度对吸附的影响Fig.1 The effect of initial concentration on the adsorption of ammo-
nia nitrogen
初始氨氮浓度由2mg·L-1增加到100mg·L-1时,吸附量由16.25mg·kg-1上升到443.52mg·kg-1。初始浓度为克服液相和固相之间的传质阻力提供了重要的推动力[9],因此氨氮初始浓度适当升高有利于提高杨树叶的吸附能力。从另一方面来说,经过低浓度氨氮吸附的杨树叶可以继续用来吸附去除高浓度的氨氮,以提高杨树叶的利用效率。
2.2 不同pH下杨树叶对氨氮的吸附
在5个锥形瓶中,用0.1mol·L-1的NaOH和0.1mol·L-1的HCl调节溶液的pH值分别为3、5、7、9、11,控制氨氮初始浓度为10 mg·L-1,杨树叶粉末投加量为40g·L-1,在温度为45℃,转速为150 r·min-1的条件下恒温振荡1h,考察不同pH值条件下杨树叶粉末对氨氮的吸附效果。不同pH值对应的氨氮吸附量变化如图2所示,在酸性(pH=3)和碱性(pH=11)条件下,杨树叶对氨氮吸附量分别为76.06mg·kg-1和78.28mg·kg-1,比中性条件下(pH=7)的吸附量(60.48mg·kg-1)有所提高。
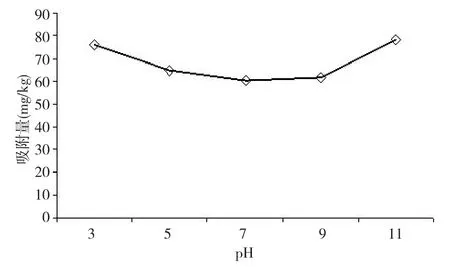
图2 pH值对氨氮吸附的影响Fig.2 Effects of pH on the adsorption of ammonia nitrogen
吸附量的变化幅度不太明显,杨树叶对氨氮的吸附呈现出较广的pH适用范围,中性条件下吸附效果略低。这主要是跟杨树叶本身的理化性质和氨氮在水中的存在形态有关。由于杨树叶粉末自身主要成分为纤维素、蛋白质等有机成分,主要以表面吸附为主,离子交换吸附较少。而NH4Cl溶液中主要有两种无机氨氮存在形式:水合氨分子NH3·H2O和游离NH4+[10]。在溶液中两者存在如式(3)中所示关系:

从式(3)中可知,溶液在碱性条件下平衡向左移动,NH3为无机氨氮的主要存在形式,NH3分子直径小于NH3·H2O分子直径。因此,有利于表面吸附作用进行,使吸附量增加。另外,在碱性条件下,杨树叶纤维溶胀,形成较大的溶胀区域,有利于对氨氮的吸附。酸性条件对杨树叶本身的理化性质改变较小,水中氨氮的主要存在形态是NH4+,尽管吸附质存在形式有所改变,但杨树叶粉末吸附主要依赖于自身表面的吸附,所以对吸附效果的影响较小[11]。
2.3 吸附剂投加量对吸附的影响
在pH=6.8,温度为45℃条件下,向氨氮初始质量浓度为40mg·L-1的模拟水样中加入不同质量的杨树叶粉末,考察杨树叶投加量对吸附效果的影响。实验结果如图3所示。
由图3可知,对于同样氨氮初始浓度的水样,随着溶液中杨树叶投加量的增加,单位质量吸附剂所吸附的氨氮量均下降。这主要是由于较少的投加量提供有限的吸附点位,迫使氨氮克服杨树叶粉末表面膜的阻力进入其表面孔道:而杨树叶投加量相对较大的溶液中,吸附则仅发生在杨树叶粉末表面[12]。因此,将杨树叶粉末用于氨氮吸附中,应综合考虑去除率和单位吸附量等因素。
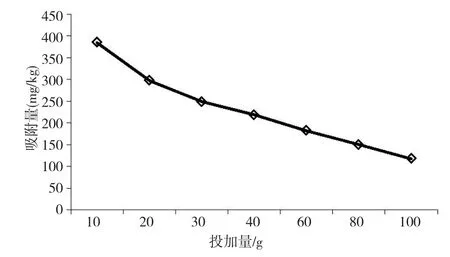
图3 杨树叶投加量对氨氮去除量的影响Fig.3 Impact of poplar leaves dosage on ammonia removal
2.4 杨树叶对氨氮的等温吸附
描述吸附过程,常用Langumuir[公式(6)、(7)]和Freundlich[公式(8)、(9)]等温吸附模型。利用这2个等温吸附模型对杨树叶吸附氨氮过程进行研究。


式中:qe为平衡时的吸附量,mg·kg-1;Ce为吸附平衡时溶液浓度,mg·L-1;qm为最大吸附量mg·kg-1;KL为Langmuir等温吸附方程式常数。


式中qe、Ce与前相同,KF、n为Freundlich 等温吸附常数。
利用Langmuir 等温吸附模型对实验数据进行拟合,即以Ce为横坐标,Ce/qe为纵坐标作图(图4)。经拟合计算得最大吸附量qm=625mg·kg-1,Langmuir系数KL=0.0258,相关性系数R2=0.9934,相关性良好。
利用Freundlich等温吸附模型对实验数据进行拟合分析,即以lnqe对lnCe作图(图5)。计算得出Freundlich 等温吸附常数KF=40.51L·kg-1,1/ n=0.5375,相关性系数R2=0.9863。一般认为,在1/ n=0.1~0.5 时,容易吸附;1/n>2 时,则较难吸附。杨树叶吸附氨氮过程中1/n=0.5375,处于低值范围,说明杨树叶对氨氮的吸附比较容易进行。
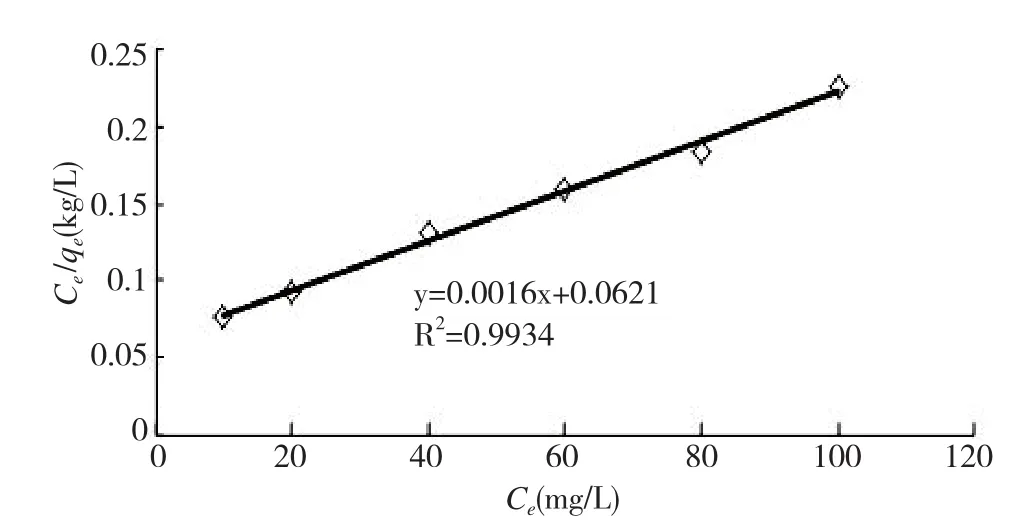
图4 Langmuir 模型的吸附等温线
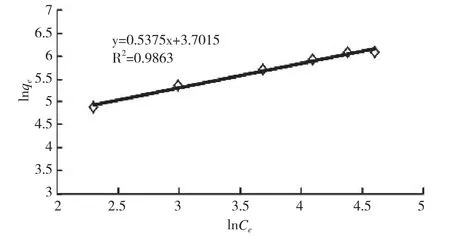
图5 Freundlich 模型的吸附等温线Fig.5 Freundlich adsorption isotherm model
3 结论
杨树叶粉末对氨氮有明显的吸附效果,随着初始浓度的升高,单位吸附量显著增加。在pH 为3~11 范围内,杨树叶对氨氮的吸附量变化不大。在同样的初始浓度下,随着杨树叶粉末投加量的增大,对氨氮的单位吸附量明显降低。Langmuir和Freundlich等温吸附模型均能较好地用于描述杨树叶粉末对氨氮的吸附特征。利用Freundlich等温吸附模型对实验数据进行分析,得出1/n接近0.5,说明杨树叶粉末对氨氮的吸附是容易和有效的。
[1] 胡晓镭.湖、库富营养化机理研究综述[J].水资源保护,2009,25(4):44-47.
[2] 易仲强,刘德富.富营养化湖库生态恢复研究探讨[J].中国农村水利水电,2010(6):26-29.
[3] Carpenter S R, Christensen D L, Cole J J, et al. Biological control of eutrophication in lakes. Environmental Science & Technology, 1995(29): 784-786.
[4] Dodds W K, Bouska W W, Eitzmann J L, et al. Eutrophication of U.S. freshwaters: analysis of potential economic damages. Environmental Science & Technology, 2009, 43(1): 12-19.
[5] 孟庆义.国内湖泊水质污染及富营养化治理[J].北京水利,2001(5):45-47.
[6] 许海,刘兆普,焦佳国,等.太湖上游不同类型过境水氮素污染状况[J].生态学杂志,2008,27(1):43-49.
[7] 李纯英.杨树在农防林建设和林产业发展中的地位与作用[J].内蒙古林业,2008(2):6-7.
[8] 氨氮的测定 苯酚次氯酸盐法 水中氨氮的测定[J].环境科学丛刊,1980(Z1):69-70.
[9] 张爱莉,朱义年,纪锐琳,等.竹炭对氨氮的吸附性能及其影响因素的研究[J].环境科学与技术,2008,31(6):19-21.
[10] 张华,张学洪,白少元,等.柚皮活性炭对氨氮吸附性能研究[J].工业水处理,2012,32(6):56-59.
[11] 陈建秋,杨轲,胡志军,等.桔皮吸附水中残杀威的研究[J].环境工程学报,2010(7):1488-1492.
[12] 王祝来,陈玉峰,周琼,等.竹炭对水溶液中氨氮的吸附特性研究[J].工业用水与废水,2009,40(4):70-73.
Adsorption Performance Study of Poplar Leaves Powder on Ammonia Nitrogen
HE Rui, JING Zhao-qian, YANG Kai-hua, MAO Jian, DONG Xiang-yun, CHEN Shuo
(College of Civil Engineering, Nanjing Forestry University, Nanjing 210 037, China)
Dry poplar leaves powder was used to investigate the adsorption properties of ammonia nitrogen in water. The results showed that the variation of pH had little inf uence on ammonia nitrogen adsorption. At the same initial ammonia concentration, unit adsorption capacity decreased obviously with dosage increased, and unit adsorption capacity increased with initial concentration rose. The adsorption isotherm of ammonia adsorption on poplar leaves powder followed Langmuir and Freundlich isotherm model.
poplar leaves; ammonia; adsorption; isotherm.
文献标识码:A
1671-9905(2015)03-00 -
2013年国家级大学生创新创业训练计划项目(201310298031);人社部2013年度留学回国择优资助项目;江苏省“十二五”重点建设专业资助项目
何瑞(1993-),男,主要从事给排水工程技术研究
荆肇乾(1975-),男,博士,副教授,E-mail:carljing@163.com,电话:025-85427691;13915967569
2015-01-12
