布地奈德吸入剂及其联合口服缓释茶碱治疗支气管哮喘的效果
2015-01-12刘广杰罗秀芳
刘广杰 胥 杰 罗秀芳
首都医科大学附属北京同仁医院呼吸内科,北京100730
布地奈德吸入剂及其联合口服缓释茶碱治疗支气管哮喘的效果
刘广杰 胥 杰 罗秀芳
首都医科大学附属北京同仁医院呼吸内科,北京100730
目的探讨布地奈德干粉吸入剂联合茶碱在支气管哮喘治疗中的效果及安全性。方法收集2011年1月~2014年12月于首都医科大学附属北京同仁医院门诊就诊的支气管哮喘患者76例,分为布地奈德干粉吸入剂组(Ⅰ组)37例和布地奈德吸入剂和茶碱联合用药组(Ⅱ组)39例。观察哮喘控制测试评分(ACT)、检测肺功能、药物不良反应,评估Ⅰ、Ⅱ组治疗前后效果。结果治疗后Ⅰ、Ⅱ组患者的临床症状均得到明显改善,两组治疗后哮喘控制率(Ⅰ组:86.5%,Ⅱ组:97.4%)、ACT评分[Ⅰ组:(23.2±3.2)分,Ⅱ组:(24.3±1.6)分]、最大呼气流量占预计值的百分比(PEF%预计值)[Ⅰ组:(88.3±6.9),Ⅱ组:(95.2±7.8)%]、第1秒用力呼气容积占预计值的百分比(FEV1%预计值)[Ⅰ组:(78.2±6.0)%,Ⅱ组:(83.9±6.0)%],分别较治疗前各指标[哮喘控制率:Ⅰ组18.9%、Ⅱ组17.9%,ACT评分:Ⅰ组(15.9±3.2)分、Ⅱ组(16.0±3.2)分,PEF%预计值:Ⅰ组(70.1±6.6)%、Ⅱ组(68.9±6.8)%,FEV1%预计值:Ⅰ组(68.1±6.4)%、Ⅱ组(69.1±5.4)%]明显改善,差异均有高度统计学意义(P<0.01)。治疗后,Ⅱ组哮喘控制率高于Ⅰ组,差异有统计学意义(P<0.05);Ⅱ组肺功能指标PEF%预计值、FEV1%预计值均优于Ⅰ组,差异均有高度统计学意义(P<0.01)。两组在治疗中均无严重不良反应发生。结论布地奈德干粉吸入治疗和布地奈德干粉吸入剂联合茶碱治疗哮喘均具有良好的效果和安全性,且布地奈德干粉吸入剂和茶碱联合治疗的疾病控制率更高,改善病情更快,疗效更好。
哮喘;茶碱;糖皮质激素;肺功能
支气管哮喘,简称哮喘,是以可逆性气流阻塞为特点、伴有气道高反应的慢性气道炎症性疾病,其病理机制为在各种刺激因子(如特异性过敏原、非特异性因素、感染等)作用下产生气道高反应,并在炎症细胞、炎症因子等介导下发生的慢性气道疾病。其特征是具有反复性发作及可逆性支气管收缩,临床症状以咳嗽、喘息、胸闷、呼吸困难为主,病理改变主要是气道炎症和平滑肌痉挛。哮喘治疗不当可致病程延长最终导致气道重塑、气道不可逆性缩窄[1]。糖皮质激素是控制哮喘最有效的药物,布地奈德吸入剂为糖皮质激素干粉吸入剂,茶碱因其具有抗感染、扩张支气管作用,为临床治疗哮喘的常用药,而茶碱缓释片具有服用后血药浓度平稳、能较长时间维持平喘作用、不良反应较少等优点[2-3]。本研究探讨应用布地奈德干粉吸入剂及其联合茶碱缓释片对中度哮喘临床症状的控制、哮喘基本控制率及其安全性等方面的影响,为哮喘临床治疗提供参考。
1 资料与方法
1.1 一般资料
选择2011年1月~2014年12月首都医科大学附属北京同仁医院门诊就诊的哮喘患者76例,诊断依照中华医学会呼吸病学分会哮喘学组制订的诊疗标准。并排除:治疗前使用糖皮质激素(4周)或有激素依赖病史,治疗前有茶碱类药物服用史(2周),心、肝、肺、肾功能异常者,患有内分泌代谢性疾病等各类慢性疾病,患有精神系统异常及惊厥等神经系统疾病者,患有未经控制的消化性溃疡,孕妇或哺乳期妇女,患肺结核、青光眼和白内障,对布地奈德、茶碱类药物过敏。76例患者中男39例,女37例,均为哮喘非急性发作期患者。将患者分布地奈德干粉吸入剂组(Ⅰ组)37例和布地奈德吸入剂和茶碱联合用药组(Ⅱ组)39例,其中Ⅰ组:男19例,女18例,年龄(34.8± 10.8)岁;Ⅱ组:男20例,女19例,年龄(35.1±11.5)岁。Ⅰ、Ⅱ组患者在年龄、性别、肺功能[最大呼气流量占预计值的百分比(PEF%预计值),第1秒用力呼气容积占预计值的百分比(FEV1%预计值)]一般资料比较,差异无统计学意义(P>0.05),具有可比性。见表1。

表1 Ⅰ、Ⅱ组患者一般情况
1.2 治疗方法
日常治疗吸入糖皮质激素,剂量含布地奈德100μg/吸(阿斯利康公司生产)。茶碱缓释片,0.1 g/片,24片/盒。Ⅰ组给予布地奈德干粉吸入剂,早、晚各1次,每次2吸,吸入完后用清水漱口。不适时可按需使用短效β2受体激动药。Ⅱ组给予上述布地奈德吸入剂及茶碱缓释片0.1~0.2 g/次,每日2次口服。疗程均为12周。
1.3 观察指标
①临床症状:采用哮喘控制测试(ACT)评分评估哮喘控制的程度,完全控制:ACT评分为25分,部分控制:ACT评分为20~<25分,未控制:ACT评分<20分,控制率=(完全控制+部分控制)/总例数×100%。②肺功能测定:治疗前后测定肺功能,观察最大呼气流量(PEF)、第1秒用力呼气容积(FEV1)。③通过治疗前后对心肌酶、肝肾功能检测以及其他不良反应评定,分析用药安全性。
1.4 统计学方法
采用采用统计软件SPSS 13.0对数据进行分析,正态分布计量资料以均数±标准差(x±s)表示,两组间比较采用t检验;计数资料以率表示,采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组治疗前,治疗4、8、12周后哮喘控制率及ACT评分比较
两组治疗4、8、12周后哮喘控制率评分及ACT与治疗前比较均有明显改善,差异均有高度统计学意义(P<0.01)。治疗12周,Ⅱ组哮喘控制率明显高于Ⅰ组,差异有统计学意义(P<0.05)。治疗4、8、12周,Ⅱ组ACT评分均高于Ⅰ组相应时间点的ACT评分,且在治疗8、12周两组ACT评分比较,差异有统计学意义(P<0.05)。见表2。

表2 两组治疗前,治疗4、8、12周后哮喘控制率及ACT评分比较
2.2 两组治疗前、后肺功能指标比较
Ⅰ、Ⅱ组治疗后肺功能指标(PEF%预计值、FEV1%预计值)均较治疗前明显改善,差异均有高度统计学意义(P<0.01)。治疗后,Ⅱ组PEF%预计值、FEV1%预计值均优于Ⅰ组,差异均有高度统计学意义(P<0.01)。见表3。
表3 两组治疗前后肺功能指标比较(%,±s)
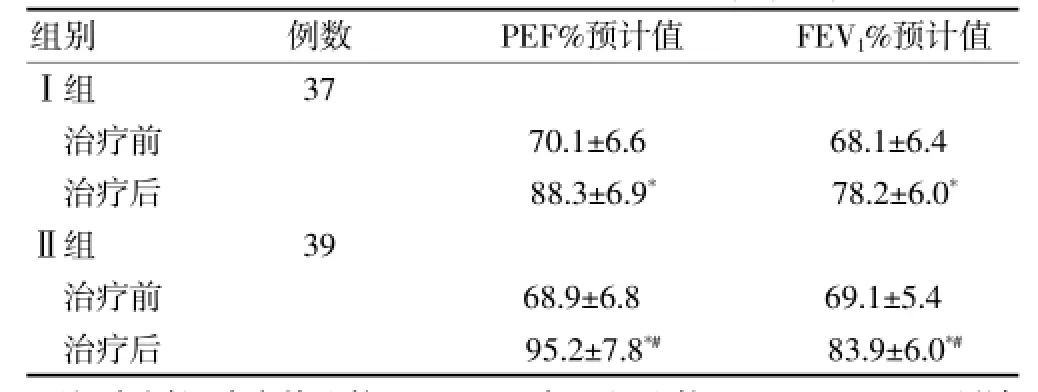
表3 两组治疗前后肺功能指标比较(%,±s)
注:与同组治疗前比较,*P<0.01;与Ⅰ组比较,#P<0.01;PEF%预计值:最大呼气流量占预计值的百分比;FEV1%预计值:第1秒用力呼气容积占预计值的百分比
组别例数PEF%预计值FEV1%预计值Ⅰ组治疗前治疗后Ⅱ组治疗前治疗后37 70.1±6.6 88.3±6.9*68.1±6.4 78.2±6.0*39 68.9±6.8 95.2±7.8*#69.1±5.4 83.9±6.0*#
2.3 两组不良反应情况
治疗12周,76例患者均未见心肌酶和肝肾功能明显异常,Ⅰ组咽部不适6例,恶心1例,共7例(18.9%),Ⅱ组咽部不适4例,恶心2例,恶心伴轻微心悸1例,共7例(17.9%),无其他不良反应。两组不良反应发生率比较,差异无统计学意义(P>0.05)。
3 讨论
支气管哮喘是由气道肥大细胞、嗜酸性粒细胞、T淋巴细胞等炎性细胞和气道上皮细胞及平滑肌细胞等结构细胞及相关细胞因子作用引起的气道炎症性疾病。气道炎症能够引起气道高反应性及可逆性气流受限,从而导致患者出现胸闷、喘息及气促等临床症状,严重可出现窒息;另外,支气管哮喘可导致肺功能下降,如治疗控制不当,可逐步发展产生气道重塑进而产生不可逆性气道缩窄,亦可引起呼吸衰竭而危及患者生命。所以,采取合适的药物进行治疗控制对支气管哮喘患者具有重要意义。目前临床上,主要采用低剂量糖皮质激素以及联合其他支气管扩张药物如茶碱、β2受体激动等进行治疗[4-7]。
茶碱是经典的平喘药物,研究表明,茶碱类药物作用机制表现为扩张支气管平滑肌作用;抗炎及免疫调节作用;增强呼吸肌作用;茶碱有强心、利尿和扩张冠脉作用。茶碱类药物同时具有扩张支气管和抗炎作用,两种作用的叠加对哮喘治疗起到重要作用。有研究表明,茶碱在哮喘治疗中的抗炎作用机制与激素不同[8-10],因此推断地奈德吸入联合茶碱在抗炎方面可能存在协同作用。另一方面,茶碱具有扩张支气管平滑肌、平喘、促进纤毛运动及黏液排除等作用,因此糖皮质激素联合使用茶碱可通过其在抗炎、支气管扩张方面的协同作用对哮喘的病情起到良好的控制[11-12]。
本研究显示Ⅱ组在治疗结束时,哮喘控制率、ACT评分均优于I组,差异有统计学意义(P<0.05),显示布地奈德吸入剂联合口服茶碱治疗对于改善哮喘患者的主观症状,增进哮喘临床控制具有良好的效果,其机制可能与联合茶碱治疗时在抗炎、扩张气管方面的协调作用有关,有待于进一步深入研究。
此外,肺功能检测显示,治疗结束后Ⅱ组FEV1%预计值明显改善,与Ⅰ组比较,差异有高度统计学意义(P<0.01)。显示布地奈德干粉吸入剂和茶碱联合治中度哮喘改善肺功能方面优于单独应用布地奈德吸入剂。其机制可能源于吸入糖皮质激素布地奈德联合茶碱具有的抗炎、支气管扩张的协同作用,二者具有明显的互补效应。此外,布地奈德吸入剂联合茶碱用药可较大程度达到哮喘自我管理,减少哮喘控制不良者过度使用缓解药物而抗炎治疗不足的问题。
本研究结果表明,Ⅰ、Ⅱ两组治疗后,患者哮喘基本控制率、ACT评分和肺功能到及患者生命质量评分均明显改善,绝大部分哮喘患者得以良好控制,与相关报道一致[13-15],Ⅰ、Ⅱ组治疗后均具有良好的效果和安全性,布地奈德干粉吸入剂联合茶碱用药疗效更优,为控制哮喘病情和维持长期稳定的有效方法。
[1]Bonsignore MR,Profita M,GagliardoR,et al.Advances in asthma pathophysiology:stepping forward from the Maurizio Vignola experience[J].Eur RespirRev,2015,24(135):30-39.
[2]中华医学会呼吸病学分会哮喘学组.支气管哮喘防治指南[J].中华结核和呼吸杂志,2008,31:177-185.
[3]Barnes PJ.Severe asthma:advances in currentmanagementand future therapy[J].JAllergy Clin Immunol,2012,129(1):48-59.
[4]Bruce R,Thompson JA,Douglass MJ,et al.Peripheral lung function in patients with stable and unstable asthma[J].J Allergy Clin Immunol,2013,131(5):1322-1328.
[5]Tamm M,David H,Bianca R,et al.Inhaled corticosteroid and long-actingβ2-agonist pharmacological profiles:effective asthma therapy in practice[J].RespirMed,2012,106(Suppl 1):S9-S19.
[6]Ohta K,Ichinose M,Nagase H,et al.Japanese guideline for adult asthma 2014[J].Allergol Int,2014,63(3):293-333.
[7]Smith HE,Jones CJ,Hankins M,et al.The effects of expressive writing on lung function,quality of life,medica-tion use,and symptoms in adults with asthma:a randomized controlled trial[J].Psychosom Med,2015,77(4):429-437.
[8]Ilmarinen P,Kankaanranta H.Eosinophil apoptosis as a therapeutic target in allergic asthma[J].Basic&Clinical Pharmacology&Toxicology,2014,114(1):109-117.
[9]Al-Alawi M,Hassan T,Sanjay H,et al.Advances in the diagnosis and management of asthma in older adults[J]. Am JMed,2014,127(5):370-378.
[10]Hagan JB,Samant SA,Volcheck GW,et al.The risk of asthma exacerbation after reducing inhaled corticosteroids a systematic review and meta-analysis of randomized controlled trials[J].Allergy,2014,69(4):510-516.
[11]Shukla D,Chakraborty S,Singh S,et al.Doxofylline:a promising methylxanthine derivative for the treatment of asthma and chronic obstructive pulmonary disease[J]. Expert Opin Pharmacother,2009,10(14):2343-2356.
[12]Boonsawat W,BoonsawatW,Thinkham rop B.Evaluation of asthma control by inhaled corticosteroids in general practice in Thailand[J].Asian Pac JAllergy Immunol,2015,33(1):21-25.
[13]Marcus P,Oppenheimer EA,Patel PA,et al.Use of nebulized inhaled corticosteroids among older adult patients:an assessment of outcomes[J].Ann Allergy Asthma Immunol,2006,96(5):736-743.
[14]Pandya D,Puttanna A,Balagopal V.Systemic effectsof inhaled corticosteroids:an overview[J].Open Respir Med J,2014,8:59-65.
[15]Dubuis E,Wortley MA,Grace MS,et al.Theophylline inhibits the cough reflex through a novelmechanism of action[J].JAllergy Clin Immunol,2014,133(6):1588-1598.
Effects of therapy of Budesonide powder for inhalation com bined w ith Theophylline on bronchial asthm a
LIUGuangjie XU Jie LUO Xiufang
Department of Respiratory Medicine,Beijing Tongren Hospital,Capital Medical University,Beijing 100730,China
Ob jective To explore the therapeutic efficacy and therapy safety of Budesonide powder for inhalation combined with Theophylline on bronchial asthma.M ethods From January 2011 to December 2014,in Outpatient Service of Beijing Tongren Hospital,Capital Medical University,76 bronchial asthma patients were divided into Budesonide powder for inhalation group(groupⅠ)with 37 patients and Budesonide powder for inhalation combined with Theophylline group(groupⅡ)with 39 patients.Asthma control test(ACT)scores,lung function(PEF%pre,FEV1%pre)and adverse drug reaction were observed,effect before and after the treatment were evaluated.Results Aftertreatment,clinical symptomsof patients in two groupswere improved significantly,the ratio of asthma control(groupⅠ:86.5%,groupⅡ: 97.4%),ACT scores[groupⅠ:(23.2±3.2)scores,groupⅡ:(24.3±1.6)scores],PEF%pre[groupⅠ:(88.3±6.9)%,groupⅡ:(95.2±7.8)%],FEV1%pre[groupⅠ:(78.2±6.0)%,groupⅡ:(83.9±6.0)%]were improved significantly than those before the treatment[ratio of asthma control:groupⅠ18.9%,groupⅡ17.9%;ACT scores:groupⅠ(15.9±3.2)scores, groupⅡ(16.0±3.2)scores,PEF%pre groupⅠ(70.1±6.6)%,groupⅡ(68.9±6.8)%;FEV1%pre:groupⅠ(68.1±6.4)%, groupⅡ(69.1±5.4)%],the differenceswere statistically significant(P<0.01).After the treatment,ratio of asthma control in groupⅡwas higher than that in groupⅠ,the difference was statistically significant(P<0.05);PEF%pre, FEV1%pre in groupⅡwere better than those in groupⅠ,the differenceswere statistically significant(P<0.01).No severe adverse drug reaction were observed in both groups.Conclusion The clinical therapeutic efficacy and safety for moderate asthma treatment are determined in both two ways of the Budesonide power for inhalation and Budesonide powder for inhalation combinated with Theophylline.It is more effective and rapid improvement of moderate asthma control by the way of Budesonide powder for inhalation combinated with Theophylline treatment.
Asthma;Theophylline;Glucocorticoid;Lung function
R562.25
A[文献标识码]1673-7210(2015)06(c)-0012-04
2015-03-15本文编辑:苏畅)
教育部留学回国人员科研启动基金资助项目。
