薤白多糖的硫酸化修饰及体外抗氧化活性
2015-01-08夏新奎豆成林
夏新奎,豆成林
信阳农林学院食品科学系,信阳 464000
多糖作为构成生命活动的基本物质之一,在抗肿瘤、抗炎、抗病毒、降血糖、抗衰老、抗凝血等方面均发挥着其特殊的生物活性作用。研究表明,多糖的活性直接或间接地受其分子结构的影响,采取一定的方法对多糖分子结构进行修饰,可以提高或赋予多糖更多活性、降低其毒副作用[1]。
薤白是一味传统的中药,为百合科植物小根蒜Allium macrostemon Bge.和薤Allium chinensis G.Don.的干燥鳞茎。性味辛、苦、温,有温中通阳,理气宽胸,通阳散结之功效[2]。其原植物除入药外还可食用,是卫生部2002 年公布的88 种药食两用中药材之一。现代研究证明,薤白具有抗氧化、防治动脉粥样硬化等作用。薤白中已分离得到挥发油、皂苷、含氮化合物、前列腺素等化学成分,但薤白多糖的研究报道较少。本文在前期对薤白粗多糖提取工艺、分离纯化及组成分析研究的基础上[3,4],对所得的薤白多糖纯品采用氯磺酸+吡啶法进行硫酸化修饰,用响应面设计法确定硫酸化的最佳条件,并对修饰前后的薤白多糖清除超氧阴离子自由基、羟自由基的能力进行研究,旨在选出硫酸化的最佳条件,为薤白多糖药物及功能性食品开发提供理论依据。
1 材料与方法
1.1 材料与仪器
薤白粗多糖及分级纯品:由本实验室提供。利用水溶醇沉法得薤白粗多糖(PAM),经DEAE-纤维素柱层析和SephadexG-150 柱层析得薤白多糖的三种级分(PAM-Ib、PAM-IIa、PAM-III’)[3,4]。
电热恒温水溶槽:北京市医疗设备厂;Z323K 高速冷冻离心机:德国HERML 公司;752 紫外可见分光光度计:上海精密科学仪器有限公司。
氯磺酸、吡啶、硫酸钾、邻二氮菲、邻苯三酚、三羟甲基氨基甲烷(Tris),以上试剂均为国产分析纯。
1.2 实验方法
1.2.1 硫酸化修饰条件设计
根据文献报道,试剂比例、反应温度和反应时间对修饰的影响较大[5],因此,在单因素试验的基础上,根据Box-Benhnken Design 中心组合试验设计原理,以试剂比例(A)、反应温度(B)和反应时间(C)为自变量,产物的硫酸根取代度(DS)为响应值,设计三因素三水平的响应面分析试验,以确定硫酸化修饰的最佳工艺条件。因素水平如表1。

表1 试验因素水平表Table 1 Factors and levels of response surface analysis
1.2.2 硫酸化试剂的制备
在带有搅拌装置和冷凝装置的250 mL 三颈烧瓶中加入预冷的无水吡啶,并将烧瓶置于冰盐浴中,较为剧烈地不停搅拌,再将氯磺酸按照表1 的比例逐滴缓慢加入(40 min 内完成)。滴加完毕后撤去冰盐浴,将酯化试剂于-20 ℃封存备用。
1.2.3 硫酸化操作
精确称取500 mg 薤白多糖(PAM),分散于30 mL 无水甲酰胺中制成薤白多糖悬液,室温下加入酯化试剂,按表1 设定的反应温度和反应时间在水浴中搅拌反应。反应结束后取出烧瓶冷却至室温,然后加入预冷的100 mL 冰水中,用1 mol/L 的NaOH 溶液中和至pH 7.5。加入四倍体积的无水乙醇,4 ℃静置过夜、过滤,将沉淀对自来水透析3 d,蒸馏水透析1 d。透析液再用四倍体积的无水乙醇沉析,沉淀经低温真空干燥得到硫酸酯化薤白多糖衍生物(sPAM)。
1.2.4 产物的硫酸根取代度测定
用硫酸钡比浊法[6]测定各种修饰产物的硫酸根质量分数。
标准曲线的绘制:配制1.0 mol/L 硫酸钾标准溶液,并吸取一系列不同体积的硫酸钾标准溶液于试管中,补充蒸馏水使其体积为10 mL,然后加入10 mL 0.18 mol/L 盐酸溶液、1 mL 0.5%明胶溶液,充分振荡混匀,迅速加入2 mL 氯化钡-明胶溶液(10 g氯化钡溶于100 mL 0.5%明胶溶液中),振荡混匀,室温放置20 min 后以蒸馏水为参比,于360 nm 处测定吸光值。以硫酸根量为横坐标,吸收值为纵坐标,绘制标准曲线。
样品取代度的测定:测定薤白多糖硫酸酯化衍生物中硫酸基含量时,取样品10 mg 用蒸馏水溶解后加一定体积的浓盐酸至HCl 浓度为3 mol/L,封口,100 ℃水解6 h,冷却,减压旋转蒸干,再用少量水溶解后再次减压旋转蒸干,重复几次后,用超纯水将残留物溶解并定容于10 mL 容量瓶中,取此样液50 μL,按照标准曲线方法测定。根据标准曲线计算硫酸基含量并根据以下公式计算取代度:

式中S%为硫酸基百分含量。
1.2.5 薤白多糖硫酸化修饰前后体外抗氧化活性测定
1.2.5.1 对·OH 的清除率的测定(H2O2/Fe2+体系法[7])
将各多糖样品配成浓度为4 mg/mL 的溶液。取6 支试管,分别加入0.75 mmol/L 邻二氮菲溶液1 mL,150 mmol/L pH 7.4 PBS 1.5 mL,充分混匀后。加入0.75 mmol/L FeSO4溶液1 mL,每加1 管立即混匀,然后向其中一管加入0.01% H2O21 mL(损伤),另一管不加H2O2(未损伤),以蒸馏水补充体积,37 ℃保温60 min 后,以磷酸盐缓冲液为参比,分别测536 nm 时吸收值,得A损伤与A未损伤。其余4 管分别加入一定的各多糖溶液(每次所加的体积不同),混匀,再分别加入0.01% H2O21 mL,37 ℃保温60 min 后以同浓度的多糖液作参比,测536 nm时的吸收值,即得A样。重复5 次,以下式计算·OH清除率:
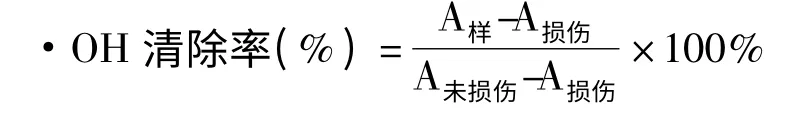
1.2.5.2 对O-·2的清除率的测定(邻苯三酚自氧化法[8])
取4.5 mL pH8.2 50 mmol/L Tris-HCl 缓冲液,4.5 mL 蒸馏水,混匀后在25 ℃预热过的邻苯三酚0.3 mL(以10 mmol/L HCl 配制,空白管用10 mmol/L HCl 代替邻苯三酚的HCl 溶液),迅速摇匀后倒入比色杯,325 nm 下每隔30 s 测定吸光度,计算线性范围内每分钟吸光度的增加。在加入邻苯三酚前,先加入一定体积的多糖溶液,蒸馏水减少,然后按下述方法计算清除率。

其中:△Ao 为邻苯三酚自氧化速率,△A 为加入多糖溶液后邻苯三酚的自氧化速率,单位均为吸光度每分钟的增加值。
2 结果与分析
2.1 标准曲线方程的建立
根据1.2.4 节方法进行试验,结果建立的S 含量(X)和吸光度(Y)标准曲线回归方程为:Y=2.4852X+0.0013,R2=0.9986。
2.2 响应面优化试验
在单因素试验的基础上,根据Box-Benhnken Design 中心组合试验设计原理,以试剂比例(A)、反应温度(B)和反应时间(C)为自变量,产物的硫酸根取代度(DS)为响应值,设计三因素三水平的响应面分析试验,试验设计及结果如表2。
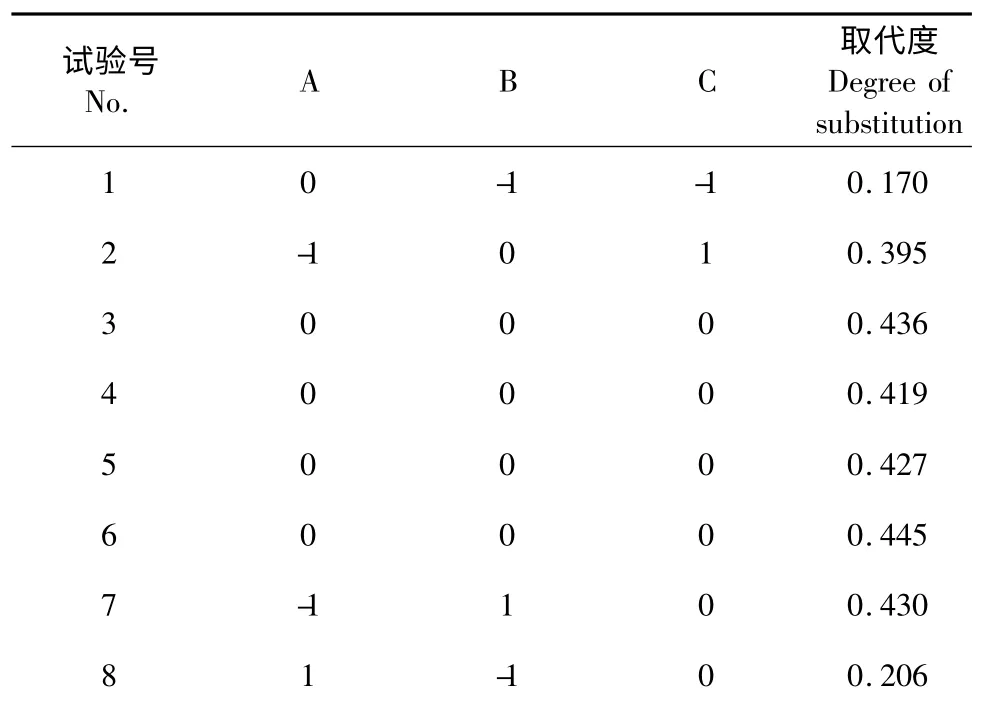
表2 响应面分析试验设计及结果Table 2 The results of RSM

2.2.1 回归方程的建立
利用Design Expert 8.0.5.0 软件对表2 数据进行多元回归拟合,得到硫酸化薤白多糖的硫酸根取代度(DS)对氯磺酸∶吡啶(v ∶v)(A)、反应温度(B)、反应时间(C)的回归方程为:

方差分析结果见表3。由表3 可知,模型P 值小于0.0001,表明该模型方程高度显著;不同处理间的差异显著,说明该方法是准确可靠的,使用该方程模拟真实的三因素三水平分析可行。失拟性检验结果表明,失拟不显著(P=0.1782),说明未知因素对试验结果干扰很小,该回归模型比较理想,可信度较高。R2Adj=0.9822,说明建立的模型能够解释98.22%响应值的变化,能很好的描述各因素对薤白多糖硫酸根取代度的变化规律。因此,该模型能准确地模拟各因素对硫酸根取代度的影响。
由表3 可以看出,各因素对试验结果的影响排序为B >A >C,即反应温度对薤白多糖硫酸根取代度的影响最大,其次为氯磺酸∶吡啶(v∶v),反应时间影响最小。因素A、B 对薤白多糖多糖硫酸根取代度的影响极显著(P<0.01),C 对薤白多糖硫酸根取代度的影响显著(P<0.05),AB、A2、B2、C2对薤白多糖硫酸根取代度的影响显著(P<0.05),AC、BC 对薤白多糖硫酸根取代度的影响不显著(P>0.05)。表明试验因素对响应值的影响不是简单的线性关系,二次项对响应值也有很大的影响。
采用Design Expert 8.0.5.0 软件作出3 个因素之间的响应曲面图如图1 所示。

表3 方差分析表Table 3 Analysis of variance

图1 氯磺酸:吡啶与反应温度(A)、氯磺酸:吡啶与反应时间(B)及反应温度与反应时间(C)对取代度影响的响应曲面图Fig.1 Response surface plots showing the effects of chlorosulfonic acid to pyridine ratio and reaction temperature (A),chlorosulfonic acid to pyridine ratio and reaction time (B)and reaction temperature and reaction time (C)on the DS
2.2.2 模型的优化和验证
利用Design Expert 8.0.5.0 软件进行优化,薤白多糖硫酸化修饰的最佳条件为:氯磺酸∶吡啶=1∶3,反应温度63.45 ℃,反应时间2.07 h,在此条件下硫酸根取代度为0.474。根据实际操作的方便情况,选择氯磺酸∶吡啶=1∶3,反应温度65 ℃,反应时间2 h,此条件下硫酸根取代度为0.470,与预测值接近,说明该模型可以很好地预测薤白多糖硫酸化条件与硫酸根取代度之间的关系。同时也证明了响应面优化法优化薤白多糖硫酸化修饰条件的可行性。
2.3 薤白多糖硫酸化修饰产物的体外抗氧化活性
2.3.1 薤白多糖硫酸化修饰前后对·OH 的清除作用
薤白多糖及各组分硫酸化修饰前后对·OH 的清除影响如表4。

表4 薤白多糖硫酸化修饰前后对·OH 的清除的影响Table 4 Scavenging effect of PAM and sPAM on ·OH
从表4 可以看出,薤白多糖硫酸化修饰后对H2O2/Fe2+体系通过Fenton 反应产生的·OH 清除率都有所提高,尤其是对PAM-IIa 影响最大。PAMIIa 修饰前几乎没有清除·OH 的作用(清除率0.08%),但硫酸化修饰后清除率提高到11.26%,说明硫酸化修饰可改变或增加多糖的生物学活性。
表5 薤白多糖硫酸化修饰前后对 的清除的影响Table 5 Scavenging effect of PAM and sPAM on

表5 薤白多糖硫酸化修饰前后对 的清除的影响Table 5 Scavenging effect of PAM and sPAM on
由表5 可以看出,薤白多糖硫酸化修饰后对邻苯三酚自氧化过程中产生的的抑制作用均有所提高,尤其对PAM-IIa、PAM-III’影响最大。PAMIIa、PAM-III’修饰前对几乎没有清除作用,但硫酸化修饰后清除效果明显,说明薤白多糖硫酸化修饰可提高其体外抗氧化性。
3 结论
本试验采用氯磺酸-吡啶法对薤白多糖进行硫酸化修饰,并通过响应面优化试验研究了各因素对取代度的影响和最优工艺条件。各因素对试验结果的影响排序为B >A >C,即反应温度对薤白多糖硫酸根取代度的影响最大,其次为氯磺酸∶吡啶(v∶v),反应时间影响最小,得到硫酸化修饰的最优工艺条件为:氯磺酸∶吡啶=1∶3,反应温度65 ℃,反应时间2 h,此条件下硫酸根取代度为0.470,与预测值接近,说明该模型可以很好地预测薤白多糖硫酸化条件与硫酸根取代度之间的关系。同时也证明了响应面优化法优化薤白多糖硫酸化修饰条件的可行性。
体外抗氧化试验表明,薤白多糖硫酸化修饰后清除·OH、O-·2 的能力明显提高,说明薤白多糖硫酸化修饰可改变或增加其生物学活性,为薤白多糖硫酸化产物在保健因子、功能性食品或药品领域的应用提供理论依据,在实践中具有指导意义。
1 Li YH(李玉华),Wang FS(王凤山),He YL(贺艳丽).Research status of the chemical modification methods of pol-ysaccharides.Chin J Biochem Pharm(中国生化药物杂志),2007,28:62-65.
2 Editorial Group of Chinese Medicine Citing(中药辞海编审组).Chinese Medicine Citing(中药辞海).Beijing:Chinese Medical Science and Technology Press,1997.
3 Xia XK(夏新奎),Yang HX(杨海霞),Li C(李纯),et al.Study on the extraction technology of polysaccharide from Allium macrosttemon Bge.J Anhui Agric Sci(安徽农业科学),2006,34:4403-4405.
4 Xia XK(夏新奎),Yang HX(杨海霞),Li C(李纯),et al.Study on extraction,purification and component of polysaccharide from Allium macrosttemon Bge.Sci Technol Food Ind(食品工业科技),2010,1:244-247.
5 Lu Y(卢宇),Hu YL(胡元亮),Sun JL(孙峻岭),et al.Optimization of sulfated modification conditions in epimedium polysaccharide.Chin Tradit Herb Drugs(中草药),2008,39:357-359.
6 Huang XY(黄小燕),Kong XF(孔祥峰),Wang DY(王德云),et al.Research progress on sulfating modification of polysaccharides and sulfated polysaccharides.Nat Prod Res Dev(天然产物研究与开发),2007,4:328-332.
7 Jia ZS(贾之慎),Wu JM(邬建敏),Tang MC(唐孟成).Colorimetric determination of hydroxyl radical from Fenton reaction.Prog Biochem Biophys(生物化学与生物物理进),1996,23:184-186.
8 Cui WX(崔文新),Zhang JJ(张静静),Geng Y(耿越).Free radical scavenging qualities of several natural edible pigments.J Shandong Normal Univ,Nat Sci(山东师范大学学报,自科版),2006,21:105-107.
