向日葵盘中果胶的提取工艺条件探究
2014-12-28李亚铎王午海张广宏宁夏师范学院化学与化学工程学院宁夏固原756000
李亚铎,俞 剑,王午海,裘 超,张广宏(宁夏师范学院化学与化学工程学院,宁夏固原756000)
果胶是以原胶、果胶、果胶酸的形态广泛分布于植物的果实、根、茎、叶中的多糖类高分子聚合物,属于亲水性植物胶。果胶是细胞壁的重要组成成分之一,伴随着纤维素而存在。按其溶解性,可分为水溶性和非水溶性果胶,非水溶性果胶可溶于六偏磷酸钠溶液或无机酸溶液。天然果胶中的原果胶不溶于水,可溶于酸、碱、盐等化学试剂成为水溶性果胶。
果胶作为一种新型、天然、功能型食品添加剂,广泛用于果酱、果冻、食品包装膜以及生物培养基等领域[1]。在食品方面可用作胶凝剂、乳化剂、增稠剂、稳定剂、增香增效剂。果胶还是维持身体健康的重要物质,具有增强胃肠蠕动,促进营养吸收的功能,对防治高血压、肥胖症等病症有较好的疗效。果胶还具有成膜的特性,因此可用于造纸和纺织的施胶剂[2],如用于尿不湿,可保护婴幼儿皮肤。随着近年来研究工作的深入,果胶的用途不断被开发出来,其发展潜力巨大,具有广阔的市场前景。
全世界果胶年需求量超过2万t,我国每年消耗果胶超过2 000 t,其中80%都要依靠进口,而且需求量每年都在高速增长[3-5]。目前,我国生产果胶大多是从柑橘皮和苹果渣中提取[6-7],原料来源受季节性和生产技术的限制,不利于果胶的连续生产,使得我国果胶需求主要依靠国外进口,但进口果胶价格昂贵,所以扩大果胶产量和提高果胶生产技术水平具有巨大的市场潜力和重要意义。
宁夏固原日照时间长、昼夜温差大、干旱少雨、春暖快、秋霜迟等气候特点有利于向日葵的生长和有机质积累。于是,具有抗盐碱、耐干旱、产量高、宜栽培等特点的向日葵便成为宁南山区避灾抗旱的主栽作物之一。宁夏固原市向日葵种植面积大,大多数农民都会将向日葵盘焚烧,造成环境污染和资源浪费。如果能利用这些价格低廉、来源广泛的原材料,经过处理将其运用于食品中,不但能变废为宝,而且还提高了农民的收入。笔者通过探究向日葵盘中果胶的最佳提取工艺,为合理利用资源[8],防止污染环境,提高经济效益提供参考,具有重要的经济和社会意义。
1 材料与方法
1.1 材料 原料:自然风干向日葵盘,采自宁夏固原。主要试剂:盐酸,氢氧化钠、乙醇,均为分析纯;蒸馏水。主要仪器:粉碎机,70目筛,滴管,量筒,烧杯,电子称,pH计,表面皿,抽滤瓶,滤纸,滤布,玻璃棒,恒温水浴锅,远红外干燥箱,研钵。
1.2 方法
1.2.1 提取原理。在果胶的生产技术领域中,采用酸提取法提取果胶。其原理是利用热的酸性水溶液将植物细胞中原果胶转化成水溶性果胶,使果胶从植物转移到水相当中,形成果胶水溶液。所用的酸一般为无机酸和有机酸2种。
1.2.2 原料预处理。试验将固原自然风干向日葵盘常温下浸泡10 min左右,经过漂洗,洗去其上面的灰尘等杂质,多次清洗后,烘箱将其烘干(或自然风干),用粉碎机粉碎过筛(70目)得到干净的原料。
1.2.3 向日葵盘中果胶提取工艺流程。预处理的向日葵盘粉末用稀酸溶液水解,恒温水浴并不断搅拌,一定时间后过滤,得果胶提取液,根据其不溶于乙醇的性质,再将其沉淀、干燥即可。
主要过程为:风干的向日葵盘→预处理→称取原料10 g→加入300 ml水→蒸煮→过滤→滤液浓缩→加乙醇浸泡→抽滤→再用乙醇浸泡→抽滤(多次进行此过程)→果胶→干燥→称重。
1.2.4 具体提取过程。用电子称称取10 g处理好的向日葵盘粉末于500 ml的烧杯中,再用500 ml量筒量取300 ml水加入烧杯中,调节好溶液pH(电子pH计)。
在一定温度下进行蒸煮相应的时间,待溶液冷却至室温用滤布过滤得到滤液,滤液在一定的温度下进行浓缩至一定体积,再加入一定量的乙醇进行浸泡沉淀,过滤弃去滤液(用乙醇多次浸泡有脱色效果),待乙醇挥发殆尽,再用远红外烘箱在40℃的温度下对其进行烘干称重。
1.2.5 含量计算。将果胶置于50℃干燥烘箱中烘至质量恒定,再用电子天平称量,计算果胶提取率。
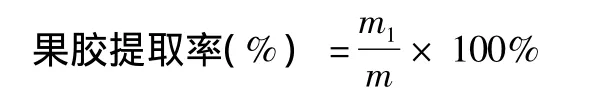
式中,m1为提取到的果胶质量(g);m为向日葵盘粉末的质量(g)。
2 结果与分析
2.1 单因素试验对向日葵盘中果胶产量的影响
2.1.1 酸性条件下pH对提取向日葵盘中果胶产量的影响。选取提取液60 ml、乙醇用量65 ml、蒸煮时间为120 min,蒸煮温度85℃,浓缩温度为70℃,比较酸度分别为0.83、1.00、1.50、2.00、2.50、3.00、4.00、5.00 时对果胶产率的影响及果胶提取率,如图1所示。
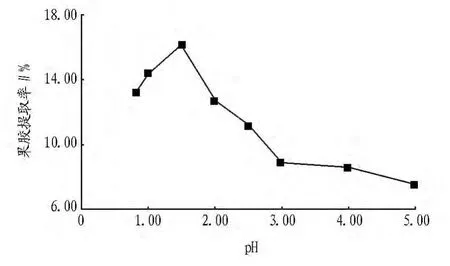
图1 酸性条件下pH对果胶提取率的影响
由图1可知,提取向日葵盘中果胶的最佳pH为1.5。当pH 1.5时,果胶的提取率最大,为16.10%;当 pH <1.0 时,果胶发生去酯反应,提取率下降;当pH>2.0时,果胶不稳定,提取率下降;当pH>3.0时,果胶会发生酯的皂化反应及β-消除反应,会诱导半乳糖醛酸残基之间的糖苷键断裂,在半乳糖醛酸C4和C5之间形成双键,并与羰基的碳氧形成共轭双键,从而果胶发生分解,导致提取率下降。
2.1.2 弱碱性条件下pH对向日葵盘中果胶产量的影响。选取提取液60 ml、乙醇用量65 ml、蒸煮时间为120 min,蒸煮温度85℃,浓缩温度为70℃,比较酸度分别为6.00、7.00、8.00、9.00、12.00、13.00、14.00 时对果胶产率的影响及果胶提取率,结果如图2所示。
由图2可见,在碱性条件下虽然能得到果胶,但是品质并不好。
2.1.3 提取时间(蒸煮时间)对向日葵盘中果胶产量的影响。选取提取液60 ml、乙醇用量65 ml、蒸煮温度85℃,浓缩温度为70 ℃、pH 为 1.5,比较蒸煮时间分别为1.0、1.5、2.0、2.5、3.0、3.5 h 时对果胶产率的影响及果胶提取率,结果如图3所示。
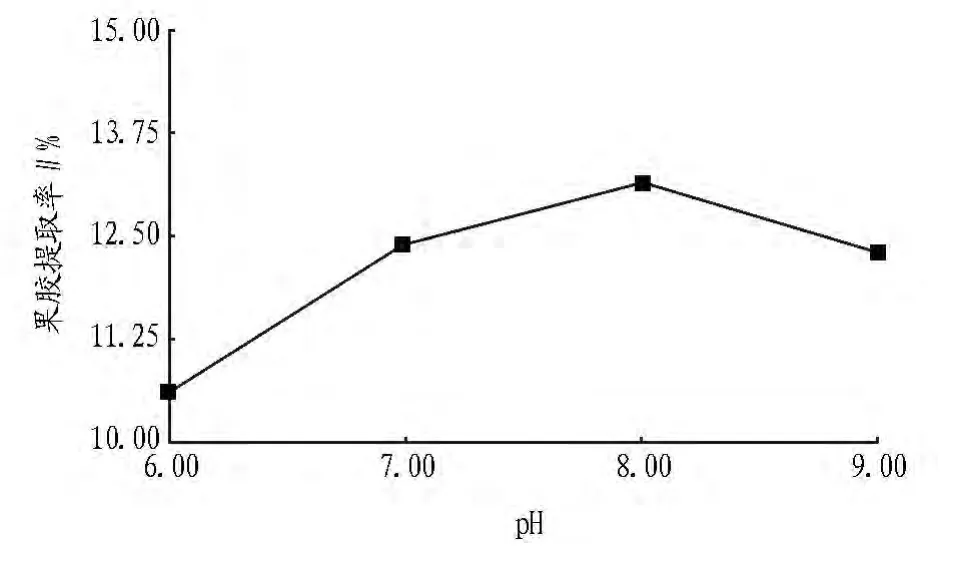
图2 弱碱条件不同pH对果胶提取率的影响
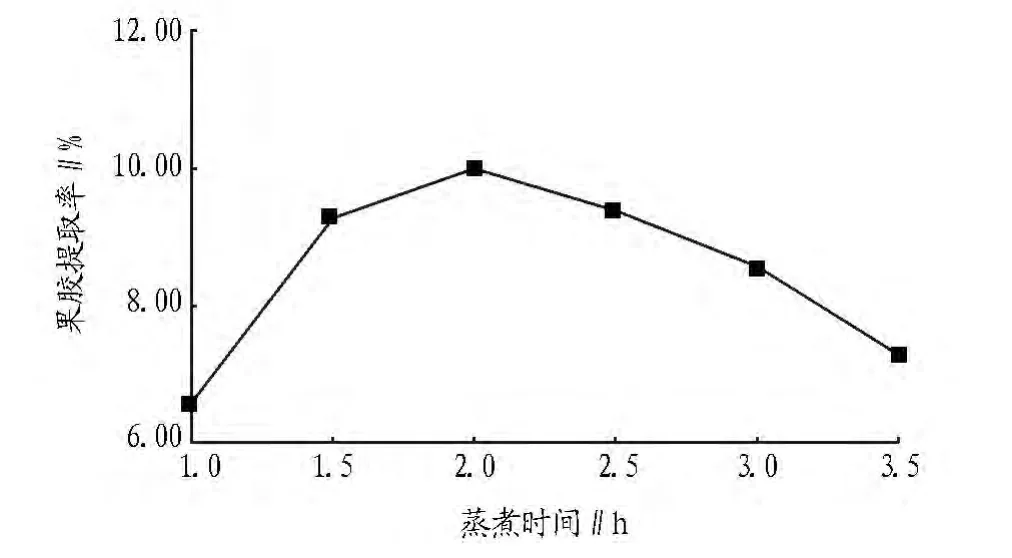
图3 不同蒸煮时间对果胶提取率的影响
由图3可知,在其他条件不变时,果胶百分含量随蒸煮时间的增长先增加达到最大值后降低。蒸煮时间为2.0 h时果胶的百分含量最高。出现这种情况的原因是蒸煮时间太短向日葵盘中果胶没有完全转化为可溶性果胶,蒸煮时间太长可溶性的果胶有可能水解为低聚糖了。
2.1.4 浓缩温度对向日葵盘中果胶产量的影响。蒸煮温度85 ℃,pH 为1.5,比较浓缩温度分别为 60、65、70、75、80、85℃时对果胶产率的影响及果胶提取率,结果如图4所示。
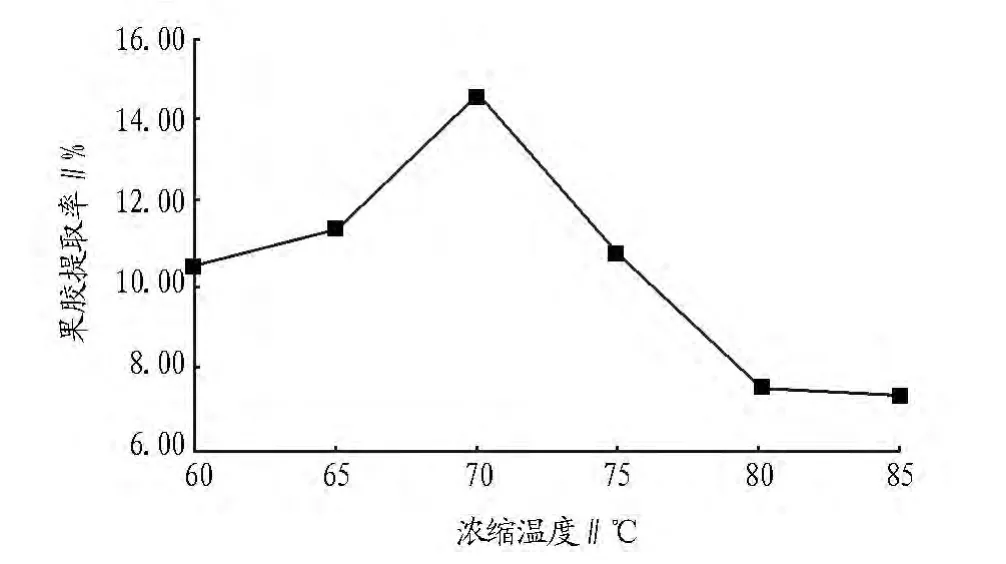
图4 不同浓缩温度对果胶提取率的影响
由图4可见,随着浓缩温度的提高,果胶提取率逐渐增加,增加到一定的温度果胶含量又降低。当浓度温度为70℃时果胶百分含量最高,浓缩温度太高会破坏果胶的结构。
2.1.5 乙醇用量对向日葵盘中果胶产量的影响。比较乙醇用量分别为40、45、50、55、60、65、70、75 ml时对果胶产率的影响及果胶提取率,结果如图5所示。
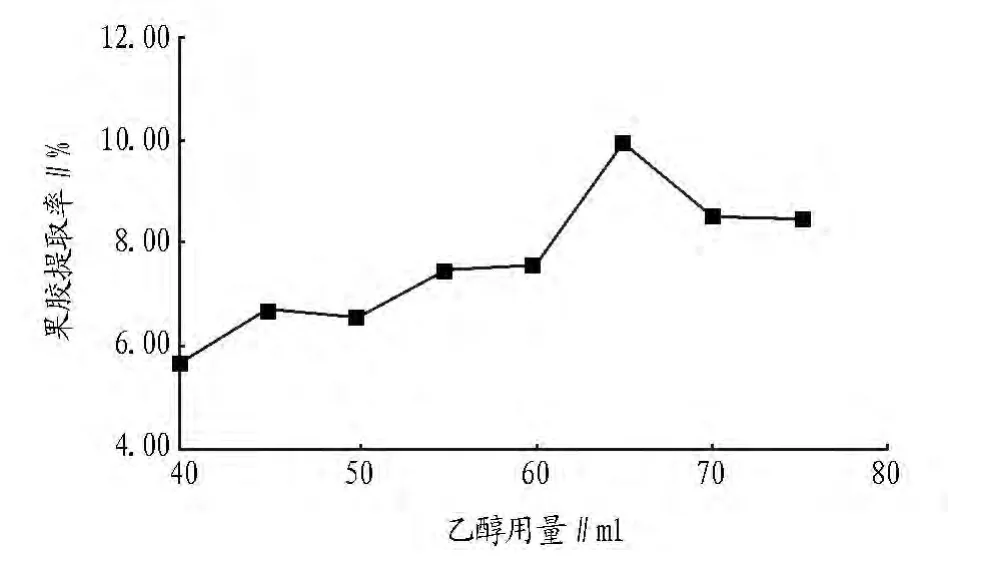
图5 不同乙醇用量对果胶提取率的影响
由图5可知,乙醇用量为65 ml时,向日葵盘中果胶提取率达到最高值。
2.2 固原向日葵盘果胶制品的理化性质 对固原向日葵盘中提取的果胶制品的理化性质指标检测,结果见表1。参照QB2484-2000国家标准[9],固原向日葵盘中提取的果胶制品的各项指标基本达到国家标准。

表1 果胶制品质量特性
3 讨论
该试验采用酸提取法以蒸煮的形式提取向日葵盘中的果胶。通过试验得知,向日葵盘中果胶的最佳提取工艺条件为蒸煮2 h、蒸煮温度为85℃、浓缩温度为70℃、提取液pH 1.5、乙醇用量为65 ml,在此条件下果胶的提取率可达16%左右。试验确定的果胶提取工艺条件是可行的,果胶质量是符合相关要求的。
经理化检验,果胶制品的总半乳糖醛酸含量为68.37%,干燥失重为7.64%,总灰分5.13%,盐酸不溶物0.93%,pH 2.18。该试验方法获得的果胶提取得率高,品质基本符合国家标准。
[1]郑志花,曹端林,李永祥.用微波加热技术从向日葵盘中提取果胶[J].华北工学院学报,2003,24(4):300 -302.
[2]田继武,刘朝良,朱保建,等.桑枝皮中果胶的提取工艺优化[J].食品科学,2011,32(16):22 -26.
[3]涂国云,王正武,王仲妮.果胶的制备与应用[J].食品与药品,2007,9(6):50 -56.
[4]WU H J.The situation and outlook of citrus processing industry in China[C].Beijing:China/FAO Citrus Symposium,2001.
[5]TEIKO M J.Citrus juice production and fresh market extension technologies[C].Beijing:China/FAO Citrus Symposium,2001.
[6]单杨.中国柑橘工业的现状、发展趋势与对策[J].中国食品学报,2008,8(1):1 -8.
[7]潘小芳,黄慰生,胡东红.永春柑桔皮提取果胶的研究[J].泉州师范学院学报:自然科学版,2001,19(4):36 -39.
[8]李巧玲.果胶的提取[J].食品研究与开发,2002,23(3):16 -17.
[9]刘莲芳,柴正荣.QB 2484-2000,食品添加剂果胶[S].北京:中国轻工业出版社,2000.
