生物质基平台化合物糠醛的研究进展
2014-12-23欧阳洪生肖竹钱蒋成君方晟毛建卫
欧阳洪生,肖竹钱,蒋成君,方晟,毛建卫
(1.浙江省农产品化学与生物加工技术重点实验室,浙江 杭州 310023;2.浙江科技学院 生物与化学工程学院,浙江 杭州 310023;3.浙江工业大学 化学工程学院,浙江 杭州 310014;4.绍兴文理学院 元培学院,浙江 绍兴 312000 )
非再生资源的大量消耗,以及人类对能源日益增长的需求,使得发掘再生生物质资源制备新型的平台化合物尤为迫切。糠醛是一种可由生物质转化制备的重要化工原料,它的分子式含有呋喃环和醛基,可以发生氢化、氧化、氯化、硝化和缩合等反应,主要衍生产物有糠醇、四氢糠醇、四氢呋喃、呋喃、呋喃丙烯酸、糠酸、糠酸乙酯和丁二酸,目前由其衍生出的化工产品可达1 600 多种。因此,对糠醛的研究及开发其下游产品,具有深远的现实意义。本文介绍了糠醛作为潜在的生物燃料平台化合物,木质纤维素在生产糠醛时面临的挑战,糠醛经加氢和酸碱催化反应转化为生物燃料的过程,并讨论了完整的呋喃生物燃料价值链。体,有苦杏仁的味道,在空气中易被氧化变成黄棕色,需密封保存,能溶解于多种有机溶剂。糠醛与水互溶,且两相组成随温度不同而变化。糠醛物性见表1。

表1 糠醛物性Table 1 Physical properties of furfural
1 糠醛物性
糠醛学名α-呋喃甲醛,是呋喃2 位上的氢原子被醛基取代的衍生物。糠醛为无色或浅黄色油状液
2 糠醛形成的原理
目前为止,糠醛只能通过生物质转化而来,生物质主要由纤维素、半纤维素、木质素组成,其中半纤维素是生产糠醛的直接原料。按多糖水解和糠醛形成过程可把制备糠醛的方法分为一步法和两步法[1],两种方法均符合共同的反应机理。生产糠醛的基本原理是半纤维素在酸和水的作用下发生水解生成戊糖,而后木糖经过异构化作用和连续三步脱水反应生成糠醛。反应过程见图1,半纤维素水解生成戊糖的反应速率相对于木糖脱水环化生成糠醛的反应速率要快,但在酸性溶液中,木糖易发生副反应,分解产生甲醛、甲酸、乙醛、乙酸等物质。其中木糖的异构化是整个反应的限速步骤,为了提高糠醛的产率和选择性,一般采用优化反应条件来减少副反应发生,选用适宜催化剂加快木糖的异构化反应。
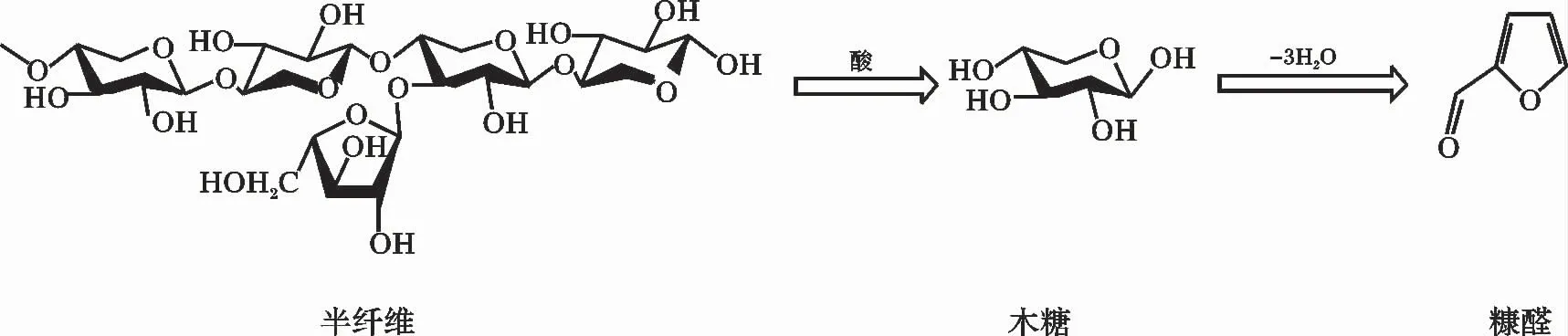
图1 糠醛的形成过程Fig.1 Formation process of furfural
3 糠醛的制备方法及工业化进展
糠醛的工业潜力取决于其生产成本,生产糠醛的原料主要为农林废弃物,主要存在于木素半纤维素中的C5糖:木糖和阿拉伯糖[2-3]。不同的原料中C5糖的类型和含量存在一定的差异,如玉米株的叶子和玉米粒均含有16%的木聚糖,而外皮通常含有22%的木聚糖[4]。玉米棒子中含约3%的阿拉伯聚糖[5],以及含量高达28% ~31%[6]的木聚糖。燕麦壳中的戊聚糖含量与玉米棒子中的相同[7]。甘蔗渣中也含有含量高达27%[8]的戊聚糖。因此,可以利用农林废弃物如玉米芯、燕麦壳和甘蔗渣等生产糠醛。这类废弃物木质纤维素含量丰富,价格低廉,具有潜在的可持续发展性[9-12]。
3.1 木糖脱水制备糠醛
在150 ~220 ℃的水中,木糖转化为糠醛的摩尔收率可高达60% ~70%,在中性条件下的反应速率小,通过加酸催化剂,特别是强酸[13]如硫酸等,反应速率加快,当酸浓度高达2. 5%时反应速率更高。该反应的副反应包括木糖生成C1~4的羧酸、醛和酮,以及糠醛的缩合[14]。
另一方面,阿拉伯聚糖转化尚未广泛研究。部分研究表明,阿拉伯聚糖转化速率慢于或类似于木聚糖的反应速率。许多研究探索了使用路易斯酸或固体酸催化剂将木糖脱水转化为糠醛。Moreau等[15-16]用HY 和HMOR 沸石在17 ℃下,在双相体系中水/甲苯将木糖转化为糠醛。除了提高了产量,双水相操作也能通过溶剂萃取回收糠醛,不需要再进行糠醛/水共沸物蒸馏。但萃取得到的糠醛里含有固体催化剂,而固体催化剂易被污染,回收率较低,且价格昂贵,大大增加了生产成本,因此这并不是最佳方案。
此外,也有研究使用纯有机溶剂,如二甲基亚砜制备糠醛,但是达不到糠醛溶剂萃取的效果。Binder J B 等[17]利用CrCl2-3的盐和有机/离子混合物的组合,在100 ℃下将木糖和木聚糖转化为糠醛。虽然非水介质中糠醛产率更高,但涉及木聚糖/木糖和溶剂纯化成本较高,所以这也并非理想的方案。
3.2 糠醛的工业化研究进程
1921 年,桂格燕麦公司以燕麦壳为原料第一个实现了糠醛的工业化[18],主要用硫酸作为催化剂将戊聚糖水解脱水得到糠醛。这些常规生产糠醛的过程依赖于丰富的半纤维素原料,如玉米芯或甘蔗渣,糠醛理论产量50% ~60%,实际收益率约10%。糠醛生产后所得的残余物被用来作为燃料,但其残留的生物质用于发电或生产生物燃料的能源利用率很低。近期的各种改进解决了低产量、高能耗的问题,通过批量处理过程减少蒸汽的使用。此外,目前国内外主流的糠醛生产工艺主要还有QuakerOats 工艺、Agrifuran 工艺、Petrole-chimie 工艺、Escher Wyss工艺及Rosenlew 工艺[19]。
4 糠醛的应用
4.1 加氢制备2-甲基呋喃
加氢反应仍然是将糠醛转化为呋喃生物燃料的主要反应。在工业上,2-甲基呋喃可由以农业废料为基础的糠醛路线生产获得。

4.1.1 在气相中生产甲基呋喃目前采用的催化剂主要有Cu-Cr 催化剂(亚铬酸铜催化剂)、合金催化剂、复合金属氧化物催化剂、负载型催化剂以及超细粉末催化剂[20]。在Cu 基催化剂催化、高温低压条件下,糠醛转化为甲基呋喃的选择性较大,其中糠醇作为反应中的一个中间体。
4.1.2 在液相中生产甲基呋喃在气相中生产甲基呋喃催化剂容易快速失活,人们考虑在液相条件下的加氢反应。5-甲基糠醛或羟甲基糠醛能在温和的条件下由Pd/C 催化加氢转变为甲基呋喃和2-甲基呋喃。Sun 等[21]报道了糠醛在聚合物负载的Pd络合物催化下氢解为甲基呋喃的反应,在18 ℃下用0.1 MPa H2反应1 h 得到100%的收率。Hamada等[22]通过5-氯甲基-2-糠醛的脱水和随后的加氢将果糖转换为2-甲基呋喃。第2 步采用Pd/C 作为催化剂,环己烯作为氢供体在60 ~80 ℃下通过转移氢解得到88%的产率。Luijkx[23]还报道了HMF 的氢解反应,反应在异丙醇中进行,在60 ℃下采用Pd/C催化剂,2-甲基呋喃的收率高达36%,副反应可使用的酸助催化剂和合适的反应溶剂来抑制。
4.2 加氢制备甲基四氢呋喃
甲基四氢呋喃是一个潜在的燃料组分,将糠醛转换为甲基四氢呋喃分两步反应。第1 个反应器中,采用钡/锰促进铜铬催化剂将糠醛转化为甲基呋喃,反应条件为175 ℃、0.1 MPa、氢气和糠醛的摩尔比约为2;第2 个反应器中,在130 ℃下用Ni 基催化剂氢化甲基呋喃使其转化为甲基四氢呋喃[24]。
采用超临界CO2和Cu-Cr 与Pd/C 组合催化剂可以制甲基四氢呋喃。超临界CO2的优点在于它的灵活性,它通过调整每个反应器中的温度,以产生糠醇、四氢糠基醇、甲基呋喃、甲基四氢呋喃或呋喃。
4.3 加氢制备戊二醇
呋喃环在高温下使用贵金属催化剂可以进一步氢化和开环产生二醇(如1,2-戊二醇和1,5-戊二醇),这些产品可以通过酯化反应转化为戊酸戊酯,或醚化反应转化为有价值的生物燃料二戊基醚。该反应中C—O 裂解的区域选择性是一个难点,而通过双金属催化剂可提高戊二醇的选择性,如在Rh/SiO2与Mo 或Re 的促进下将四氢糠醇转换为1,5-戊二醇的选择性大于80%,而没有Mo 或Re 的促进下,Rh 催化剂催化选择性地产生1,2-戊二醇[25]。

4.4 加氢制备脂肪烃
单聚和低聚呋喃组分通过脱氧加氢可转换为脂肪烃。Corma A 等[26]将羟甲基糠醛与酮的耦合物,以甲基呋喃三聚体用铂基催化剂(如Pt/NbPO5、Pt/C 和Pt/TiO2),通过环加氢和随后的脱氧加氢制备C10+烃化物。Chatterjee M 等[27]采用双官能团Pd基催化剂(Pd/SiO2-Al2O3或Pd/沸石),在80 ℃和超临界CO2条件下,呋喃成分能发生脱氧加氢反应。
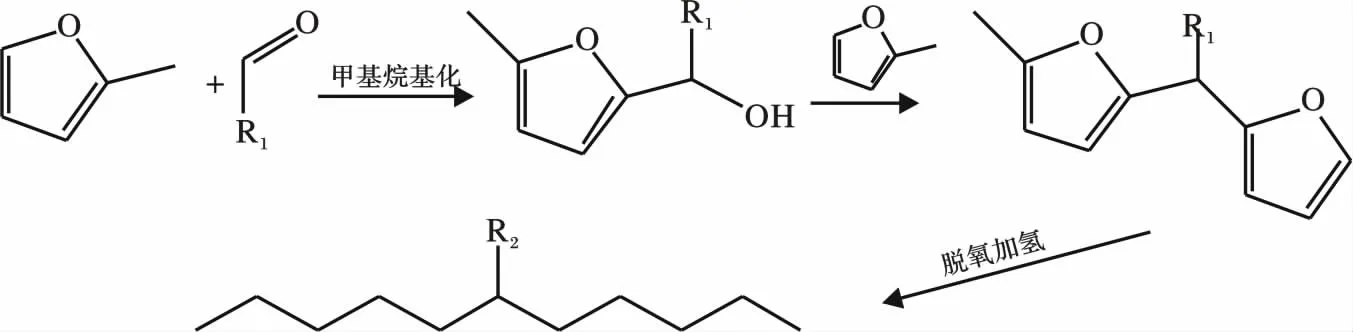
4.5 重排制备乙酰丙酸酯
用Cu 基催化剂可催化糠醛选择性加氢制取糠醇[28],随后在酸条件下醇解得到乙酰丙酸酯。糠醛转化成乙酰丙酸酯后,可进一步转化戊酸正丁酯,戊烯酸酯和聚丁烯等生物燃料,由于反应中糠醛转换得较少,糠醛的副产物乙酰丙酸成为主要产物。反应过程中盐酸和硫酸会对反应设备形成腐蚀,且难以从反应中回收产品,因此不少研究者选择固体酸性催化剂,如酸性沸石可将糠醇和乙醇催化转化为乙酰丙酸酯[29],反应中伴随着醚副产品产生,提高这一过程的经济潜力。糠醛制备乙酰丙酸酯的反应如下:
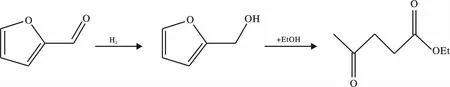
4.6 甲基呋喃的低聚
Corma 等[30]提出一种用酸催化生产呋喃低聚物的方法,在硫酸中加热生产4-氧代戊醛和烷基化的开环产物,在原来的位置上与其他两分子MF 生成C15含氧化合物,并得到甲基呋喃三聚体。此外,三聚体产物自发地从水相中分离出来,通过脱氧加氢反应可得C15烷烃,这是一种以甲基呋喃为基本物增长碳链制取支链烷烃的有效方法。

5 结论
近年来,受传统能源价格、环保和全球气候变化的影响,世界各国日益重视生物燃料的发展,糠醛平台化合物生产生物燃料具有十分广阔的应用前景。糠醛可转化为各种燃料,如汽油或柴油的混合组分,一般是通过除去醛基的极性以溶于烃类化合物,其中不饱和的单体呋喃类化合物具有优异的汽油混合性,特别是相对于辛烷值而言。
糠醛制备最大和最具挑战性的是,木素纤维素材料的预处理过程昂贵,并在产生的戊聚糖中反应,有时需要使用昂贵的反应介质,此外从稀水溶液中回收糠醛或其前体木糖也需要相当大的能量和投资成本。因此糠醛生产有生物燃料的技术仍需要改进,解决水解木素纤维素的产率低和能耗高,以及进一步改善糠醛转化的选择性和催化剂寿命,这些对进一步加强糠醛下游产品的深度开发和应用具有重要意义。
[1] 高美香,刘宗章,张敏华.生物质转化制糠醛工艺的研究进展[J].化工进展,2013,32(4):878-884.
[2] 王东.糠醛产业现状及其衍生物的生产与应用[J].化工中间体,2003,21:19-22.
[3] 许栓善.糠醛的系列衍生物[J]. 甘肃化工,1992(2):28-32.
[4] Liu L,Ye X P,Womac A R,et al. Variability of biomass chemical composition and rapid analysis using FT-NIR techniques[J].Carbohydr Polym,2010,81(4):820-829.
[5] Win D T,Au J T.Furfural-gold from garbage[J].AU J T,2005,8(4):185-190.
[6] Van Eylen D,F van Dongen,M Kabel,et al. Corn fiber,cobs and stover:Enzyme-aided saccharification and cofermentation after dilute acid pretreatment[J]. Bioresource Technology,2011,102:5995-6004.
[7] Du B,Sharma L N,Becker C,et al.Effect of varying feedstock-pretreatment chemistry combinations on the formation and accumulation of potentially inhibitory degradation products in biomass hydrolysates[J]. Biotechnology and Bioengineering,2010,107(3):430-440.
[8] Alves E F,Bose S K,Francis R C,et al.Carbohydrate composition of eucalyptus,bagasse and bamboo by a combination of methods[J].Carbohydr Polymers,2010,82(4):1097-1101.
[9] Lange J P. Lignocellulose conversion:an introduction to chemistry,process and economics[J]. Biofuels Bioprod Bioref,2007,1:39-48.
[10] Berndes G,Hanson J. Furfural production by‘acidic steam stripping’of lignocellulose[J].Energy Policy,2007,35:5965-5979.
[11]Heinen R,Johnson E.Carbon footprints of biofuels & petrofuels[J].Ind Biotechnol,2008,4:257-261.
[12] Yan X,Inderwildi O R,King D A.Life cycle energy and greenhouse gas analysis for algae-derived biodiese[J].Energy Environ Sci,2010,3:190-197.
[13]Gravitis J,Vedernikov N,Zandersons J,et al.Furfural and levoglucosan production from deciduous wood and agricultural wastes[J].Symp Ser,2001,784:110-122.
[14]Aida T M,Shiraishi N,Kubo M,et al.Reaction kinetics of D-xylose in sub-and supercritical water[J]. Supercritical Fluids,2010,55:208-216.
[15] Moreau C,Durand R,Razigade S,et al. Dehydration of fructose to 5-hydroxymethylfurfural over H-mordenites[J].Appl Catal A:Gen,1996,145:211-224.
[16] Moreau C,Durand R,Peyron D,et al. Selective preparation of furfural from xylose over microporous solid acid catalysts[J].Ind Crops Prod,1998,7:95-99.
[17]Binder J B,Blank J J,Cefali A V,et al.Synthesis of furfural from xylose and xylan[J]. Chem Sus Chem,2010,3:1268-1272.
[18]Jing Q,Lu X,Chin J.Kinetics of non-catalyzed decomposition of D-xylose in high temperature liquid water[J].Chem Eng,2007,15:666-669.
[19]张璐鑫,于宏兵. 糠醛生产工艺及制备方法研究进展[J].化工进展,2013,32(2):425-432.
[20]李长海,李国安. 糠醛气相加氢制2-甲基呋喃新型配合物催化剂研究[J].工业催化,2008,16(8):60-64.
[21]Linares G E G,Nudelman N S.Reactions of lithiated aromatic heterocycles with carbon monoxide[J]. Phys Org Chem,2003,16:569-576.
[22] Hamada K,Yoshihara H,Suzukamo G,et al. Novel synthetic route to 2,5-disubstituted furan derivatives through surface active agent-catalysed dehydration of D-fructose[J].Journal of Oleo Science,2001,50:533-536.
[23]Gerard C A Luijkx,Wilfred van der Horst,Satu O A Koskinen,et al.Hydrothermal formation of hydroxylated benzenes from furan derivatives[J]. Analytical and Applied Pyrolysis,1994,28(2):245-254.
[24]刘保健,黄宁选,李文清. 糠醛和呋喃的生产、合成进展[J].化工时刊,2007(21):66-68.
[25]张力平.糠醛深加工产品的应用前景[J]. 化学工程师,1994,3(41):33-34.
[26] Corma A,O de La Torre,Renz M,et al. Production of high-quality diesel from biomass waste products[J].Chem,2011,123:2423-2426.
[27] Chatterjee M,Matsushima K,Ikushima Y,et al. Production of linear alkane via hydrogenative ring opening of a furfural-derived compound in supercritical carbon dioxide[J].Green Chem,2010,12:779-782.
[28] Capai B,Lartigau G. Preparation of laevulinic acid:US,5175358 A[P].1992-12-29.
[29] Lange J P,W D van de Graaf,Haan R J. Conversion of furfuryl alcohol into ethyl levulinate using solid acid catalysts[J].Chem Sus Chem,2009,2(1):437-441.
[30]Tejero J,Cunill F,Iborra M,et al.Dehydration of 1-pentanol to di-n-pentyl ether over ion-exchange resin catalysts[J].Chem,2002,182:541-554.
