高温液相添加剂对纳米LiBr溶液表面张力和沸腾温度的影响
2014-12-22李云翔解国珍田泽辉李小双
李云翔 解国珍 安 龙 田泽辉 李小双
(北京建筑大学 北京 100044)
1 引言
能源是人类赖以生存和发展的重要基础,也是经济发展的原动力。随着经济高速增长,中国的能源消费量与日俱增,此时不得不面对的是环境污染、资源和能源短缺等硬性约束。据调查中国能源利用率仅为约30%,大量余热以各种形式被排放到大气中,可再生能源在能源结构中所占比例不足8%。因此,回收利用余热在提高中国一次能源利用率方面具有举足轻重的作用[1-2]。在暖通空调领域,寻求能够降低溴化锂(LiBr)机组发生器沸腾温度的工质,便能降低所需热源的温度,此时工业余热、废热等低品味热源便可得到广泛应用,其对节能减排的战略起到重要作用[3-5]。
解国珍等[6]通过在LiBr溶液中添加纳米材料A和分散剂B的试验研究,得到纳米LiBr溶液的发生温度与纳米颗粒的关系,随着纳米颗粒添加量在LiBr溶液中的增加,发生温度呈现出先降低后增高的趋势。王莉等[7]通过研究在LiBr溶液中添加单一型分散剂和复合型分散剂,发现在研究的纳米颗粒质量组分变化的范围内,纳米颗粒会降低溶液的发生温度。
本文则是通过在纳米LiBr溶液中添加3种不同的高沸点表面活性剂,试图通过改变表面张力而降低溶液沸腾温度。此外对比了3种表面活性剂对纳米LiBr溶液的表面张力和沸腾温度的影响,并从机理角度做了深入分析。
2 实验材料、仪器及测量原理
2.1 试验材料
本实验所用 LiBr的纯度为 99.9%;氧化铜(CuO),平均粒径 30nm;柠檬酸铵(C6H5O7(NH4)3);阿拉伯树胶(E414);异辛醇(C8H18O);壬醇(C9H20O);癸醇(C10H22O)。
其中C8H18O、C9H20O和C10H22O是表面活性剂,C6H5O7(NH4)3是分散剂,E414既属于表面活性剂也属于分散剂。表面活性剂,是指具有固定的亲水亲油基团,在溶液的表面能定向排列,并能使表面张力显著下降的物质[8-9]。分散剂是指吸附于液固界面并能显著降低界面自由能,使固体粉末均匀的分散在液体或熔体中,并使之不再聚集的一类物质[10]。
2.2 实验仪器及其原理
本试验表面张力值采用吊板法测量,如图1所示:白金板因被测溶液的表面张力而将其向下拉,当总表面张力与液体的重量平衡时,通过测量白金板浸入待测溶液的深度,便可知溶液的表面张力值[11],其原理见式(1)。
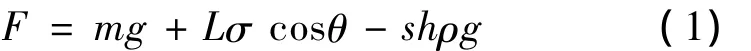
式中:F为平衡力,N;m为感测白金板的重量,kg;s为感测白金板横截面面积,m2;h为浸入待测溶液的深度,m;L为感测白金板周长,m;σ为待测溶液的表面张力,mN/m;g为重力加速度,N/kg;θ为待测溶液和白金板的接触角,°;ρ为待测溶液的密度,kg/m3。
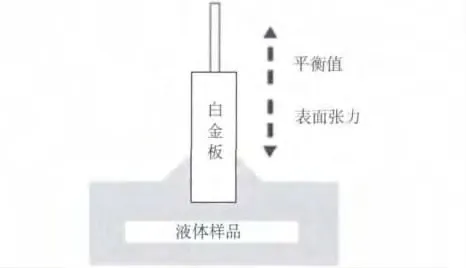
图1 表面张力测量原理图Fig.1 Schematic diagram of hanging plate method
溶液沸腾温度测试原理如图2所示,在试管中放入一定量的待测溶液,用温度逐渐升高的油浴来加热试管使溶液沸腾,采用搅拌装置使油浴温度均匀,由热电偶测俩溶液的起泡温度。
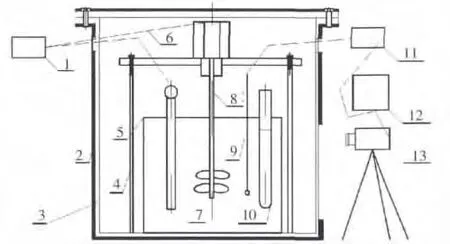
图2 溶液沸腾特性测试原理示意图Fig.2 Testing principle diagram of solution boiling characteristic
3 试验结果及其机理分析
为了便于观察3种表面活性剂对纳米LiBr-H2O表面张力和沸腾温度的影响,实验测量了不含此3种表面活性剂的纳米LiBr-H2O的表面张力和沸腾温度,见表1。
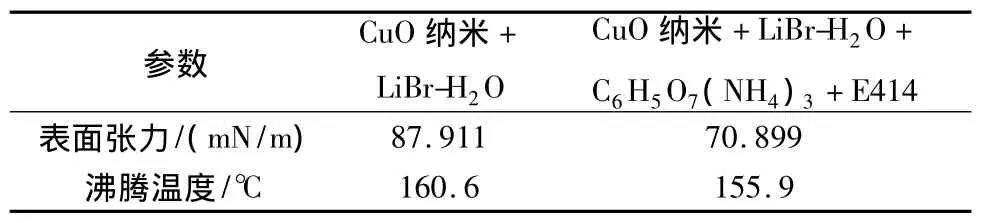
表1 纳米LiBr-H 2O表面张力和沸腾温度Table 1 Boiling temperature and the surfacetension of nano LiBr-H 2 O
3.1 含有不同表面活性剂的纳米溴化锂溶液表面张力
气泡成核理论提出表面张力改变能直接影响形成汽核所需的最大活化能[12-14],因此在研究纳米流体的沸腾温度之前应当对流体的表面张力进行测量分析。
3.1.1 添加有C8H18O的纳米LiBr-H2O表面张力
图3是分别以纳米LiBr-H2O为基液和以CuO:E414:C6H5O7(NH4)3:LiBr-H2O 按 1:5:1:993 的比例混合的溶液为基液并添加不同浓度表面活性剂C8H18O的LiBr溶液的表面张力,为叙述方便简称纳米 LiBr-H2O基液为 A基液,CuO:E414:C6H5O7(NH4)3:LiBr-H2O溶液按1:5:1:993的比例混合的基液为B基液。
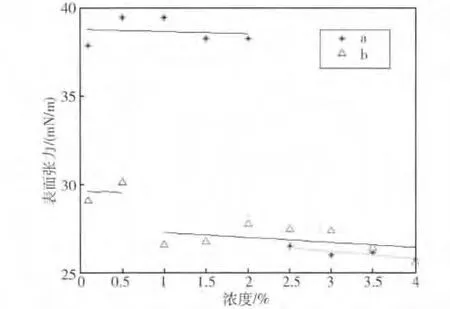
图3 添加C8 H 18 O纳米LiBr-H 2 O的表面张力Fig.3 Surface tension of Nano-LiBr aqueous and C8 H 18 O
图3中曲线a是在A基液中添加C8H18O时,混合溶液表面张力随C8H18O的浓度变化,曲线b是在B基液中添加C8H18O时,混合溶液表面张力随C8H18O的浓度变化。
从图3中可看出,添加了表面活性剂C8H18O的纳米LiBr-H2O表面张力大致可分两个阶段,当浓度小于2%时,表面张力保持在37¯40 mN/m之间,当浓度大于2.5%时,表面张力接近此浓度下C8H18O水溶液的表面张力。之所以有分段现象是因为,前半部分C8H18O未覆盖整个溶液表面,随着浓度增加,C8H18O的表面吸附效应导致它覆盖整个溶液表面,因此后者的测量值相当于C8H18O的表面张力值。在2%¯2.5%之间,溶液的表面张力取决于外部条件,包括测量环境,温度等。
添加了表面活性剂C8H18O、表面活性剂E414和分散剂C6H5O7(NH4)3的纳米LiBr-H2O表面张力与单独添加表面活性剂C8H18O的纳米LiBr-H2O表面张力相似,也可分两个阶段,但不同之处在于前者分界点在2%¯2.5%之间,后者分界点前提至0.5%¯1.0%之间。即当浓度小于0.5%时,表面张力保持在30 mN/m附近波动。当浓度大于1.0%时,表面张力接近前者,也即此浓度下C8H18O水溶液的表面张力。存在分段现象的原因同前所述,由此也可证明当C8H18O的浓度增大到一定程度时,其表面张力将接近此浓度下C8H18O水溶液的表面张力。在0.5%¯1.0%之间,溶液的表面张力取决于外部条件,包括测量环境,温度等。
3.1.2 添加有C9H20O的纳米流体的表面张力
图4中曲线a是在A基液中添加C9H20O时,混合溶液表面张力随C9H20O的浓度变化,曲线b是在B基液中添加C9H20O时,混合溶液表面张力随C9H20O的浓度变化。
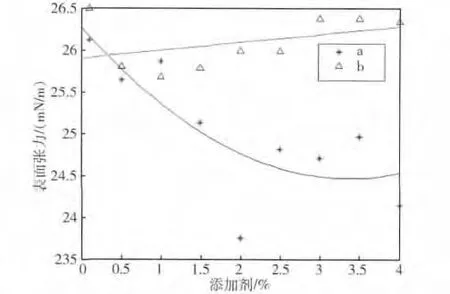
图4 添加C9H 20O纳米LiBr-H 2O的表面张力Fig.4 Surface tension of nano-LiBr aqueous and C9 H 20 O
从图4中可发现,与添加 C8H18O相同,添加C9H20O时纳米LiBr-H2O的表面张力也有较大程度的减小。并且当C9H20O的浓度超过1%以后,含有E414和C6H5O7(NH4)3的溶液表面张力大于不含E414和C6H5O7(NH4)3的表面张力,这是因为当C9H20O的浓度大于临界胶束浓度后,E414和C6H5O7(NH4)3的加入阻碍了C9H20O分子在水面的富集,因此混合溶液的表面张力较当独添加C9H20O时的大。
3.1.3 添加有C10H22O的纳米流体的表面张力
图5中曲线a是在A基液中添加C10H22O时,混合溶液表面张力随C10H22O的浓度变化,曲线b是在B基液中添加C10H22O时,混合溶液表面张力随C10H22O的浓度变化。
从图5中可看出与添加C9H20O相似,当C9H20O的浓度超过0.5%以后,含有E414和C6H5O7(NH4)3的溶液表面张力大于不含E414和C6H5O7(NH4)3的表面张力,其机理与添加C9H20O相同。并且与添加C8H18O相比添加C9H20O和C10H22O时溶液达到平衡时表面活性剂的浓度更小。这是因为随着烷醇中烷基数增加,羟基在整个分子中的影响因素逐渐减弱,体系的疏水作用增加,因此临界胶束浓度值降低[15]。并且发现添加C9H20O和C10H22O时纳米Li-Br-H2O的表面张力平衡值更低,同样是因为其疏水作用强,分子更容易在表面吸附与铺展[16]。
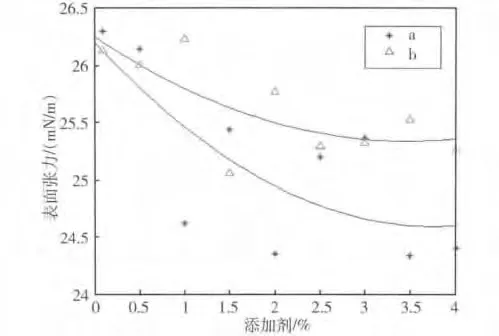
图5 添加C10 H 22 O纳米LiBr-H 2 O的表面张力Fig.5 Surface tension of Nano-LiBr aqueous and C10 H22 O
3.2 添加添加剂后纳米流体沸腾温度
由上述试验可知,3种表面活性剂都能降低纳米流体的表面张力,且根据气泡动力学可知其必会对流体的发生温度产生影响,为了验证上述观点和进一步探索影响纳米流体沸腾温度的因素,对纳米流体的沸腾温度进行了测量。
3.2.1 添加有C8H18O的纳米LiBr-H2O沸腾温度
图6是含表面活性剂C8H18O的纳米溴化锂溶液沸腾温度,观察图6发现,相比未添加液相添加剂C8H18O,添加后的溶液沸腾温度有明显降低,这主要取决于添加有C8H18O时,溶液表面张力大幅度降低。但在实验范围内,沸腾温度无明显变化,这是因为实验范围内溶液表面张力的变化程度不太大。
并且从图6中发现与未添加C8H18O相比,添加后的溶液沸腾温度存在随着添加剂浓度的增加,沸腾温度逐渐升高的现象。分析这个现象主要有两个成因:
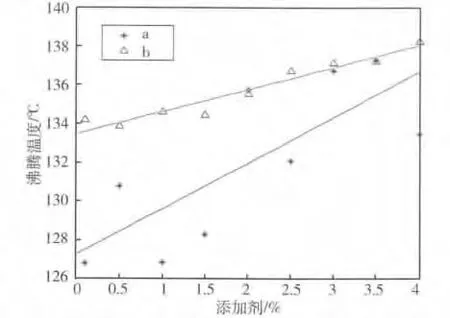
图6 含C8H 18O的纳米LiBr-H 2O沸腾温度Fig 6 Boiling temperature of nano LiBr-H 2 O containing surfactant C8 H 18 O
(1)随着表面活性剂C8H18O含量的增加,且由于表面活性剂在溶液表面的富集作用,导致试管中表面活性剂层的厚度增加,从而增大了LiBr-H2O表面的压力[17]。
(2)实验中将一定浓度的表面活性剂与纳米Li-Br-H2O混合时是采用体积比1:1混合的,且由于表面活性剂在溶液表面的富集作用,导致混合时带入LiBr-H2O中的水含量不同,从而引起 LiBr-H2O浓度的改变,导致沸点升高[18]。
3.2.2 添加有C9H20O的纳米流体的沸腾温度
从图7中可看出同添加C8H18O,添加C9H20O时溶液沸腾温度有明显降低,原因是溶液表面张力大幅度降低。但是从图7中可发现在基液B中加入C9H20O时,当C9H20O的浓度超过2%时沸腾温度会呈直线上升,这是由于在这种情况下震荡之后的纳米流体中的纳米颗粒会聚集在表层的C9H20O当中,被C9H20O包覆,破坏了纳米流体的性质。
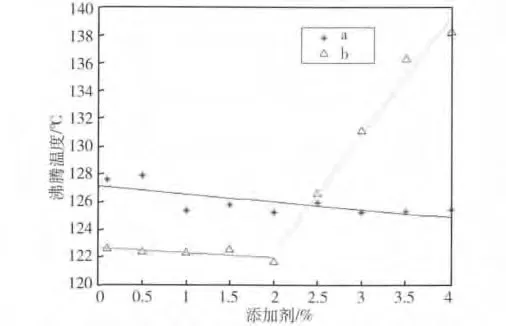
图7 含C9H 20O的纳米LiBr-H 2O沸腾温度Fig7 Boiling temperature of nano LiBr-H 2 O containing surfactant C9 H 20 O
3.2.3 添加有C10H22O的纳米流体的沸腾温度
图8是含表面活性剂C10H22O的纳米LiBr-H2O沸腾温度,从图中可发现沸腾温度随着添加剂浓度的增加有先降低后增加的趋势。
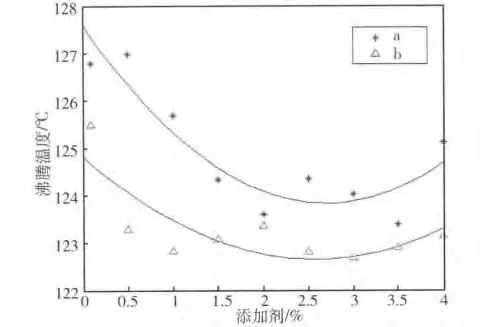
图8 含C10H 22O的纳米LiBr-H 2O沸腾温度Fig.8 Boiling temperature of nano LiBr-H 2 O containing surfactant C10H 22O
分析影响沸腾温度的主要因素,这里主要考虑表面张力、重力和LiBr浓度的影响。如同对C8H18O的分析,可知随添加剂浓度的增大,LiBr浓度增大,会使沸腾温度升高,同时重力对添加剂的影响也将不利于沸腾温度降低,而表面张力的影响则相反。并且由图5可看出,当添加剂浓度低时,表面张力表现出降低的趋势,上述因素相互耦合,最终使得沸腾温度在前半段逐渐降低。而当添加剂浓度超过1.5%时,沸腾温度不再降低,并且随着浓度进一步增大到2.5%以后,沸腾温度有上升的趋势,因为此时表面张力已趋于平衡,但重力和浓度的影响仍在进一步增强。
4 结论
通过实验发现表面活性剂C8H18O、C9H20O和C10H22O都能降低纳米LiBr-H2O的表面张力,使得溶液的沸腾温度分别降低了20¯30℃(添加C8H18O)和30¯35℃(添加C9H20O或C10H22O);此外随着烷醇中烷基数增加,体系的疏水作用增加,分子更容易在表面吸附与铺展,表面张力更低,使得沸腾温度也进一步降低;但是从添加 C9H20O的情况可知,在含有分散剂的条件下当C9H20O的浓度超过2%时会出现纳米流体被包覆现象,破坏了纳米流体的性质从而使得流体沸腾温度直线上升。
1 李海燕.低品位余热利用技术的研究现状困境和新策略[J].科技导报.2010,28(17):112-117.Li Haiyan.Current research status,difficulties and new strategy in utilization of low grade heat[J].Science & Technology Review.2010,28(17):112-117.
2 祁先进.金属基相变复合蓄热材料的实验研究[D].昆明:昆明理工大学,2005.Qi Xinajin.Experimental study on composite heat storage material with metal and molten[D].Kunming:Kunming University of Science and Technology,2005.
3 高洪涛.不同添加方式对添加剂强化吸收的影晌[J].大连海事大学学报,2008 .34(1):20-24.Gao Hongtao.Effects of different addition methods on additive absorption enhancement[J].Journal of Dalian Maritime University,2008,34(1):20-24.
4 高洪涛,李豪.界面活性剂的混合添加对溴化锂溶液吸收水蒸气的影响[J].制冷学报,2007,28(3):11-14.Gao Hongtao,Li Hao.Effect of Compound Surfactants on Water Vapor Absorption of Aqueous LiBr Solution[J].Journal of Refrigeration .2007,28(3):11-14.
5 李 豪.界面活性剂强化吸收机理的实验研究[D].大连:大连海事大学,2007.Li Hao.In Partial fulfillment of the requirements for the degree of master of engineering[D].Dalian:Dalian Maritime University,2007.
6 解国珍,李国栋,法晓明,等.纳米颗粒对溴化锂溶液发生温度的影响研究[J].制冷与空调,2008,(8)增刊:80-82.Xie Guozhen,Li Guodong,Fa Xiaoming,et al.Influence of nano-particles on generating temperature of LiBr solution[J].Refrigeration and Air-Conditioning,2008(8)Suppl.:80-82.
7 王 莉,解国珍,管 燕.添加纳米颗粒及其相应分散剂的溴化锂溶液发生温度和耐高温性能研究[C].走中国创造之路-2011中国制冷学会学术年会,南京:2011:1299-1303.Wang Li,Xie Guozhen,Guan Yan.Study on generating temperature of LiBr aqueous solution added nano-particles and relevant dispersants under high temperature working-conditions[C].Go the way of China to create-2011 China Refrigeration Institute Academic Annual Meeting,Nanjing:2011.1299-1303.
8 宋志超.可聚合聚氨酯型表面活性剂的制备及性能研究[D].青岛:中国海洋大学,2006.Song Zhichao.Synthesis and Properties of Polymerizable Urethane Surfactants[D].Qindao:Ocean University of China,2006.
9 王可为.非离子Gemini表面活性剂的合成及性能表征[D].大连:大连理工大学,2003.Wang Kefei.non-ionic Gemini surfactant synthesize and characterization of properties[D].Dalian:Dalian University of Technology,2003.
10 吁松瑞.新型除草活性农药先导化合物及农药助剂分散剂的研究;(I)新型除草活性农药先导化合物的合成与生物活性测定;(II)羧酸盐磺酸盐类分散剂的合成及性能测试[D].上海:上海师范大学,2009.Xu Songrui.Research of new herbicidal activity pesticide lead com-pounds and pesticide dispersant additives;(I)Synthesis and herbicidal activity research of new herbicidal activity pesticide lead compounds;(II)Synthesis and dispersion research of the copolymers of acrylic acid,styrene sulfonic sodium and maleic anhydride[D].Shanghai:Shanghai Normal University,2009.
11 全自动表面/界面张力仪操作手册[S].美国科诺工业有限公司.Full Automatic Surface&Interface Tensiometer coperation manual[S].USA kono industrial co.,LTD.
12 王亮亮.纳米微粒对溴化锂溶液表面张力及其沸腾特性的影响和机理[D].北京:北京建筑大学,2013.Wang Liangliang.Influence and mechanism of nano-particles on surface tension and boiling characteristic of LiBr aqueous solution[D].Beijing:Beijing University of Civil Engineering and Architecture,2013.
13 Hu Zicheng,Gu Jiaqiang ,Song Xinnan ,et al.Pool boiling heat transfer of aqueous surfactant solutions[C].Fourth International Conference on Intelligent Computation Technology and Automation Jiangsu University,Zhenjiang,Jiangsu,2013.841-844.
14 胡自成.表面活性剂水溶液池核沸腾传热强化的研究[D].镇江:江苏大学,2012.Hu Zicheng.Research on nucleate pool boiling heat transfer enhancement of aqueous surfactant solutions[D].Zhenjiang:Jiangsu University,2012.
15 北京市教育局教材编写组编.化学第三册.北京:人民出版社,1976.74.The Education Bureau of Bejing Teaching Materials Writing Group.Chemistry Volume III.Beijin:People's Publishing House,1976.74.
16 万 伟.D5反胶束体系的制备及其在活性染料染色中的应用[D].杭州:浙江理工大学,2010.Wan Wei.Preparation of D5 reverse micelle systems and their application in dyeing with reactive dyes[D].杭州:Zhejiang Sci-Tech U-niversity,2010.
17 孙仁义.不挥发溶质对混合溶剂沸点及蒸气压的影响[J].化工学报.2002:53(9)885-891.Sun Renyi.Effect of non-volatile solutes on boiling point and vapor pressure of mixed solvent[J].Journal of Chemical Industry and Engineering.2002:53(9)885-891.
18 何杰主编.物理化学.[M].北京:化学工业出版社,2011:171.He Jie.Physical Chemistry.[M].Beijing:Chemical industry press,2011:171.
