蒸汽灭菌过程中液体装载非无菌可能性的评价
2014-12-16苏乐陈小彬兰志岭牛志彬
苏乐 陈小彬 兰志岭 牛志彬
(1.北京天坛生物制品股份有限公司质量保证部验证室 北京 100024;2.北京天坛生物制品股份有限公司质量保证部 北京 100024)
我们已经实施了SHINVA脉动真空灭菌柜(XG1.GMF-1.5B型号)的确认-验证工作。以下的实验为饱和蒸汽脉动真空周期的装载包含50个250ml瓶子内装200ml葡萄糖肉汤培养基的验证程序。
葡萄糖肉汤培养基是热敏感培养基,在高压灭菌工艺中容易发生理化性质改变。所以,灭菌参数必须仔细选择。
本文中所指的微生物实验室使用灭菌培养基进行非无菌产品微生物检验和培养。
1 材料和方法
根据药典推荐[1],液体培养基的参考灭菌条件(121℃暴露15分钟)。初步试验确定装载的滞后时间特性。首先用50个瓶装有200ml自来水来模拟装载。
为了监测装载条件下腔室获得的温度,16个探头放置在腔室的多个位点,另外12个放置在瓶子所含液体的中部。 腔室温度探头的放置和装载图见图1热分布。
当放置在排水口的温度探头达到灭菌温度时开始计算延迟时间。当放置于装载中的最后一个探头温度达到灭菌温度时计时结束[2]。
热穿透试验与生物指示剂试验同时实施。含有5*106数量的嗜热脂肪芽孢杆菌孢子安瓿放置在每一个装载中温度探头旁。对于安瓿瓶,按12个热穿透瓶子的编号分配。在插入热温度探头后,灭菌的安瓿在55-60℃培养7天,以灭菌的安瓿做阳性对照,并每天检测细菌生长情况。作为一种确认灭菌效率的方法,灭菌后50瓶葡萄糖肉汤培养基中的5瓶在32℃培养5天。培养基每天检测其细菌生长性[3]。

图1 热分布放置示意图
检测灭菌后培养基效度,葡萄糖肉汤培养基依据生长促进试验。在枯草杆菌芽孢存在的条件下在37℃培养48小时检测培养基的生长促进试验。
另一种确认培养基和缓冲液物理性质完整性的方法是在灭菌前后检测其PH值。对于葡萄糖肉汤培养基pH应在7.3±0.2。
2 结果
对于同样的装载,测量到延迟50分钟。培养基粘性略高于自来水。除了所需暴露时间15分钟外,平衡50分钟可认为足够。
应用装载内的温度探头所记录的温度分布表明在暴露期装载的温度略低于设定温度121℃。验证试验应用的设定温度121℃30分钟。图1是热分布示意图,排水口的探头为15号,3次运行的热分布温度探头获得的数据总结见表3。培养基瓶热穿透的数据总结见表4。
当观察到热分布每次运行计算出平均温度时,要清楚5位置是腔室热点。导轨下的15和16位置作为腔室冷点考虑。分析排水管位置和腔室其它几何位置的平均温度数据进行t检验并无统计学显著差异95%的可信度。(除了3号,位于腔室上角远离蒸汽进气口,这个非关键因素,因为没有装载会达到这个位置)。
热穿透温度数据表明23和26位是温度高点17和28位是冷点,多点记录数据证明在95%可信限无统计学差异(图4)。
每30秒温度读取计算F0值,计算如下:
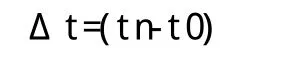
该循环的总时间温度大于100℃获得的杀菌效果 ,计算包括加热的整个暴露阶段和部分升温及冷却阶段。灭菌器温度探头达到灭菌温度的时间作为t0,而后循环开始。分析致死率确定各次运行间F0均值95%置信区间(表5)。
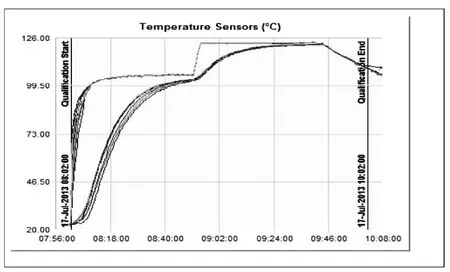
图2 热分布于热穿透时间曲线
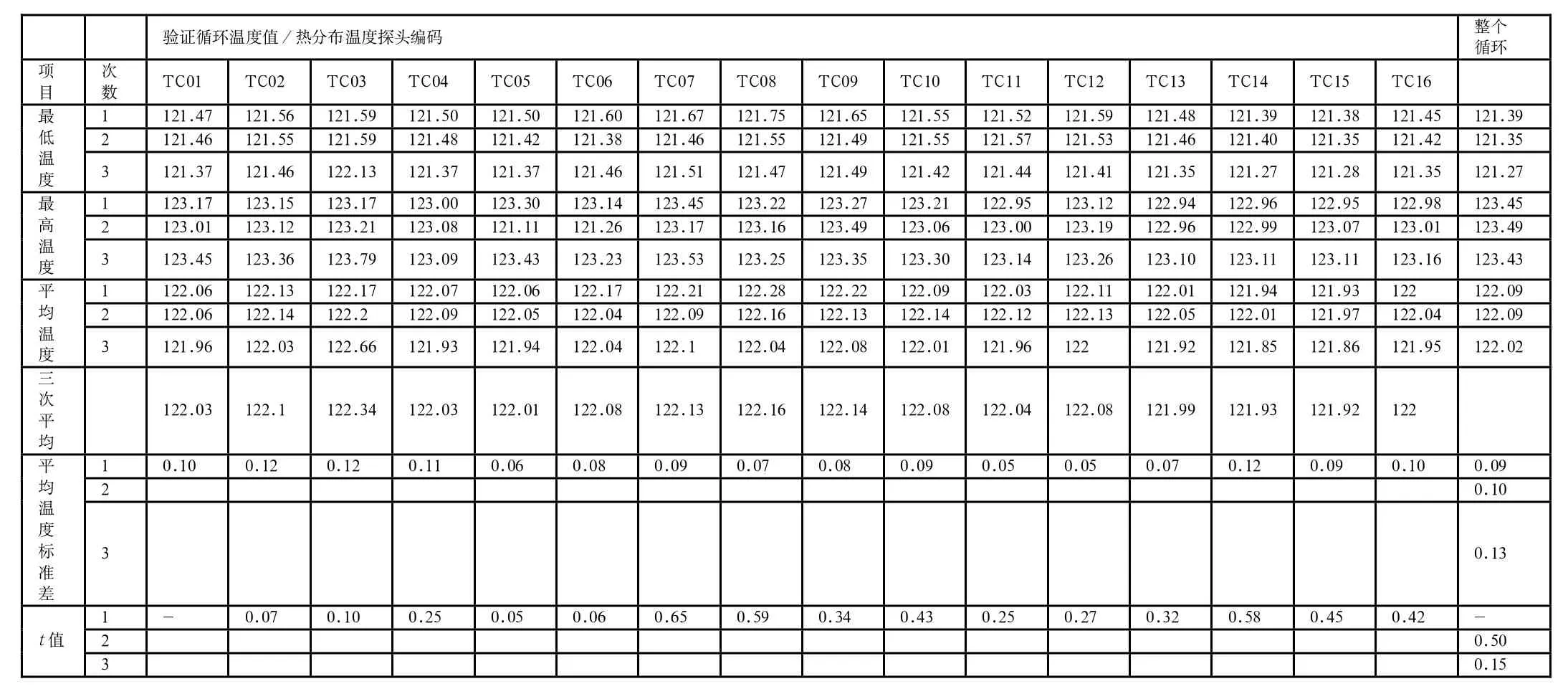
表3 暴露期热分布温度数值
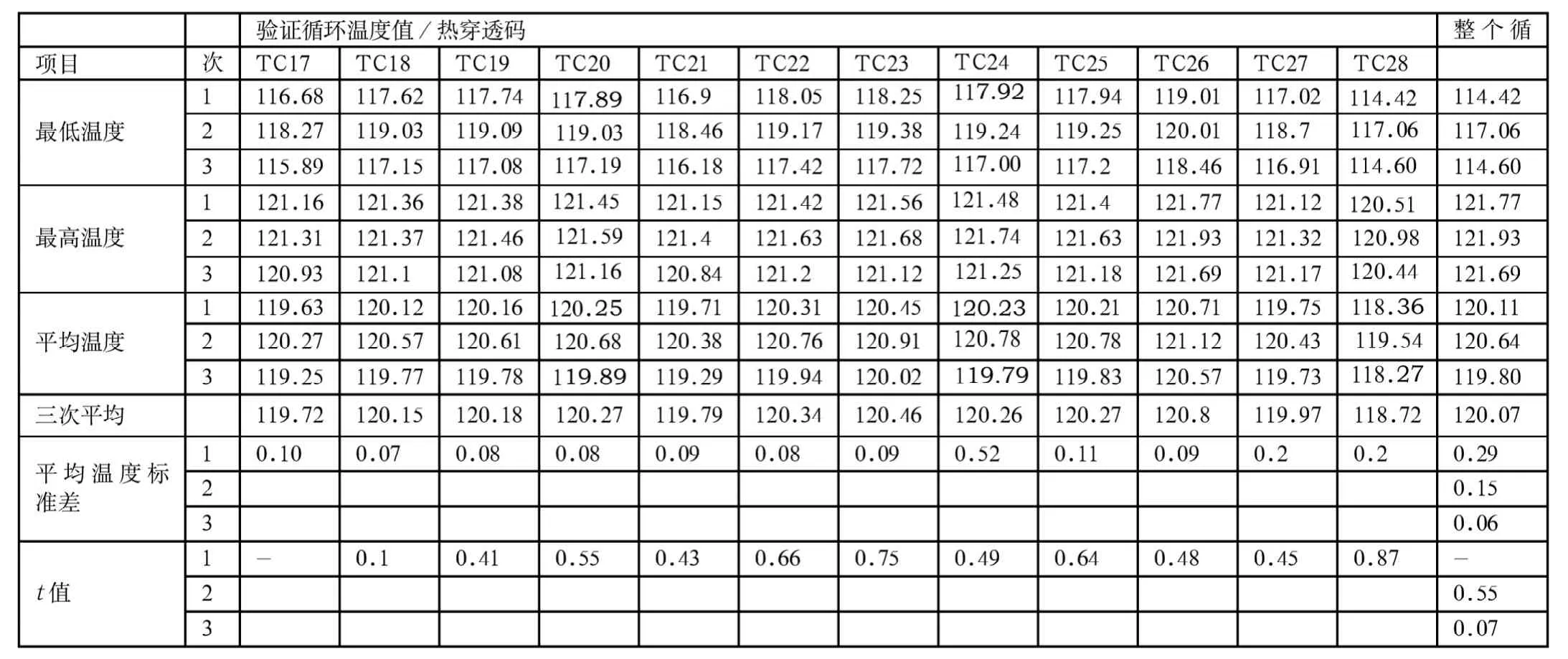
表4 暴露期热穿透温度值
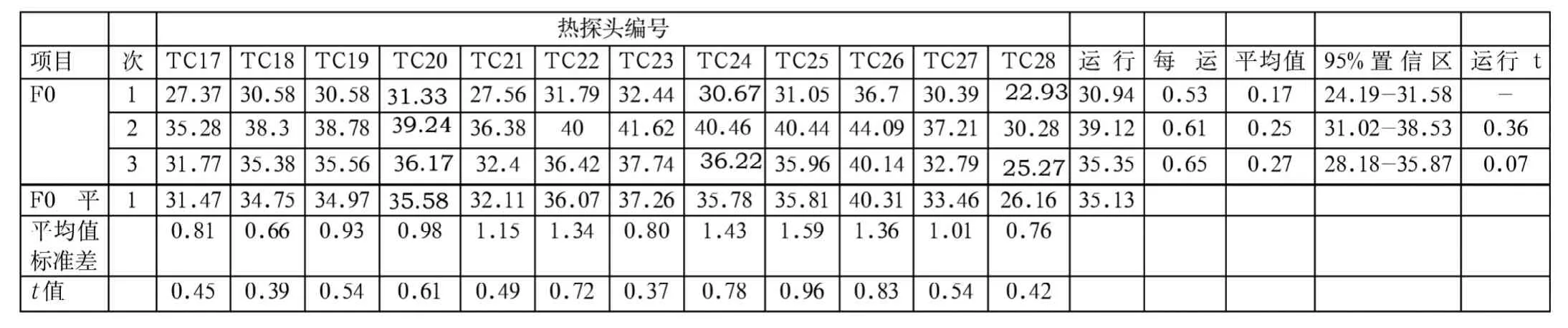
表5 热穿透累积F0值

表6 每次运行所获得的无菌保障水平
每次运行确定所达到的无菌保证水平,计算低限95%置信区间带入用于计算F0等式,重新排列等式,即可确定概率P作为绝对值Nt。
正如制造商所提供的合格证书中显示,D121被确定为1.5分钟,N0为106.计算所得的95%置信区间的Nt下限显示在表6中。可以得出结论,如果按照本研究所采用的装载,95%置信区间一个生物体存在的概率是10-10或更低。
3 讨论
前述方法基于最坏情况的假设即每件物品上存在106孢子必须被灭菌,生物负荷的微生物与噬热脂肪肝菌芽孢同样的热抗性。然而达到无菌保证水平10-12就没有必要,因为用于准备培养基的原材料为纯化品及低的生物负荷。
实验中所使用的生物指示剂同样表明有足够的无菌保证水平。灭菌后,安瓿瓶中所有芽孢被杀灭,而后进行7天50-60℃的培养。培养期后阳性对照显示有细菌生长。
培养后5天目视检查显示无细菌生长。一瓶未灭菌的培养基作为阳性对照进行培养,在培养基变浑浊。这将确定灭菌工艺有效性的结论。
培养基在灭菌后的活度同样经过促生长试验确认。灭菌后,培养基接种谷草芽孢杆菌37℃培养48小时,显示阳性芽孢生长。培养基变浑浊的事实确认其稳定性及在灭菌过程中化学成分没有发生变化,接种合适的微生物仍能支持生长。
灭菌后进行三次pH检测。所有pH值在7.15-1.17范围内,确认了灭菌后保留了培养基的理化性质。当然,灭菌后三人独立的目视检测确认无颜色变化或沉淀现象。
可以断定的是,对于所研究的生物负荷,已经达成PQ阶段研究的目标。在灭菌阶段获得的监测物理参数揭示运行中腔室内温度的均匀分布,即装载中所有的热穿透,亦能通过三次重复。所有运行均能达到药典SAL为10-6或更高的要求。
用于负载灭菌的条件是介于过杀和生物负载法之间。这种方法提供在灭菌程度和培养基稳定性间可接受的理想的平衡。我们的结论是高压灭菌柜连续三次在功能参数范围内良好的工作并提供SAL 10-10或更高。
4 结语
尽管验证方法遵循诸多标准步骤,但并不能提供准确的方法,因为存在着许多高压灭菌柜类型和每个单元有特异的操作参数。对于热不稳定物品,既节约能源的角度,我们每一次都需在物理参数与生物负载之间找到平衡。
[1]《中华人民共和国药典》2010年版.微生物检测灭菌法.
[2]Technical Report No.1 Validation of Moist Heat Sterilization Processes:Cycle Design, Development, Qualification and Onging Control,Vol. supplement. (2007).
[3]《中华人民共和国药典》2010年版,附录XI J微生物限度检查.