化学镀铜溶液中稳定剂的研究
2014-12-05孔德龙谢金平范小玲黎德育
孔德龙, 谢金平, 范小玲, 肖 宁, 黎德育, 李 宁,
(1.哈尔滨工业大学化工学院,黑龙江哈尔滨 150001;2.广东致卓精密金属科技有限公司,广东佛山 528247)
引 言
金属铜具有很好的导电、导热和延展性,由于化学镀与电镀相比具有设备简单,镀层均匀,不受基体导电性影响等特点[1],因此化学镀铜在非金属材料的金属化[2-3]、复合材料制备[4]及电磁屏蔽材料[5-6]的制备中得到了广泛的应用。通常化学镀铜的沉积速率较低,无法满足化学镀厚铜的要求。Paunovic[7]的研究表明,四羟丙基乙二胺与铜离子的配合物解离速率较快,可以获得较高的沉积速率,但是成本较高。郑雅洁等[8-10]以EDTA代替部分四羟丙基乙二胺,对四羟丙基乙二胺和EDTA双络合剂化学镀铜进行了研究。为了提高镀液的稳定性,申晓妮等[11]对以四羟丙基乙二胺和EDTA为络合剂的化学镀铜溶液的稳定剂进行了研究。然而,实际生产中对镀液稳定性要求较高。本文对以四羟丙基乙二胺和EDTA为络合剂的化学镀铜溶液中使用的稳定剂进行研究,以期提高镀液稳定性,从而达到生产要求,并对稳定剂的作用机理进行了研究。
1 实验部分
1.1 试剂
实验所用试剂有硫酸铜、四羟丙基乙二胺(BASF)、EDTA、甲醛(37%)、氢氧化钠、硫脲、亚硫酸钠、吐温-60、二巯基苯并噻唑(2-MBT)、2,2-联吡啶、1,10-菲绕啉、硫氰酸钠、亚铁氰化钾和十六烷基三甲基溴化铵(CTAB),0.18g/L PdCl2(自配)。基体为环氧树脂板(PCB)。
1.2 前处理及施镀工艺
1.2.1 镀前处理
基体的镀前处理工艺流程为:除油→水洗→预浸→活化→水洗→解胶(加速)→水洗→化学镀铜。各工序的药品及工艺参数为:
1)除油。IMT-8715除油液,在 47℃下除油5min。2)预浸。IMT-8730预浸盐,室温下预浸1min。3)活化。IMT-8736活化剂,在 42℃下活化5min。
4)解胶。IMT-8746加速剂,室温下加速1min。
1.2.2 施镀工艺
化学镀铜基础镀液组成为:12g/L硫酸铜、10ml/L甲醛(37%)、10ml/L四羟丙基乙二胺、9g/L EDTA2Na、10mg/L 联吡啶,pH=12.5,施镀 θ为60℃。
1.3 表征方法
用称量法测镀层沉积速率,其计算公式如下:
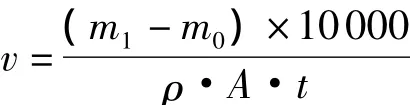
式中,v为沉积速率,μm/h;m0和m1分别为试片镀前与镀后的质量,g;ρ为铜的相对密度,8.9g/cm3;A为试样暴露于镀液中的面积,cm2;t为施镀时间,h。
用氯化钯加速试验测试镀液稳定性:向50mL镀液中加入 15mL PdCl2(0.18g/L),θ为 60℃,记录镀液分解时间。
采用CHI-760D电化学工作站进行电化学测试,参比电极为饱和甘汞电极(SCE),辅助电极为铂电极,用线性扫描法在铂电极表面沉积一层完整的铜层后作为工作电极,沉积过程中溶液为不含甲醛的基础镀铜液,扫描速率为 10mV/s,扫描范围为-0.4~1.4V,扫描次数为2次。进行交流阻抗测试时,初始电位为开路电位,频率范围为100kHz~0.01Hz,幅值为5mV。
采用JSM-6510/X-Act型扫描电子显微镜对镀层的微观形貌进行分析。
2 实验结果与讨论
2.1 化学镀铜稳定剂的初步筛选
由于不同稳定剂的用量范围不同,因此在筛选时根据文献的相关报道,选取各添加剂的适宜用量,结果如表1所示。首先在基础镀液中加入添加剂,通过高温大负载(2.7dm2/L)下的施镀实验对稳定剂进行初步筛选,施镀t为30min,如果镀液在施镀过程中不分解,则认为该添加剂能起到稳定镀液的作用,初步筛选的结果如表1所示。
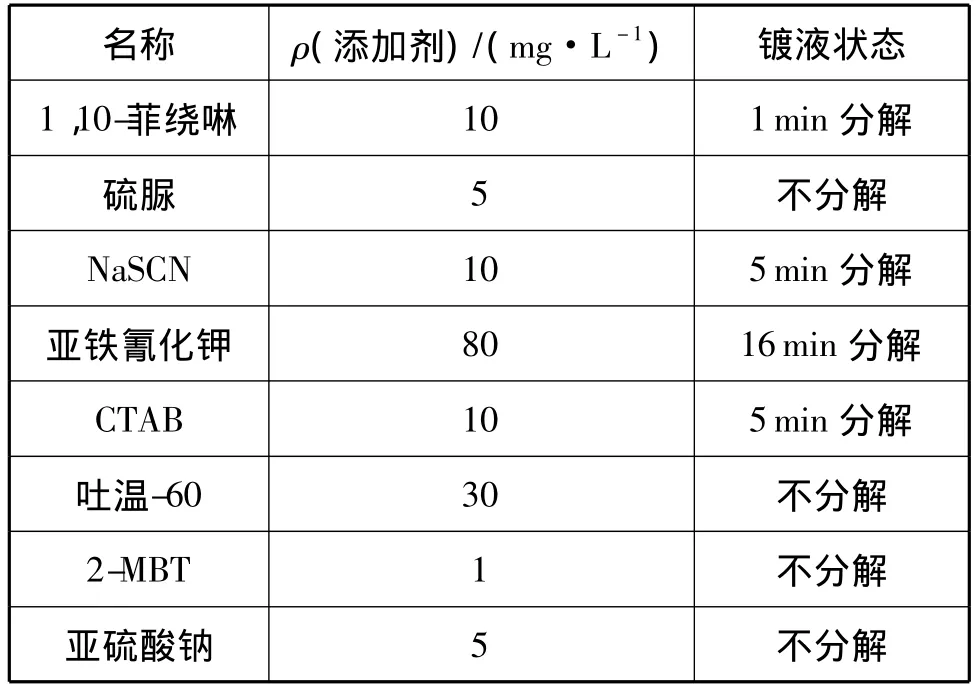
表1 添加剂的筛选结果
从表1中可以看出,硫脲、亚硫酸钠、吐温-60和2-MBT均能在施镀过程中维持镀液30min不分解,说明这四种添加剂有利于提高镀液的稳定性。
2.2 添加剂对沉积速率和镀液稳定性的影响
对初选出的四种添加剂进行沉积速率和稳定性的影响研究。
2.2.1 硫脲对沉积速率和稳定性的影响
硫脲对化学镀铜沉积速率和镀液稳定性的影响如图1所示。从图1可以看出,硫脲质量浓度小于7mg/L时,质量浓度变化对沉积速率的影响较小;硫脲质量浓度大于7mg/L后,沉积速率随硫脲质量浓度增加明显下降,在硫脲质量浓度为10mg/L时,v仅为1.42μm/h,远远低于7mg/L 时的7.1μm/h。镀液分解时间随硫脲质量浓度提高而延长,说明硫脲质量浓度提高,镀液稳定性越好,综合硫脲对沉积速率的影响,确定硫脲的质量浓度为7mg/L适宜。

图1 ρ(硫脲)对稳定性和沉积速率的影响
2.2.2 2-MBT对沉积速率和稳定性的影响
2-MBT对化学镀铜沉积速率和镀液稳定性的影响如图2所示。从图2可以看出,随着2-MBT质量浓度增加,沉积速率呈增长趋势,沉积速率可以达到10μm/h以上,因此可以推断2-MBT还具有加速作用。但是在2-MBT质量浓度小于7mg/L时,氯化钯加速试验中镀液分解时间很短,而ρ(2-MBT)大于3mg/L时,施镀过程中会伴随有黄色粉末出现,可能为硫化物,这些物质在镀层中夹杂,则会引起镀层性能下降,因此认为2-MBT不适宜作为高稳定性镀液的添加剂。

图2 ρ(2-MBT)对稳定性和沉积速率的影响
2.2.3 吐温-60对沉积速率和稳定性的影响
吐温-60对化学镀铜沉积速率和镀液稳定性的影响如图3所示。从图3可以看出,随着吐温-60质量浓度提高,沉积速率下降,但吐温-60质量浓度对沉积速率的影响不大,在吐温-60质量浓度为60mg/L时,仍可获得较快的沉积速率(6.47μm/h)。加入吐温-60后能显著提高镀液的稳定性,随着吐温-60质量浓度增加,镀液稳定性明显提高,即使在30mg/L时,氯化钯加速试验中镀液分解t也可以达到40min。但是以吐温-60为稳定剂时镀层表面有铜颗粒吸附,镀层发暗,而且吐温质量浓度越高,该现象越严重,因此结合吐温-60对镀液稳定性和沉积速率的影响,确定吐温-60的质量浓度为40~50mg/L。
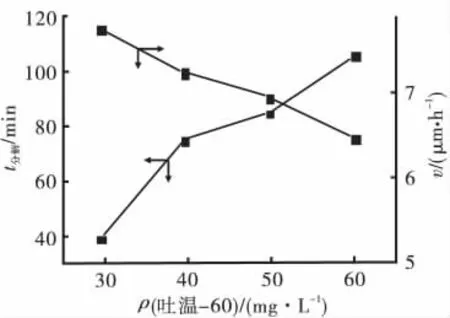
图3 ρ(吐温-60)对稳定性和沉积速率的影响
2.2.4 亚硫酸钠对沉积速率和稳定性的影响
亚硫酸钠对化学镀铜沉积速率和镀液稳定性的影响如图4所示。从图4可以看出,随着亚硫酸钠质量浓度增加,镀液的分解时间明显延长,亚硫酸钠质量浓度大于7mg/L后,镀液分解t达到1h以上,说明亚硫酸钠的加入,可以有效地提高镀液的稳定性,但随着亚硫酸钠质量浓度增加,镀液沉积速率下降,因此综合考虑镀液稳定性与沉积速率,确定亚硫酸钠的质量浓度为5mg/L。
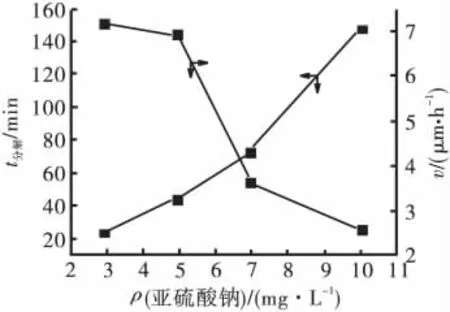
图4 ρ(亚硫酸钠)对沉积速率和稳定性的影响
同时,在基础镀液中分别按适宜的质量浓度加入稳定剂,进行了稳定剂对化学镀铜层的影响研究,化学镀铜表面形貌照片如图5所示。

图5 镀铜层的表面形貌(1000×)
从图5中可以看出,以硫脲为稳定剂时得到的化学镀铜层较差,表面多为细碎花状物质,这可能是镀液分解的产物在镀层夹杂引起的,而以2-MBT、吐温-60和亚硫酸钠为稳定剂得到的镀层表面颗粒均匀细致,排列紧密。加入三种稳定剂得到的镀层颗粒大小的顺序,亚硫酸钠 <吐温-60<2-MBT;镀层颗粒紧凑程度的顺序,亚硫酸钠 >2-MBT>吐温-60。
由于2-MBT不利于得到高稳定的镀液,硫脲形成的镀层有杂质的夹杂,而亚硫酸钠和吐温-60有利于提高稳定性,并保持较高的沉积速率,同时镀层较好,因此对亚硫酸钠和吐温-60进行复配,组成复合稳定剂,以期进一步提高镀液的稳定性,复配后的添加剂进行化学镀铜,结果如表2所示。

表2 亚硫酸钠与吐温-60复配对镀层的影响
从表2中可以看出,当5mg/L亚硫酸钠和20mg/L吐温-60进行复配时,镀液稳定性和沉积速率都较好,同时镀层外观光亮、平整,无起皮。与商品化镀液的分解时间(65min)和沉积速率(5.9μm/h)相比,两者均有提高。
2.3 添加剂机理的研究
用线性扫描(LSV)和交流阻抗(EIS)的方法对稳定剂的作用机理进行研究。
图6为亚硫酸钠质量浓度对化学镀铜沉积速率的影响。由图6可以看出,当化学镀铜溶液中未加入亚硫酸钠时,铜的沉积峰在-1.2V左右[8],加入亚硫酸钠后在-0.95V左右出现还原峰而-1.2V处的还原峰消失。镀液中发生还原反应的可能为Cu2+或Cu+的络合物,由于镀液中络合剂四羟丙基乙二胺与Cu2+的络合物稳定常数较大(lgK CuT(OH)2=26.9,lgK CuT2(OH)2=29.1),因此认为在 -0.95V 处为亚硫酸钠与Cu2+络合物的放电过程的可能性很小,而应为亚硫酸钠与Cu+络合物的还原。
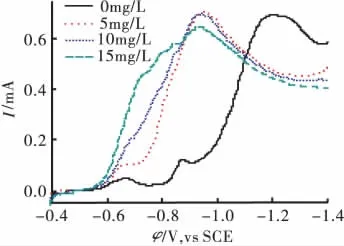
图6 ρ(亚硫酸钠)对铜沉积过程的影响
图7为基础镀液中加入亚硫酸钠的Nyquist图。
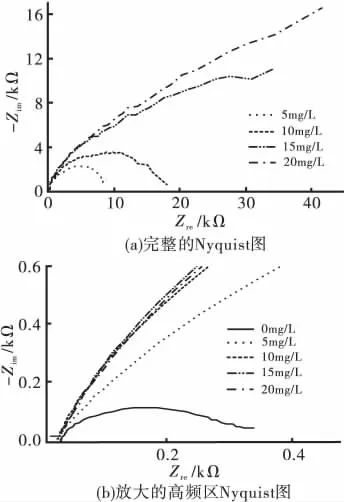
图7 基础镀液中加入亚硫酸钠后的Nyquist图
从图7中可以看出,随着亚硫酸钠质量浓度升高,高频段半圆半径增大,反应的阻力增大,低频段在亚硫酸钠质量浓度大于10mg/L后呈现出扩散控制的特性,这与亚硫酸钠和Cu+络合,减少电极表面的反应物的质量浓度有关。而镀液稳定性正是由于亚硫酸钠与Cu+的络合作用而得到提高。
图8为吐温-60质量浓度对化学镀铜沉积过程的影响。

图8 ρ(吐温-60)对铜沉积过程的影响
从图8中可以看出,化学镀铜溶液中加入吐温-60后铜的沉积电位几乎不发生变化,因此推测吐温-60与镀液中的Cu+没有络合作用或络合作用很弱。根据文献报道[11],聚乙二醇可以吸附在铜粒子表面使其钝化,由于吐温-60含有与聚乙二醇相似的官能团,相对分子质量较大,因此认为吐温-60的稳定作用主要是对Cu0吸附并使其失去催化活性。在实验中发现,化学镀铜溶液分解时并不是在镀槽壁上形成“铜镜”,而是在镀槽底部形成散落的铜粉末,进一步验证了吐温-60降低Cu0催化活性的推测。
3 结论
对四羟丙基乙二胺和EDTA双络合剂化学镀铜溶液稳定剂进行了研究,主要结论如下。
1)通过对稳定剂进行筛选,得到了硫脲、2-MBT、吐温-60和亚硫酸钠四种添加剂,能提高镀液稳定性。
2)采用硫脲、2-MBT、吐温-60和亚硫酸钠对化学镀铜沉积速率、镀液稳定性及镀层的影响进行研究,认为亚硫酸钠和吐温-60可以获得较高的沉积速率和稳定性,亚硫酸钠和吐温-60组合后复合的稳定剂,能显著提高镀液稳定性,沉积速率可以达到7.29μm/h。
3)对亚硫酸钠和吐温-60提高镀液稳定性的作用机理进行研究,表明亚硫酸钠主要与Cu+络合,形成稳定的配合物,而吐温-60则是吸附在Cu0表面并使其失去催化活性。
[1] 李宁.化学镀实用技术[M].北京:化学工业出版社,2012:1.
[2] 朱焱,孔小雁,江茜,等.表面活性剂在陶瓷化学镀铜工艺中的作用[J].中国表面工程,2012,25(1):76-82.
[3] 宋秀峰,傅仁利,何洪,等.氧化铝陶瓷基板化学镀铜金属化及镀层结构[J].电子元件与材料,2007,26(2):40-42.
[4] 张振忠,赵芳霞,丘泰.钨粉表面化学镀铜研究[J].铸造技术,2006,27(11):1241-1244.
[5] Sun L,Li J,Wang L.Electromagnetic interference shielding material from electroless copper plating on birch veneer[J].Wood Science and Technology,2012,46(6):1061-1071.
[6] Deepa J P,Resmi V G,Rajan T P D,et al.Studies on the effect of processing parameters on electroless coating of copper on boron carbide particles[J].Transactions of the Indian Institute of Metals,2011,64(1-2):47-51.
[7] Paunovic M.Ligand Effects in Electroless Copper Deposition[J].Journal of the Electrochemical Society,1977,124(3),349-354.
[8] 邹伟红.快速化学镀铜工艺及机理研究[D].湖南:中南大学冶金物理化学,2005:41-49.
[9] 郑雅杰,邹伟红,易丹青,等.四羟丙基乙二胺和EDTA·2Na盐化学镀铜体系研究[J].材料保护,2006,39(2):20-24.
[10] 邹伟红,郑雅杰.THPED化学镀铜溶液中Cu(Ⅱ)的存在形式与阴极还原[J].电镀与涂饰,2010,(02):30-32.
[11] 申晓妮,赵冬梅,任凤章,等.添加剂对四羟丙基乙二胺(THPED)化学镀厚铜的影响[J].中国腐蚀与防护学报,2011,(05):362-366.
