用732 强酸性阳离子交换树脂去除铬酸盐钝化液中的锌离子
2014-11-25车淳山黄清孔纲卢锦堂张双红
车淳山*,黄清,孔纲,卢锦堂,张双红
(华南理工大学材料科学与工程学院,广东 广州 510640)
铬酸盐钝化是热镀锌工业中常用的钝化处理工艺。铬酸盐钝化液通常是用重铬酸盐、铬酸或铬酸酐作为主盐配制而成,并通过后续添加主盐来维持钝化液所需Cr(VI)浓度。然而在实际生产中,铬酸盐钝化液在使用一段时间后,虽通过后续添加主盐使Cr(VI)含量保持在合理水平,但钝化效果会变差。经研究发现,这是由于镀锌件表面的锌在钝化过程中不断溶入钝化液,使钝化液中的锌离子浓度升高。当锌离子浓度达到一定值后就会对钝化效果产生明显的影响。
为解决上述问题,本课题组进行了铬酸盐钝化液的再生研究,既能将钝化液中的锌离子除去,又不对其他成分产生影响。离子交换技术是目前用于溶液去离子的技术之一[1-7],它具有选择性吸附等优点。本文利用732 强酸性阳离子交换树脂进行钝化液的再生研究。
1 实验
1.1 主要原料与仪器
732 强酸性阳离子交换树脂、717 强碱性阴离子交换树脂,分析纯,杭州争光树脂有限公司;纯锌(纯度≥99.995%),分析纯,四川宏达;铬酸酐,分析纯,深圳市吉田化工有限公司;硝酸、盐酸,分析纯,广州化学试剂厂;氢氧化钠,分析纯,广州市东红化工厂萝岗化学试剂分厂;EDTA 二钠,分析纯,江苏强盛功能化学股份有限公司;蒸馏水,自制。
JB-3 型磁力搅拌器,上海雷磁创益仪器仪表有限公司;PHS-3C 酸度计,上海佑科仪器仪表有限公司;ACL-210.3 电子天平,ACCULAB Sartorius Group;Z-2000 塞曼偏振原子吸收分光光度计,日本日立。
1.2 实验方法
1.2.1 树脂的预处理
将732 强酸性阳离子交换树脂用10%的NaCl 溶液先淋洗、浸泡8 h 后用蒸馏水反复淋洗。然后用5%的NaOH 溶液浸泡8 h,接着用蒸馏水冲洗至出水呈中性。再用HCl 溶液[V(盐酸)∶V(蒸馏水)=1∶8]浸泡8 h,将树脂转化为H 型。最后用去离子水冲洗至出水呈弱酸性(pH=5~6),在干燥箱内70°C 下干燥后储存备用。
1.2.2 钝化液的配制
用HNO3[V(硝酸)∶V(蒸馏水)=1∶3]溶解纯锌,用铬酸酐(60°C 下干燥2 h)作主盐,配制成含1 g/L铬酸酐、不同锌浓度的钝化液。用HNO3和NaOH 调pH。
1.2.3 树脂静态吸附试验
量取一定体积的钝化液在250 mL 的锥形瓶中,加入一定质量的预处理后的732 强酸性阳离子交换树脂,用磁力搅拌器以恒定转速180 r/min 在室温(实验期间温度为22~25°C)下进行交换处理。搅拌一定时间后,待树脂沉淀,取上层溶液按GB/T 9723–2007《化学试剂 火焰原子吸收光谱法通则》用火焰原子吸收光谱法(锌浓度<50 mg/L)和专利《一种热镀锌用六价铬钝化液中锌含量的测试方法》(申请号201410184714.2)中的滴定法(先用717 强碱性阴离子交换树脂将钝化液中的Cr(VI)吸附除去,取适量交换后的溶液,加入缓冲液及若干滴铬黑T 指示剂,用EDTA 滴定锌的含量)测定锌离子的浓度(锌浓度>50 mg/L)。按 GB/T 4698.11–1996《海绵钛、钛及钛合金化学分析方法 硫酸亚铁铵滴定法测定铬量(不含钒)》测定Cr(VI)浓度。因该溶液中铬以铬酸盐形式存在,故省却三价铬酸盐的氧化步骤。
树脂的吸附量按下式[8]计算:

其中,q──吸附量,mg/g;ρ0──吸附前溶液中Zn(II)质量浓度,mg/L;ρ1──吸附后溶液中Zn(II)质量浓度,mg/L;m──树脂的质量,g;V──钝化液的体积,L。
树脂对钝化液中锌或铬的吸附率wx按下式计算:

其中,ρi──吸附前溶液中Zn(II)或Cr(VI)的质量浓度,mg/L;ρe──吸附平衡后溶液中Zn(II)或Cr(VI)的质量浓度,mg/L。
1.2.4 树脂的脱附再生和使用寿命试验
取吸附饱和后的树脂,用蒸馏水洗涤2~4 次,然后用一定体积的HCl 溶液,以磁力搅拌180 r/min 进行脱附再生处理,时间30 min。
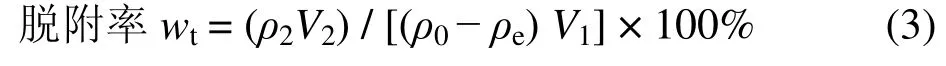
其中,V1──钝化液的体积,L;ρ2──HCl 溶液中脱附出来的Zn(II)质量浓度,mg/L;V2──HCl 溶液体积。
脱附再生后的树脂用去离子水冲洗后在70°C 干燥,再用该树脂进行钝化液交换处理。如此反复进行“吸附─再生─吸附”的实验若干次。
2 结果与讨论
2.1 交换处理时间对树脂吸附量的影响
按1.2.3 的实验方法,用预处理后的树脂对pH=3、含600 mg/L Zn(II)的钝化液进行交换处理。钝化液100 mL,树脂用量分别为0.50 g和1.00 g,交换处理时间0、5、10、15、20、30、45、60、120 min。
由图1a 可见,交换时间在0~15 min时,由于树脂上可交换吸附的位置较多,在吸附初期进行了大量离子交换,树脂的吸附量快速增加。当树脂用量为1.00 g时,钝化液中的Zn(II)浓度比树脂用量为0.50 g时下降更快,最终达到平衡时Zn(II)浓度更低(见图1b),树脂的平衡吸附量更小。这是因为随着树脂用量增加,树脂上可吸附交换空位增多,吸附速率增大,吸附效率提高。当吸附达到平衡时,树脂上的未饱和吸附位增多,因而单位质量树脂对钝化液中Zn(II)的吸附量反而下降[9]。

图1 交换处理时间对732 阳离子交换树脂吸附Zn(II)的影响Figure 1 Effect of contact time on adsorption of Zn(II)by 732 cation exchange resin
当交换时间为15~30 min,树脂的吸附量开始趋于平缓,30 min 后吸附量基本不再有明显变化,即吸附已达到平衡。
2.2 pH 对Zn(II)和Cr(VI)吸附率的影响
按1.2.3 的实验方法,用预处理后的树脂对不同pH(pH=1、2、3、4、5、6)、含600 mg/L Zn(II)的钝化液进行交换处理。钝化液体积100 mL,树脂用量1.00 g,交换处理120 min。
图2为pH 对吸附率的影响关系曲线图。

图2 pH 对732 阳离子交换树脂上Zn(II)和Cr(VI)吸附率的影响Figure 2 Effect of pH on adsorption percentages of Zn(II)and Cr(VI)with 732 cation exchange resin
从图2 可见,随pH 升高,树脂的Zn(II)吸附率从67.2%上升到97.3%。当pH为3~6时,随pH 上升,树脂吸附率已趋于平衡,即pH 对树脂的吸附量影响较小。而当钝化液的初始pH 在1~3时,pH 越低,树脂对Zn(II)吸附率越小。这是由于溶液中的H+与Zn(II)产生竞相吸附作用[10]。当pH 越小,溶液中的H+浓度越高,竞相吸附作用越强烈,越不利于树脂对Zn(II)的吸附。pH 从1 上升到2时,H+浓度降低10 倍,竞相吸附作用减弱,树脂对Zn(II)的吸附量从40.3 mg/g上升到53.5 mg/g,当pH 上升到3时,树脂的吸附量上升到57.3 mg/g。有研究者认为,溶液中H+浓度越高,离子交换树脂上交换基团─SO3H 的解离度越小[11],越不利于离子交换。因此,用该树脂再生处理铬酸盐钝化液时,钝化液pH 控制在3~6 最好,这也是目前国内批量热镀锌工厂常用钝化液的pH 控制范围。
由图2 可知,用树脂交换吸附Zn(II)后,溶液中Cr(VI)浓度(用滴定法测)不变,表明用树脂再生钝化液不会对Cr(VI)浓度产生影响,达到了“去锌保铬”的目的。
此外,当钝化液的pH 调整为7时,钝化液中出现大量Zn(OH)2白色沉淀。过滤除去沉淀物后测滤液中Zn(II)和Cr(VI)浓度,发现溶液中的Zn(II)浓度下降了83.5%,但同时Cr(VI)浓度也下降了约20.0%。由此可见,通过沉淀的方法虽然也能降低钝化液中Zn(II)浓度,但同时会将Cr(VI)吸附除去,不能达到“去锌保铬”的目的。
2.3 树脂用量对Zn(II)吸附率的影响
按1.2.3 的实验方法,用预处理后的树脂对pH=3、含600 mg/L Zn(II)的钝化液进行交换处理。钝化液体积100 mL,树脂用量分别为0.25、0.50、0.75、1.00、1.25和1.50 g,交换处理120 min。
从图3 可见,随树脂用量增加,树脂对钝化液中Zn(II)吸附率增大。当树脂用量达到1.00 g时,平衡吸附率趋于最大值,此时再增加树脂的用量,吸附率基本不再有很大变化。因此,对于100 mL 含锌600 mg/L的钝化液,1.00 g 732 强酸性阳离子交换树脂就可有效地降低锌离子浓度到理想水平(<30 mg/L)。
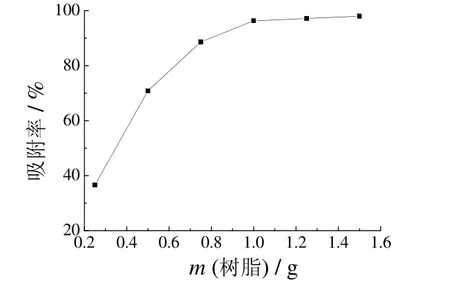
图3 732 阳离子交换树脂用量对Zn(II)吸附率的影响Figure 3 Effect of dosage of 732 cation exchange resin on adsorption percentage of Zn(II)
2.4 初始浓度对吸附量的影响
按1.2.3 的实验方法,用预处理后的树脂对pH=3,分别含100、200、300、400、500、600和800 mg/L Zn(II)的钝化液进行交换处理。钝化液体积100 mL,树脂用量0.50 g,交换处理120 min。
交换处理后,计算树脂在不同初始浓度下的平衡吸附量qe(mg/g)。分别用Langmuir和Freundlich方程[12-13]进行拟合。
Langmuir 吸附等温式:ρe/ qe=(1/qm)ρe+1/(qmKl)。
Freundlich 吸附等温式:lgqe=lgKf+(1/n)lgρe。其中,qm──饱和吸附量,mg/g;Kl、Kf、n──常数。
如图4 所示,树脂的平衡吸附量随Zn(II)初始浓度的增加而增大。当Zn(II)初始浓度增大到600 mg/L时,树脂吸附趋于饱和状态,Zn(II)初始浓度的继续增加无益于增大树脂的平衡吸附量。树脂对Zn(II)的饱和吸附量约为85.6 mg/g。
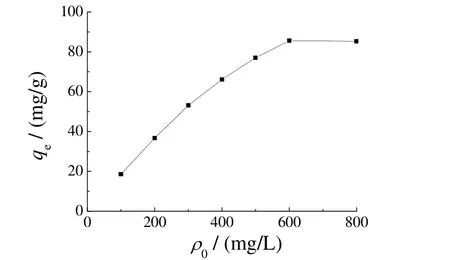
图4 Zn(II)初始质量浓度对其在732 阳离子交换树脂上吸附量的影响Figure 4 Effect of initial concentration of Zn(II)on its adsorption amount on 732 cation exchange resin
图5为按Langmuir 吸附等温式和Freundlich 吸附等温式进行拟合的吸附等温线。从图5 可见,Langmuir吸附等温线的线性相关度(以R2表征)比Freundlich 吸附等温线高,表明732 强酸性阳离子交换树脂对钝化液中Zn(II)的吸附更符合理想单分子层吸附,具有吸附饱和性。
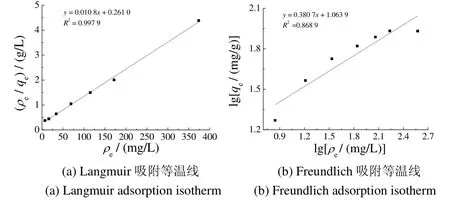
图5 Zn(II)在732 阳离子交换树脂上的吸附等温线Figure 5 Adsorption isotherm for Zn(II)on 732 cation exchange resin
2.5 树脂的脱附再生性
按1.2.3 的实验方法,用1.00 g 树脂对pH=3、含600 mg/L Zn(II)的100 mL 钝化液进行交换处理30 min 后,将树脂滤出,用去离子水冲洗并干燥后置于250 mL 锥形瓶中,加入100 mL HCl 溶液对树脂进行脱附再生处理。
从表1 可见,树脂多次再生后吸附性能依然良好,吸附量维持在较高水平。经过5 次脱附再生,吸附量仅下降约6.2%。树脂的脱附性能也非常好,脱附速率较快,经过30 min 脱附处理后,脱附率达98.0%以上。

表1 再生若干次后732 阳离子交换树脂的脱附性能与吸附量Table 1 Desorption performance and adsorption amount of 732 cation exchange resin after regeneration for several times
综上,732 阳离子交换树脂的脱附再生性能好,使用寿命长,适合工厂中铬酸盐钝化液的再生处理,具有非常好的经济、环保效益。
3 总结
(1)采用732 强酸性阳离子交换树脂吸附铬酸盐钝化液中的Zn(II),吸附速率快,在30 min 后基本达到吸附平衡。
(2)732 强酸性阳离子交换树脂吸附铬酸盐钝化液中Zn(II)的最佳pH为3~6。
(3)732 强酸性阳离子交换树脂再生钝化液不会对Cr(VI)浓度产生影响,能达到“去锌保铬”的目的。
(4)732 强酸性阳离子交换树脂对钝化液中Zn(II)的吸附符合单分子层吸附规律,具有饱和吸附性,饱和吸附量约为85.6 mg/g。
(5)732 强酸性阳离子交换树脂的吸附性能和脱附再生性能良好,可同时达到铬酸盐钝化液再生和树脂多次再生利用的目的。
[1]GALÁN B,CALZADA M,ORTIZ I.Separation and concentration of Cr(VI)from ground waters by anion exchange using Lewatit MP-64:Mathematical modelling at acidic pH [J].Solvent Extraction and Ion Exchange,2006,24 (4):621-637.
[2]GODE F,PEHLIVAN E.Removal of chromium(III)from aqueous solutions using Lewatit S 100:The effect of pH,time,metal concentration and temperature [J].Journal of Hazardous Materials,2006,136 (2):330-337.
[3]DEMIRBAS A,PEHLIVAN E,GODE F,et al.Adsorption of Cu(II),Zn(II),Ni(II),Pb(II),and Cd(II)from aqueous solution on Amberlite IR-120 synthetic resin [J].Journal of Colloid and Interface Science,2005,282 (1):20-25.
[4]TILLMAN G M.Water Treatment:Troubleshooting and Problem Solving [M].Boca Raton:CRC Press LLC,1996.
[5]SHI T H,WANG Z C,LIU Y,et al.Removal of hexavalent chromium from aqueous solutions by D301,D314 and D354 anion-exchange resins [J].Journal of Hazardous Materials,2009,161 (2/3):900-906.
[6]XU X,GAO B Y,YUE Q Y,et al.Preparation of new types of anion exchange resins from agricultural by-products and their utilization in the removal of various toxic anions from solutions [J].Chemical Engineering Journal,2011,167 (1):104-111.
[7]李红艳,李亚新,李尚明.离子交换技术在重金属工业废水处理中的应用[J].水处理技术,2008,34 (2):12-15,20.
[8]曾君丽,邵友元,易筱筠,等.D301 弱碱性阴离子交换树脂吸附Cr(VI)的研究[J].环境科学与技术,2012,35 (8):10-15,25.
[9]RENGARAJ S,JOO C K,KIM Y H,et al.Kinetics of removal of chromium from water and electronic process wastewater by ion exchange resins:1200H,1500H and IRN97H [J].Journal of Hazardous Materials,2003,102 (2/3):257-275.
[10]WONG C W,BARFORD J P,CHEN G H,et al.Kinetics and equilibrium studies for the removal of cadmium ions by ion exchange resin [J].Journal of Environmental Chemical Engineering,2014,2 (1):698-707.
[11]ALYÜZ B,VELI S.Kinetics and equilibrium studies for the removal of nickel and zinc from aqueous solutions by ion exchange resins [J].Journal of Hazardous Materials,2009,167 (1/3):482-488.
[12]杨金杯,韩淑萃,余美琼,等.001×14.5 强酸性树脂对铬(III)的吸附性能[J].中国有色金属学报,2012,22 (6):1791-1797.
[13]黄晓霞,刘茹.201×4 强碱性阴离子交换树脂吸附Cr(VI)的机理研究[J].广东化工,2010,37 (5):86-89.
