聚邻甲苯胺/纳米二氧化钛环氧复合涂层的性能
2014-11-25胡传波郑燕升王发龙莫春燕青勇权王勇莫倩
胡传波 ,郑燕升, *,王发龙,莫春燕,青勇权,王勇,莫倩
(1.广西科技大学生物与化学工程学院,广西 柳州 545006;2.广西科技大学鹿山学院,广西 柳州 545616)
防护涂料被广泛用于金属的腐蚀控制,使用导电聚合物作为腐蚀抑制剂已经逐渐引起人们的重视。在这些导电聚合物中,聚苯胺由于易于合成、具有良好的环境稳定性和潜在的商业利用价值,通常被认为是重要的导电聚合物。自从DeBerry[1]首次发现聚苯胺对铁基金属具有阳极保护作用以来,国内外陆续有很多关于聚苯胺对金属基底防腐性能的研究报道。与传统涂料富含重金属而危害人类健康和造成环境问题不同,聚苯胺涂料由于不含重金属、无毒性、对环境友好等特点,而深受越来越多的研究者所关注。
然而,聚苯胺由于分子链刚性强且链间具有较强的相互作用,导致其加工性能和溶解性能差,极大地限制了其应用和发展。有研究发现,聚苯胺分子苯环或醌环上的氢原子被氨基、烷基、烷氧基等给电子基团取代后,可以提高聚苯胺分子的溶解性和分散性[2];还有研究证实,给电子取代基修饰的聚苯胺分子比吸电子取代基修饰的聚苯胺分子具有更好的耐蚀性[3-4]。Sathiyanarayanan 等[5-6]将TiO2作为填充材料,与苯胺单体通过原位聚合法制备了聚苯胺/TiO2复合材料,将表面涂饰有聚苯胺涂层和聚苯胺/TiO2复合涂层的碳钢试样浸泡于3.0% NaCl 溶液中,发现复合材料比纯聚苯胺表现出更好的耐腐蚀性能。本文以过硫酸铵为氧化剂,采用原位聚合法制备了聚邻甲苯胺/纳米TiO2复合物,并研究了聚邻甲苯胺/纳米TiO2环氧复合涂层的耐腐蚀性能。
1 实验
1.1 试剂及仪器
苯胺(ANI,使用前减压蒸馏)、正丁醇和N−甲基吡咯烷酮(NMP),天津市科密欧化学试剂有限公司;盐酸、氨水、氯化钠、过硫酸铵(APS)和邻苯二甲酸二丁酯(DBP),西陇化工股份有限公司;邻甲苯胺(OT,使用前减压蒸馏)和无水乙醇,成都市科龙化工试剂厂;乙酸乙酯,广东省化学试剂工程技术研究开发中心。以上试剂均为分析纯。金红石型纳米TiO2,粒径10 nm,上海沪江实业有限公司;环氧树脂(EP)和聚酰胺树脂(低分子650),江西宜春远大化工有限公司;去离子水,实验室自制。
DF-101S 型集热式恒温加热磁力搅拌器,巩义市予华仪器有限责任公司;JJ-1 精密增力电动搅拌器,常州国华电器有限公司;ZFD-A5040A 全自动新型鼓风干燥箱,上海智城分析仪器制造有限公司;S-3400N扫描电子显微镜,日本HITACHI;DX-2700X 射线衍射仪,上海精密仪器仪表有限公司;UV-2102PC 紫外可见分光光度计,尤尼柯(上海)仪器有限公司;Nicolet380 傅里叶变换红外光谱仪,美国ThermoFisher公司;CHI660D 电化学测试仪,上海辰华仪器有限公司。
1.2 聚苯胺、聚邻甲苯胺/纳米TiO2复合物的制备
(1)按文献[7]的方法制备聚苯胺,标记为PANI。
(2)将10.71 g 邻甲苯胺加入盛有100 mL、1.0 mol/L盐酸溶液的烧杯中,机械搅拌5 min,得到无色澄清的邻甲苯胺盐溶液,然后依次配制2 份相同的溶液。向3 份溶液中各自加入质量分数为0.0%、7.5%、14.9%的纳米TiO2粒子,机械搅拌10 min,超声20 min;接着将混合乳液加入三口烧瓶中,冰水浴中磁力搅拌30 min,得到均匀分散的乳白色体系;称取22.82 g APS 溶于150 mL、1.0 mol/L 的盐酸溶液中,将该APS/HCl 溶液通过恒压漏斗缓慢滴加到上述混合体系中,15 min 内混合乳液的颜色由乳白色、浅蓝色、深蓝色转变至墨绿色,说明在纳米TiO2表面有聚邻甲苯胺形成,整个滴加过程持续2.5 h。滴加结束后,在冰水浴中继续磁力搅拌10 h,然后过滤,用乙醇和去离子水反复洗涤所得到的滤饼,直至滤液无色。将得到的墨绿色滤饼转移至烧杯中,向其中加入500 mL 1.0 mol/L 的氨水溶液,常温下磁力搅拌3 h;重复过滤和洗涤,将所得紫色滤饼置于60°C 干燥箱中20 h。最后,依次得到纳米TiO2质量分数为0.0%、7.5%、14.9%的聚邻甲苯胺/纳米TiO2复合物,分别标记为POT、PTC1和PTC2。
1.3 涂层的制备
在5.0 g 环氧树脂中加入1.5 mL 正丁醇和0.5 mL N−甲基吡咯烷酮混合溶剂,机械搅拌均匀;再加入1.5 g固化剂聚酰胺,继续搅拌;最后加入0.48 mL 增塑剂邻苯二甲酸二丁酯和0.56 mL 消泡剂乙酸乙酯,超声10 min 以便分散均匀。待复合涂料黏稠时涂刷于碳钢工作电极(25 mm × 18 mm)表面,置于60°C 干燥箱中固化12 h,得到环氧涂层。以PANI、POT、PTC1和PTC2为填充物,按照质量分数3%和5%分别加到5.0 g环氧树脂中,按照同样的方法在碳钢表面制得EP/PANI-1、EP/PANI-2,EP/POT-1、EP/POT-2,EP/PTC1-1、EP/PTC1-2,EP/PTC2-1、EP/PTC2-2 等涂层。
1.4 材料的表征
采用扫描电子显微镜对试样进行形貌观察,扫描电压范围为25~30 kV。采用KBr 压片法,用傅里叶红外吸收光谱分析试样的官能团,测试波数范围500~4 000 cm−1。用紫外–可见分光光度计确定物质的结构,测试波长范围200~850 nm。用X 射线衍射仪对试样进行物相分析,测试条件为:Cu 靶Kα 辐射,波长0.15 406 nm,管电压40 kV,管电流30 mA,扫描速率4°/min,步长0.03°,扫描角度10°~90°。
1.5 涂层的性能测试
按照GB/T 6739–2006《色漆和清漆 铅笔法测定漆膜硬度》测定涂层的硬度;按照GB/T 9286–1998《色漆和清漆 漆膜的划格试验》测定涂层的附着力,然后浸泡于3.5% NaCl 溶液中观察涂层是否出现剥落现象;按照GB/T 1731–1993《漆膜柔韧性测定法》测定涂层的柔韧性;按照GB/T 1732–1993《漆膜耐冲击测定法》测定涂层的冲击强度。按照GB/T 1763–1989《漆膜耐化学试剂性测定法》的甲法测定涂层的耐盐水性。
将涂刷有涂层的碳钢试样浸泡在3.5% NaCl 溶液中,采用电化学测试仪三电极体系测试涂层的极化曲线和交流阻抗。以饱和甘汞电极(SCE)为参比电极,铂电极(Pt)为辅助电极,待测碳钢试样为工作电极,研究涂层试样在3.5% NaCl 溶液中的耐腐蚀性能。极化曲线测试扫描电压范围−1.2~1.2 V,扫描速率5 mV/s;交流阻抗测试频率100 kHz~10 mHz。
2 结果与讨论
2.1 表面形貌分析
图1a、1b、1c、1d 和1e 分别为纳米TiO2、均聚物PANI 和POT 以及复合物POT/TiO2的SEM 照片。

图1 纳米TiO2、聚苯胺、聚邻甲苯胺和不同纳米TiO2含量的聚邻甲苯胺复合物的SEM 照片Figure 1 SEM images of nano-TiO2,polyaniline,poly-otoluidine,and poly-o-toluidine-based composite with different contents of nano-TiO2
图1a 中,较多的纳米TiO2粒子团聚在一起,形貌均一;图1b 中,PANI 由颗粒状絮状物构成不规则团聚体,有较多孔隙;图1c 中,POT 由大小不一的块状和颗粒状物构成不规则的团聚体,它们之间相互连接在一起,有一定的孔隙。从图1d、1e 可以看出,复合物的微观形貌与纳米粒子的含量密切相关,随着TiO2含量从7.5%增加到14.9%,纳米粒子分散不均匀,部分TiO2未被POT 分子包覆;当TiO2的含量为7.5%时,适量的纳米粒子在邻甲苯胺盐溶液中分散均匀,在氧化剂作用下引发邻甲苯胺单体从不同的方向吸附在其表面而发生聚合,使得纳米TiO2被包覆于POT分子内部,填补了聚合物的孔隙,形成表面结构致密性较好的复合物。
2.2 红外光谱分析
图2 为纳米TiO2、均聚物PANI、POT 与复合物POT/TiO2的红外图谱。其中,谱线b 上PANI 的特征吸收峰1 593 cm−1和1 504 cm−1处分别为醌环和苯环的C=C 伸缩振动吸收峰,1 307 cm−1和3 450 cm−1处分别为与苯环相连的C─N 和N─H 伸缩振动吸收峰,在1 156 cm−1和828 cm−1处的吸收峰分别为质子化的C─H 平面内伸缩振动和苯环的平面外弯曲振动[8-9];谱线c 上POT 则在波数为3 395、1 597、1 493、1 302、1 161和816 cm−1等处出现与PANI 相似的特征吸收峰,在2 913 cm−1处的吸收峰为甲基的C─H 伸缩振动吸收峰。谱线d 和e 是POT 包覆TiO2的FT-IR 谱图,与谱线a 和c 相比,复合物PTC 与POT 主要特征吸收峰相同。谱线a 上TiO2在670 cm−1左右的吸收峰为Ti─O伸缩振动吸收峰,由于POT 分子包覆在纳米粒子表面,使得整个复合物在该波数处的吸收峰变得非常微弱,整体吸收峰位置发生了轻微变化。这可能是邻甲苯胺单体在纳米粒子表面聚合的过程中,生成的POT 分子与纳米TiO2之间产生类似于氢键的相互作用,使得POT 分子的C=C、C─N 和N─H 等特征吸收峰强度弱化[10],从而导致复合物相应的吸收峰发生轻微移动。由此可以看出,复合物PTC 特征吸收峰与TiO2含量无关,POT 仍然按照自身的聚合机理发生聚合。
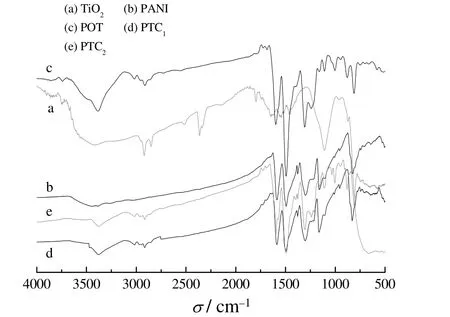
图2 纳米TiO2、聚苯胺、聚邻甲苯胺及含不同质量分数纳米TiO2的聚邻甲苯胺复合物的红外光谱Figure 2 FT-IR spectra of nano-TiO2,polyaniline,poly-o-toluidine,and poly-o-toluidine-based composites containing different mass fractions of nano-TiO2
2.3 紫外可见光谱分析
图3 为均聚物PANI、POT 与复合物POT/TiO2的紫外谱图。谱线a 中,PANI 在波长325 nm 和635 nm的2 个特征吸收峰分别属于苯环结构的π–π*电子跃迁和苯式到醌式的n–π*极化子转变[11-12];谱线b 中,POT在波长311 nm 和618 nm 处出现与PANI 相似的吸收峰,这可能是聚苯胺分子链中苯环或醌环上的氢原子被甲基取代后,甲基中C─H 的σ 键与苯环或醌环的键发生超共轭作用和空间位阻效应造成分子链扭曲,从而导致POT 分子相应的π–π*电子跃迁和n–π*极化子转变发生蓝移[13]。复合物PTC1和PTC2相应的吸收峰则分别位于波长295、615、293 和616 nm 处,吸收强度降低,吸收峰分别向短波方向移动。这是由于包覆的纳米TiO2粒子与POT分子之间存在类似氢键的相互作用,影响到了POT 分子链的规整性和共轭程度,导致复合物的特征吸收峰发生蓝移。
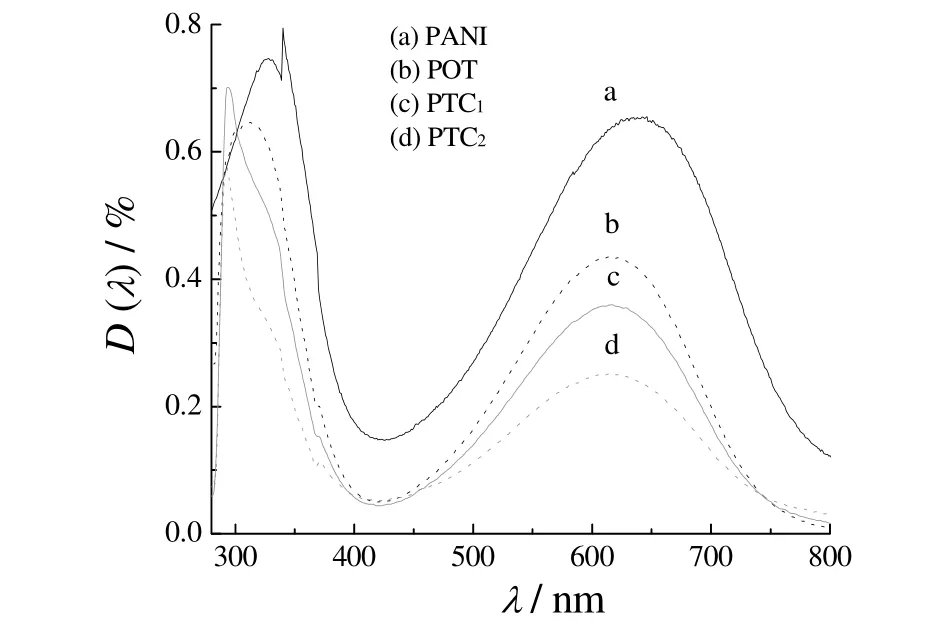
图3 聚苯胺、聚邻甲苯胺和聚邻甲苯胺/TiO2复合物的紫外光谱Figure 3 UV-vis spectra of polyaniline,poly-o-toluidine,and poly-o-toluidine/TiO2composites
2.4 XRD 分析
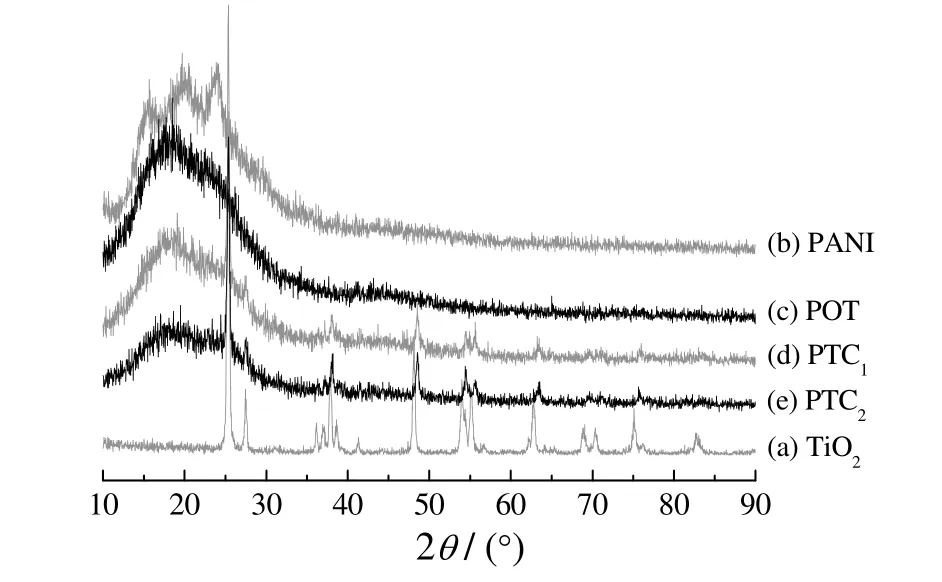
图4 纳米TiO2、聚苯胺、聚邻甲苯胺和聚邻甲苯胺/TiO2复合物的XRD 图谱Figure 4 XRD spectra of nano-TiO2,polyaniline,poly-o-toluidine,and poly-o-toluidine/TiO2composites
图4 为纳米TiO2、均聚物PANI 和POT 以及复合物POT/TiO2的XRD 谱图。其中,PANI 分别在2θ=16°、20°和25°处出现衍射峰,表明PANI 存在一定程度的结晶行为;POT 在2θ=20°处出现单一强衍射峰,可能是取代甲基的存在影响了整体聚合物的规整性,从而导致部分结晶行为被覆盖。从图4d、4e 可以看出,复合物PTC 同时具有POT 和TiO2的衍射特征,只是其特征衍射峰有所弱化,这可能是非晶态的有机聚合物包覆在纳米粒子表面,降低了纳米粒子产生衍射条件的质量数和体积数,从而削弱了复合物中POT 和纳米TiO2的特征衍射峰[14-15]。
2.5 涂层的力学性能测试
表1 是环氧涂层以及环氧分别与3%和5%的PANI、POT、PTC1和PTC2制得的涂层的力学性能测试结果。
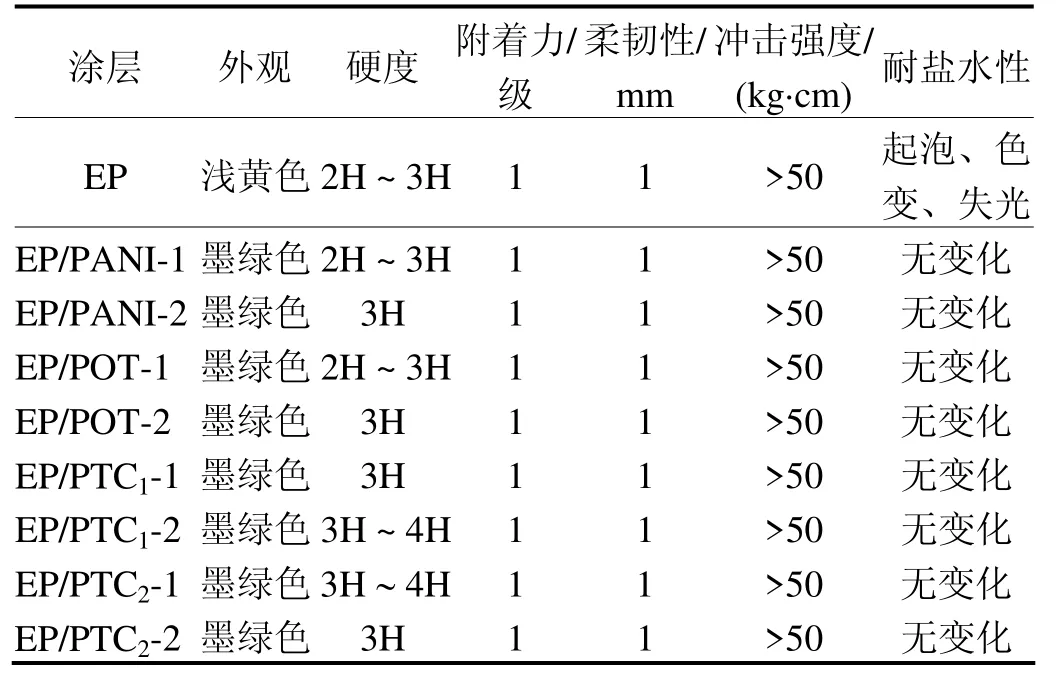
表1 不同涂层的力学性能Table 1 Mechanical properties of different coatings
由表1 可见,9 种涂层的附着力均达到了1 级,柔韧性均为1 mm,冲击强度均大于50 kg·cm。涂层EP/PANI、EP/POT 和EP/PTC1的硬度随填充物添加量的增加而增大,涂层EP/PTC2硬度随填充物添加量的增加而降低。这主要是由于复合物POT/TiO2的刚性较大,作为填料增强了环氧涂层的刚性,使得涂层硬度增大;而复合物PTC2结构中部分纳米粒子分散不均匀,作为填料添加到环氧涂层后,涂层均匀性随着添加量的增加而下降,硬度也相应地降低。9 种涂层在3.5% NaCl 溶液中浸泡15 d 后发现,环氧涂层EP 有轻微起泡、变光、失色等现象,可能是腐蚀介质浸透到了金属表面,引起涂层内部结构变化;另外8 种涂层无起泡、失色、生锈现象,说明填充物具有增强环氧涂层对腐蚀介质的阻隔性能。将划格后的涂层浸泡于3.5% NaCl 溶液中,发现涂层EP/PANI-2、EP/POT-2、EP/PTC1-2 和EP/PTC2-1 未出现明显的剥落现象,附着力最好。这是由于PANI 或POT 表面极性基团与环氧树脂极性基团相互作用,增强了涂层的粘结强度,随着均聚物或PTC1的增加,涂层的附着力逐渐增强;复合物PTC2因为纳米粒子分散不均匀,加至环氧涂料中后容易发生团聚,导致涂层的结构和机械性能变差,使得H2O、O2、Cl−等腐蚀介质容易通过涂层表面浸到金属基底,降低了涂层的附着力。环氧涂层EP 因为没有加入具有屏蔽作用的填充物,虽然引入的聚酰胺固化剂具有较强的固化效果,但是固化剂同时含有亲水性胺基,容易引起水在涂层中的渗透。因此,通过以上方法对涂层的物理性能测试表明,均聚物PANI 和POT、复合物PTC1在复合涂层中的质量分数为5%,复合物PTC2在复合涂层中的质量分数为3%时,涂层的力学性能最佳。
2.6 极化曲线测试
图5 为力学性能测试效果较好的EP/PANI-2、EP/POT-2、EP/PTC1-2、EP/PTC2-1 等4 种涂层在3.5%NaCl 溶液中浸泡一段时间后的极化曲线,表2 为利用直线外推法从对应的极化曲线中得到的电极腐蚀电位(φcorr)和腐蚀电流密度(jcorr)。

表2 不同环氧涂层电极的腐蚀电位和腐蚀电流密度Table 2 Corrosion potentials and corrosion current densities of the electrodes with different epoxy coatings
通过分析得知,涂层EP/PTC1-2 的腐蚀电位比涂层EP/PTC2-1 正移了117 mV,腐蚀电流密度下降了1个数量级;涂层 EP/PTC2-1 的腐蚀电位比涂层EP/POT-2 正移了123 mV,腐蚀电流密度下降了1 个数量级;涂层EP/POT-2 的腐蚀电位比涂层EP/PANI-2正移了31 mV,腐蚀电流密度仅为其1/3。结合腐蚀速率vcorr可以看出4 种涂层的耐腐蚀性能为EP/PTC1-2 >EP/PTC2-1 >EP/POT-2 >EP/PANI-2,表明给电子取代基修饰的聚邻甲苯胺的防腐能力强于聚苯胺,聚邻甲苯胺与纳米粒子的复合改性进一步提高了环氧涂层的耐腐蚀性能。这是因为表面结构存在一定孔隙的POT 分子与较小粒径的纳米TiO2复合后,复合物结构致密性和在环氧涂层中的分散性均得到了提高。POT 分子具有比碳钢高的氧化还原电位,当均匀分布的EP/POT/TiO2涂层开始被腐蚀介质浸透后,能够刺激复合物POT/TiO2在碳钢金属表面形成比均聚物POT 更强的Fe2O3钝化层,以阻隔腐蚀介质的浸透[16-17]。另外,纳米TiO2粒子的加入使得复合涂层中又增加了一种类似栅栏的屏障,使得气体分子和腐蚀溶液浸透到碳钢金属表面所经历的阻碍增多,从而延缓了腐蚀反应时间。因此,分子链较大的聚邻甲苯胺比聚苯胺更能增强环氧涂层的耐腐蚀性能。同时,纳米粒子的添加量也会影响到涂层的耐腐蚀性。以含7.5%纳米TiO2粒子的聚邻甲苯胺复合物为填充料的环氧涂层其耐蚀性优于以含14.9%纳米TiO2粒子的聚邻甲苯胺复合物为填充物的环氧涂层,原因是适量的纳米TiO2均匀分散在聚合物中增强了环氧涂层的屏障效应,但过量的纳米粒子在聚合物中分散不均匀,使环氧涂层出现堆积现象,从而导致腐蚀介质从涂层分散不均匀的界面浸透进入碳钢表面。
2.7 交流阻抗测试
图6 为涂层EP/PANI-2、EP/POT-2、EP/PTC1-2 和EP/PTC2-1 在3.5% NaCl 溶液中浸泡相同时间的交流阻抗谱。阻抗谱中极化电阻越小,腐蚀速率就越高,涂层耐腐蚀性能越差[18]。
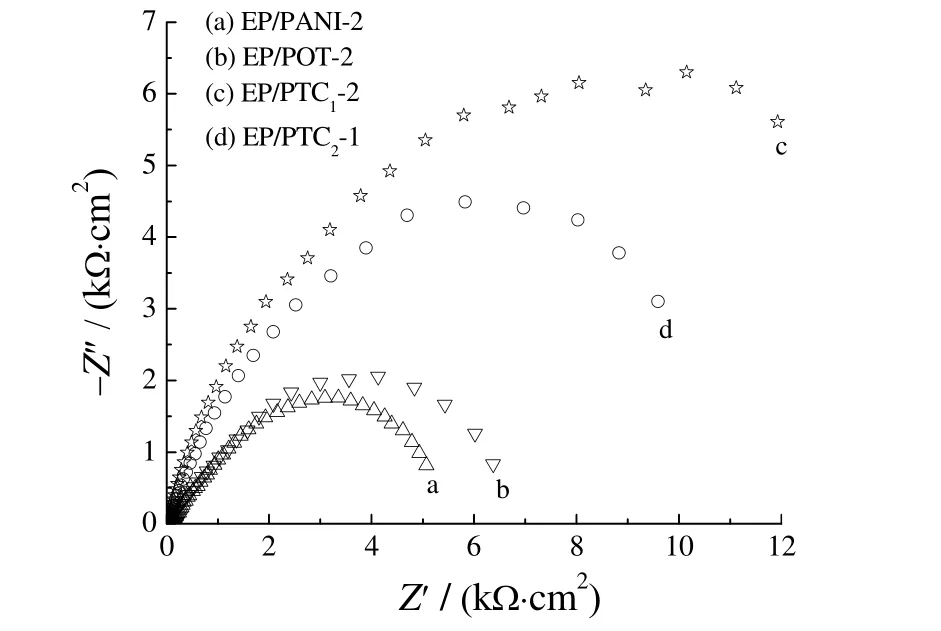
图6 不同环氧涂层的Nyquist 图Figure 6 Nyquist plots for different epoxy coatings
在图6 中,所有的谱线均显示为圆弧状,表现出明显的电容特征,具有较高的阻抗值,说明涂层在腐蚀介质中相对完好。复合涂层不仅阻隔了活性Cl−和水的浸透,而且也阻隔了氧气和电子的自由传递,抑制了碳钢金属表面的腐蚀。由图6可以看出,涂层EP/PTC1-2容抗弧半径最大,涂层EP/PANI-2 容抗弧半径最小,表明在3.5% NaCl 溶液中,涂层EP/PTC1-2 的阻抗值最大,对腐蚀介质的阻隔强度最大,腐蚀溶液和气体难于浸透到碳钢金属表面,有效地保护了金属基底;涂层EP/PTC2-1 由于纳米粒子分散不均匀,有轻微团聚现象发生,造成该涂层对腐蚀介质的阻隔强度有所降低,使得腐蚀溶液和气体容易在涂层分散不均匀的部分扩散,部分降低了涂层的防腐效果。结合SEM 及光谱分析结果可知,涂层EP/PTC1-2 由于适量的纳米TiO2粒子均匀致密地分布于聚邻甲苯胺孔隙部分,使得聚邻甲苯胺与无机纳米粒子之间存在较强的相互作用力,提高了复合物的颗粒分散性和结构致密性;而且聚邻甲苯胺分子邻位甲基给电子取代基与苯环或醌环的相互作用也能够增强复合物的反应活性,提高复合涂层对碳钢的表面吸附作用;分散在环氧涂层中的纳米TiO2自身也存在类似栅栏效果的阻隔性质,多种机理相互作用从物理方式上降低了腐蚀溶液和气体向碳钢表面浸透的速度,延缓了腐蚀反应时间。
3 结论
(1)采用化学氧化聚合法制备了均聚物聚苯胺和聚邻甲苯胺,通过原位聚合法制备了纳米TiO2添加量不同的POT/TiO2复合物。
(2)SEM 分析表明,聚邻甲苯胺/TiO2复合物孔隙率较均聚物少,致密性得到较大提高。纳米TiO2在邻甲苯胺单体聚合过程中被包覆于聚合物内部,含14.9%纳米TiO2的POT/TiO2复合物开始出现团聚现象,使其分散性降低;红外和紫外–可见光谱分析表明,聚邻甲苯胺与纳米TiO2之间存在类似氢键的相互作用,导致复合物的特征吸收峰发生迁移;XRD 分析表明,纳米TiO2对聚邻甲苯胺分子链结晶产生一定的影响,使复合物的晶型发生轻微变化。
(3)含3%和5%的聚苯胺、聚邻甲苯胺、聚邻甲苯胺/TiO2复合物的环氧涂层的力学性能测试表明,含5%的聚苯胺、聚邻甲苯胺和聚邻甲苯胺/TiO2(质量分数7.5%)复合物以及含3%的聚邻甲苯胺/TiO2(质量分数14.9%)复合物的环氧涂层的力学性能较佳。将这4 种涂层置于3.5% NaCl 溶液中浸泡一段时间后进行电化学分析,结果发现,含5%聚邻甲苯胺/TiO2(质量分数7.5%)复合物的环氧涂层的防腐性能最佳,其腐蚀电位为−445 mV,腐蚀电流密度为7.62 × 10−8A/cm2。
[1]DEBERRY D W.Modification of the electrochemical and corrosion behavior of stainless steels with an electroactive coating [J].Journal of the Electrochemical Society,1985,132 (5):1022-1026.
[2]刘先勇,刘军.聚苯胺衍生物的研究[J].化工新型材料,2005,33 (2):32-34,38.
[3]BENCHIKH A,AITOUT R,MAKHLOUFI L,et al.Soluble conducting poly(aniline-co-orthotoluidine)copolymer as corrosion inhibitor for carbon steel in 3% NaCl solution [J].Desalination,2009,249 (2):466-474.
[4]HÜR E,BEREKET G,ŞAHIN Y.Anti-corrosive properties of polyaniline,poly(2-toluidine),and poly(aniline-co-2-toluidine)coatings on stainless steel [J].Current Applied Physics,2007,7 (6):597-604.
[5]SATHIYANARAYANAN S,AZIM S S,VENKATACHARI G.Preparation of polyaniline–TiO2composite and its comparative corrosion protection performance with polyaniline [J].Synthetic Metals,2007,157 (4/5):205-213.
[6]SATHIYANARAYANAN S,AZIM S S,VENKATACHARI G.A new corrosion protection coating with polyaniline–TiO2composite for steel [J].Electrochimica Acta,2007,52 (5):2068-2074.
[7]胡传波,郑燕升,王发龙,等.聚苯胺/纳米碳酸钙复合物的制备及其防腐性能[J].电镀与涂饰,2014,33 (10):407-412.
[8]SAKHRI A,PERRIN F X,BENABOURA A,et al.Corrosion protection of steel by sulfo-doped polyaniline-pigmented coating [J].Progress in Organic Coatings,2011,72 (3):473-479.
[9]KANG E T,NEOH K G,TAN K L.Polyaniline:A polymer with many interesting intrinsic redox states [J].Progress in Polymer Science,1998,23 (2):277-324.
[10]LI X W,WANG G C,LI X X,et al.Surface properties of polyaniline/nano-TiO2composites [J].Applied Surface Science,2004,229 (1/4):395-401.
[11]KIM H J,PARK S H,PARK H J.Synthesis of a new electrically conducting nanosized Ag–polyaniline–silica complex using γ-radiolysis and its biosensing application [J].Radiation Physics and Chemistry,2010,79 (8):894-899.
[12]DENG J G,HE C L,PENG Y X,et al.Magnetic and conductive Fe3O4–polyaniline nanoparticles with core–shell structure [J].Synthetic Metals,2003,139 (2):295-301.
[13]郭亚平,郭亚军,吕君英.甲基对聚邻甲苯胺结构和性能的影响[J].高分子材料科学与工程,2005,21 (5):94-97.
[14]PAWAR S G,PATIL S L,CHOUGULE M A,et al.Polyaniline:TiO2nanocomposites:synthesis and characterization [J].Archives of Applied Science Research,2010,2 (2):194-201.
[15]WANG H,WANG R X,WANG L,et al.Preparation of multi-core/single-shell OA-Fe3O4/PANI bifunctional nanoparticles via miniemulsion polymerization [J].Colloids and Surfaces A:Physicochemical and Engineering Aspects,2011,384 (1/3):624-629.
[16]WESSLING B.Scientific and commercial breakthrough for organic metals [J].Synthetic Metals,1997,85 (1/3):1313-1318.
[17]魏亦军,褚道葆,姚文俐.纳米TiO2/聚苯胺复合膜电极的制备及其电化学性能[J].合成化学,2004,12 (1):69-72.
[18]KILMARTIN P A,TRIER L,WRIGHT G A.Corrosion inhibition of polyaniline and poly(o-methoxyaniline)on stainless steels [J].Synthetic Metals,2002,131 (1/3):99-109.
