IgA肾病伴IgG4相关性间质性肾炎1例报道
2014-11-05李聚敏周焕芝邹万忠黄巍王昱景张五星张智敏周伟赵学伟
李聚敏,周焕芝,邹万忠,黄巍,王昱景,张五星,张智敏,周伟,赵学伟
IgG4相关性疾病(IgG4-related disease,IgG4-RD)的发现可追溯至对自身免疫性胰腺炎(autoimmune pancreatitis,AIP)的研究。AIP首先于1995年由Yoshida等[1]提出,并认为该病的发病机制与自身免疫性因素显著相关。2003年Kamisawa等[2]首次引入IgG4系统性疾病概念后,临床医师对AIP等临床症候群进行了重新审视和深入研究。2010年Takahashi等[3]撰文正式宣告IgG4相关性疾病的诞生,并于2012年由Stone等[4]执笔公布了IgG4-RD的规范命名。IgG4-RD累及肾脏主要表现为间质性肾炎,合并其他肾病并不罕见,但合并IgA肾病尚未见公开报道。解放军309医院2013年收治了1例IgA肾病伴IgG4相关性间质性肾炎患者,现就其诊治与转归并相关文献复习报告如下,探讨IgG4-RD临床特点、发病机制及诊疗措施。
1 病例资料
患者男性,64岁。高血压病史3年,口服药物治疗,血压控制欠佳,最高血压可达180/120mmHg。2013年3月无明显诱因逐渐出现食欲不振、恶心、纳差、烦渴、多饮,不伴尿频、血尿、浮肿、消瘦。曾就诊于某中医院,经中草药治疗后,自觉症状改善。8月初,恶心、纳差逐渐加重,就诊于外院,查血Hb 113g/L、SCr 727μmol/L、K+7.19mmol/L、IgG 32g/L、IgA 5.6g/L,泌尿系超声提示双肾中度积水。临床诊断为“高钾血症,急性肾衰竭,梗阻性肾损害”,予血液透析治疗。进一步行腹部增强CT检查,提示腹膜后纤维化压迫双肾输尿管导致双肾积水,遂在膀胱镜下行双侧输尿管支架置入术。
2013年8月15日转入我院。入院检查:体温36.6℃,心率72/min,呼吸19/min,血压130/80mmHg,慢性病容,全身体检未触及淋巴结肿大,双肾区无叩击痛,输尿管行径无压痛。尿量2000ml/24h。血常规检查WBC 4.64×109/L,RBC 3.39×1012/L,Hb 96g/L,PLT 180×109/L;血生化检查BUN 18.04mmol/L,Cr 650μmol/L,UA 310μmol/L,TP 70.8g/L,ALB 37.2g/L,GLOB 33.6g/L,前白蛋白(pALB)306mg/L,同型半胱氨酸(HCY)41.9μmol/L,肾小球滤过率(GFR)8.001ml/min,Glu 5.74mmol/L,TCO221.2mmol/L,ALT 1U/L,AST 13U/L,ALP 62U/L、CHOL 3.84mmol/L,TG 1.75mmol/L,PL 2.16mmol/L,Ca2+2.22mmol/L,P3+1.64mmol/L,Na+136mmol/L,K+4mmol/L,Cl-98mmol/L;血清HBV、HCV、HIV病毒抗原抗体检查均阴性;血清IgG 17.37g/L,IgA 3.33g/L,IgM 0.47g/L,IgE 112g/L,C3 0.922g/L,C4 0.23g/L;自身抗体谱(ANA、ANCA、抗RNP/Sm、抗Sm、抗SS-A、Ro-52、抗SS-B、抗Scl-70、Pm-Scl、抗Jo-1、CENP-B、PCNA、抗ds-DNA、核小体、组蛋白、核糖体P蛋白)阴性,AMA(抗线粒体抗体)弱阳性;蛋白电泳白蛋白51.65%, α15%,α210.25%, β14.35%, β26.65%,γ 22.35%;尿液:白细胞0.7/HP,红细胞5.04/HP,上皮细胞0.27/HP,细菌0.02/HP,管型0.41/HP,相对密度≤1.005,pH6.5。入院诊断:急性肾功能不全,双侧肾积水,双侧输尿管支架置入术后。
2 治疗经过
给予血液透析(每周3次,每次4h)等治疗。入院后辅助检查:超声检查见右侧肾盂不规则无回声区(4.2cm×5.4cm)。泌尿系造影提示右肾及右侧中上段输尿管积水。CT扫描:头颅未见明显异常;右肺散在数个小结节,前段者较大;两肺门区未见异常;气管、支气管通畅;纵隔内未见肿大淋巴结;心影不大;冠状动脉壁钙化,升主动脉壁增厚;双侧输尿管走行区可见双J管影,其上端位于肾盂、下端位于膀胱区,右肾可见引流管影;双肾实质内未见异常密度影;膀胱充盈欠佳,未见明显异常密度影。心电图提示窦性心律,左心室肥厚,ST-T段改变,可疑异常Q波。9月3日复查BUN 17.95mmol/L,SCr 488 μmol/L,Hb 109g/L;超声测量左肾4.1cm×4.4cm×9.8cm,右肾4.0cm×4.3cm×9.8cm,前列腺2.8cm×3.8cm×3.1cm。
为明确肾脏病理改变,在超声引导下行右侧肾穿刺活检术。肾脏病理报告:光镜可见肾穿刺组织中有26个肾小球,其中2个缺血性硬化,其余肾小球系膜细胞和基质轻度弥漫性增生,局灶节段性中度加重伴内皮细胞增生,系膜区嗜复红蛋白沉积,大部分缺血皱缩,其中1个小细胞纤维性新月体形成;肾小管上皮空泡及颗粒变性,多灶状及片状萎缩;肾间质多灶状及片状淋巴细胞、单核细胞及浆细胞浸润伴纤维化;小动脉管壁增厚,管腔狭窄。免疫荧光检查可见2个肾小球,IgG(-)、IgA()、IgM(-)、C3()、FRA(-)、C1q(-),沿系膜区呈团块状沉积。免疫组化检查显示,CD138+的浆细胞在肾间质多灶状浸润,其中IgG4+的浆细胞>40%。电镜检查可见肾小球系膜细胞和基质增生,伴电子致密物沉积,上皮细胞足突节段性融合;肾小管萎缩;肾间质胶原纤维增生伴淋巴细胞、单核细胞浸润。肾脏病理诊断:局灶增生性IgA肾病伴IgG4相关性间质性肾炎(图1)。
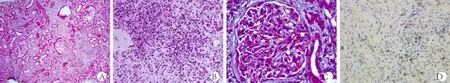
图1 肾活检组织病理Fig.1 Histopathology of renal biopsy
临床给予甲泼尼龙片(32mg,口服,1次/d)等治疗,肾功能明显改善。9月10日停止血液透析治疗。9月16日在全麻下经膀胱镜行双侧输尿管支架置换术,尿量2200ml/24h。患者基本情况明显好转,肾功能逐渐恢复,出院转门诊继续治疗。2013年12月CT报告右肺散在小结节较前无明显变化,腹膜后纤维化较前减少。2014年1月检查血清IgG亚型IgG1 5.49g/L,IgG2 1.6g/L,IgG3 0.386g/L,IgG4 0.452g/L。
3 讨 论
IgG4-RD多发生于中老年男性,属于免疫介导性疾病,几乎累及所有器官系统,肾外器官中胰腺、泪腺和唾液腺最常受累。胰腺受累时(旧称自身免疫性胰腺炎),以胰腺弥漫性肿大、胰管广泛狭窄为特点,血IgG4水平升高具有很高的敏感性(95%)和特异性(97%),临床表现和影像学检查均与胰腺癌相似[5]。泪腺及唾液腺受累时(旧称米库利兹病),以对称性泪腺、唾液腺及颌下腺等腺体肿胀、且肿胀的腺体中有大量淋巴细胞浸润为特点。该病也常累及肝胆管系统、眼、硬脑膜、垂体、甲状腺、主动脉、肺脏、胸膜、心包、胸腔纵隔、腹膜后、肠系膜、皮肤、淋巴结、乳腺及前列腺等组织器官,其特征性组织学表现均为组织中大量淋巴细胞和IgG4阳性浆细胞浸润伴纤维化或硬化[6]。IgG4-RD导致的组织学损伤,如进展性纤维化和器官损伤,通常被认为与Th2淋巴细胞参与的免疫调节反应相关。尽管IgG4抗体在IgG4-RD时显著增多,但并无证据显示其参与了对靶器官的损伤。IgG4-RD对糖皮质激素反应良好(减量和停药容易复发),但长期预后尚有待进一步观察。利妥昔单抗也可使血清IgG4水平快速下降,并使IgG4-RD的临床和组织学损伤得到快速逆转。
日本的Okazaki课题组和Umehara课题组反复修订并于2012年联合提出了IgG4-RD的诊断标准[7]。临床特征条件:①尿液、肾功能检查有任何异常,血清学检查有高IgG血症、低补体血症、高IgE血症中任何一项;②影像学有特征性的异常改变(弥漫性肾脏肿大、肾实质多发性低密度区域、单发性肾肿瘤、肾盂壁肥厚);③有高IgG4血症(≥1350mg/L);④肾脏病理有以下两种改变:(A)有明显的淋巴细胞、浆细胞浸润,IgG4或IgG阳性浆细胞比≥40%和(或)IgG4阳性浆细胞数量>10个/HP;(B)浸润细胞周围有特征性的纤维化改变;⑤肾脏以外的脏器组织病理学检查有淋巴细胞、浆细胞浸润伴纤维化改变,IgG4或IgG阳性浆细胞比例≥40%和(或)IgG4阳性浆细胞数量>10个/HP。诊断标准:第一,(1)①+③+④(A,B),(2)②+③+④(A,B),(3)②+③+⑤,(4)①+③+④(A)+⑤,具有以上4种组合之一者即可临床确诊;第二,(1)①+④(A,B),(2)②+④(A,B),(3)②+⑤,(4)③+④(A,B),具有以上4种组合之一者即可临床拟诊;第三,(1)①+③,(2)②+③,(3)①+④(A),(4)②+④(A),具有以上4种组合之一者即可临床疑诊。
肾脏损害病理表现主要为肾小管间质性肾炎[8],光镜可见弥漫或片状淋巴细胞、浆细胞浸润,病变部位与非病变部位界线清楚,病变常累及肾皮质、肾髓质、肾被膜、腹膜等,且IgG4和IgG阳性浆细胞比例≥40%和(或)IgG4阳性浆细胞数量>10个/HP。浸润细胞周围有特征性的纤维化,呈螺旋环状(鸟眼征),伴肾小管萎缩。免疫荧光检查可见IgG、C3、κ、λ沿毛细血管壁呈颗粒样沉积,偶可见沉积于系膜区,呈颗粒样。电镜检查80%以上病变部位肾小管基底膜可见电子致密物沉积,包曼囊、肾间质也常可见免疫复合物沉积。
IgG4相关性间质性肾炎通常伴发特发性膜性肾病[9-11],而伴发IgA肾病尚未见文献报道,其发病原因、机制,以及两者是否有内在关联尚不清楚。本例患者因双侧输尿管受后腹膜纤维化增生压迫导致梗阻,肾功能急骤恶化,解除泌尿系梗阻后肾功能稍有改善,这与梗阻性肾病及肾后性因素导致的肾衰竭明显不同。为进一步明确肾衰竭病因,排查是否存在可能的肾性因素,择期予以肾活检病理检查,其病理诊断“局灶增生性IgA肾病伴IgG4相关性间质性肾炎”支持临床推断,即该患者肾衰竭同时存在肾性和肾后性因素。临床给予甲泼尼龙片治疗,患者后腹膜纤维化及输尿管梗阻显著缓解,肾功能明显改善。
综上所述,笔者认为,IgG4相关性间质性肾炎临床上多表现为急性或慢性肾功能不全,影像学上可见肾脏受累,组织病理以间质大量IgG4阳性浆细胞浸润的小管间质性肾炎为主要特征,临床工作中如发现梗阻性肾脏疾病伴血清lgG4增高及肾脏或肾外组织中特征性lgG4阳性浆细胞增多,临床医师需考虑此病。
[1]Yoshida K, Toki F, Takeuchi T, et al. Chronic pancreatitis caused by an autoimmune abnormality. Proposal of the concept of autoimmune pancreatitis[J]. Dig Dis Sci, 1995, 40(7): 1561-1568.
[2]Kamisawa T, Funata N, Hayashi Y, et al. A new clinicopathological entity of IgG4-related autoimmune disease[J]. J Gastroenterol,2003, 38(10): 982-984.
[3]Takahashi H, Yamamoto M, Suzuki C, et al. The birthday of a new syndrome: IgG4-related diseases constitute a clinical entity[J]. Autoimmun Rev, 2010, 9(9): 591-594.
[4]Stone JH, Khosroshahi A, Deshpande V, et al. Recommendations for the nomenclature of IgG4 related disease and its individual organ system manifestations[J]. Arthritis Rheum, 2012, 64(10):3061-3067.
[5]Jing L, Li D, Li YL. Autoimmune pancreatitis complicating associated IgG4 cholangitis: a case report[J]. Chin J Pract Int er Med, 2013, 33(12): 987-989. [荆雷, 李丹, 李异玲. 自身免疫性胰腺炎合并IgG4相关性胆管炎1例报告[J]. 中国实用内科杂志, 2013, 33(12): 987-989.]
[6]Dong LL. Laboratory and pathologic characteristics of immunoglobulin G4 related diseases and notes on its diagnosis[J]. Chin J Pract Inter Med, 2013, 33(12): 928-930.[董凌莉. IgG4相关性疾病的实验室病理特点及其诊断注意事项[J]. 中国实用内科杂志, 2013, 33(12): 928-930.]
[7]Umehara H, Okazaki K, Masaki Y, et al. Comprehensive diagnostic criteria for IgG4-related disease (IgG4-RD), 2011[J].Mod Rheumatol, 2012, 22(1): 21-30.
[8]Cornell LD. IgG4-related kidney disease[J]. Semin Diagn Pathol,2012, 29(4): 245-250.
[9]Wada Y, Saeki T, Yoshita K, et al. Development of IgG4-related disease in a patient diagnosed with idiopathic membranous nephropathy[J]. Clin Kidney J, 2013, 6(5): 486-490.
[10]Stone JH. IgG4: a tantalizing link between causes of membranous glomerulonephritis and systemic disease[J]. Kidney Int, 2013,83(3): 348-350.
[11]Alexander MP, Larsen CP, Gibson IW, et al. Membranous glomerulonephritis is a manifestation of IgG4-related disease[J ].Kidney Int, 2013, 83(3): 455-462.
