系统性红斑狼疮患者血清基质金属蛋白酶-9浓度变化的Meta分析
2014-10-24侯传云张源潮蚌埠医学院第一附属医院风湿免疫科安徽蚌埠33004山东省立医院风湿免疫科济南500
侯传云,赵 萍,张源潮(.蚌埠医学院第一附属医院风湿免疫科,安徽蚌埠 33004;.山东省立医院风湿免疫科,济南 500)
系统性红斑狼疮(SLE)是一种可累及多系统、多脏器的自身免疫性疾病,其发病机制至今尚未完全明确,临床表现复杂多变,病情迁延反复,晚期患者多因累及肺、肾等重要脏器的严重并发症而死亡。基质金属蛋白酶-9(MMP-9)可通过降解血管基底膜的主要成分,使内皮细胞通透性增加,有利于炎性细胞侵入血管壁引起炎性反应,并可与肿瘤坏死因子-α(TNF-α)及白细胞介素(IL)-1β等细胞因子相互作用放大炎性反应[1]。但目前关于SLE患者血清MMP-9浓度变化及与病情活动性的关系文献报道结论并不一致,血清 MMP-9浓度能否作为SLE协助诊断及病情活动判断的指标尚存在争议。
Meta分析通过将同类研究结果进行定量综合,能达到增大标本量、改进和提高统计学检验功效的目的。它不仅可以定量估计研究效应的平均水平,对有争议甚至互相矛盾的研究结果得出较为明确的结论;而且还能发现以往研究的不足之处、揭示单个研究中存在的不确定性并提出新的课题和研究方向。
因此,对SLE患者血清MMP-9浓度变化进行Meta分析,以期能够进一步明确SLE患者血清MMP-9浓度的变化情况及其临床意义。
1 材料与方法
1.1 文献的获取 使用计算机检索,采用主题词和自由词相结合的方法在Pubmed文献数据库、中国生物医学(CBM)文献数据库、中国知网(CNKI)文献数据库及维普(VIP)科技期刊数据库中分别检索“lupus erythematosus,systemic”和“matrix metalloproteinase 9”及“基质金属蛋白酶9”和“红斑狼疮,系统性”,对检索结果进行手工甄别并同时进行文献追溯,收集国内外公开发表的有关血清MMP-9浓度与SLE的研究文献,并严格进行筛选。
1.1.1 文献纳入标准 (1)以人类为研究对象;(2)使用酶联免疫吸附试验(ELISA)检测血清 MMP-9浓度;(3)有原始数据的文献;(4)独立的病例对照研究;(5)论著性文献。
1.1.2 文献剔除标准 (1)动物模型中的研究;(2)未检测或未用ELISA检测血清 MMP-9浓度;(3)自身对照研究;(4)综述性文献或病例报道;(5)重复报告、报道信息太少而无法使用的文献。
1.1.3 文献筛选及资料提取 2名文献评价员独立检索并提取资料,意见不一致时经讨论决定。查找纳入文献全文并填写文献信息登记表。
1.2 数据分析
1.2.1 数据提取 根据此次 Meta分析的研究目的,设计信息提取表,显示研究者、发表时间、例数、均数和标准差等信息。
1.2.2 统计学处理 使用Rev Man 5.0软件进行Meta分析。首先判断各组间是否存在异质性(检验水准为α=0.1)。如组内各研究间存在异质性(P<0.1,I2>50%),则采用随机效应模型;如组内各研究间无异质性(P≥0.1,I2≤50%)则采取固定效应模型。以森林图形式展示所得结果,使用倒漏斗图分析发表偏倚。
2 结 果
2.1 入选文献 初步检索得到相关外文文献50篇,中文文献41篇。严格按照纳入标准和剔除标准筛选,最终有7篇文献入选。入选文献基本特征见表1。
2.2 Meta分析结果
2.2.1 SLE患者与健康对照组血清MMP-9浓度的比较 所选7篇文献均对SLE患者血清MMP-9浓度与健康对照组进行了比较,各研究间存在异质性(P<0.01,I2=96%),采用随机效应模型进行Meta分析,结果显示,SLE患者血清MMP-9浓度与健康对照组相比差异无统计学意义[MD=17.87,95%CI-23.40~59.15,P=0.40]。详见图1。
2.2.2 活动期SLE患者与非活动期SLE患者血清 MMP-9浓度的比较 所选7篇文献中有2篇对活动期SLE患者血清MMP-9浓度与非活动期SLE患者进行了比较,研究间不存在异质性(P=0.50,I2=0%),采用固定效应模型进行 Meta分析,结果显示,活动期SLE患者血清MMP-9浓度较非活动期SLE患者降低,其差异有统计学意义[MD=-109.86,95%CI-183.29~36.43,P=0.003]。详见图2。
2.2.3 发表偏倚评估 对所有入选的文献结果进行倒漏斗图分析,结果显示不对称,提示存在发表偏倚,可能存在阴性结果未能发表,如图3所示。

表1 纳入文献的基本特征

图1 SLE患者与健康对照组血清MMP-9浓度比较
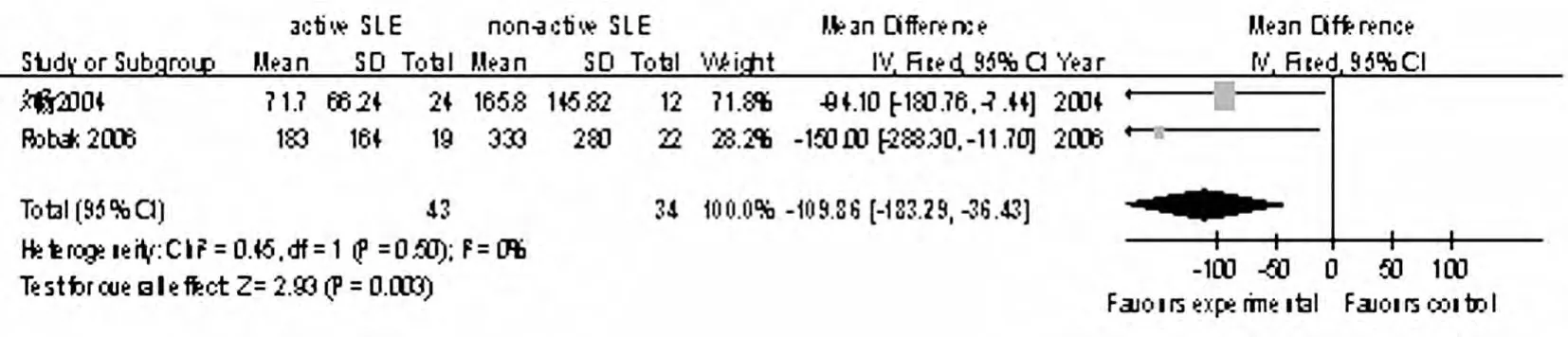
图2 活动期SLE患者与非活动期SLE患者血清MMP-9浓度比较

图3 SLE患者血清MMP-9浓度Meta分析倒漏斗图
3 讨 论
MMP-9是一种糖基化蛋白酶,是基质金属蛋白酶家族成员之一,属明胶酶,主要降解细胞外基质的各型胶原、明胶、蛋白聚糖及弹性蛋白等。MMP-9在SLE发生、发展中的作用越来越为人们所关注,不断有研究提示MMP-9参与SLE发病的多个环节,在SLE发生、发展中起到重要作用。关于SLE患者血清MMP-9浓度的变化,已有文献报道,但结论并不一致。
因此本文对SLE患者血清MMP-9浓度与健康对照比较的研究进行Meta分析,结果显示SLE患者血清MMP-9浓度与健康对照相比并无差异。既往研究普遍认为SLE患者PBMCs分泌MMP-9的能力增高,SLE患者血清 MMP-9水平及活动期SLE患者血清MMP-9水平没有随之相应增高的原因考虑与MMP-9在靶器官的局部沉积有关。Sekiuchi等[8]使用免疫荧光、原位杂交及免疫电镜等方法发现MMP-9在狼疮性肾炎(LN)患者肾组织弥漫性表达,而有关LN患者血清MMP-9浓度的研究多提示LN患者血清MMP-9浓度降低,提示SLE患者受损脏器局部有MMP-9的大量沉积。
既往对SLE患者血清MMP-9浓度变化研究结论不一致甚至相互矛盾的结果考虑为以下原因所致:(1)大多研究并未对所纳入的SLE患者中活动期患者所占比例进行描述,可能存在活动期患者比例不同,活动期患者比例高者患者组MMP-9浓度偏低,而活动期患者比例偏低者患者组MMP-9浓度偏高;(2)血清MMP-9浓度受白细胞、血小板数目影响较大,各研究中血液系统受损情况不明,并发低白细胞血症及低血小板血症者所占比例高的患者组MMP-9浓度偏低,而此类患者比例偏低的患者组 MMP-9浓度偏高;(3)Jung[9]研究表明,对同样一批标本,使用空白试管、加入促凝剂的试管和不同抗凝剂的试管收集全血并分离血清,所得MMP-9浓度各不相同,可能亦为研究结果不一致的原因之一。以上分析提示临床做类似研究时对血标本的处理应采用统一规范的方法进一步避免误差的产生。
虽然既有文献对SLE患者血清MMP-9浓度变化结果并不一致,但关于活动期SLE患者与非活动期相比的研究均认为活动期患者血清MMP-9浓度降低。SLE患者PBMCs分泌MMP-9增加,而血小板是SLE患者 MMPs的来源之一,但SLE患者多存在血液系统损害,白细胞及血小板常有不同程度的减少,为病情活动的表现之一,可能为活动期SLE患者血清MMP-9浓度减低的原因之一;其次,病情活动时多出现不同程度的脏器受累,而多项研究表明,SLE受累脏器局部出现MMP-9的沉积,亦可使得活动期SLE患者血清 MMP-9浓度减低。
本文对有关活动期、非活动期SLE患者血清MMP-9浓度研究的Meta分析显示活动期SLE患者血清MMP-9浓度低于非活动期患者。但由于其纳入研究例数仅为2例,活动期患者共计43例,非活动期患者共计34例,标本量偏小,且血清MMP-9浓度受患者白细胞数目、血小板数目和脏器受累情况影响较大,可为低白细胞血症、低血小板血症、狼疮肾炎、狼疮脑病的伴发现象。
此外,MMP-9常以酶原形式存在,特定条件下被激活成活化状态方起生物学作用,既往研究多是使用ELISA检测总MMP-9的浓度,不足以表明MMP-9的功能状态;提示以后的研究可使用明胶酶谱分析法检测MMP-9的活性变化。
近年关于 MMP-9的研究又有新突破,Cauwe等[10]研究表明MMP-9可通过清除具有免疫原性底物的自身表位来抑制系统性自身抗体介导的自体免疫,在抑制淋巴细胞增殖和系统性自身免疫发展中起到保护作用,推翻了长期以来将MMP抑制剂应用于自身免疫性淋巴细胞增殖症及SLE中的观念,提示MMP-9在SLE等自身免疫性疾病中作用复杂,机制未明,以后的研究可侧重于其功能状态、在自身免疫炎症发生发展中的具体作用及调控因素等方面。
综上所述,血清 MMP-9浓度不能用于协助诊断SLE,在临床上作为病情活动及疗效判断指标应用价值十分有限。
[1] 洪华,张玲英,王智斌,等.系统性红斑狼疮患者血清MMP-9、TIMP-1及 TNF-α水平测定及意义[J].四川医学,2009,30(1):127-129.
[2] Chang YH,Lin IL,Tsay GJ,et al.Elevated circulatory MMP-2and MMP-9levels and activities in patients with rheumatoid arthritis and systemic lupus erythematosus[J].Clin Biochem,2008,41(12):955-959.
[3] Hou C,Zhang Y.Expression of reversion-inducing cysteine-rich protein with Kazal motifs in peripheral blood mononuclear cells from patients with systemic lupus erythematosus:links to disease activity,damage accrual and matrix metalloproteinase 9secretion[J].J Int Med Res,2008,36(4):704-713.
[4] Robak E,Wierzbowska A,Chmiela M,et al.Circulating total and active metalloproteinase-9and tissue inhibitor of metalloproteinases-1in patients with systemic lupus erythomatosus[J].Mediators Inflamm,2006,(1):17898.
[5] Ainiala H,Hietaharju A,Dastidar P,et al.Increased serum matrix metalloproteinase 9levels in systemic lupus erythematosus patients with neuropsychiatric manifestations and brain magnetic resonance imaging abnormalities[J].Arthritis Rheum,2004,50(3):858-865.
[6] Liu Y,Zheng M,Yin WH,et al.Relationship of serum levels of HGF and MMP-9with disease activity of patients with systemic lupus erythematosus[J].Zhejiang Da Xue Xue Bao Yi Xue Ban,2004,33(4):340-343.
[7] Fujimoto N,Hosokawa N,Iwata K,et al.A one-step sandwich enzyme immunoassay for human matrix metalloproteinase 9using monoclonal antibodies[J].Clin Chim Acta.,1994,231(1):79-88.
[8] Sekiuchi M,Kudo A,Nakabayashi K,et al.Expression of matrix metalloproteinases 2and 9and tissue inhibitors of matrix metalloproteinases 2and 1in the glomeruli of human glomerular diseases:the results of studies using immunofluorescence,in situ hybridization,and immunoelectron microscopy[J].Clin Exp Nephrol,2012,16(6):863-874.
[9]Jung K.Careful attention to blood sampling as a preanalytical determinant of circulating matrix metalloproteinase 9to avoid misinterpretations:comment on the article by Ainiala et al[J].Arthritis Rheum,2005,52(2):673-678.
[10]Cauwe B,Martens E,Sagaert X,et al.Deficiency of gelatinase B/MMP-9aggravates lpr-induced lymphoproliferation and lupus-like systemic autoimmune disease[J].J Autoimmun,2011,36(3/4):239-252.
