炎症致巨噬细胞和血管平滑肌细胞低密度脂蛋白受体反馈调控差异的研究*
2014-10-24范忠才郑文武郑舒展泸州医学院附属医院心血管内科四川泸州646000重庆医科大学附属第一院心血管内科40006
叶 强,雷 寒,范忠才,郑文武,郑舒展(.泸州医学院附属医院心血管内科,四川泸州 646000;2.重庆医科大学附属第一院心血管内科 40006)
低密度脂蛋白受体(LDLr)是结合血浆LDL胆固醇及调控血浆胆固醇浓度的主要受体。LDLr活性受依赖于细胞内胆固醇水平的负反馈系统的严密调控,细胞内胆固醇处于稳态水平,故生理条件下天然LDL孵育细胞不能致细胞泡沫化[1]。LDLr抑制50%所需LDL浓度定义为IC50(Inhibition Concentration50),代表LDLr下调敏感性。
本课题组以往研究显示,炎症应激可以扰乱人肾脏系膜细胞和肝脏细胞LDLr反馈调控,允许胆固醇摄入增加,导致过多胆固醇沉积。同时实验显示,肝细胞和肾脏系膜细胞对胆固醇摄取有不同的能力和敏感性。生理条件下,肾脏系膜细胞LDLr对胆固醇负荷诱导的下调反应比肝细胞敏感,而肝细胞LDLr对下调表现出抵抗表型。然而,炎症应激改变了LDLr调控从敏感到抵抗的表型,从而增加了肾脏系膜细胞LDL摄入阈值,使肾脏系膜细胞从功能上类似肝细胞最大化摄入LDL,导致泡沫化[2-8]。巨噬细胞和血管平滑肌细胞均为脂质代谢的外周细胞,也是参与动脉硬化的主要细胞类型。然而,LDLr调控差异在外周细胞中仍不是很清楚。本研究探讨生理条件下,人单核细胞系(THP-1)巨噬细胞和血管平滑肌细胞LDLr负反馈调控的差异,以及炎症应激怎样以细胞特异性方式改变LDLr反馈调控。
1 材料与方法
1.1 材料 THP-1购于美国典藏生物中心(ATCC),No:TIB-202;人原代冠状动脉平滑肌细胞(VSMCs)购于TCS cell works(Buckinghamshire,UK);细胞生长培养基 DMEM/F12、RPMI1640、胎牛血清(FCS)购于北京 Hyclone公司。小牛血清清蛋白(BSA)、青霉素、链霉素、LPS(Escherichia coli)、佛波酯(PMA)、四乙酸乙二胺(EDTA)、叔丁基对甲酚(BHT)和二甲基亚砜(DMSO)均购于美国Sigma公司。LDL采用两步法密度梯度超速离心方法,从人新鲜液体血浆中自行制备;细胞内胆固醇测定试剂购于美国Sigma公司;总RNA提取试剂盒及荧光定量PCR试剂盒购于大连Takara公司;逆转录试剂盒购于美国ABI公司。
1.2 方法
1.2.1 细胞培养及分组 THP-1生长至对数期,加入PMA诱导分化为巨噬细胞,实验培养基(为含抗氧化剂EDTA及BHT的无血清培养基)培养24h,进入实验分组;VSMCs在生长培养基中生长至实验所需数量后,用实验培养基处理24h,进入实验分组,对照组:实验培养基继续培养;高脂组:实验培养基中加入LDL,终浓度为0~200μg/mL;高脂加LPS刺激组:实验培养基中加入LDL,再加入LPS,终浓度为0~1 000 ng/mL;以上各组细胞培养24h后收获。
1.2.2 总RNA提取及反转录聚合酶链反应(RT-PCR) 根据RNAiso试剂盒操作说明分别提取实验THP-1单核细胞、THP-1巨噬细胞和VSMCs细胞总RNA,500ng总RNA作为模板,选用 ABI逆转录试剂盒,逆转录体系20μL,含:50 mmol/l KCl,10mmol/L Tris.HCl,5mmol/L MgCl2,每 种dNTP浓度为1mmol/L,2.5μmol/L六碱基随机引物,20U RNAsin和50UMoloney小鼠白血病病毒;逆转录在DNA Thermal Cycler(Eppendorf)中进行,参数为:25℃ 10min,37℃120min,85℃5s;cDNA合成后,用SYBR Green I PCR Master Mix(Takara)在Opticon 2RT-PCR Detector(Bio-Rad)进行荧光定量PCR反应,热循环条件包括50℃2min,95℃5 min,95℃20s,55℃20s,共40个循环,95℃1min,55℃ 1 min,55~95℃每增加0.5℃读板,作溶解曲线。实验在细胞水平重复4次。β-actin作为参照基因。RRl-PCR结果以CT值来表示起始模板的数量,CT值越小起始模板的数量越大。本实验均用比较CT值法-ΔΔCT来表示基因的表达水平,计算公式如下:实验组相对于对照组基因表达水平的倍数=-exp(ΔΔCT),其中ΔΔCT=实验组ΔCT-对照组ΔCT,ΔCT=靶基因CT值-β-actin CT值。引物序列:LDLr上游5′-GTG TCA CAG CGG CGA ATG-3′,下游 5′-CGC ACT CTT TGA TGG GTT CA-3′;SREBP2 上 游 5′-CCG CCT GTT CCG ATG TAC AC-3′,下游 5′-TGC ACA TTC AGC CAG GTT CA-3′;SCAP上游 5′-GGG AAC TTC TGG CAG AAT GAC T-3′,下游5′-CTG GTG GAT GGT CCC AAT G-3′;β-actin上游5′-CCT GGC ACC CAG CAC AAT-3′,下游5′-GCC GAT CCA CAC ACG GAG TAC T-3′;所有引物由ABI公司Primer Express Software version 2.0System设计。
1.2.3 细胞内胆固醇浓度测定 测定THP-1巨噬细胞和VSMCs内胆固醇浓度采用酶染色法,细胞经实验条件处理24h后,用磷酸盐缓冲液(PBS)洗涤2次,氯仿/甲醇2∶1混合物提取细胞内脂质,后真空干燥,Lowry法测定细胞总蛋白含量,酶法测定总胆固醇浓度(TC),游离胆固醇浓度(FC),经公式胆固醇酯(CE)=TC-FC,计算出胆固醇酯水平,最后结果用细胞蛋白含量校正。
1.3 统计学方法 统计学分析由SPSS17.0统计软件处理,计量数据用±s表示,采用两样本比较t检验,以P<0.05为差异有统计学意义。
2 结 果
2.1 生理条件 下,THP-1 单核细胞、THP-1 巨 噬 细 胞 和VSMCs LDLr mRNA水平的比较 生理条件下,THP-1单核细胞的LDLr mRNA水平最高(1),经佛波酯(PMA)诱导分化为巨噬细胞后,其LDLr mRNA表达水平下降(0.26±0.11),VSMCs LDLr mRNA水平(0.12±0.05)较 THP-1巨噬细胞低,差异均有统计学意义(P<0.05)。

图1 LDL及LPS负荷对巨噬细胞和血管平滑肌细胞LDLr mRNA水平的影响
2.2 LDL和LPS对THP-1巨噬细胞和VSMCs LDLr mRNA水平的影响 实验数据提示,LDL呈浓度依赖性抑制THP-1巨噬细胞和VSMCs LDLr mRNA表达水平(图1A)。用直线回归方程计算两种细胞LDLr mRNA被抑制50%的LDL浓度即IC50,VSMCs的IC50为11.25μg/mL,而 THP-1巨噬细胞IC50为18.125μg/mL,提示在生理条件下,当LDL负荷时VSMCs LDLr mRNA反馈调控较THP-1巨噬细胞敏感迅速。图1B显示,当给予THP-1巨噬细胞和VSMCs不同浓度LPS处理后,LDL对LDLr mRNA反馈抑制效应被逆转,LPS呈浓度依赖性上调LDLr mRNA水平。通过计算发现,200ng/mL LPS使 THP-1巨噬细胞LDLr mRNA上调0.33倍,而相同浓度LPS仅使VSMCs LDLr mRNA上调0.04倍,400ng LPS使VSMCs LDLr mRNA上调0.22倍。这些数据提示,在 LPS刺激 下,THP-1巨 噬细胞 LDLr mRNA 比VSMCs更容易上调。本实验确定,25μg/mL LDL作为后续实验中两种细胞抑制LDLr mRNA有效浓度,200ng/mL LPS作为THP-1巨噬细胞有效炎症刺激浓度,400ng/mL作为VSMCs有效炎症刺激浓度。
2.3 细胞内胆固醇水平测定结果 当细胞培养基中仅有25 μg/mL LDL存在时,两种细胞内胆固醇水平轻度增加,当同时有200、400ng/mL LPS存在时,细胞内胆固醇水平显著增加。应用LDLr阻断剂肝素钠(heparin)后,两种细胞内胆固醇水平显著减少,而清道夫受体阻断剂聚肌苷酸钠[Poly(I)]不能减少巨噬细胞内胆固醇沉积(图2A)。同时通过计算发现,200 ng/mL LPS使巨噬细胞内胆固醇酯水平增加3.21μg/mg,而400ng/mg LPS使VSMCs内胆固醇酯水平增加1.44μg/mg,提示在LPS刺激下,THP-1巨噬细胞通过LDLr途径聚集更多胆固醇酯。
2.4 LPS对THP-1巨噬细胞及 VSMCs SREBP2和SCAP mRNA水平的影响 25μg/mL LDL抑制THP-1巨噬细胞SREBP2和SCAP mRNA水平(0.71±0.61和0.76±0.32),200ng/mL LPS打破25μg/mL LDL对上述两种基因的反馈抑制效应,上调其表达(1.69±0.31和1.21±0.52);25μg/mL LDL抑制VSMCs SREBP2和SCAP mRNA水平(0.25±0.09和0.53±0.13),400ng/mL LPS打破25μg/mL LDL对SREBP2和SCAP mRNA的反馈抑制效应,上调其表达(0.41±0.20和1.01±0.38)。比较分析显示,25μg/mL LDL负荷下,巨噬细胞SREBP2和SCAP mRNA受抑制程度不及VSMCs,而LPS刺激下,巨噬细胞SREBP2和SCAP mRNA表达升高程度大于VSMCs,这一结果同两种细胞LDLr mRNA水平及细胞内胆固醇水平比较结果一致。
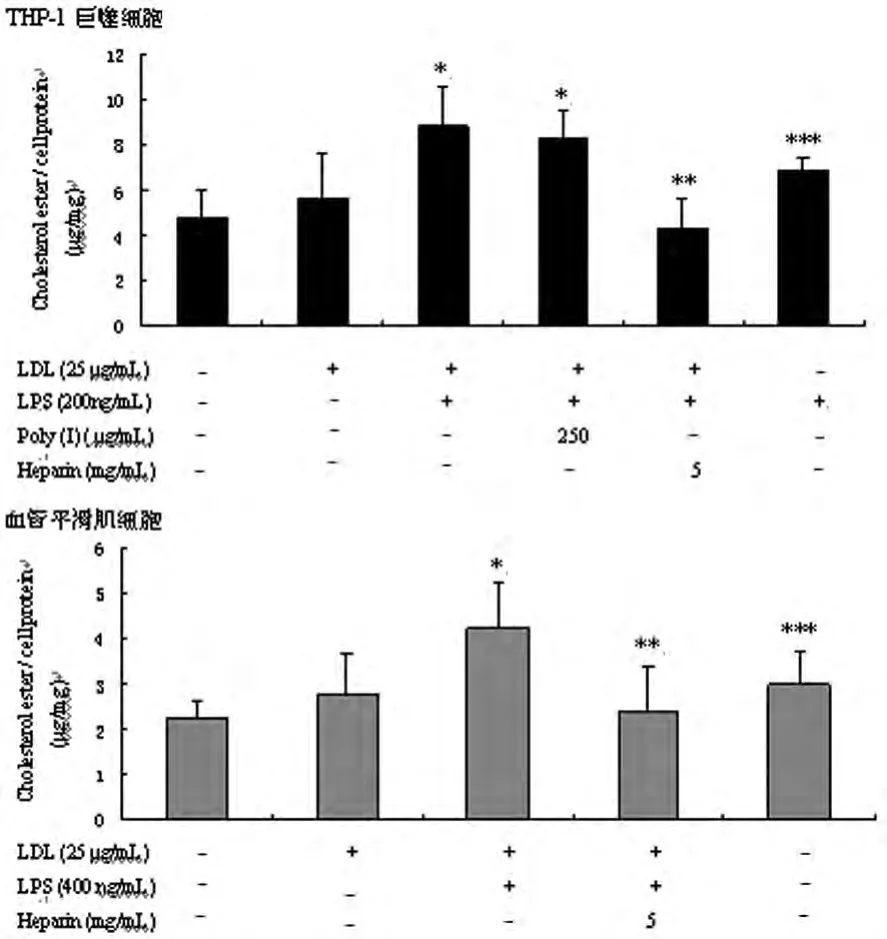
图2 LPS对巨噬细胞和平滑肌细胞内胆固醇水平的影响
3 讨 论
传统观念认为,巨噬细胞是泡沫细胞的主要来源,因为巨噬细胞表达清道夫受体;然而本研究发现平滑肌细胞也可以转化为泡沫细胞。Rosenfeld和Ross[9]应用放射自显影技术和细胞特异性标志物的免疫染色法,发现在WHHL兔的进展期斑块上有30%细胞为巨噬细胞表型,而45%细胞为平滑肌细胞表型。
本研 究观察 THP-1单核细 胞、THP-1巨噬细 胞 和VSMCs LDLr mRNA水平差别,发现单核细胞LDLr mRNA水平最高,其次为巨噬细胞,最低者为VSMCs。研究发现,生理条件下THP-1巨噬细胞和VSMCs的LDLr对LDL负荷有不同的敏感性和反应能力。如图1A示,VSMCs的IC50比THP-1巨噬细胞低,提示VSMCs的LDLr下调比THP-1巨噬细胞的LDLr敏感,即摄入外源性胆固醇能力弱于巨噬细胞,摄入胆固醇仅用于保证细胞基本功能,不易泡沫化,而巨噬细胞的LDLr对下调不敏感,允许更多胆固醇进入细胞;加入炎症刺激物LPS后,在两种细胞均能观察到LPS克服LDL负荷对LDLr mRNA反馈抑制效应,LDLr mRNA表达均增高,提示LPS诱导的炎症应激打破了LDL负荷下的LDLr负反馈调控,允许过多的LDL经LDLr途径进入细胞内,致泡沫细胞形成(图2)。本研究还发现,200ng/mL LPS使 THP-1巨噬细胞LDLr mRNA上调0.33倍,而相同浓度LPS仅上调VSMCs mRNA 0.04倍,提示THP-1巨噬细胞的LDLr对LPS诱导的上调效应比VSMCs敏感。进一步细胞内胆固醇测定证实,200ng/mL LPS刺激下,THP-1巨噬细胞内胆固醇酯增加3.21μg/mg,400ng/mL LPS仅增加VSMCs内胆固醇酯1.44μg/mg,这一结果与两种细胞LDLr对LPS的上调效应的差异一致。为了排除清道夫受体途径参与细胞内胆固醇聚集,分别使用清道夫受体阻断剂聚肌苷酸钠Poly(I)和LDLr抑制剂肝素钠(heparin)。实验发现Poly(I)不能减少LPS诱导的细胞内胆固醇聚集,而肝素钠抑制LPS诱导的胆固醇沉积(图2);同时培养基中含有强力抗氧化剂BHT和EDTA,因而细胞内胆固醇沉积可以除外清道夫受体和氧化LDL参与,这些数据提示LDLr是炎症应激下THP-1巨噬细胞和VSMCs内胆固醇聚集的主要途径之一;并且THP-1巨噬细胞和VSMCs对于LDL和LPS负荷具有明显细胞差异性,即LDLr在细胞膜上表达水平高低不是决定胞内胆固醇水平的因素,LDLr反馈调控的差异性才是决定胞内胆固醇水平的关键。
继续研究LPS逆转高浓度LDL对LDLr反馈抑制的分子机制,发现调控LDLr表达的两个重要分子SREBP2和SCAP的mRNA水平同样可以被高浓度LDL抑制;但是相同浓度LDL负荷时,VSMCs的SCAP和SREP2mRNA被抑制程度更大,而LPS同样可以逆转高浓度LDL对SCAP和SREBP2的mRNA抑制,上调两种基因表达,但THP-1巨噬细胞的上调幅度更大(图2)。这些数据提示,LPS诱导的炎症应激彻底打破了细胞内胆固醇负反馈调控,上调SCAP和SREBP2表达,可能导致SCAP过多从内质网转位至高尔基体,进而上调LDLr表达,促进天然LDL进入胞内,致泡沫细胞形成。
综上所述,生理条件下,THP-1巨噬细胞和血管平滑肌细胞对胆固醇负荷有不同能力和敏感性,巨噬细胞由于其LDLr对LDL负荷不敏感,因而对LDL摄取能力较强,而VSMCs对LDL负荷敏感,LDLr表达迅速下调。LPS诱导的炎症应激显著增加巨噬细胞LDLr表达,致泡沫细胞形成。VSMCs LDLr对LPS诱导的上调效应不敏感,这可能是炎症应激下巨噬细胞更容易泡沫化的原因。
[1] Nohturfft A,Yabe D,Goldstein JL,et al.Regulated step in cholesterol fee dback localized to budding of SCAP from ER membranes[J].Cell,2000,102(3):315-323.
[2] C hen Y,Ruan XZ,Li Q,et al.Inflammatory cytokines disrupt LDL-receptor feedback regulation and cause statin resistance:a comparative study in human hepatic cells and mesangial cells[J].Am J Physiol Renal Physiol,2007,293(3):F680-F687.
[3] Ma KL,Ruan XZ,Powis SH,et al.Inflammatory stress exacerbates lipid accumulation in hepatic cells and fatty livers of apolipoprotein E knockout mice[J].Hepatology,2008,48(3):770-781.
[4] R uan XZ,Moorhead JF,Varghese Z.Lipid redistribution in renal dysfunction[J].Kidney Int,2008,74(4):407-409.
[5] C hen YX,Ruan XZ,Huang AL,et al.Mechanisms of dysregulation of low-density lipoprotein receptor expression in HepG2cells induced by inflammatory cytokines[J].Chin Med J(Engl),2007,120(24):2185-2190.
[6] Zhao L,Chen Y,Tang R,et al.Inflammatory stress exacerbates hepatic cholesterol accumulation via increasing cholesterol uptake and de novo synthesis[J].J Gastroenterol Hepatol,2011,26(5):875-883.
[7] Xu ZE,Chen Y,Huang A,et al.Inflammatory stress exacerbates lipid-mediated renal injury in ApoE/CD36/SRA triple knockout mice[J].Am J Physiol Renal Physiol,2011,301(4):713-722.
[8] Qiang Ye,Han Lei,Zhongcai Fan,et al.Difference in LDL receptor feedback regulation in macrophages and vascular smooth muscle cells:foam cell transformation under inflammatory stress[J].Inflammation,2014,37(2):555-565
[9] Rosenfeld ME,Ross R.Macrophage and smooth muscle cell proliferation in atherosclerotic lesions of WHHL and comparably hypercholesterolemic fat-fed rabbits[J].Arteriosclerosis,1990,10(5):680-687.
