铋电极差分脉冲伏安法测定水中痕量2,4-二硝基苯肼
2014-10-12石登武李建平
马 飞,石登武,李建平
(桂林理工大学 化学与生物工程学院,广西 桂林 541004)
2,4-二硝基苯肼主要用于炸药制造,也可作为鉴别醛、酮的化学试剂。2,4-二硝基苯肼对环境的危害主要表现为燃烧时释放出有毒的刺激性烟雾,通过吸入、食入、皮肤吸收等途径进入人体,不仅刺激眼和皮肤,还可能引起高铁血红蛋白血症,使人出现紫绀[1]。含有2,4-二硝基苯肼的工业废水剧毒,如果未经处理排放到环境中,即使微量也会对环境造成重大污染。因此,建立一种简单易行的2,4-二硝基苯肼测定方法非常必要。目前,2,4-二硝基苯肼的测定主要是利用显色法或色谱法[2-3],前者灵敏度不高,后者复杂烦琐,且需大型仪器。铋电极因具有电位窗宽、使用方便、环保低毒、成本低廉等优点,在分析测试中引起了研究人员的极大兴趣,并已利用铋及铋膜电极测定了铅、镉、锌、锡、锰等金属离子[4-6]及一些有机物[7-8]。但采用铋电极测定2,4-二硝基苯肼的研究尚未见报道。
本工作建立了铋电极差分脉冲伏安法测定水中痕量2,4-二硝基苯肼的分析方法,研究了2,4-二硝基苯肼在自制铋电极上的电化学行为,同时对实验条件进行了考察。为了验证电极的性能,将其应用于工业废水中痕量2,4-二硝基苯肼的测定。
1 实验部分
1.1 试剂、材料和仪器
铋:上海正宜化学药品厂,片状,纯度99%。2,4-二硝基苯肼、KCl、NaOH、Hg(NO3)2:分析纯。实验用水:二次蒸馏水。
2,4-二硝基苯肼储备液:1.0×10-4mol/L;NaOH+KCl储备液:0.1 mol/L NaOH+0.1 mol/L KCl混合溶液(pH=13.0);测定底液:取一定量的上述2,4-二硝基苯肼储备液置于10 mL比色管中,然后用不同的测定底液配制溶液稀释到10 mL,制得所需2,4-二硝基苯肼浓度的测定底液;空白底液:不加2,4-二硝基苯肼的测定底液。溶液均为现配使用。
2,4-二硝基苯肼工业废水:取自广西省桂林市某工业区,测定前过滤去除悬浮物和杂质。
CHI660C型电化学工作站:上海辰华仪器公司;GS28-B型电子恒速搅拌器:上海安亭电子仪器厂;PHS-2C型精密酸度计:上海雷磁精密仪器有限公司。
1.2 工作电极的制备
截取一段内径3 mm、长5 cm的移液管,抛光外表面。取一小块铋片置于坩埚中,用酒精喷灯灼烧至熔融状后,吸入移液管内3~5 mm,并将长6 cm直径为1 mm的铜棒从另一端迅速插入移液管内,铜棒与移液管之间的缝隙用蜡封固定。将铋表面抛光后即制得实验用铋电极。
汞膜电极的制备参考文献[9]。将玻碳电极置于5×10-5mol/L镀汞液(用1%(w)的硝酸和Hg(NO3)2配成)中,采用计时电流法在-1.0 V下电解60 s,这时电极表面镀上灰白色的汞膜,取出后用水冲洗电极,即制得实验用汞膜电极。
1.3 2,4-二硝基苯肼的电化学测定
自制铋电极为工作电极,铂丝电极为对电极,Ag/AgCl为参比电极(内充饱和KCl)。将三电极置于盛有10 mL测定底液的烧杯中,采用差分脉冲伏安法(DPV)测定不同2,4-二硝基苯肼浓度下的氧化峰电流。电极使用后,用铝粉抛光,并在无水乙醇中超声清洗2 min,用水冲洗后静置备用。
2 结果与讨论
2.1 2,4-二硝基苯肼的铋电极DPV表征结果
以NaOH+KCl储备液配制测定底液,在2,4-二硝基苯肼浓度为1.0×10-6mol/L、扫描速率为100 mV/s的条件下,空白底液(a)和测定底液(b)的铋电极DPV曲线见图1。由图1可见:曲线a在-0.45 V附近出现一个氧化峰p1,推测是铋的氧化峰[5];曲线b在-0.45 V附近的氧化峰p2与p1基本重合,在-0.53 V附近出现灵敏的新峰p3,推测是2,4-二硝基苯肼的氧化峰。本实验选择-0.53 V处的氧化峰电流进行2,4-二硝基苯肼的定量测定。
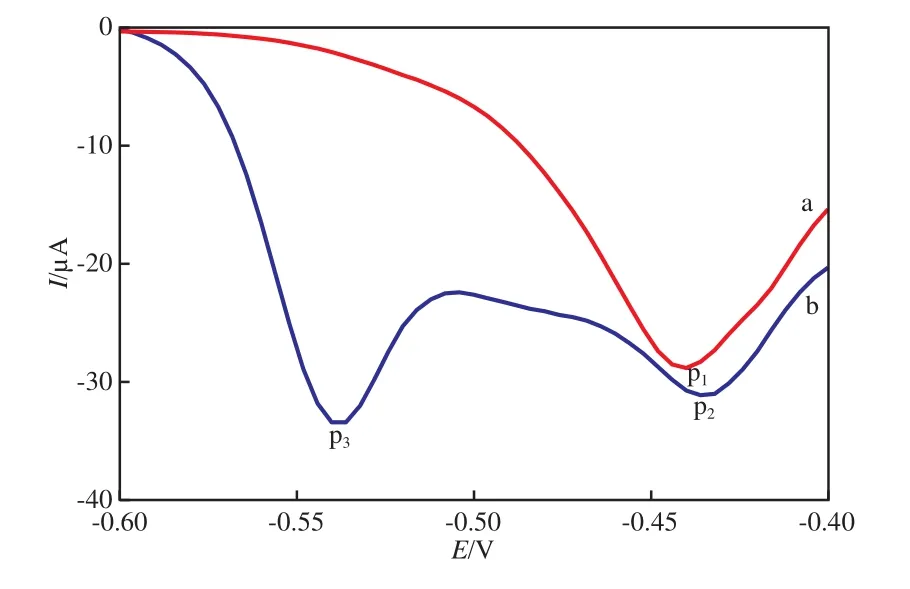
图1 空白底液(a)和测定底液(b)的铋电极DPV曲线
以NaOH+KCl储备液配制测定底液,在2,4-二硝基苯肼浓度为1.0×10-6mol/L、扫描速率为100 mV/s的条件下,测定底液在汞膜电极(a)和铋电极(b)上的DPV曲线见图2。由图2可见:与铋电极的DPV曲线相比,汞膜电极的DPV曲线未出现氧化峰;而铋电极在-0.53 V处出现氧化峰p,峰电流大小为-33 μA左右。在2,4-二硝基苯肼的测定中,相较于汞膜电极,自制的铋电极有明显的优势。
2.2 测定条件的优化
2.2.1 测定底液配制溶液种类的影响
在2,4-二硝基苯肼浓度为1.0×10-6mol/L、扫描速率为100 mV/s的条件下,考察了分别以Britton-Robinson缓冲溶液(pH=5.0)、醋酸-醋酸钠缓冲溶液(pH=5.2)、磷酸缓冲溶液(pH=6.8)、0.1 mol/L HCl+0.1 mol/L KCl混合溶液(pH=1.0)、NaOH+KCl储备液配制测定底液时对测定结果的影响。实验结果表明,在以NaOH+KCl储备液配制的测定底液中,测定结果最为稳定,峰型及峰强度均令人满意。因此,选择以NaOH+KCl储备液配制测定底液。
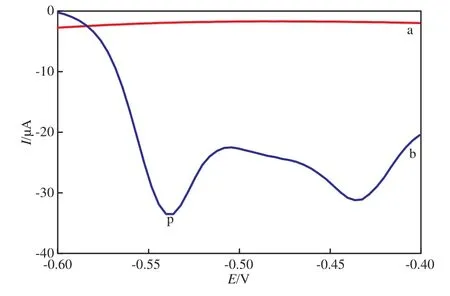
图2 测定底液在汞膜电极(a)和铋电极(b)上的DPV曲线
2.2.2 测定底液pH的影响
在2,4-二硝基苯肼浓度为1.0×10-6mol/L、扫描速率为100 mV/s的条件下,以NaOH+KCl储备液配制测定底液,以盐酸或NaOH调节pH,考察了不同的测定底液pH(12.0~13.5)对测定结果的影响。实验结果表明:pH=13.0时,峰电流强度最高,峰型也好;且氧化峰电位随溶液的pH增大而负移,说明该电极过程与溶液pH有关。因此,选择测定底液pH为13.0。实验中2,4-二硝基苯肼的加入对pH的影响可忽略不计,以NaOH+KCl储备液配制测定底液时,测定底液的pH可视为13.0,故无需进行调节。
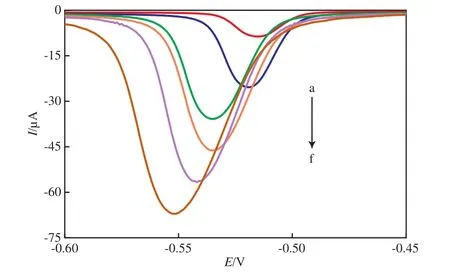
图3 不同扫描速率下测定底液的铋电极DPV曲线
2.2.3 扫描速率的影响
以NaOH+KCl储备液配制测定底液,在2,4-二硝基苯肼浓度为1.0×10-6mol/L的条件下,不同扫描速率下测定底液的铋电极DPV曲线见图3。
由图3可见,随扫描速率的增大,峰电流强度增大,且氧化峰逐渐负移。氧化峰电流(Ip)在扫描速率(v)10~250 mV/s范围内与扫描速率的平方根呈良好的线性关系,线性方程为:Ip= 7.9v1/2+9.0(相关系数为0.997),Ip~v1/2拟合曲线见图4。根据Randles-Sevcik方程可知,2,4-二硝基苯肼在铋电极/溶液界面上的电极反应为扩散控制。综合考虑扫描时间、所得信号的强度、扫描结果的稳定性,选取100 mV/s作为最佳扫描速率。
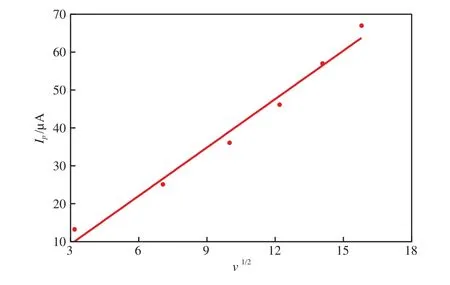
图4 Ip~v1/2拟合曲线
2.3 工作曲线
以NaOH+KCl储备液配制测定底液,在扫描速率为100 mV/s的条件下,以2,4-二硝基苯肼溶液浓度的对数值(lgc)为横坐标,以空白和试样的氧化峰电流强度差值(ΔIp,μA)为纵坐标,绘制工作曲线(见图5)。由图5可见,ΔI与lgc呈线性关系。在lgc=-7.522 9~-5.000 0,即c= 3.0×10-8~1.0×10-5mol/L范围内,工作曲线方程为ΔIp= 30.64+12.40lgc(相关系数为0.993),计算得到的检出限为8.37×10-9mol/L。
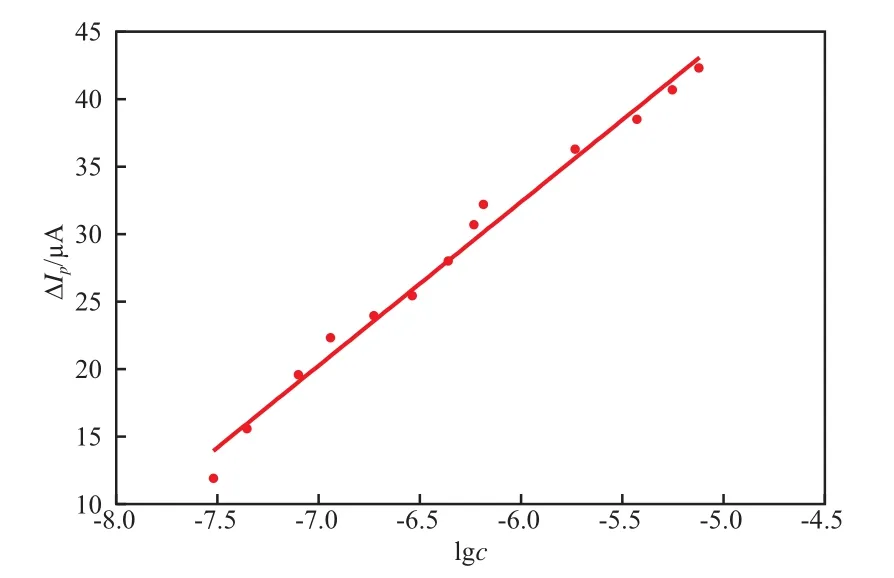
图5 工作曲线
2.4 方法的重复性
通过对1.0×10-6mol/L的2,4-二硝基苯肼溶液进行30次的检测,发现铋电极的电化学信号没有明显变化,峰电流强度的变化维持在±5%以内,使得测定结果的变化幅度也在±5%以内。
2.5 干扰实验
对浓度为1.0×10-6mol/L的2,4-二硝基苯肼溶液进行干扰实验。实验结果表明,100倍浓度的常见爆炸物(如2-氨基酚、对硝基苯酚、邻苯二胺、邻苯二酚),500倍浓度的葡萄糖、蔗糖、柠檬酸、甲醇、乙醇,以及1 000倍浓度的常见离子(如Ca2+,Mg2+,Zn2+,Fe3+,Cr3+,Cu2+,NH4+,SO42-)对2,4-二硝基苯肼测定结果的影响小于±5%。
2.6 实际废水水样的测定
对实际废水水样进行加标回收测定(n=5),实际废水水样的测定结果见表1。由表1可见,回收率在95.6%~103.1%之间,相对标准偏差小于3%,说明该铋电极能应用于工厂废水中2,4-二硝基苯肼的测定,测定结果准确可靠。

表1 实际废水水样的测定结果
2.7 电极反应机理
在2,4-二硝基苯肼浓度为1.0×10-6mol/L、扫描速率为100 mV/s的条件下,以NaOH+KCl储备液配制测定底液,以盐酸或NaOH调节pH,测定底液pH在12.0~13.5范围内,氧化峰电位(Ep,V)与pH呈良好的线性关系,回归方程为Ep= -0.036 9pH-0.142(相关系数为0.998),即氧化峰电位随溶液pH的增大以36.9 mV/pH的速率向负电位移动,说明电极反应与pH有关,且pH增大有利于反应的进行,电流值更大。此现象说明OH-参加了反应,而不是H+参加了反应。对于不可逆的电极反应过程,参照文献[10]报道的方法,在室温(298 K)条件下由能斯特方程可推算出参加反应的电子数为2。由以上结果可推测反应的机理为:
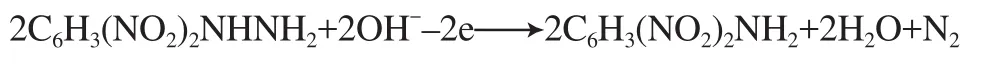
3 结论
a)以NaOH+KCl储备液配制测定底液,在2,4-二硝基苯肼浓度为1.0×10-6mol/L、扫描速率为100 mV/s的条件下,2,4-二硝基苯肼于-0.53 V处产生灵敏的氧化峰;在2,4-二硝基苯肼浓度为3.0×10-8~1.0×10-5mol/L范围内,空白和试样的氧化峰电流强度差值与对应2,4-二硝基苯肼浓度的对数呈良好的线性关系。
b)铋电极差分脉冲伏安法测定2,4-二硝基苯肼的结果准确可靠,检出限低(8.37×10-9mol/L),且电极制作方法简单、成本低廉、绿色环保。将该方法应用于工业废水中痕量2,4-二硝基苯肼的检测,结果令人满意。
[1] 孙维生. 常见危险化学品的危害及防治[M]. 北京:化学工业出版社,2005:16-18.
[2] 姜荻,侯晓虹,康利荥. 2,4-二硝基苯肼吸收液法测定空气中醛、酮类化合物[J]. 环境保护科学,2010,36(5):56-58.
[3] 李凌凌,吕早生,黄乐繁,等. 2,4-二硝基苯肼显色法测定环己酮含量[J]. 化学与生物工程,2010,27(5):89-91.
[4] 李建平,彭图治,张雪君. 铋膜电极电位溶出法测定痕量铅,镉,锌[J]. 分析化学,2002,30(9):1092-1095.
[5] 高云涛,刘琼,李乔丽,等. 铋膜电极微分电位溶出法测定矿区土壤中锡[J]. 冶金分析,2010,31(11):20-24.
[6] 陈林,刘成伦,周庆华,等. 镀铋膜修饰玻碳电极差分脉冲伏安法测试土壤中锰[J]. 冶金分析,2010,31(3):27-29.
[7] 李志英,肖阳,周长利,等. 茜素S复合铋膜电极电催化还原氯霉素[J]. 分析试验室,2011,30(3):35-39.
[8] 杨阿喜,金根娣,葛纪龙. 汞膜修饰玻碳电极测定文法拉新的研究[J]. 药物分析杂志,2009,29(7):1134-1137.
[9] 朱爱花,朱亚玲,崔胜云. 玻碳汞膜电极上还原型谷胱甘肽的电化学行为及分析应用[J]. 延边大学学报,2010,36(2):149-154.
[10] 保尔 M S 蒙克. 电分析化学基础[M]. 朱俊杰,罗鲲,潘宏程,译. 北京:化学工业出版社,2012:52-53.
