雌、孕激素下降对大鼠肾脏组织中水通道蛋白表达的影响
2014-10-08王贵宪徐纪中袁维堂
卫 红,王贵宪,徐纪中,袁维堂,卫 军
1)河南司法警官职业学院实验中心 郑州 450000 2)郑州大学第一附属医院肛肠外科 郑州 450052 3)武警河南总队医院感染管理科 郑州 450052
卵巢甾类激素通过调节肾脏对水分的重吸收等一系列复杂机制参与机体水代谢的调节[1]。血液循环中雌激素或孕酮水平的增高[2]或降低[3]都会导致明显的水钠潴留、血容量增加[4]。研究[5]表明,分布于肾脏的水通道蛋白(aquaporin,AQP)与水的重吸收关系密切。雌激素和孕酮可通过影响血浆垂体后叶激素如血管加压素(AVP)和催产素的分泌从而调节肾脏 AQP表达,进而调控水代谢平衡[6]。该研究观察了卵巢切除(ovariectomy,OVX)后大鼠肾脏组织AQP表达的改变以及伴随的肾脏水代谢异常,报道如下。
1 材料与方法
1.1 实验动物及分组 选择3个月的雌性慕尼黑大鼠60只,初始体重200 g左右,喂养环境为12 h:12 h人工白天、黑夜循环,室内温度维持在(21±2)℃,湿度维持在55% ±2%。采用随机数字表法将大鼠分为2组,即OVX组(n=30)和对照组(Sham组,n=30)。OVX组:采用氟烷吸入麻醉,将大鼠放置在自动调节的加温平台上,使其在手术期间直肠内温度维持在35.5~37.0℃。采用腹部正中切口,显露卵巢和输卵管,结扎输卵管后,切除双侧卵巢。Sham组:在氟烷吸入麻醉下行剖腹探查,显露卵巢和输卵管,但不结扎切除。
1.2 标本采集 实验动物单独放置在代谢笼内,每日留取尿样待检。术后0、2、4周2组分别取10只大鼠,在氟烷吸入麻醉下,先通过主动脉抽血,留取血样待检;然后快速切除双侧肾脏,左侧肾脏置入40 g/L的多聚甲醛中用于免疫组化检测;右侧肾脏放置在冰面上,分离出内髓和皮质,切碎后分别加入含蛋白酶抑制剂的解剖缓冲液后匀浆,匀浆液在4℃、4000 g条件下离心15 min,保留上清液待检。
1.3 检测指标 分别于术后0、2、4周进行检测。
1.3.1 体重、饮水量、尿量、尿和血浆渗透压 2组均在处死动物留取标本前1 d使用代谢笼记录动物尿量和饮水量,使用电子称重仪测定动物体重,使用渗透压测定仪测定尿和血浆渗透压。
1.3.2 血浆雌、孕激素和AVP水平 使用自动电化学发光免疫分析仪测量血浆中雌、孕激素和AVP水平。
1.3.3 肾脏组织AQP 用Shimadz分光光度计对各个标本的总蛋白浓度进行测定,计算出在相同的蛋白量时所需要点样的样本量,细微的误差通过在120 g/L的聚丙烯酰胺胶板上进行考马斯亮兰校正,再进行免疫印迹法测定。抗体为AQP2(稀释度为1∶1000)、p-AQP2(稀释度为 1∶1000)、AQP1(稀释度为1∶500)和AQP3(稀释度为1∶100),所有抗体均来源于丹麦奥胡斯大学水盐研究中心,阻断抗体是P448(为羊抗兔抗体,稀释度1∶3000)。免疫组化SP法检测及定量采用文献[7]的方法。
1.4 统计学处理 应用SPSS 10.0进行数据分析,采用重复测量数据的方差分析对各指标进行比较,检验水准 α=0.05。
2 结果
2.1 2组大鼠体重、饮水量、尿量、尿和血浆渗透压结果见表1。
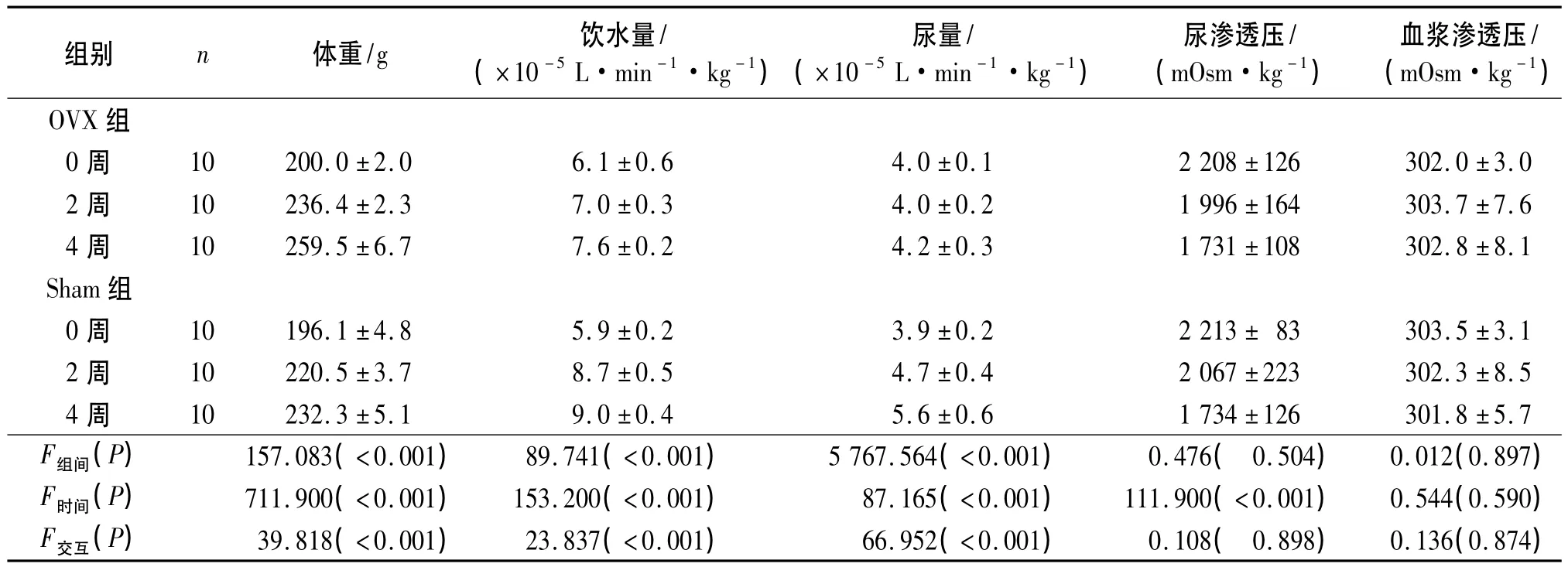
表1 2组大鼠体重、饮水量、尿量、尿和血浆渗透压的比较
2.2 2组大鼠血浆雌、孕激素和AVP水平 结果见表2。
2.3 2组大鼠肾脏组织AQP的表达 结果见图1、2和表2。

表2 2组大鼠血浆雌、孕激素和AVP水平及肾脏组织AQP表达水平的比较

图1 2组术后2周肾脏组织中AQP2、p-AQP2、AQP1及AQP3的表达情况(SP,×400)

图2 2组术后2周肾脏组织中AQP2(A)、p-AQP2(B)、AQP1(C)及AQP3(D)表达的免疫印迹结果
3 讨论
该研究发现大鼠OVX后血浆雌激素和孕激素水平下降,血浆AVP水平升高,肾脏AQP2、AQP1、AQP3的表达增强,且伴随着明显的尿量减少和体重增加,提示OVX后的尿量减少和水潴留与肾脏AQP2、AQP1、AQP3的表达上升有关。由此推测绝经期妇女女性激素水平的下降和血浆AVP水平的升高在肾脏对水的异常处理中发挥了重要作用。
3.1 OVX后尿量减少的同时AQP2的表达增加AQP2分布在肾小管主细胞表膜以及胞质内[8],AVP使主细胞胞质内的AQP2转移至胞膜上,从而增加对水分的重吸收,为快速调节机制[9]。而慢调节机制是通过 AQP2 mRNA转录,增加蛋白表达总量[10]。该实验证实了OVX后2和4周AQP2的表达明显增加,与之相对应的是血浆AVP水平升高,推测OVX后AVP的升高导致了AQP2的表达增强,使肾小管对水分的吸收增加,致使尿量减少。但是OVX后2和4周的具体调节机制(快速调节机制/慢调节机制)并不清楚,需要进一步研究。p-AQP2是 PKA引发的磷酸化 AQP2,当胞质内的AQP2转移至胞膜时,是p-AQP2的形式[5]。该实验发现OVX后2和4周,p-AQP2的表达均升高,推测血浆AVP的升高致使AQP2磷酸化增加,从而增加了水分重吸收,致使尿量减少。另外,该研究发现p-AQP2和AQP2表达量均明显上升,说明2种调节机制均参与了OVX后肾小管对水的重吸收。
3.2 OVX后肾脏组织AQP3和AQP1的表达增加 AQP1位于肾脏近端小管和亨利袢的降枝细段细胞的顶膜和基底膜上,主要作用是使水分穿透细胞膜的顶膜和基底膜,重吸收水分[11]。研究[12]发现缺乏AQP1时,在应用AVP或缺水状态时,会表现出尿液浓缩障碍。该研究中OVX后AQP1表达的持续增高,可能与雌激素水平下降后机体的水潴留有关,其调节机制需进一步探讨。
AQP2吸收到主细胞内的水分通过分布在主细胞侧基底膜上的 AQP3和 AQP4进入体循环[5]。AVP调节下集合管对尿液的浓缩也主要是通过AQP2、AQP3 和 AQP4 完成[10]。剔除了 AQP3 和AQP4的小鼠出现明显的多尿以及尿液浓缩功能受损[13]。该研究结果显示OVX后伴随着AQP2表达的升高,AQP3的表达也同样升高。有研究[13]表明除了AQP2调节以外,AQP3也参与了AVP和体内水平衡变化的调节。研究[14]显示AQP3主要存在于细胞的侧基底膜上,几乎没有发现胞质内颗粒,这提示AQP3没有像AQP2那样的快速调节机制。
综上所述,OVX后雌、孕激素水平下降而血浆AVP水平上升,致使肾脏组织 AQP2、AQP1、AQP3表达升高,与之相应的是尿量减少和体重增加。推测OVX后雌、孕激素的减少产生的体内液体潴留可能与肾脏对水分的重吸收增加有关,其作用至少部分是通过AVP对AQP的调节途径进行。
[1]Skowsky WR,Swan L,Smith P.Effects of sex steroid hormones on arginine vasopressin in intact and castrated male and female rats[J].Endocrinology,1979,104(1):105
[2]Schrier RW,Cadnapaphornchai MA,Ohara M.Water retention and aquaporins in heart failure,liver disease and pregnancy[J].J R Soc Med,2001,94(6):265
[3]柳献巧.绝经期妇女的激素与心理治疗[J].山西医药杂志,2013,42(23):1386
[4]徐培渝,李芳,李群英.绝经期对妇女体重的影响[J].预防医学情报杂志,2002,18(1):48
[5]Schey KL,Grey AC,Nicklay JJ.Mass spectrometry of membrane proteins:a focus on aquaporins[J].Biochemistry,2013,52(22):3807
[6]Nielsen S,Kwon TH,Frokiaer J,et al.Regulation and dysregulation of aquaporins in water balance disorders[J].J Intern Med,2007,261(1):53
[7]文建国,任川川,吕宇涛,等.促红细胞生成素对单侧输尿管部分梗阻幼鼠肾脏水通道蛋白2表达的影响[J].中华实用儿科临床杂志,2013,28(5):337
[8]Nielsen S,Chou CL,Marples D,et al.Vasopressin increases water permeability of kidney collecting duct by inducing translocation of aquaporin-CD water channels to plasma membrane[J].Proc Natl Acad Sci USA,1995,92(4):1013
[9]Fenton RA,Pedersen CN,Moeller HB.New insights into regulated aquaporin-2 function[J].Curr Opin Nephrol Hypertens,2013,22(5):551
[10]Ohara M,Martin PY,Xu DL,et al.Upregulation of aquaporin 2 water channel expression in pregnant rats[J].J Clin Invest,1998,101(5):1076
[11]Li ZZ,Zhao ZZ,Wen JG,et al.Early alteration of urinary exosomal aquaporin 1 and transforming growth factor β1 after release of unilateral pelviureteral junction obstruction[J].J Pediatr Surg,2012,47(8):1581
[12]Verkman AS.Physiological importance of aquaporins:lessons from knockout mice[J].Curr Opin Nephrol Hypertens,2000,9(5):517
[13]Li ZZ,Xing L,Zhao ZZ,et al.Decrease of renal aquaporins 1-4 is associated with renal function impairment in pediatric congenital hydronephrosis[J].World J Pediatr,2012,8(4):335
[14]Ecelbarger CA,Nielsen S,Olson BR,et al.Role of renal aquaporins in escape from vasopressin-induced antidiuresis in rat[J].J Clin Invest,1997,99(8):1852
