均质纤维素膜的制备及其正渗透性能研究
2014-09-25张兵涛侯立安
张兵涛,张 林,黄 和,侯立安,3
(1.南京工业大学生物与制药工程学院材料化学工程国家重点实验室,南京 210009;2.浙江大学生物质化工教育部重点实验室,化学工程与生物工程学系,杭州 310027;3.第二炮兵后勤科学技术研究所,北京 100011)
均质纤维素膜的制备及其正渗透性能研究
张兵涛1,张 林2,黄 和1,侯立安2,3
(1.南京工业大学生物与制药工程学院材料化学工程国家重点实验室,南京 210009;2.浙江大学生物质化工教育部重点实验室,化学工程与生物工程学系,杭州 310027;3.第二炮兵后勤科学技术研究所,北京 100011)
以纤维素(cellulose)为膜材料,离子液体1-乙基-3甲基咪唑醋酸盐(EMIMAc)为溶剂,水为非溶剂,无纺布作为支撑层,通过相转化法制备了纤维素均质膜。采用红外、X-射线衍射和扫描电子显微镜表征了膜的结构及形貌,考察了该膜的正渗透性能。结果表明:纤维素溶解再生过程中没有发生化学变化,但晶型发生了转变;当原料液为0.6 mol/L的氯化钠水溶液,汲取液为特制的营养液时,所制备的正渗透膜的水通量为3.534 L/(m2·h),截盐率达到99%以上。
正渗透;离子液体;纤维素膜;相转化;膜制备
1 前言
正渗透(forward osmosis,FO)又称渗透,是一种自然界广泛存在的物理现象,即水自发的由水化学位高的区域(低渗透压侧)向水化学位低的区域(高渗透压侧)转移的过程[1]。该过程的推动力是两种溶液中溶剂的化学位差或溶液的渗透压差。与目前在脱盐方面应用最为广泛的反渗透相比,作为新兴技术的FO技术以其低能耗、低污染以及过程易于实现等优点[2]在盐差发电[3~5]和脱盐[6~8]等领域均表现出较好的发展前景,另外,在盐差医学领域如药物控制释放及食品浓缩领域[9~11]也显示出了良好的优越性。
高性能的正渗透膜通常具有以下几个特征:a.致密、低孔隙率的皮层,高截留率;b.膜的皮层具有较好的亲水性、较高的水通量;c.膜支撑层尽量薄,孔隙率;d.较高的机械强度;e.耐酸碱的抗化学腐蚀能力,可以在较宽的pH范围及不同组成的溶液中正常运行。目前最好的商业化正渗透膜是美国HTI公司的支撑型高强度膜[12],该膜主要成分为醋酸纤维素类高分子,由3层结构组成:致密皮层,多孔支撑层和网格支撑结构。其中,膜皮层和多孔支撑层亲水,呈电中性,厚度约50 μm。
与HTI正渗透膜所用醋酸纤维素性质类似,纤维素也具有良好的亲水性、高结晶度和化学稳定性,但其在常规溶剂中难以被溶解的特点限制了作为常规的膜材料。有为数不多的研究报道了利用离子液体作为溶剂,将纤维素制备成超滤膜和纳滤膜。陈洪章等[13]用离子液体1-butyl-3-methylimidazolium chloride作为溶剂制备了纤维素超滤膜;林金友等[14]制备了纤维素超滤膜用作废水处理;李小林等[15]制备了纤维素纳滤膜,这些膜均表现出一定的稳定性和良好的分离性。纤维素膜所具有高亲水性和致密膜结构能够很好的满足正渗透膜的要求,但迄今为止,尚未见以纤维素为材料的正渗透膜研究报道。
本文以纤维素为膜材料,以离子液体1-乙基-3甲基咪唑醋酸盐作为溶剂,以无纺布作为支撑层,通过相转化法制备了纤维素正渗透膜,并研究了其正渗透性能,期望通过本研究能够拓宽正渗透膜材料的选择范围,实现纤维素在更多领域中的资源化应用。
2 实验材料及方法
2.1 实验材料
纤维素粉(粒径:25 μm)购自阿拉丁试剂(上海)有限公司,1-乙基-3-甲基咪唑醋酸盐(EMIMAc)离子液体购于中国科学院兰州化学物理研究所,营养液和商业膜由广东顺德亿港科技有限公司提供,NaCl购于国药集团化学试剂有限公司。
2.2 铸膜液的制备
取适量纤维素粉在80℃下真空干燥12 h后溶于离子液体EMIMAc中,配制成8 wt%的铸膜液。在70℃的恒温浴中搅拌至纤维素完全溶解,静置脱泡,待刮膜用。
2.3 纤维素正渗透膜的制备
将适量铸膜液倾倒在贴有无纺布的玻璃平板上,然后用刮膜刀以一定的速度匀速刮膜。在空气中静置1 min后,浸入去离子水的冰水浴中进行分相。成膜后,用大量去离子水冲洗、浸泡,除去残留的离子液体。然后将膜放在去离子水中保存,以备后续的测试和表征所用。
2.4 纤维素正渗透膜的表征
采用傅里叶红外光谱仪(FTIR,Nicolet5700 spectrometer,ThermoFisher Co,美国)表征膜的化学结构,采用X-射线衍射仪(XRD,X’Pert PRO diffractometer)研究纤维素晶型的变化,扫描电子显微镜(SEM,Ultral 55,CorlzeisD,德国)用来表征膜表面和断面的形貌与结构。
2.5 纤维素正渗透膜性能测试
FO膜性能测试装置如图1所示。有效膜面积为56.72 cm2。原料液为0.6 mol/L的氯化钠水溶液时,汲取液为糖营养液;原料液为纯水时,汲取液为2 mol/L的氯化钠水溶液。膜的活性层(即分离层)都朝向汲取液,调节原料液和汲取液的体积流量均为0.24 L/min。
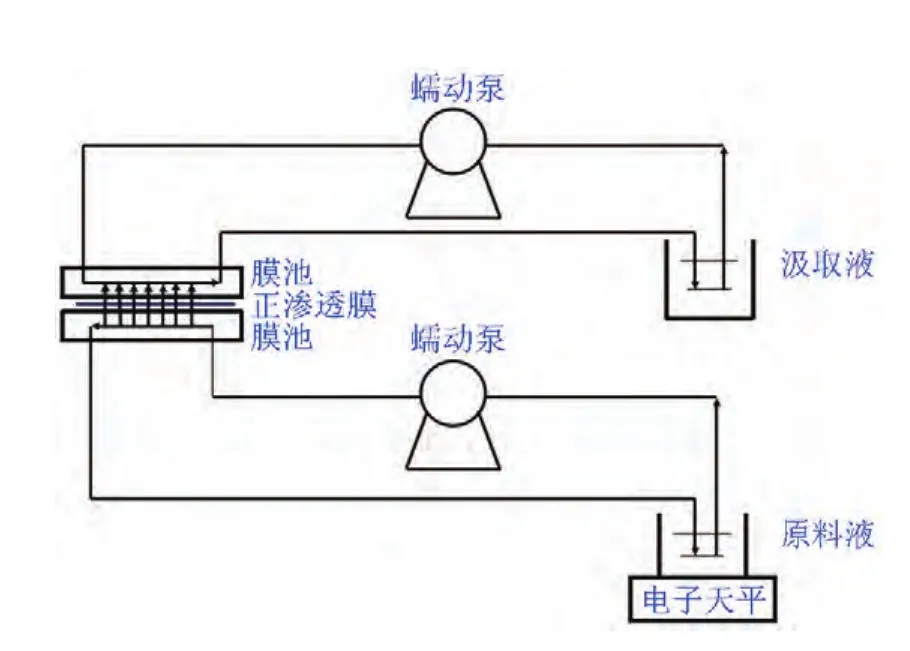
图1 正渗透膜性能测试装置示意图Fig.1 Schematic diagram of the forward osmosis system
水通量是表征FO膜性能最为重要的指标之一,即单位时间内透过单位膜面积的纯水量。水通量(L/(m2·h))可以通过测量FO运行过程中原料液质量的变化用式(1)计算得到:

式(1)中,ΔW为原料液质量的减少,kg;ρ为水的密度,kg/m3;S为膜的有效面积,m2;t为运行时间,h。
截盐率通过式(2)来计算:

式(2)中,Cp为透过液中盐的浓度,g/L;Cf为初始料液中盐的浓度,g/L。Cp可以通过电导率仪来测量进而得到。
3 结果与讨论
3.1 纤维素膜的物化性质
由于离子液体对纤维素的溶解作用是因为阴阳离子在溶解过程中处于游离状态,并与纤维素的羟基相互作用,生成了络合物,从而消弱了纤维素分子内和分子间的氢键,因此,在纤维素溶解和再生过程中可能会对其物化性质有所影响,因此,利用红外光谱和XRD对纤维素原粉和所制备的再生纤维素膜的物化性质进行表征和比较。纤维素原粉和采用离子液体为溶剂成膜后的再生纤维素红外图谱如图2所示,从图中可以看出,两者的主要特征峰十分相似,说明在纤维素再生成膜过程中化学结构没有发生变化,即离子液体EMIMAc是纤维素的直接溶剂。

图2 纤维素原粉和再生纤维素的红外图谱Fig.2 FT-IR spectra of original cellulose and regenerated cellulose
图3为纤维素原粉和成膜后再生纤维素的XRD图谱。纤维素晶型I的典型XRD衍射峰为2θ =14.9°、16.3°、22.5°和34.3°,纤维素晶型II的典型的XRD衍射峰为2θ=20.0°和 21.7°。如图3所示,纤维素原粉的晶型属于纤维素晶型I,再生纤维素的晶型属于纤维素晶型II。说明纤维素经离子液体EMIMAc溶解和再生后,纤维素的晶型由晶型I变为晶型II。与原始纤维素相比,再生纤维素XRD衍射峰的强度下降,结晶度也有所降低。说明离子液体EMIMAc在溶解纤维素的过程中破坏了原始纤维素分子间和分子内的氢键。另外,纤维素成膜的再生过程十分短暂,造成纤维素不能充分结晶。

图3 纤维素原粉和再生纤维素的XRD图谱Fig.3 X-ray diffractogram patterns of original cellulose and regenerated cellulose
3.2 纤维素膜的结构与形貌
图4为纤维素正渗透膜平表面和断面的电子显微镜图。表面和断面中没有出现明显的孔,说明在相转化过程中,以离子液体EMIMAc为溶剂的纤维素铸膜液分相行为与其他传统铸膜液不同。形成这一结构的原因可能是:a.纤维素在离子液体中状态和传统溶剂不同,纤维素的羟基质子和羟基氧与离子液体EMIMAc中的无机阴离子和有机阳离子之间存在静电的作用,使得离子液体EMIMAc在相转化过程中向凝胶浴中扩散的很慢;b.铸膜液的粘度很大,造成凝胶浴中的水向刚形成的纤维素膜中扩散很慢。以上因素延长了相转化的时间,从而减少了形成大孔的机会。

图4 纤维素正渗透膜平面和断面的电子显微镜照片Fig.4 Surface and cross-section SEM image of the cellulose forward osmosis membrane
3.3 纤维素正渗透膜的性能
为了验证所制备的纤维素膜正渗透性能,采用纯水为原料液,2 mol/L氯化钠溶液为汲取液,膜的活性层(即分离层)朝向汲取液,调节原料液和汲取液的体积流量均为0.24 L/min,原料液和汲取液的流向相同,测定膜的通量和截留率。由图5可知,所制的纤维素膜在该体系中运行240 min,水通量基本维持在1 L/(m2·h),最高水通量达到了3.02 L/(m2·h),对氯化钠的截留率都在99%以上,最高截留率达到了99.9%,具有良好的正渗透性能。

图5 水通量和截留率随时间的变化图Fig.5 Variation of water flux and rejection over time
为了进一步验证纤维素正渗透膜在应急供水等领域的实用性,以与海水浓度相当的0.6 mol/L氯化钠水溶液为原料液,汲取液为糖液,膜的活性层(即分离层)都朝向汲取液,调节原料液和汲取液的体积流量均为0.24 L/min,原料液和汲取液的流向相同,测定水通量和盐截留率,并与HTI的商业化正渗透膜做比较。由图6可知,自制的纤维素正渗透膜在该体系中运行240 min,水通量基本维持在2 L/(m2·h),最高水通量达到了3.534 L/(m2·h)。商业膜在该正渗透体系中运行240 min,水通量基本维持在5 L/(m2·h),最高水通量达到了5.54 L/(m2·h)。由此可见,在该测试体系中自制的纤维素正渗透膜的水通量比商业膜的水通量低,但自制的纤维素正渗透膜对NaCl的截留率略有提高,均在99%以上,最高达到了99.9%,而商业膜对NaCl的截留率最高为99.6%。
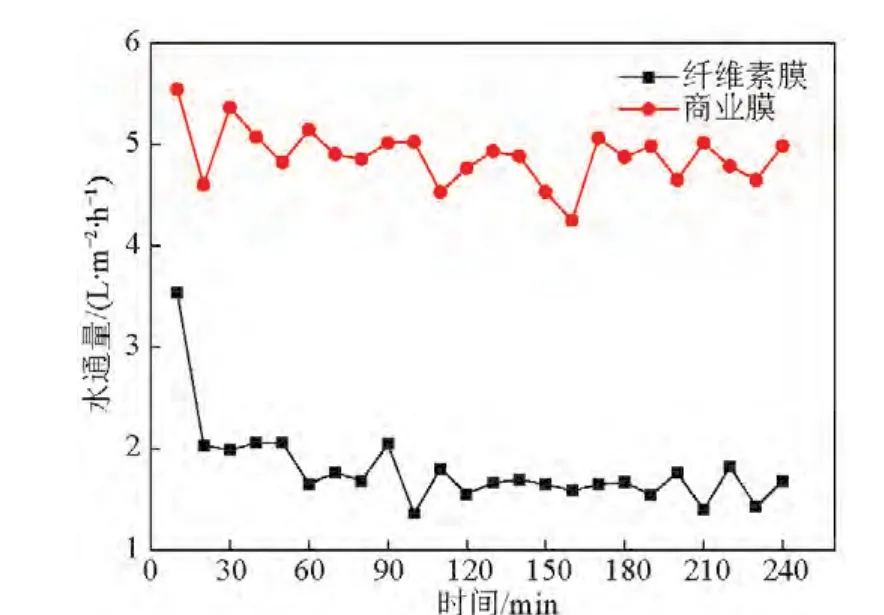
图6 水通量随时间的变化图Fig.6 Variation of water flux over time
4 结语
本文以纤维素为膜材料,无纺布作为支撑材料,利用相转化法制备了正渗透膜。红外表征结果显示纤维素溶解成膜过程中化学结构没有发生变化,但XRD结果显示纤维素溶解成膜过程中晶型由晶型Ⅰ变为了晶型Ⅱ,SEM结果表明所制备膜为无孔的均质膜。
所制备的纤维素正渗透膜在原料液为纯水,汲取液为2 mol/L氯化钠溶液的正渗透体系中水通量基本维持在1 L/(m2·h),最高水通量达到了3.02 L/(m2·h),截留率高达99.9%。在处理氯化钠浓度为0.6 mol/L的水溶液时,水通量基本维持在2 L/(m2·h)以上,较商业化正渗透膜低,但截留率最高达到99.9%,略高于商品膜的值。该膜在正渗透海水淡化过程中表现出了较好的应用潜质。
[1]李 刚,李雪梅,柳 越,等.正渗透原理及浓差极化现象[J].化学进展,2008,22(5):812-821.
[2]李 刚,李雪梅,王铎,等.正渗透技术及其应用[J].化工进展,2010,29(8):1388-1398.
[3]Pattle R E.Production of electric power by mixing fresh and salt water in the hydroelectric pile[J].Nature,1954,174:660.
[4]Weinstein J N,Leitz F B.Electric power from differences in salinity:the dialytic battery[J].Science,1976,191:557-559.
[5]Wick G L,Schmitt W R.Prospects for renewable energy from sea[J].Marine Technology Society Journal,1977,11:16-21.
[6]Kravath R E,Davis J A.Desalination of sea water by direct osmosis[J].Desalination,1975,16:151-155.
[7]Kessler J Q,Moody C D.Drinking water from sea water by forward osmosis[J].Desalination,1976,18:297-306.
[8]Moody C D,Kessler J O.Forward osmosis extractors[J].Desalination,1976,18:283-295.
[9]King C W,Webber M E.Water intensity of transportation[J].Environmental Science&Technology,2008,42:7866-7872.
[10]Petrotos K B,Lazarides H N.Osmotic concentration of liquid foods[J].Journal of Food Engineering,2001,49:201-206.
[11]Lee K L,Baker R W,Lonsdale H K.Membranes for power generation by pressure-retarded osmosis[J].Journal of Membrane Science,1981,8:141-171.
[12]Zhao S F,Zou L D,Tang C Y Y,et al.Recent developments in forward osmosis:Opportunities and challenges[J].Journal of Membrane Science,2012,396:1-21.
[13]Chen H Z,Wang N,Liu L Y.Regenerated cellulose membrane prepared with ionic liquid 1-butyl-3-methylimidazolium chloride as solvent using wheat straw[J].Journal of Chemical Technology and Biotechnology,2012,87(12):1634-1640.
[14]Lin J Y,Ding B,Yang J M,et al.Mechanical robust and thermal tolerant nanofibrous membrane for nanoparticles removal from aqueous solution[J].Materials Letters,2012,69:82-85.
[15]Li X L,Zhu L P,Zhu B K,et al.High-flux and anti-fouling cellulose nanofiltration membranes prepared via phase inversion with ionic liquid as solvent[J].Separation and Purification Technology,2011,83:66-73.
Preparation and performance of homogeneous cellulose forward osmosis membrane
Zhang Bingtao1,Zhang Lin2,Huang He1,Hou Li’an2,3
(1.State Key Laboratory of Materials-Oriented Chemical Engineering,College of Biotechnology and Pharmaceutical Engineering,Nanjing Tech University,Nanjing 210009,China;2.Engineering Research Centre of Membrane and Water Treatment Technology of MOE,Department of Chemical and Biological Engineering,Zhejiang University,Hangzhou 310027,China;3.Institute for Logistic Science and Technology of the Second Artillery,Beijing 100011,China)
The nonporous homogeneous cellulose membrane for forward osmosis was prepared via phase inversion method using ionic liquid 1-ethyl-3-methyl-imidazolium acetate(EMIMAc)as solvent,water as nonsolvent on a non-woven fabric substrate.The characterizations of Fourier transform infrared(FTIR)and X-ray diffraction(XRD)spectroscopies showed that no obvious change occurred in the chemical structure of cellulose after membrane formation,but the crystallinity had a certain degree of decline.The cross-section and the surface morphologies of the cellulose forward osmosis membrane were analyzed by scanning electron microscopy(SEM).The membrane performance were investigated by measuring water flux and rejection of simulated seawater.The water flux of the cellulose forward osmosis membrane,which the cellulose concentration is 8%(wt)in casting solution,was 3.534 L/m2·h and the rejection for NaCl was more than 99%,using 0.6 mol/L NaCl solution as the feed solution and lab-made nutrient solution as the draw solution.
forward osmosis;ionic liquid;cellulose membrane;phase inversion;membrane preparation
X703
A
1009-1742(2014)07-0057-05
2014-05-11
国家自然科学基金重点资助项目(51238006);广东顺德科技计划资助项目(2013CXTD08)
黄 和,1974年出生,男,湖北武汉市人,教授,主要研究方向为生物工程;E-mail:biotech@njut.edu.cn
